7.1.1 烷烃的结构 课件(共35张PPT) 高中化学人教版(2019)必修第二册
文档属性
| 名称 | 7.1.1 烷烃的结构 课件(共35张PPT) 高中化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 16.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-25 00:00:00 | ||
图片预览









文档简介
(共35张PPT)
第一节 认识有机化合物
第1课时:烷烃的结构
第七章 有机化合物
有机物中碳原子的成键特点
01
认识烷烃
02
学习目标
1.通过阅读思考、模型制作、动画演示等,认识甲烷的分子结构特点,掌握甲烷的结构式、电子式,建立甲烷的立体结构模型,知道甲烷的正四面体结构。
2.通过对比分析、归纳总结,认识烷烃同系物在组成、结构上的共同点,形成同系物的概念,并能对同系物进行判断。
碳在地壳中的含量很低,但是含有碳元素的有机化合物却分布很广。有机化合物不仅构成了生机勃勃的生命世界,也是燃料、材料、食品和药物的主要来源。
有机物中碳原子的成键特点
有机物中碳原子的成键特点
任务一、认识最简单的有机物—甲烷
学生活动1:阅读教材“前言”相关内容,观察图片,联系生活实
际,举例说明什么是有机化合物?与无机物相比有何特点?
①有机化合物是指含有C元素的化合物,简称有机物, CO2、H2CO3及其盐等除外。②有机化合物与人类生活有密切的关系,在衣、食、住、行、医疗、能源、材料、科学技术及工农业生产等领域中都起着重要作用,迄令为止已经超过2000万种。
衣
食
住
行
有机物中碳原子的成键特点
任务一、认识最简单的有机物—甲烷
③与无机物相比,有机物不仅数量很多,而且分布极广。如常见燃料中的汽油、煤油、柴油;建材中的木材、黏合剂、涂料、油漆;日用品中的塑料、橡胶、纤维、清洁剂;食物中的营养餐—糖类、油脂、蛋白质等都是有机化合物。
④有机化合物除一定含有碳元素外,它还可以含有氢、氧、氮、硫、磷、卤素等。
有机物中碳原子的成键特点
任务一、认识最简单的有机物—甲烷
学生活动2:阅读教材P60页内容,结合教材P62页图7-5,思考甲烷
分子结构有哪些表示方法?完成下表内容。
类别 表示方法 含义
分子式
电子式
结构式
用元素符号表示物质分子组成的式子,可反映一个分子中原子的种类和数目
用小黑点等符号代替电子,表示原子最外层电子成键情况的式子
CH4
具有化学式所能表示的意义,能反映物质的结构;表示分子中原子的结合或排列顺序的式子,不表示空间构型
有机物中碳原子的成键特点
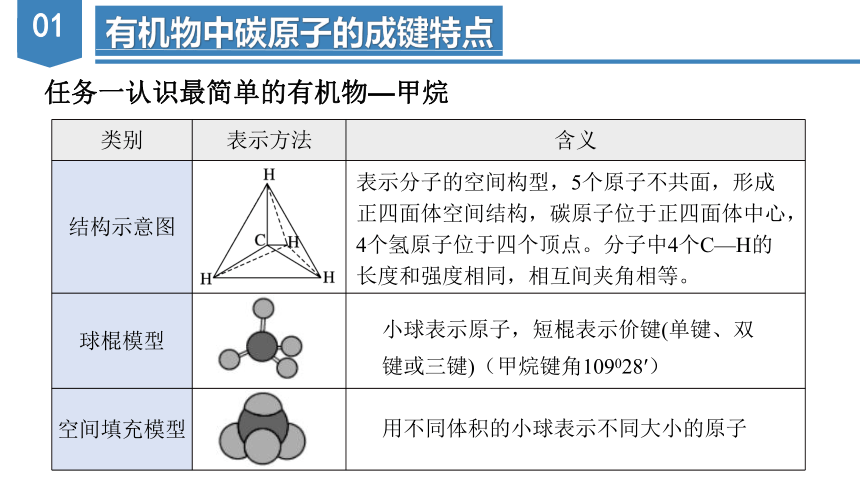
任务一认识最简单的有机物—甲烷
类别 表示方法 含义
结构示意图
球棍模型
空间填充模型
小球表示原子,短棍表示价键(单键、双键或三键)(甲烷键角109028′)
用不同体积的小球表示不同大小的原子
表示分子的空间构型,5个原子不共面,形成正四面体空间结构,碳原子位于正四面体中心,4个氢原子位于四个顶点。分子中4个C—H的长度和强度相同,相互间夹角相等。
有机物中碳原子的成键特点
【典例1】下列说法正确的是( )
A.含碳元素的化合物都是有机物 B.易溶于汽油、酒精、苯等有机溶剂的物质一定是有机化合物 C.大多数有机物分子中碳原子与碳原子之间或碳原子与其他原子之
间相结合的化学键是非极性共价键或极性共价键 D.有机物完全燃烧只可能生成CO2和H2O
【解析】有机物通常是指含碳元素的化合物,但CO2、Na2CO3等少数物质,其性质却跟无机物相似,一般把它们归为无机物,A错误;易溶于汽油、苯等有机溶剂物质不一定是有机化合物,如溴单质,B错误;有机物中碳原子与碳原子之间均形成非极性共价键,而碳原子与其他元素原子之间形成的化学键为极性共价键,C正确;有些有机物除含碳、氢、氧外,还含有氮、硫、卤素、磷等,完全燃烧可能还会生成SO2、氮的氧化物等物质,D错误。
C
有机物中碳原子的成键特点
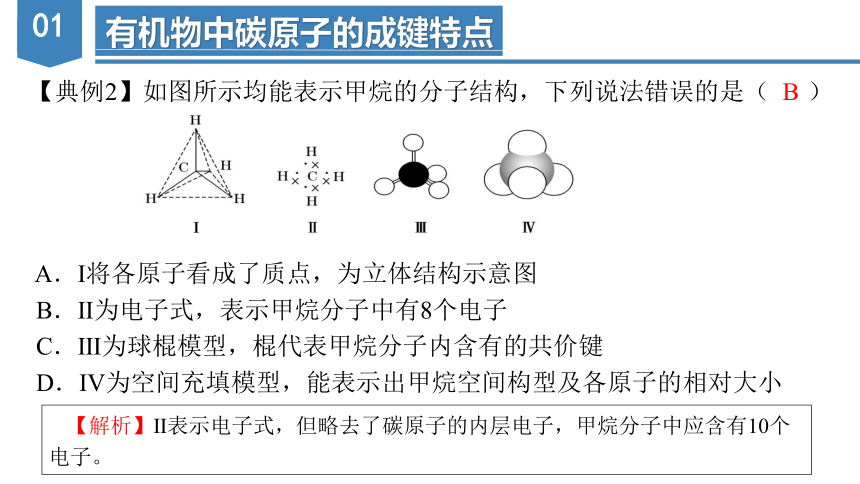
【解析】Ⅱ表示电子式,但略去了碳原子的内层电子,甲烷分子中应含有10个电子。
【典例2】如图所示均能表示甲烷的分子结构,下列说法错误的是( )
A.Ⅰ将各原子看成了质点,为立体结构示意图
B.Ⅱ为电子式,表示甲烷分子中有8个电子
C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键
D.Ⅳ为空间充填模型,能表示出甲烷空间构型及各原子的相对大小
B
有机物中碳原子的成键特点
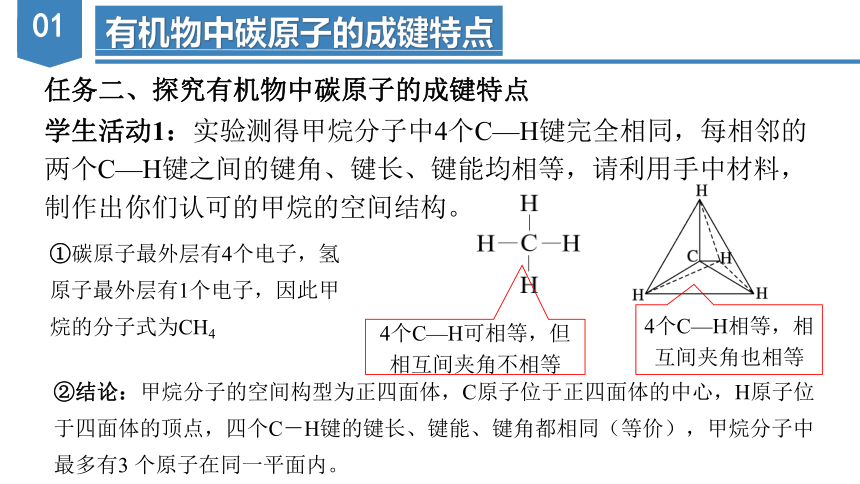
任务二、探究有机物中碳原子的成键特点
学生活动1:实验测得甲烷分子中4个C—H键完全相同,每相邻的
两个C—H键之间的键角、键长、键能均相等,请利用手中材料,
制作出你们认可的甲烷的空间结构。
①碳原子最外层有4个电子,氢原子最外层有1个电子,因此甲烷的分子式为CH4
②结论:甲烷分子的空间构型为正四面体,C原子位于正四面体的中心,H原子位于四面体的顶点,四个C-H键的键长、键能、键角都相同(等价),甲烷分子中最多有3 个原子在同一平面内。
4个C—H可相等,但相互间夹角不相等
4个C—H相等,相互间夹角也相等
有机物中碳原子的成键特点
任务二、探究有机物中碳原子的成键特点
学生活动2:结合教材P60页及P61页“思考与讨论”内容,观察图
7-1和7-3,利用两个或多个碳原子及多个氢原子制作更多的有机物
分子空间模型,分析有机物种类繁多的主要原因是什么?
①用2个碳原子,氢原子数目任选,拼出你认为合理的有机物。
方法:先关注碳原子,搭建碳骨架,再按照“碳四价”原则,补充连接其他原子。
单键
双键
叁键
有机物中碳原子的成键特点
任务二、探究有机物中碳原子的成键特点
②用3个碳原子、拼插你认为合理的有机物的碳骨架。
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
③用4个碳原子,以碳碳单键相连,拼插你认为合理的有机物的链状骨架。
图7-3 4个碳原子相互结合的几种方式
【温馨提示】有机物种类繁多的原因
①碳原子所成价键多:有机化合物中,碳原子最外层有4个单电子,可以形成4个
共价键,比氮、氧、氢或卤素原子所成价键都要多。
②碳原子成键方式多样:含有多个碳原子的有机化合物,碳原子间成键方式较多,
可以形成单键,也可以形成双键或三键。
③碳骨架多样:碳原子间所成骨架有多种,可以是直链,也可以成环,也可以带
支链。
④成链原子及种类多而灵活:有机物分子中碳原子可以与一个或若干个碳原子成
键,也可以和其他原子成键,数目不等。
有机物中碳原子的成键特点
有机物中碳原子的成键特点
【典例1】只含C、H元素的有机物分子中的碳原子与其他原子的结合
方式是( )
A.通过两个共价键 B.通过非极性键
C.形成四对共用电子对 D.通过离子键和共价键
【解析】碳原子核外最外层有四个电子,在形成有机化合物时与其他原子可形成四对共用电子对,C正确,故选C。
C
有机物中碳原子的成键特点
【典例2】有机物种类繁多的原因是( )
A.碳元素在地壳中的含量大,且属于非金属
B.碳原子间能以共价键结合,形成多种链状和环状结构
C.碳元素所形成的化合物性质稳定,且共价键键能大
D.碳原子中质子数和中子数相等
【解析】有机物分子中碳原子间能以共价键结合形成4个共价键,而且可以形成链状或环状等结构,是导致有机物种类繁多的原因,B正确。
B
认识烷烃
认识烷烃
任务一、探究烷烃的结构
学生活动1:阅读教材P62页内容,结合“思考与讨论”栏目,完
成表格填空,根据碳原子的成键规律和下表中提供的信息,试着写
出丁烷的结构烷、丙烷、丁烷等一系列的有机化合物分子式,并
归纳出该类有机物分子式的通式式什么?
烷烃 乙烷 丙烷 正丁烷
分子中碳原子数 2 3 4
分子式
结构式
结构简式
C2H6
C3H8
C4H10
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
认识烷烃
任务一、探究烷烃的结构
烷烃 乙烷 丙烷 正丁烷
分子结构模型
通式 【温馨提示】①定义:只含有碳和氢两种元素的化合物叫烃,烃分子中的碳原子之间都以单键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”。这样的一类有机化合物称为饱和烃,也称为烷烃。
CnH2n+2
认识烷烃
任务一、探究烷烃的结构
②注意:烷烃中碳原子间结合成链状,链状不是“直线状”,而是呈锯齿状,链上也可以分出支链。例如:
正丁烷
(熔点-138.4℃,沸点-0.5℃)
异丁烷
(熔点-159.4℃,沸点-11.6℃)
图7-7 正丁烷和异丁烷的分子结构模型
认识烷烃
任务一、探究烷烃的结构
学生活动2:阅读教材P63页第二自然段,思考如何对烷烃进行命名?
什么叫有机物的结构简式?
①烷烃种最简单的是甲烷,其余随碳原子数的增多,依次为乙烷、丙烷、丁烷等。
②碳原子数不多于 10 时,以甲、乙、丙、丁、戊、己、庚、辛、壬、癸依次代表碳原子数;碳原子数在 11 以上时,以数字来表示,例如,十二烷[CH3(CH2)10CH3]。即:
n≤10 1 2 3 4 5 6 7 8 9 10
甲烷 乙烷 丙烷 丁烷 戊烷 己烷 庚烷 辛烷 壬烷 癸烷
n>10 用汉字数字代表,如C11H24:十一烷 【温馨提示】碳原子数n相同结构不同时,用正、异、新表示,如C4H10的两种分子的命名:无支链时,CH3CH2CH2CH3:正丁烷,有支链时, 异丁烷。
又叫习惯命名法
认识烷烃
任务一、探究烷烃的结构
③书写有机物的结构式时,我们通常是将其写成直线形式,但同一个碳上连接的4个价键的位置是可以互相调换的,因为在空间内4个价键是可以旋转的。
④若把有机物分子的结构式中表示共价单键的“一”删去或部分删去,如乙烷:CH3CH3、丙烷:CH3CH2CH3、丁烷:CH3CH2CH2CH3等。这种变形后的式子书写起来比较方便,称之为有机物的结构简式。
【温馨提示】在书写有机物分子的结构简式时,若遇到像丁烷这样分子中有两个或多个相同的成分时,还可以写成CH3(CH2)2CH3。由于结构简式书写方便,且仍能表示出分子结构的简况,所以,更多情况下常使用结构简式。
认识烷烃
【典例1】下列关于有机物结构特点的说法中,正确的是( ) A.CH3CH2CH3分子含有极性键和非极性键
B.碳原子之间只能形成C-C单键 C.含碳元素的物质都是有机物
D.碳原子之间只能形成碳链
A
【解析】A.CH3CH2CH3中存在C-H极性键和C-C非极性键,故A正确;B.碳原子之间能形成碳碳单键,碳碳双键,碳碳三键,故B错误;C.含碳元素的物质不一定都是有机物,比如CO,故C错误;D.碳原子之间能形成碳链,也可以形成碳环,故D错误。故选:A。
认识烷烃
【典例2】下列说法正确的是( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定
是饱和链烃
B.分子组成符合CnH2n+2的烃一定是烷烃
C.正戊烷分子中所有的碳原子均在同一条直线上
D.碳、氢原子个数比为1∶3的烷烃有两种
B
【解析】A项中环烷烃也符合要求,但它不是链烃,属于环烃;C项中由碳原子的成键方式和键角特征知,碳原子呈折线方式排列,因此正戊烷中的碳原子不在同一直线上;D项中n(C)∶n(H)=1∶3时必为C2H6,一定是乙烷。
认识烷烃
任务一、认识同系物
学生活动1:阅读教材P63页第三自然段,根据甲烷、乙烷、丙烷、
丁烷、十二烷等烷烃分子的结构简式,思考什么是同系物?
。
①甲烷、乙烷、丙烷、丁烷、十二烷分子的结构简式分别为:CH4、CH3CH3、CH3CH2CH3、CH3CH2CH2CH3、CH3(CH2)10CH3。
②这些分子结构相似—只含C—C键,碳原子的剩余价键均与氢原子结合;分子组成相差一个或若干个“CH2”原子团。
③定义:像这些结构相似,在分子组成上相差一个或若干个“CH2”原子团的化合物互称为同系物。
认识烷烃
任务二、认识同系物
学生活动2:讨论同系物有何特点,如何理解烷烃同系物概念的?
①同系物特点:属于同一类物质,且有相同的通式;式量相差一定是14的倍数;化学性质相似,物理性质随着碳原子数的增加而发生规律性的变化。
②烷烃同系物:结构相似是指分子中原子全部以单键相结合,与支链或直链无关,如丙烷(CH3CH2CH3)是直连结构,异丁烷[(CH)(CH3)3]含支连结构,但二者是同系物,烷烃的组成可以用通式CnH2n+2表示。
【温馨提示】在判断同系物的时候,要严格把握同系物概念的两个方面:一是分子结构相似,二是分子组成上相差一个或若干个 CH2原子团,二者要联系在一起应用,缺一不可。当然,还应注意,同系物的关系不光是只有烷烃分子之间存在,在其他的有机物内也存在着同系物的关系。
认识烷烃
【典例1】下列关于同系物的说法中,错误的是( )
A.同系物具有相同的分子式
B.同系物符合同一通式
C.相邻的同系物在组成上相差一个CH2原子团
D.同系物的化学性质基本相似
A
【解析】同系物的结构相似,属于同一类物质,因此符合同一通式,但一定不具有相同的分子式,A错误,B正确;相邻同系物在分子组成上相差一个CH2原子团,C正确;同系物的结构相似,所以化学性质基本相似,D正确。
认识烷烃
【典例2】下列叙述中正确的是( )
A. 含个碳原子的有机物,每个分子中最多可形成个键
B. 正丁烷分子中所有碳原子在一条直线上
C. 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定符合通式
D. 分子式为与的两种有机物一定互为同系物
D
【解析】A.如果5个碳原子成环,则碳碳键数量为5。B.碳的4个键是有角度的,故正丁烷的4个碳不在一条直线上。C.若果是环状,则不满足通式。故答案为D。
1.下列说法不正确的是( )
A.有机物分子中一定含有一个或多个碳原子
B.有机物分子中的碳原子可以相互连接成链状或环状
C.有机物分子中的碳原子可以与其它元素的原子连接
D.分子中含有碳原子的化合物一定是有机化合物
D
【解析】A. 含有碳元素的化合物是有机化合物,有机物分子中一定含有一个或多个碳原子,A正确;B. 有机物分子中的碳原子可以相互连接成链状或环状,B正确;C. 有机物分子中的碳原子可以与其它元素的原子连接,C正确;D. 分子中含有碳原子的化合物不一定是有机化合物,例如CO2等,D错误。
2.下列关于碳原子的成键特点及成键方式的理解中正确的是( )
A.饱和碳原子不能发生化学反应
B.碳原子只能与碳原子形成不饱和键
C.具有六个碳原子的苯与环己烷的结构不同
D.五个碳原子最多只能形成四个碳碳单键
C
【解析】饱和碳原子可以发生取代反应或裂化反应等,A错;碳原子也可以与氧原子或氮原子等形成不饱和键,B错;五个碳原子若构成环戊烷,可以形成5个碳碳单键,D错。
3.如图为含4个碳原子的6种有机物分子模型(氢原子没有画出),下列叙述中正确的是( )
A.与d互为同分异构体的是c B.b、c、f的分子式均为C4H8
C.a和f均为链状烷烃 D.同种物质中只能含碳链或碳环
B
【解析】d和c的分子式不同,不互为同分异构体,A错误;b、c、f的分子式均为C4H8,互为同分异构体,B正确;f为环烷烃,C错误;同种物质中可能同时含有碳链和碳环,D错误。
4.下列有关烷烃的说法中正确的是( )
A.烷烃的分子组成都满足CnH2n+2(n≥1),彼此都是同系物
B.戊烷(C5H12)有三种同分异构体
C.CH3Cl只有一种结构,说明甲烷是正四面体结构而不是平面结构
D.正丁烷的四个碳原子可以在同一条直线上
B
【解析】符合通式CnH2n+2的一定是烷烃,但符合通式CnH2n+2的不同物质一定互为同系物,还可能是同分异构体,A错误;C H 的同分异构体一共有三种,分别为正戊烷、异戊烷和新戊烷,B正确;无论甲烷分子是以碳原子为中心的正四面体结构,还是平面正方形结构,CH3Cl都不存在同分异构体,即CH3Cl只有一种结构,不能说明甲烷是正四面体结构还是平面结构,C错误;烷烃分子中有多个碳原子呈锯齿形连接,碳原子不在一条直线上,D错误。
延时符
有机化合物
碳原子间成键方式
碳原子的成键特点
成键数目
含有碳元素的化合物。氧化物、碳酸及其盐等除外
习惯命名法
可形成单键(C—C)、
双键(C=C)、叁键(C C)
每个碳原子可以形成4个共价键
同系物
烷烃的结构
碳原子间都以单键结合,剩余价键均与氢原子结合,使碳原子化合价都达到“饱和”
结构相似,在分子组成上相差一个或若干个“CH2”原子团的化合物
结构
命名
第1课时 烷烃的结构
第一节 认识有机化合物
第1课时:烷烃的结构
第七章 有机化合物
有机物中碳原子的成键特点
01
认识烷烃
02
学习目标
1.通过阅读思考、模型制作、动画演示等,认识甲烷的分子结构特点,掌握甲烷的结构式、电子式,建立甲烷的立体结构模型,知道甲烷的正四面体结构。
2.通过对比分析、归纳总结,认识烷烃同系物在组成、结构上的共同点,形成同系物的概念,并能对同系物进行判断。
碳在地壳中的含量很低,但是含有碳元素的有机化合物却分布很广。有机化合物不仅构成了生机勃勃的生命世界,也是燃料、材料、食品和药物的主要来源。
有机物中碳原子的成键特点
有机物中碳原子的成键特点
任务一、认识最简单的有机物—甲烷
学生活动1:阅读教材“前言”相关内容,观察图片,联系生活实
际,举例说明什么是有机化合物?与无机物相比有何特点?
①有机化合物是指含有C元素的化合物,简称有机物, CO2、H2CO3及其盐等除外。②有机化合物与人类生活有密切的关系,在衣、食、住、行、医疗、能源、材料、科学技术及工农业生产等领域中都起着重要作用,迄令为止已经超过2000万种。
衣
食
住
行
有机物中碳原子的成键特点
任务一、认识最简单的有机物—甲烷
③与无机物相比,有机物不仅数量很多,而且分布极广。如常见燃料中的汽油、煤油、柴油;建材中的木材、黏合剂、涂料、油漆;日用品中的塑料、橡胶、纤维、清洁剂;食物中的营养餐—糖类、油脂、蛋白质等都是有机化合物。
④有机化合物除一定含有碳元素外,它还可以含有氢、氧、氮、硫、磷、卤素等。
有机物中碳原子的成键特点
任务一、认识最简单的有机物—甲烷
学生活动2:阅读教材P60页内容,结合教材P62页图7-5,思考甲烷
分子结构有哪些表示方法?完成下表内容。
类别 表示方法 含义
分子式
电子式
结构式
用元素符号表示物质分子组成的式子,可反映一个分子中原子的种类和数目
用小黑点等符号代替电子,表示原子最外层电子成键情况的式子
CH4
具有化学式所能表示的意义,能反映物质的结构;表示分子中原子的结合或排列顺序的式子,不表示空间构型
有机物中碳原子的成键特点
任务一认识最简单的有机物—甲烷
类别 表示方法 含义
结构示意图
球棍模型
空间填充模型
小球表示原子,短棍表示价键(单键、双键或三键)(甲烷键角109028′)
用不同体积的小球表示不同大小的原子
表示分子的空间构型,5个原子不共面,形成正四面体空间结构,碳原子位于正四面体中心,4个氢原子位于四个顶点。分子中4个C—H的长度和强度相同,相互间夹角相等。
有机物中碳原子的成键特点
【典例1】下列说法正确的是( )
A.含碳元素的化合物都是有机物 B.易溶于汽油、酒精、苯等有机溶剂的物质一定是有机化合物 C.大多数有机物分子中碳原子与碳原子之间或碳原子与其他原子之
间相结合的化学键是非极性共价键或极性共价键 D.有机物完全燃烧只可能生成CO2和H2O
【解析】有机物通常是指含碳元素的化合物,但CO2、Na2CO3等少数物质,其性质却跟无机物相似,一般把它们归为无机物,A错误;易溶于汽油、苯等有机溶剂物质不一定是有机化合物,如溴单质,B错误;有机物中碳原子与碳原子之间均形成非极性共价键,而碳原子与其他元素原子之间形成的化学键为极性共价键,C正确;有些有机物除含碳、氢、氧外,还含有氮、硫、卤素、磷等,完全燃烧可能还会生成SO2、氮的氧化物等物质,D错误。
C
有机物中碳原子的成键特点
【解析】Ⅱ表示电子式,但略去了碳原子的内层电子,甲烷分子中应含有10个电子。
【典例2】如图所示均能表示甲烷的分子结构,下列说法错误的是( )
A.Ⅰ将各原子看成了质点,为立体结构示意图
B.Ⅱ为电子式,表示甲烷分子中有8个电子
C.Ⅲ为球棍模型,棍代表甲烷分子内含有的共价键
D.Ⅳ为空间充填模型,能表示出甲烷空间构型及各原子的相对大小
B
有机物中碳原子的成键特点
任务二、探究有机物中碳原子的成键特点
学生活动1:实验测得甲烷分子中4个C—H键完全相同,每相邻的
两个C—H键之间的键角、键长、键能均相等,请利用手中材料,
制作出你们认可的甲烷的空间结构。
①碳原子最外层有4个电子,氢原子最外层有1个电子,因此甲烷的分子式为CH4
②结论:甲烷分子的空间构型为正四面体,C原子位于正四面体的中心,H原子位于四面体的顶点,四个C-H键的键长、键能、键角都相同(等价),甲烷分子中最多有3 个原子在同一平面内。
4个C—H可相等,但相互间夹角不相等
4个C—H相等,相互间夹角也相等
有机物中碳原子的成键特点
任务二、探究有机物中碳原子的成键特点
学生活动2:结合教材P60页及P61页“思考与讨论”内容,观察图
7-1和7-3,利用两个或多个碳原子及多个氢原子制作更多的有机物
分子空间模型,分析有机物种类繁多的主要原因是什么?
①用2个碳原子,氢原子数目任选,拼出你认为合理的有机物。
方法:先关注碳原子,搭建碳骨架,再按照“碳四价”原则,补充连接其他原子。
单键
双键
叁键
有机物中碳原子的成键特点
任务二、探究有机物中碳原子的成键特点
②用3个碳原子、拼插你认为合理的有机物的碳骨架。
C
C
C
C
C
C
C
C
C
C
C
C
C
C
C
③用4个碳原子,以碳碳单键相连,拼插你认为合理的有机物的链状骨架。
图7-3 4个碳原子相互结合的几种方式
【温馨提示】有机物种类繁多的原因
①碳原子所成价键多:有机化合物中,碳原子最外层有4个单电子,可以形成4个
共价键,比氮、氧、氢或卤素原子所成价键都要多。
②碳原子成键方式多样:含有多个碳原子的有机化合物,碳原子间成键方式较多,
可以形成单键,也可以形成双键或三键。
③碳骨架多样:碳原子间所成骨架有多种,可以是直链,也可以成环,也可以带
支链。
④成链原子及种类多而灵活:有机物分子中碳原子可以与一个或若干个碳原子成
键,也可以和其他原子成键,数目不等。
有机物中碳原子的成键特点
有机物中碳原子的成键特点
【典例1】只含C、H元素的有机物分子中的碳原子与其他原子的结合
方式是( )
A.通过两个共价键 B.通过非极性键
C.形成四对共用电子对 D.通过离子键和共价键
【解析】碳原子核外最外层有四个电子,在形成有机化合物时与其他原子可形成四对共用电子对,C正确,故选C。
C
有机物中碳原子的成键特点
【典例2】有机物种类繁多的原因是( )
A.碳元素在地壳中的含量大,且属于非金属
B.碳原子间能以共价键结合,形成多种链状和环状结构
C.碳元素所形成的化合物性质稳定,且共价键键能大
D.碳原子中质子数和中子数相等
【解析】有机物分子中碳原子间能以共价键结合形成4个共价键,而且可以形成链状或环状等结构,是导致有机物种类繁多的原因,B正确。
B
认识烷烃
认识烷烃
任务一、探究烷烃的结构
学生活动1:阅读教材P62页内容,结合“思考与讨论”栏目,完
成表格填空,根据碳原子的成键规律和下表中提供的信息,试着写
出丁烷的结构烷、丙烷、丁烷等一系列的有机化合物分子式,并
归纳出该类有机物分子式的通式式什么?
烷烃 乙烷 丙烷 正丁烷
分子中碳原子数 2 3 4
分子式
结构式
结构简式
C2H6
C3H8
C4H10
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
认识烷烃
任务一、探究烷烃的结构
烷烃 乙烷 丙烷 正丁烷
分子结构模型
通式 【温馨提示】①定义:只含有碳和氢两种元素的化合物叫烃,烃分子中的碳原子之间都以单键结合,碳原子的剩余价键均与氢原子结合,使碳原子的化合价都达到“饱和”。这样的一类有机化合物称为饱和烃,也称为烷烃。
CnH2n+2
认识烷烃
任务一、探究烷烃的结构
②注意:烷烃中碳原子间结合成链状,链状不是“直线状”,而是呈锯齿状,链上也可以分出支链。例如:
正丁烷
(熔点-138.4℃,沸点-0.5℃)
异丁烷
(熔点-159.4℃,沸点-11.6℃)
图7-7 正丁烷和异丁烷的分子结构模型
认识烷烃
任务一、探究烷烃的结构
学生活动2:阅读教材P63页第二自然段,思考如何对烷烃进行命名?
什么叫有机物的结构简式?
①烷烃种最简单的是甲烷,其余随碳原子数的增多,依次为乙烷、丙烷、丁烷等。
②碳原子数不多于 10 时,以甲、乙、丙、丁、戊、己、庚、辛、壬、癸依次代表碳原子数;碳原子数在 11 以上时,以数字来表示,例如,十二烷[CH3(CH2)10CH3]。即:
n≤10 1 2 3 4 5 6 7 8 9 10
甲烷 乙烷 丙烷 丁烷 戊烷 己烷 庚烷 辛烷 壬烷 癸烷
n>10 用汉字数字代表,如C11H24:十一烷 【温馨提示】碳原子数n相同结构不同时,用正、异、新表示,如C4H10的两种分子的命名:无支链时,CH3CH2CH2CH3:正丁烷,有支链时, 异丁烷。
又叫习惯命名法
认识烷烃
任务一、探究烷烃的结构
③书写有机物的结构式时,我们通常是将其写成直线形式,但同一个碳上连接的4个价键的位置是可以互相调换的,因为在空间内4个价键是可以旋转的。
④若把有机物分子的结构式中表示共价单键的“一”删去或部分删去,如乙烷:CH3CH3、丙烷:CH3CH2CH3、丁烷:CH3CH2CH2CH3等。这种变形后的式子书写起来比较方便,称之为有机物的结构简式。
【温馨提示】在书写有机物分子的结构简式时,若遇到像丁烷这样分子中有两个或多个相同的成分时,还可以写成CH3(CH2)2CH3。由于结构简式书写方便,且仍能表示出分子结构的简况,所以,更多情况下常使用结构简式。
认识烷烃
【典例1】下列关于有机物结构特点的说法中,正确的是( ) A.CH3CH2CH3分子含有极性键和非极性键
B.碳原子之间只能形成C-C单键 C.含碳元素的物质都是有机物
D.碳原子之间只能形成碳链
A
【解析】A.CH3CH2CH3中存在C-H极性键和C-C非极性键,故A正确;B.碳原子之间能形成碳碳单键,碳碳双键,碳碳三键,故B错误;C.含碳元素的物质不一定都是有机物,比如CO,故C错误;D.碳原子之间能形成碳链,也可以形成碳环,故D错误。故选:A。
认识烷烃
【典例2】下列说法正确的是( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定
是饱和链烃
B.分子组成符合CnH2n+2的烃一定是烷烃
C.正戊烷分子中所有的碳原子均在同一条直线上
D.碳、氢原子个数比为1∶3的烷烃有两种
B
【解析】A项中环烷烃也符合要求,但它不是链烃,属于环烃;C项中由碳原子的成键方式和键角特征知,碳原子呈折线方式排列,因此正戊烷中的碳原子不在同一直线上;D项中n(C)∶n(H)=1∶3时必为C2H6,一定是乙烷。
认识烷烃
任务一、认识同系物
学生活动1:阅读教材P63页第三自然段,根据甲烷、乙烷、丙烷、
丁烷、十二烷等烷烃分子的结构简式,思考什么是同系物?
。
①甲烷、乙烷、丙烷、丁烷、十二烷分子的结构简式分别为:CH4、CH3CH3、CH3CH2CH3、CH3CH2CH2CH3、CH3(CH2)10CH3。
②这些分子结构相似—只含C—C键,碳原子的剩余价键均与氢原子结合;分子组成相差一个或若干个“CH2”原子团。
③定义:像这些结构相似,在分子组成上相差一个或若干个“CH2”原子团的化合物互称为同系物。
认识烷烃
任务二、认识同系物
学生活动2:讨论同系物有何特点,如何理解烷烃同系物概念的?
①同系物特点:属于同一类物质,且有相同的通式;式量相差一定是14的倍数;化学性质相似,物理性质随着碳原子数的增加而发生规律性的变化。
②烷烃同系物:结构相似是指分子中原子全部以单键相结合,与支链或直链无关,如丙烷(CH3CH2CH3)是直连结构,异丁烷[(CH)(CH3)3]含支连结构,但二者是同系物,烷烃的组成可以用通式CnH2n+2表示。
【温馨提示】在判断同系物的时候,要严格把握同系物概念的两个方面:一是分子结构相似,二是分子组成上相差一个或若干个 CH2原子团,二者要联系在一起应用,缺一不可。当然,还应注意,同系物的关系不光是只有烷烃分子之间存在,在其他的有机物内也存在着同系物的关系。
认识烷烃
【典例1】下列关于同系物的说法中,错误的是( )
A.同系物具有相同的分子式
B.同系物符合同一通式
C.相邻的同系物在组成上相差一个CH2原子团
D.同系物的化学性质基本相似
A
【解析】同系物的结构相似,属于同一类物质,因此符合同一通式,但一定不具有相同的分子式,A错误,B正确;相邻同系物在分子组成上相差一个CH2原子团,C正确;同系物的结构相似,所以化学性质基本相似,D正确。
认识烷烃
【典例2】下列叙述中正确的是( )
A. 含个碳原子的有机物,每个分子中最多可形成个键
B. 正丁烷分子中所有碳原子在一条直线上
C. 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定符合通式
D. 分子式为与的两种有机物一定互为同系物
D
【解析】A.如果5个碳原子成环,则碳碳键数量为5。B.碳的4个键是有角度的,故正丁烷的4个碳不在一条直线上。C.若果是环状,则不满足通式。故答案为D。
1.下列说法不正确的是( )
A.有机物分子中一定含有一个或多个碳原子
B.有机物分子中的碳原子可以相互连接成链状或环状
C.有机物分子中的碳原子可以与其它元素的原子连接
D.分子中含有碳原子的化合物一定是有机化合物
D
【解析】A. 含有碳元素的化合物是有机化合物,有机物分子中一定含有一个或多个碳原子,A正确;B. 有机物分子中的碳原子可以相互连接成链状或环状,B正确;C. 有机物分子中的碳原子可以与其它元素的原子连接,C正确;D. 分子中含有碳原子的化合物不一定是有机化合物,例如CO2等,D错误。
2.下列关于碳原子的成键特点及成键方式的理解中正确的是( )
A.饱和碳原子不能发生化学反应
B.碳原子只能与碳原子形成不饱和键
C.具有六个碳原子的苯与环己烷的结构不同
D.五个碳原子最多只能形成四个碳碳单键
C
【解析】饱和碳原子可以发生取代反应或裂化反应等,A错;碳原子也可以与氧原子或氮原子等形成不饱和键,B错;五个碳原子若构成环戊烷,可以形成5个碳碳单键,D错。
3.如图为含4个碳原子的6种有机物分子模型(氢原子没有画出),下列叙述中正确的是( )
A.与d互为同分异构体的是c B.b、c、f的分子式均为C4H8
C.a和f均为链状烷烃 D.同种物质中只能含碳链或碳环
B
【解析】d和c的分子式不同,不互为同分异构体,A错误;b、c、f的分子式均为C4H8,互为同分异构体,B正确;f为环烷烃,C错误;同种物质中可能同时含有碳链和碳环,D错误。
4.下列有关烷烃的说法中正确的是( )
A.烷烃的分子组成都满足CnH2n+2(n≥1),彼此都是同系物
B.戊烷(C5H12)有三种同分异构体
C.CH3Cl只有一种结构,说明甲烷是正四面体结构而不是平面结构
D.正丁烷的四个碳原子可以在同一条直线上
B
【解析】符合通式CnH2n+2的一定是烷烃,但符合通式CnH2n+2的不同物质一定互为同系物,还可能是同分异构体,A错误;C H 的同分异构体一共有三种,分别为正戊烷、异戊烷和新戊烷,B正确;无论甲烷分子是以碳原子为中心的正四面体结构,还是平面正方形结构,CH3Cl都不存在同分异构体,即CH3Cl只有一种结构,不能说明甲烷是正四面体结构还是平面结构,C错误;烷烃分子中有多个碳原子呈锯齿形连接,碳原子不在一条直线上,D错误。
延时符
有机化合物
碳原子间成键方式
碳原子的成键特点
成键数目
含有碳元素的化合物。氧化物、碳酸及其盐等除外
习惯命名法
可形成单键(C—C)、
双键(C=C)、叁键(C C)
每个碳原子可以形成4个共价键
同系物
烷烃的结构
碳原子间都以单键结合,剩余价键均与氢原子结合,使碳原子化合价都达到“饱和”
结构相似,在分子组成上相差一个或若干个“CH2”原子团的化合物
结构
命名
第1课时 烷烃的结构
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
