第八单元金属和金属材料单元练习人教版化学九年级下册(含答案)
文档属性
| 名称 | 第八单元金属和金属材料单元练习人教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 555.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-26 00:00:00 | ||
图片预览




文档简介
第八单元 金属和金属材料 单元练习
一、多选题
1.现有一定质量的AgNO3和Fe(NO3)2的混合溶液,向其中加入3g锌粉,充分反应后过滤,得到一定温度下的不饱和溶液和滤渣。下列有关说法中,正确的是( )
A.滤渣的质量可能为3g
B.滤渣中一定有单质Ag
C.若滤渣中有Ag和Fe,则滤液一定为无色
D.若滤渣中只有Ag,则滤液中至少含两种金属阳离子
2.用“W”型玻璃管进行微型实验。将注射器中的过氧化氢溶液推入管中与二氧化锰接触。下列说法不正确的是
A.过氧化氢分解能生成氧气
B.若a处粉末是木炭粉,观察到有二氧化碳生成
C.若a处粉末是硫粉,b处应接尾气处理装置
D.若a处粉末是铜粉,能看到粉末由黑色变为红色
3.科学家研制出一种新型的催化剂,可以有效去除装修残留的甲醛(化学式为CH2O), 该反应过程的微观示意图如下。下列说法中,正确的是
A.该化学反应前后氧元素的化合价不变
B.该化学反应类型不属于置换反应
C.该化学反应前后分子、原子的种类均发生改变
D.该化学反应的生成物质量比为 22 : 9
4.室温下,向含有CuSO4、MgSO4的混合溶液中加入ag锌粉,充分反应后过滤,得到滤渣和滤液(不饱和)。取少许滤渣,滴入稀盐酸,无明显现象。则下列判断中,正确的是
A.滤液一定是蓝色溶液 B.滤液中一定含有Zn2+、Mg2+
C.滤渣的质量一定小于ag D.滤渣中一定只有Cu
5.一定条件下,在托盘天平的左右两盘上各放一只烧杯,均加入质量分数相同、体积相等的稀盐酸、调整天平呈平衡状态。下列实验操作,最终仍能使天平保持平衡的是
A.向左、右两烧杯中分别加入5.6gFe和1.8gAl,两种金属完全溶解
B.向左、右两烧杯中分别加入相等质量的Mg、Al,反应后两种金属均有剩余
C.向左、右两烧杯中分别加入5.6gFe、5.4gCaO,反应后盐酸有剩余
D.向左、右两烧杯中分别加入相等质量的Al、Zn,两种金属完全溶解
二、选择题
6.下列实验操作不能达到实验目的的是
选项 实验目的 主要实验操作
A 除去CaO中的CaCO3 高温煅烧
B 区分真黄金和假黄金(铜锌合金 取样品放入稀硫酸中,观察是否有气泡
C 鉴别CO2和CO 将气体通入石蕊溶液中、观察现象
D 量取8mL水 向100mL量筒中加水至8mL刻度
A.A B.B C.C D.D
7.元素化合价发生改变的反应都是氧化还原反应。下列判断正确的是
A.化合反应都属于氧化还原反应 B.置换反应都属于氧化还原反应
C.分解反应都属于氧化还原反应 D.复分解反应都属于氧化还原反应
8.生产生活中的以下想法或做法科学合理的是( )
A.循环用水以节约水资源
B.CO2会污染环境,溶于雨水形成酸雨
C.锈蚀的钢铁不值得回收利用
D.生活废水不会造成污染,可直接排放
9.已知甲、乙两种物质在光照条件下能发生化学反应生成丙和丁,其微观示意图如图(说明:一种小球代表一种原子),则下列说法正确的是( )
A.图示中的反应物都是化合物
B.该反应不是置换反应
C.该反应原子种类与分子种类都不变,因此符合质量守恒定律
D.图示中的反应物、生成物质量比为 1:1:1:1
10.向一定量的AgNO3与Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤.分析判断下列说法正确的是
A.滤渣中一定有Zn,可能有Ag
B.滤渣中一定有Cu、Ag,可能有Zn
C.滤液中只有Zn(NO3)2
D.滤液中一定有Zn(NO3)2,可能有Cu(NO3)2
11.钛和钛合金被认为是21世纪重要的稀有金属材料,被誉为“未来金属”。为了探究铜、铝、钛的三种金属活泼性顺序,化学兴趣小组进行如下实验:将三块大小差不多的金属片先用砂布擦亮,再将它们分别投入等浓度、等体积的稀盐酸中。观察到钛片放出气泡缓慢,铝片放出气泡较快,而铜片无明显现象。试判断三种金属活动性顺序应为( )
A.铝>钛>铜 B.铜>铝>钛 C.钛>铝>铜 D.铜>钛>铝
12.如图是某化学反应的微观模拟示意图,下列说法中错误的是
A.该反应属于置换反应 B.化学反应前后原子种类和数目不变
C.生成物中C、D分子个数比是1:3 D.反应前后元素的化合价均不发生改变
13.下列金属中,在常温下就容易与氧气反应,点燃的该金属在氧气中剧烈燃烧,发出耀眼的白光,该金属是
A.镁 B.铁 C.金 D.铜
14.生活中的下列一些做法,其中对科学知识的应用合理的是
A.油锅着火用锅盖盖灭是利用移离可燃物的灭火原理
B.用稀盐酸除铁锈要控制好酸的用量,因为铁也能和稀盐酸发生反应
C.冬天汽车的雪地胎采用大花纹且花纹较深是为了减小摩擦
D.用扳手将课桌上的螺丝拧紧是利用了费力杠杆
15.下列排序正确的是
A.利用金属的年代: B.铁元素的质量分数:
C.碳元素的化合价: D.空气中物质的含量:
三、综合应用题
16.金属在生产、生活和社会发展中应用广泛。
(1)铜丝、铝丝常用作导线,是因为它们具有良好的 性。
(2)锂原子的结构示意图为,锂(Li)在反应中易形成离子,锂离子的符号为 ;锂一水电池常用作潜艇的储备电源。锂与水反应生成氢氧化锂和一种可燃性气体,该反应的化学方程式为 。
(3)图模拟炼铁的原理,a处反应的化学方程式为 ;若b处溶液改为紫色石蕊试液,b处的现象是 。
(4)在AgNO3、和的混合溶液中加入一定量的锌粉,充分反应后过滤。请回答下列问题:
①若向滤渣中滴加稀盐酸,有气泡产生,滤渣中肯定含有的物质为 。
②写出能使反应后溶液质量减小的反应的化学方程式 。
(5)若用电解熔融氧化铝的方法得到铝和氧气,生产50t纯度为99%的铝锭,则理论上消耗氧化铝多少吨 ?
17.铁及其化合物在生产生活中有广泛的应用。
(一)铁的应用和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁元素,反应的化学方程式为 。
(2)铁锈主要成分是Fe2O3 nH2O ,铁生锈主要与空气中的 有关。
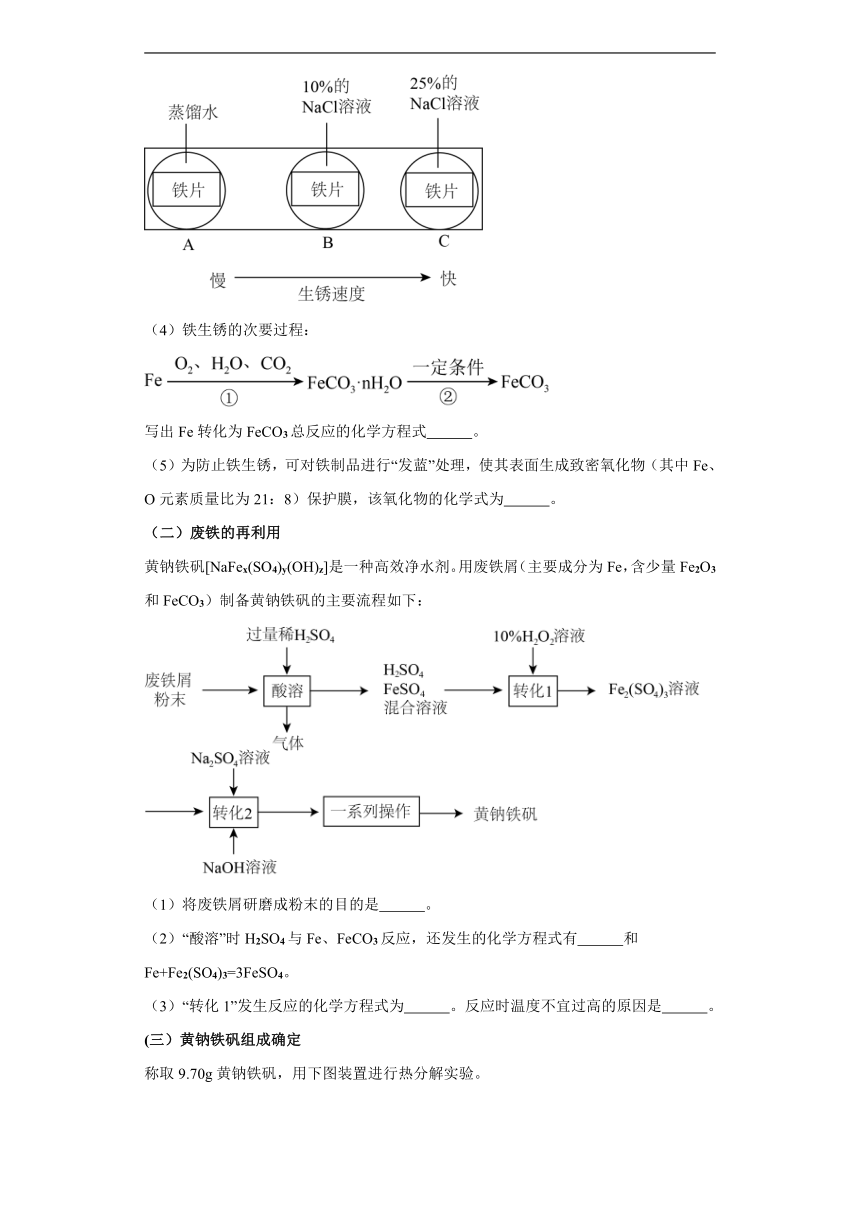
(3)如图实验说明NaCl在铁生锈中的作用是 。
(4)铁生锈的次要过程:
写出Fe转化为FeCO3总反应的化学方程式 。
(5)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为 。
(二)废铁的再利用
黄钠铁矾[NaFex(SO4)y(OH)z]是一种高效净水剂。用废铁屑(主要成分为Fe,含少量Fe2O3和FeCO3)制备黄钠铁矾的主要流程如下:
(1)将废铁屑研磨成粉末的目的是 。
(2)“酸溶”时H2SO4与Fe、FeCO3反应,还发生的化学方程式有 和Fe+Fe2(SO4)3=3FeSO4。
(3)“转化1”发生反应的化学方程式为 。反应时温度不宜过高的原因是 。
(三)黄钠铁矾组成确定
称取9.70g黄钠铁矾,用下图装置进行热分解实验。
【资料】①NaFex(SO4)y(OH)z在T1℃分解会生成H2O(气态),提高温度至T2℃继续分解产生SO3气体,并得到Fe203和Na2SO4。
②浓硫酸可用于吸收SO3。
(1)装配好实验装置后,先要 。
(2)分别控制温度在T1℃、T2℃对A中固体加热。
①控制温度在T1℃加热,实验后测得B装置质量增加1.08g。
②用D装置替换B装置,控制温度在T2℃,加热至反应完全。
③T1℃、T2℃时,加热后均通入一段时间N2,目的是 。
(3)完全反应后,将A装置中固体溶于足量水,过滤、洗涤、烘干得4.80g固体,将滤液蒸干得1.42g固体(不含结晶水)。
结论:NaFex(SO4)y(OH)z中,x:y:z= 。
反思:若该实验过程中缺少C装置,则x:z的值 (选填“偏大”、“偏小”或“不变”)。
18.科学技术的发展提高了人类的生活水平和质量。请回答下列问题:
(1)我国铜冶炼技术具有悠久的历史。《格致粗谈》记载“赤铜入炉甘石炼为黄铜,其色如金”,把赤铜(Cu2O)和炉甘石、木炭粉混合高温制得黄铜:。则炉甘石主要成分X的化学式为 ,反应中体现还原性的物质是 (填化学式)。
(2)某班级用Fe(NO3)2、Cu(NO3)2、AgNO3混合废液,研究铁、铜、银的金属活动性,并回收Ag。
①步骤Ⅱ和步骤Ⅳ的名称 ;
②滤液A的溶质是 ;
③步骤Ⅲ中加入足量AgNO3溶液的目的是 ;
(3)某兴趣小组的同学究为确定CO和CuO反应的最佳温度,小组同学利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图所示,据图回答下列问题:
①400℃时,反应的固体产物中含有 。
②用CO还原CuO制取纯净的Cu,反应温度至少要控制在 ℃以上。
参考答案:
1.ABD
2.BD
3.BD
4.BCD
5.BC
6.D
7.B
8.A
9.B
10.D
11.A
12.D
13.A
14.B
15.B
16. 导电 Li+ 紫色溶液变红色 Ag、Cu和Zn 解:设需要电解氧化铝的质量为x
x=93.5t
答:理论上消耗氧化铝93.5吨。
17. Fe + 2HCl= FeCl2 + H2↑ 水和氧气(或H20和O2) 加快铁的腐蚀 2Fe + O2 + 2CO2 == 2FeCO3 Fe3O4 增大接触面积,加快反应速率(或提高铁的浸取率) Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O 2FeSO4 + H2O2 + H2SO4 == Fe2(SO4)3 + 2H2O 防止H2O2分解 检查装置的气密性 使生成的H2O和SO3分别被B装置和D装置充分吸收 3:2:6 偏小
18.(1) ZnCO3 C
(2) 过滤 Fe(NO2)2、Cu(NO2)2 除去过量的铜,得到纯净的银
(3) Cu、CuO和Cu2O 500
一、多选题
1.现有一定质量的AgNO3和Fe(NO3)2的混合溶液,向其中加入3g锌粉,充分反应后过滤,得到一定温度下的不饱和溶液和滤渣。下列有关说法中,正确的是( )
A.滤渣的质量可能为3g
B.滤渣中一定有单质Ag
C.若滤渣中有Ag和Fe,则滤液一定为无色
D.若滤渣中只有Ag,则滤液中至少含两种金属阳离子
2.用“W”型玻璃管进行微型实验。将注射器中的过氧化氢溶液推入管中与二氧化锰接触。下列说法不正确的是
A.过氧化氢分解能生成氧气
B.若a处粉末是木炭粉,观察到有二氧化碳生成
C.若a处粉末是硫粉,b处应接尾气处理装置
D.若a处粉末是铜粉,能看到粉末由黑色变为红色
3.科学家研制出一种新型的催化剂,可以有效去除装修残留的甲醛(化学式为CH2O), 该反应过程的微观示意图如下。下列说法中,正确的是
A.该化学反应前后氧元素的化合价不变
B.该化学反应类型不属于置换反应
C.该化学反应前后分子、原子的种类均发生改变
D.该化学反应的生成物质量比为 22 : 9
4.室温下,向含有CuSO4、MgSO4的混合溶液中加入ag锌粉,充分反应后过滤,得到滤渣和滤液(不饱和)。取少许滤渣,滴入稀盐酸,无明显现象。则下列判断中,正确的是
A.滤液一定是蓝色溶液 B.滤液中一定含有Zn2+、Mg2+
C.滤渣的质量一定小于ag D.滤渣中一定只有Cu
5.一定条件下,在托盘天平的左右两盘上各放一只烧杯,均加入质量分数相同、体积相等的稀盐酸、调整天平呈平衡状态。下列实验操作,最终仍能使天平保持平衡的是
A.向左、右两烧杯中分别加入5.6gFe和1.8gAl,两种金属完全溶解
B.向左、右两烧杯中分别加入相等质量的Mg、Al,反应后两种金属均有剩余
C.向左、右两烧杯中分别加入5.6gFe、5.4gCaO,反应后盐酸有剩余
D.向左、右两烧杯中分别加入相等质量的Al、Zn,两种金属完全溶解
二、选择题
6.下列实验操作不能达到实验目的的是
选项 实验目的 主要实验操作
A 除去CaO中的CaCO3 高温煅烧
B 区分真黄金和假黄金(铜锌合金 取样品放入稀硫酸中,观察是否有气泡
C 鉴别CO2和CO 将气体通入石蕊溶液中、观察现象
D 量取8mL水 向100mL量筒中加水至8mL刻度
A.A B.B C.C D.D
7.元素化合价发生改变的反应都是氧化还原反应。下列判断正确的是
A.化合反应都属于氧化还原反应 B.置换反应都属于氧化还原反应
C.分解反应都属于氧化还原反应 D.复分解反应都属于氧化还原反应
8.生产生活中的以下想法或做法科学合理的是( )
A.循环用水以节约水资源
B.CO2会污染环境,溶于雨水形成酸雨
C.锈蚀的钢铁不值得回收利用
D.生活废水不会造成污染,可直接排放
9.已知甲、乙两种物质在光照条件下能发生化学反应生成丙和丁,其微观示意图如图(说明:一种小球代表一种原子),则下列说法正确的是( )
A.图示中的反应物都是化合物
B.该反应不是置换反应
C.该反应原子种类与分子种类都不变,因此符合质量守恒定律
D.图示中的反应物、生成物质量比为 1:1:1:1
10.向一定量的AgNO3与Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤.分析判断下列说法正确的是
A.滤渣中一定有Zn,可能有Ag
B.滤渣中一定有Cu、Ag,可能有Zn
C.滤液中只有Zn(NO3)2
D.滤液中一定有Zn(NO3)2,可能有Cu(NO3)2
11.钛和钛合金被认为是21世纪重要的稀有金属材料,被誉为“未来金属”。为了探究铜、铝、钛的三种金属活泼性顺序,化学兴趣小组进行如下实验:将三块大小差不多的金属片先用砂布擦亮,再将它们分别投入等浓度、等体积的稀盐酸中。观察到钛片放出气泡缓慢,铝片放出气泡较快,而铜片无明显现象。试判断三种金属活动性顺序应为( )
A.铝>钛>铜 B.铜>铝>钛 C.钛>铝>铜 D.铜>钛>铝
12.如图是某化学反应的微观模拟示意图,下列说法中错误的是
A.该反应属于置换反应 B.化学反应前后原子种类和数目不变
C.生成物中C、D分子个数比是1:3 D.反应前后元素的化合价均不发生改变
13.下列金属中,在常温下就容易与氧气反应,点燃的该金属在氧气中剧烈燃烧,发出耀眼的白光,该金属是
A.镁 B.铁 C.金 D.铜
14.生活中的下列一些做法,其中对科学知识的应用合理的是
A.油锅着火用锅盖盖灭是利用移离可燃物的灭火原理
B.用稀盐酸除铁锈要控制好酸的用量,因为铁也能和稀盐酸发生反应
C.冬天汽车的雪地胎采用大花纹且花纹较深是为了减小摩擦
D.用扳手将课桌上的螺丝拧紧是利用了费力杠杆
15.下列排序正确的是
A.利用金属的年代: B.铁元素的质量分数:
C.碳元素的化合价: D.空气中物质的含量:
三、综合应用题
16.金属在生产、生活和社会发展中应用广泛。
(1)铜丝、铝丝常用作导线,是因为它们具有良好的 性。
(2)锂原子的结构示意图为,锂(Li)在反应中易形成离子,锂离子的符号为 ;锂一水电池常用作潜艇的储备电源。锂与水反应生成氢氧化锂和一种可燃性气体,该反应的化学方程式为 。
(3)图模拟炼铁的原理,a处反应的化学方程式为 ;若b处溶液改为紫色石蕊试液,b处的现象是 。
(4)在AgNO3、和的混合溶液中加入一定量的锌粉,充分反应后过滤。请回答下列问题:
①若向滤渣中滴加稀盐酸,有气泡产生,滤渣中肯定含有的物质为 。
②写出能使反应后溶液质量减小的反应的化学方程式 。
(5)若用电解熔融氧化铝的方法得到铝和氧气,生产50t纯度为99%的铝锭,则理论上消耗氧化铝多少吨 ?
17.铁及其化合物在生产生活中有广泛的应用。
(一)铁的应用和防护
(1)某麦片中含微量铁粉,食用后铁粉与胃酸反应转化为人体可吸收的铁元素,反应的化学方程式为 。
(2)铁锈主要成分是Fe2O3 nH2O ,铁生锈主要与空气中的 有关。
(3)如图实验说明NaCl在铁生锈中的作用是 。
(4)铁生锈的次要过程:
写出Fe转化为FeCO3总反应的化学方程式 。
(5)为防止铁生锈,可对铁制品进行“发蓝”处理,使其表面生成致密氧化物(其中Fe、O元素质量比为21:8)保护膜,该氧化物的化学式为 。
(二)废铁的再利用
黄钠铁矾[NaFex(SO4)y(OH)z]是一种高效净水剂。用废铁屑(主要成分为Fe,含少量Fe2O3和FeCO3)制备黄钠铁矾的主要流程如下:
(1)将废铁屑研磨成粉末的目的是 。
(2)“酸溶”时H2SO4与Fe、FeCO3反应,还发生的化学方程式有 和Fe+Fe2(SO4)3=3FeSO4。
(3)“转化1”发生反应的化学方程式为 。反应时温度不宜过高的原因是 。
(三)黄钠铁矾组成确定
称取9.70g黄钠铁矾,用下图装置进行热分解实验。
【资料】①NaFex(SO4)y(OH)z在T1℃分解会生成H2O(气态),提高温度至T2℃继续分解产生SO3气体,并得到Fe203和Na2SO4。
②浓硫酸可用于吸收SO3。
(1)装配好实验装置后,先要 。
(2)分别控制温度在T1℃、T2℃对A中固体加热。
①控制温度在T1℃加热,实验后测得B装置质量增加1.08g。
②用D装置替换B装置,控制温度在T2℃,加热至反应完全。
③T1℃、T2℃时,加热后均通入一段时间N2,目的是 。
(3)完全反应后,将A装置中固体溶于足量水,过滤、洗涤、烘干得4.80g固体,将滤液蒸干得1.42g固体(不含结晶水)。
结论:NaFex(SO4)y(OH)z中,x:y:z= 。
反思:若该实验过程中缺少C装置,则x:z的值 (选填“偏大”、“偏小”或“不变”)。
18.科学技术的发展提高了人类的生活水平和质量。请回答下列问题:
(1)我国铜冶炼技术具有悠久的历史。《格致粗谈》记载“赤铜入炉甘石炼为黄铜,其色如金”,把赤铜(Cu2O)和炉甘石、木炭粉混合高温制得黄铜:。则炉甘石主要成分X的化学式为 ,反应中体现还原性的物质是 (填化学式)。
(2)某班级用Fe(NO3)2、Cu(NO3)2、AgNO3混合废液,研究铁、铜、银的金属活动性,并回收Ag。
①步骤Ⅱ和步骤Ⅳ的名称 ;
②滤液A的溶质是 ;
③步骤Ⅲ中加入足量AgNO3溶液的目的是 ;
(3)某兴趣小组的同学究为确定CO和CuO反应的最佳温度,小组同学利用原位X射线粉末衍射仪来测定不同温度下反应4小时后的固体物质成分,实验结果如图所示,据图回答下列问题:
①400℃时,反应的固体产物中含有 。
②用CO还原CuO制取纯净的Cu,反应温度至少要控制在 ℃以上。
参考答案:
1.ABD
2.BD
3.BD
4.BCD
5.BC
6.D
7.B
8.A
9.B
10.D
11.A
12.D
13.A
14.B
15.B
16. 导电 Li+ 紫色溶液变红色 Ag、Cu和Zn 解:设需要电解氧化铝的质量为x
x=93.5t
答:理论上消耗氧化铝93.5吨。
17. Fe + 2HCl= FeCl2 + H2↑ 水和氧气(或H20和O2) 加快铁的腐蚀 2Fe + O2 + 2CO2 == 2FeCO3 Fe3O4 增大接触面积,加快反应速率(或提高铁的浸取率) Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O 2FeSO4 + H2O2 + H2SO4 == Fe2(SO4)3 + 2H2O 防止H2O2分解 检查装置的气密性 使生成的H2O和SO3分别被B装置和D装置充分吸收 3:2:6 偏小
18.(1) ZnCO3 C
(2) 过滤 Fe(NO2)2、Cu(NO2)2 除去过量的铜,得到纯净的银
(3) Cu、CuO和Cu2O 500
同课章节目录
