2024年广东省梅州市部分学校3月中考模拟考试化学试题(含答案)
文档属性
| 名称 | 2024年广东省梅州市部分学校3月中考模拟考试化学试题(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 308.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-27 09:22:54 | ||
图片预览


文档简介
2024年广东省梅州市部分学校3月中考模拟考试化学试题
可能用到的相对原子质量:H-1 C-12 O-16 N-14 Na-23 Mg-24 Al-27 Cl-35.5
S-32 Fe-56 Zn-65
一、选择题(本大题共15小题,每小题 3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.下列过程属于化学变化的是( )
A.水果榨汁 B.白糖熔化 C.葡萄酿酒 D.丹桂飘香
2.液氮可做制冷剂,它属于( )
A.纯净物 B.混合物 C.氧化物 D.化合物
3.下列实验基本操作中,正确的是( )
A.倾倒液体 B.过滤 C.加热液体 D.熄灭酒精灯
4.下列物质在空气或氧气中燃烧时,现象描述正确的是( )
A.镁条在空气中燃烧,冒出浓烈的白烟,放出热量,生成黑色粉末
B.木炭在氧气中燃烧,发出白光,放出热量,产生能使澄清石灰水变浑浊的气体
C.铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成红色粉末
D.硫在氧气中燃烧,发出微弱的淡蓝色火焰,放出热量,产生没有气味的气体
5.生活中一些物质的pH如下表所示,下列说法中错误的是( )
物质 橘子 西瓜 牙膏 肥皂 草木灰
pH 3~4 5~6 8~9 10 11
A.西瓜汁显酸性 C.草木灰可改良酸性土壤
B.胃酸过多的人不宜吃橘子 D.肥皂水可使紫色石蕊溶液变红
6.下列食物中富含蛋白质的是( )
A.牛肉、鲜奶 B.米饭、红薯 C.土豆 D.苹果
7.2021 年 12 月9日,“天空课堂”在中国空间站精彩开讲。铁酸镍(化学式:NiFe2O4)可以将航天员呼出的废气转化为航天员需要的气体,而本身的质量和化学性质都不变化,NiFe2O4中若铁元素的化合价是+3价,则镍(Ni)元素的化合价是( )
A.-2 B.+4 C.-1 D.+2
8.合理施用化肥,能提高农作物的产量,下列属于复合肥的是( )
A.尿素 B.硝酸钾 C.磷矿粉 D.氯化钾
9.如图所示是某化学反应的微观示意图。下列有关该化学反应的说法正确的是( )
A.化学反应前后原子种类不变 B.该反应是置换反应
C.甲、乙、丙、丁四种物质都是单质 D.反应生成的丙、丁分子个数比为1:1
10.广东地区因气候等原因喜欢饮用凉茶,凉茶具有清热解毒、凉血利咽功效,主要成分是黑芥子甙(C10H17NO9S2),可以预防感冒。下列有关说法正确的是( )
A.黑芥子试中氢、氧、硫元素的质量比为17:9:2
B.黑芥子甙中含有39个原子
C.黑芥子戒中的氮元素的质量分数最小
D.黑芥子甙在氧气中充分燃烧只生成 CO2和 H2O
11.将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如表所示:下列有关说法正确的是( )
12.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
13.下列各组物质能大量共存,并形成无色溶液的是( )
A.NH4Cl、Na2SO4、HNO3 B.BaCl2、Na2CO3、CuCl2
C.BaCl2、NaHCO3、K2SO4 D.FeCl3、NaOH、NaCl
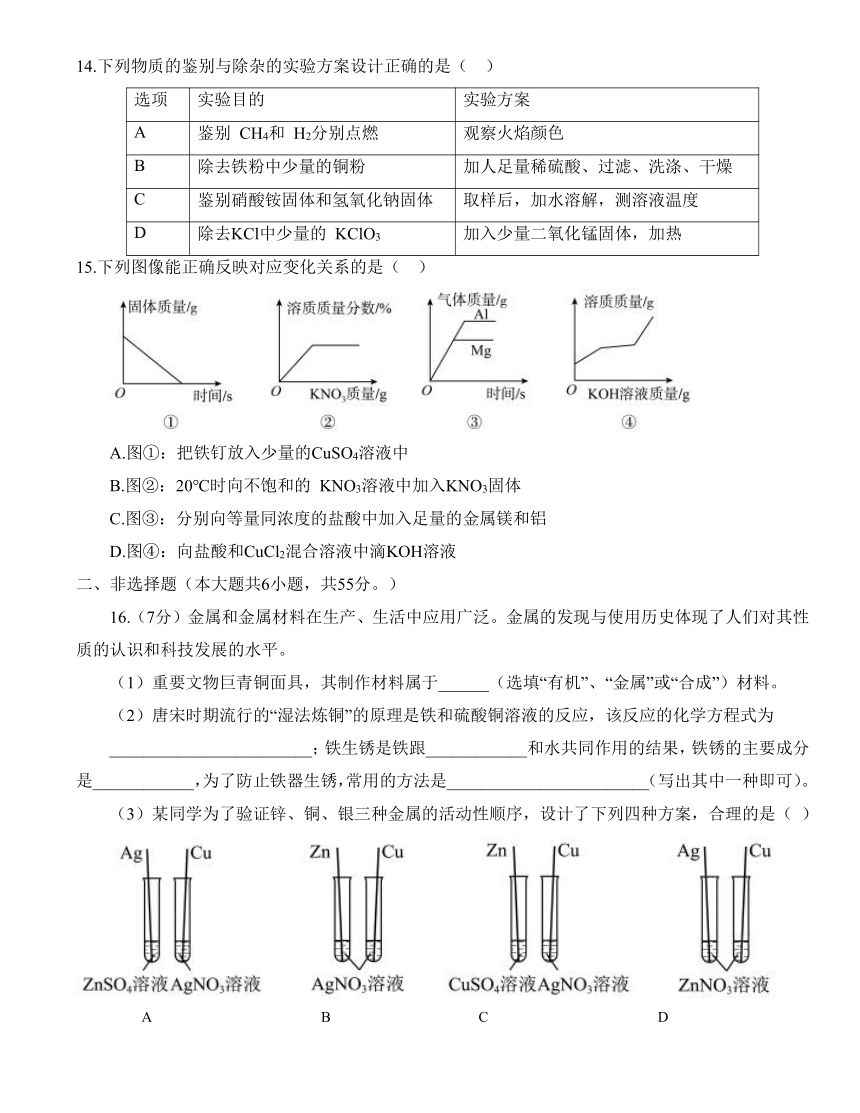
14.下列物质的鉴别与除杂的实验方案设计正确的是( )
选项 实验目的 实验方案
A 鉴别 CH4和 H2分别点燃 观察火焰颜色
B 除去铁粉中少量的铜粉 加人足量稀硫酸、过滤、洗涤、干燥
C 鉴别硝酸铵固体和氢氧化钠固体 取样后,加水溶解,测溶液温度
D 除去KCl中少量的 KClO3 加入少量二氧化锰固体,加热
15.下列图像能正确反映对应变化关系的是( )
A.图①:把铁钉放入少量的CuSO4溶液中
B.图②:20℃时向不饱和的 KNO3溶液中加入KNO3固体
C.图③:分别向等量同浓度的盐酸中加入足量的金属镁和铝
D.图④:向盐酸和CuCl2混合溶液中滴KOH溶液
二、非选择题(本大题共6小题,共55分。)
16.(7分)金属和金属材料在生产、生活中应用广泛。金属的发现与使用历史体现了人们对其性质的认识和科技发展的水平。
(1)重要文物巨青铜面具,其制作材料属于______(选填“有机”、“金属”或“合成”)材料。
(2)唐宋时期流行的“湿法炼铜”的原理是铁和硫酸铜溶液的反应,该反应的化学方程式为
________________________;铁生锈是铁跟____________和水共同作用的结果,铁锈的主要成分是____________,为了防止铁器生锈,常用的方法是________________________(写出其中一种即可)。
(3)某同学为了验证锌、铜、银三种金属的活动性顺序,设计了下列四种方案,合理的是( )
A B C D
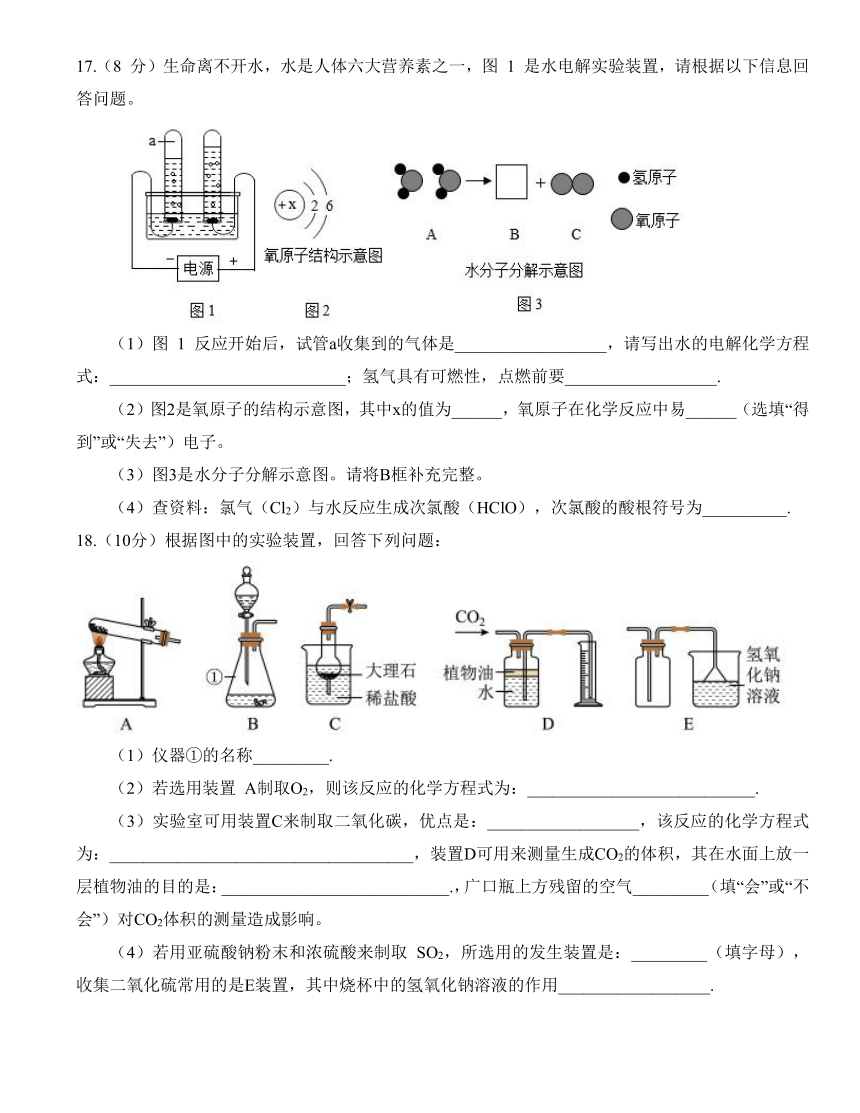
17.(8 分)生命离不开水,水是人体六大营养素之一,图 1 是水电解实验装置,请根据以下信息回答问题。
(1)图 1 反应开始后,试管a收集到的气体是__________________,请写出水的电解化学方程式:____________________________;氢气具有可燃性,点燃前要__________________.
(2)图2是氧原子的结构示意图,其中x的值为______,氧原子在化学反应中易______(选填“得到”或“失去”)电子。
(3)图3是水分子分解示意图。请将B框补充完整。
(4)查资料:氯气(Cl2)与水反应生成次氯酸(HClO),次氯酸的酸根符号为__________.
18.(10分)根据图中的实验装置,回答下列问题:
(1)仪器①的名称_________.
(2)若选用装置 A制取O2,则该反应的化学方程式为:___________________________.
(3)实验室可用装置C来制取二氧化碳,优点是:__________________,该反应的化学方程式为:____________________________________,装置D可用来测量生成CO2的体积,其在水面上放一层植物油的目的是:___________________________.,广口瓶上方残留的空气_________(填“会”或“不会”)对CO2体积的测量造成影响。
(4)若用亚硫酸钠粉末和浓硫酸来制取 SO2,所选用的发生装置是:_________(填字母),收集二氧化硫常用的是E装置,其中烧杯中的氢氧化钠溶液的作用__________________.
19.(10 分)2021 年 3月 20日,三星堆遗址发布最新考古成果,青铜神树、青铜面具等破土而出。化学兴趣小组从生活中的铜制品上提取绿色的铜锈,开启“课外考古”探究。
【查阅资料】
①铜锈俗称铜绿,化学式为Cu2(OH)2CO3,受热易分解;
②无水CuSO4为白色粉末,遇水变蓝;
③碱石灰是 CaO 和 NaOH 的固体混合物,能吸收二氧化碳和水蒸气;
④碳粉不与稀盐酸反应,也不溶于稀盐酸。
【发现问题】
小组同学将少量铜锈放入试管中加热,发现固体由绿色变成黑色。
探究一:生成的黑色固体成分。
【猜想与假设】
猜想一:黑色固体是C粉;猜想二:黑色固体是CuO;猜想三:黑色固体是____________.
【设计方案】
实验操作 实验现象 实验结论
取少量样品于试管中,加人足量稀硫酸 黑色固体溶解________(填“全部”或“部分”),溶液变______色 猜想二正确
探究二:铜锈受热分解还会生成哪些物质。
【进行实验】选择如图所示装置进行验证。
步骤一:连接A和B,打开弹簧夹,通入一段时间的空气;
步骤二:关闭弹簧夹,依次连接装置A→B→__________(选填“C→D”或"D→C");
步骤三:点燃酒精灯,观察到固体由绿色变成⑤色后,停止加热。当观察到无水CuSO4变蓝色,说明铜锈受热分解生成了__________。当观察到装置D中澄清石灰水变__________,则进一步说明铜锈受热分解生成了CO2.
【反思与评价】
(1)装置A的作用是____________________________________.
(2)装置B中发生反应的化学方程式为___________________________.
20.(10 分)我国承诺:2030 年“碳达峰”,2060年“碳中和”,体现大国担当。丁仲礼院士认为“碳中和”是让人为排放的CO2,被人为努力和自然过程所吸收。
图 1
I.碳排放
(1)查阅图 1,动植物呼吸____________(选填“能”或“不能”)释放 CO2。
Ⅱ.碳中和
(2)(2分)自然吸收:查阅图 1,CO2的自然吸收途径有____________(填图中序号)。
(3)人为努力:工业上一种利用NaOH溶液实现“碳捕集”技术的流程如图2所示。
①大气中二氧化碳含量过高时可能会形成________效应。
②反应、分离室中发生的复分解反应的化学方程式为________________________________.
③高温反应室中发生的化学方程式为________________________________,该反应的基本反应类型是________________反应。
④流程中可循环利用的物质有CaO、________.
21.(10分)为测定某黄铜(Cu、Zn合金)中铜的质量分数,某同学取20g黄铜样品放人盛有200g稀硫酸的烧杯中,恰好完全反应(铜与稀硫酸不反应),生成气体的质量与加入稀硫酸的质量关系如图所示(假设生成的气体全部逸出)。试计算:
(1)生成氢气的质量为_________g.(2分)
(2)该黄铜样品中铜的质量分数。(写出计算过程)(6分)
(3)在下列坐标中画出上述反应中生成硫酸锌的变化关系图,要求有图像和坐标值。(2分)
参考答案
一、选择题(本大题共15小题,每小题 3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
C A C B D A D B A C D B A C D
二、非选择题(本大题共6小题,共55分。)
16. (1)金属
(2)Fe+CuSO4=FeSO4+Cu ;氧气;Fe2O3 ;刷漆
(3)C
17. (1)氢气 ; 2H2O2H2+ O2;验纯
(2) 8;得到
(3)
(4)ClO-
18. (1)锥形瓶
(2)2KClO3 KCl+3O2
(3)可随时控制反应的发生与停止 ;CaCO3+2HCl=CaCl2+H2O+CO2
防止二氧化碳溶于水,与水发生反应; 不会
(4)B ;吸收过多的SO2的气体,防止污染空气(或尾气处理等)
19. 【猜想与假设】:C和CuO的混合物
【设计方案】:全部 ;蓝
【进行实验】:C→D ;水; 变浑浊
【反思与评价】:(1)除去空气中的CO2和水蒸气
(2)CO2+Ca(OH)2=CaCO2+H2O
20. (1)能
(2)④⑥
(3)①温室;
②Ca(OH)2+Na2CO3=CaCO3+2NaOH
③CaCO3CaO+ CO2;分解
④NaOH
21. (1)0.2g
(2)解:设黄铜中锌的质量为x.
Zn + H2SO4 = ZnSO4 + H2
65 2
x 0.2g
=
x=6.5g
黄铜样品中铜的质量分数为:
答:黄铜样品中铜的质量分数为67.5%
(3)解:设生成硫酸锌质量为y.
Zn + H2SO4 = ZnSO4 + H2
161 2
y 0.2g
=
y=16.1g
生成硫酸锌的变化关系图如下
可能用到的相对原子质量:H-1 C-12 O-16 N-14 Na-23 Mg-24 Al-27 Cl-35.5
S-32 Fe-56 Zn-65
一、选择题(本大题共15小题,每小题 3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.下列过程属于化学变化的是( )
A.水果榨汁 B.白糖熔化 C.葡萄酿酒 D.丹桂飘香
2.液氮可做制冷剂,它属于( )
A.纯净物 B.混合物 C.氧化物 D.化合物
3.下列实验基本操作中,正确的是( )
A.倾倒液体 B.过滤 C.加热液体 D.熄灭酒精灯
4.下列物质在空气或氧气中燃烧时,现象描述正确的是( )
A.镁条在空气中燃烧,冒出浓烈的白烟,放出热量,生成黑色粉末
B.木炭在氧气中燃烧,发出白光,放出热量,产生能使澄清石灰水变浑浊的气体
C.铁丝在氧气中剧烈燃烧,火星四射,放出热量,生成红色粉末
D.硫在氧气中燃烧,发出微弱的淡蓝色火焰,放出热量,产生没有气味的气体
5.生活中一些物质的pH如下表所示,下列说法中错误的是( )
物质 橘子 西瓜 牙膏 肥皂 草木灰
pH 3~4 5~6 8~9 10 11
A.西瓜汁显酸性 C.草木灰可改良酸性土壤
B.胃酸过多的人不宜吃橘子 D.肥皂水可使紫色石蕊溶液变红
6.下列食物中富含蛋白质的是( )
A.牛肉、鲜奶 B.米饭、红薯 C.土豆 D.苹果
7.2021 年 12 月9日,“天空课堂”在中国空间站精彩开讲。铁酸镍(化学式:NiFe2O4)可以将航天员呼出的废气转化为航天员需要的气体,而本身的质量和化学性质都不变化,NiFe2O4中若铁元素的化合价是+3价,则镍(Ni)元素的化合价是( )
A.-2 B.+4 C.-1 D.+2
8.合理施用化肥,能提高农作物的产量,下列属于复合肥的是( )
A.尿素 B.硝酸钾 C.磷矿粉 D.氯化钾
9.如图所示是某化学反应的微观示意图。下列有关该化学反应的说法正确的是( )
A.化学反应前后原子种类不变 B.该反应是置换反应
C.甲、乙、丙、丁四种物质都是单质 D.反应生成的丙、丁分子个数比为1:1
10.广东地区因气候等原因喜欢饮用凉茶,凉茶具有清热解毒、凉血利咽功效,主要成分是黑芥子甙(C10H17NO9S2),可以预防感冒。下列有关说法正确的是( )
A.黑芥子试中氢、氧、硫元素的质量比为17:9:2
B.黑芥子甙中含有39个原子
C.黑芥子戒中的氮元素的质量分数最小
D.黑芥子甙在氧气中充分燃烧只生成 CO2和 H2O
11.将甲、乙、丙、丁四种物质置于一个完全密闭的容器中,在一定条件下反应,已知反应前后各物质的质量如表所示:下列有关说法正确的是( )
12.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
13.下列各组物质能大量共存,并形成无色溶液的是( )
A.NH4Cl、Na2SO4、HNO3 B.BaCl2、Na2CO3、CuCl2
C.BaCl2、NaHCO3、K2SO4 D.FeCl3、NaOH、NaCl
14.下列物质的鉴别与除杂的实验方案设计正确的是( )
选项 实验目的 实验方案
A 鉴别 CH4和 H2分别点燃 观察火焰颜色
B 除去铁粉中少量的铜粉 加人足量稀硫酸、过滤、洗涤、干燥
C 鉴别硝酸铵固体和氢氧化钠固体 取样后,加水溶解,测溶液温度
D 除去KCl中少量的 KClO3 加入少量二氧化锰固体,加热
15.下列图像能正确反映对应变化关系的是( )
A.图①:把铁钉放入少量的CuSO4溶液中
B.图②:20℃时向不饱和的 KNO3溶液中加入KNO3固体
C.图③:分别向等量同浓度的盐酸中加入足量的金属镁和铝
D.图④:向盐酸和CuCl2混合溶液中滴KOH溶液
二、非选择题(本大题共6小题,共55分。)
16.(7分)金属和金属材料在生产、生活中应用广泛。金属的发现与使用历史体现了人们对其性质的认识和科技发展的水平。
(1)重要文物巨青铜面具,其制作材料属于______(选填“有机”、“金属”或“合成”)材料。
(2)唐宋时期流行的“湿法炼铜”的原理是铁和硫酸铜溶液的反应,该反应的化学方程式为
________________________;铁生锈是铁跟____________和水共同作用的结果,铁锈的主要成分是____________,为了防止铁器生锈,常用的方法是________________________(写出其中一种即可)。
(3)某同学为了验证锌、铜、银三种金属的活动性顺序,设计了下列四种方案,合理的是( )
A B C D
17.(8 分)生命离不开水,水是人体六大营养素之一,图 1 是水电解实验装置,请根据以下信息回答问题。
(1)图 1 反应开始后,试管a收集到的气体是__________________,请写出水的电解化学方程式:____________________________;氢气具有可燃性,点燃前要__________________.
(2)图2是氧原子的结构示意图,其中x的值为______,氧原子在化学反应中易______(选填“得到”或“失去”)电子。
(3)图3是水分子分解示意图。请将B框补充完整。
(4)查资料:氯气(Cl2)与水反应生成次氯酸(HClO),次氯酸的酸根符号为__________.
18.(10分)根据图中的实验装置,回答下列问题:
(1)仪器①的名称_________.
(2)若选用装置 A制取O2,则该反应的化学方程式为:___________________________.
(3)实验室可用装置C来制取二氧化碳,优点是:__________________,该反应的化学方程式为:____________________________________,装置D可用来测量生成CO2的体积,其在水面上放一层植物油的目的是:___________________________.,广口瓶上方残留的空气_________(填“会”或“不会”)对CO2体积的测量造成影响。
(4)若用亚硫酸钠粉末和浓硫酸来制取 SO2,所选用的发生装置是:_________(填字母),收集二氧化硫常用的是E装置,其中烧杯中的氢氧化钠溶液的作用__________________.
19.(10 分)2021 年 3月 20日,三星堆遗址发布最新考古成果,青铜神树、青铜面具等破土而出。化学兴趣小组从生活中的铜制品上提取绿色的铜锈,开启“课外考古”探究。
【查阅资料】
①铜锈俗称铜绿,化学式为Cu2(OH)2CO3,受热易分解;
②无水CuSO4为白色粉末,遇水变蓝;
③碱石灰是 CaO 和 NaOH 的固体混合物,能吸收二氧化碳和水蒸气;
④碳粉不与稀盐酸反应,也不溶于稀盐酸。
【发现问题】
小组同学将少量铜锈放入试管中加热,发现固体由绿色变成黑色。
探究一:生成的黑色固体成分。
【猜想与假设】
猜想一:黑色固体是C粉;猜想二:黑色固体是CuO;猜想三:黑色固体是____________.
【设计方案】
实验操作 实验现象 实验结论
取少量样品于试管中,加人足量稀硫酸 黑色固体溶解________(填“全部”或“部分”),溶液变______色 猜想二正确
探究二:铜锈受热分解还会生成哪些物质。
【进行实验】选择如图所示装置进行验证。
步骤一:连接A和B,打开弹簧夹,通入一段时间的空气;
步骤二:关闭弹簧夹,依次连接装置A→B→__________(选填“C→D”或"D→C");
步骤三:点燃酒精灯,观察到固体由绿色变成⑤色后,停止加热。当观察到无水CuSO4变蓝色,说明铜锈受热分解生成了__________。当观察到装置D中澄清石灰水变__________,则进一步说明铜锈受热分解生成了CO2.
【反思与评价】
(1)装置A的作用是____________________________________.
(2)装置B中发生反应的化学方程式为___________________________.
20.(10 分)我国承诺:2030 年“碳达峰”,2060年“碳中和”,体现大国担当。丁仲礼院士认为“碳中和”是让人为排放的CO2,被人为努力和自然过程所吸收。
图 1
I.碳排放
(1)查阅图 1,动植物呼吸____________(选填“能”或“不能”)释放 CO2。
Ⅱ.碳中和
(2)(2分)自然吸收:查阅图 1,CO2的自然吸收途径有____________(填图中序号)。
(3)人为努力:工业上一种利用NaOH溶液实现“碳捕集”技术的流程如图2所示。
①大气中二氧化碳含量过高时可能会形成________效应。
②反应、分离室中发生的复分解反应的化学方程式为________________________________.
③高温反应室中发生的化学方程式为________________________________,该反应的基本反应类型是________________反应。
④流程中可循环利用的物质有CaO、________.
21.(10分)为测定某黄铜(Cu、Zn合金)中铜的质量分数,某同学取20g黄铜样品放人盛有200g稀硫酸的烧杯中,恰好完全反应(铜与稀硫酸不反应),生成气体的质量与加入稀硫酸的质量关系如图所示(假设生成的气体全部逸出)。试计算:
(1)生成氢气的质量为_________g.(2分)
(2)该黄铜样品中铜的质量分数。(写出计算过程)(6分)
(3)在下列坐标中画出上述反应中生成硫酸锌的变化关系图,要求有图像和坐标值。(2分)
参考答案
一、选择题(本大题共15小题,每小题 3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
C A C B D A D B A C D B A C D
二、非选择题(本大题共6小题,共55分。)
16. (1)金属
(2)Fe+CuSO4=FeSO4+Cu ;氧气;Fe2O3 ;刷漆
(3)C
17. (1)氢气 ; 2H2O2H2+ O2;验纯
(2) 8;得到
(3)
(4)ClO-
18. (1)锥形瓶
(2)2KClO3 KCl+3O2
(3)可随时控制反应的发生与停止 ;CaCO3+2HCl=CaCl2+H2O+CO2
防止二氧化碳溶于水,与水发生反应; 不会
(4)B ;吸收过多的SO2的气体,防止污染空气(或尾气处理等)
19. 【猜想与假设】:C和CuO的混合物
【设计方案】:全部 ;蓝
【进行实验】:C→D ;水; 变浑浊
【反思与评价】:(1)除去空气中的CO2和水蒸气
(2)CO2+Ca(OH)2=CaCO2+H2O
20. (1)能
(2)④⑥
(3)①温室;
②Ca(OH)2+Na2CO3=CaCO3+2NaOH
③CaCO3CaO+ CO2;分解
④NaOH
21. (1)0.2g
(2)解:设黄铜中锌的质量为x.
Zn + H2SO4 = ZnSO4 + H2
65 2
x 0.2g
=
x=6.5g
黄铜样品中铜的质量分数为:
答:黄铜样品中铜的质量分数为67.5%
(3)解:设生成硫酸锌质量为y.
Zn + H2SO4 = ZnSO4 + H2
161 2
y 0.2g
=
y=16.1g
生成硫酸锌的变化关系图如下
同课章节目录
