化学人教版(2019)选择性必修3 1.1.2有机化合物中的共价键(共31张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 1.1.2有机化合物中的共价键(共31张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-28 00:00:00 | ||
图片预览







文档简介
(共31张PPT)
第一节 有机化合物的结构特点
第一章 有机化合物的结构特点与研究方法
第2课时 有机化合物中的共价键
1
认识有机化合物分子结构中碳原子的成键特点、共价键的类型和共价键的极性。
能初步根据有机化合物分子的结构特点对其化学性质和有机 反应规律进行分析预测
2
通过分析共价键的极性对有机化合物性质的影响,深化对“结构决定性质”的理解。
3
一、 有机化合物中的共价键类型
在有机化合物的分子中,碳原子通过共用电子对与其它原子形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大影响。
1.为什么甲烷的空间构型为正四面体,乙烯为平面形,而乙炔为直线形?
2.乙烯、乙炔的化学性质同乙烷相比,存在较大差异的原因?
思考与交流
01
有机化合物中的共价键
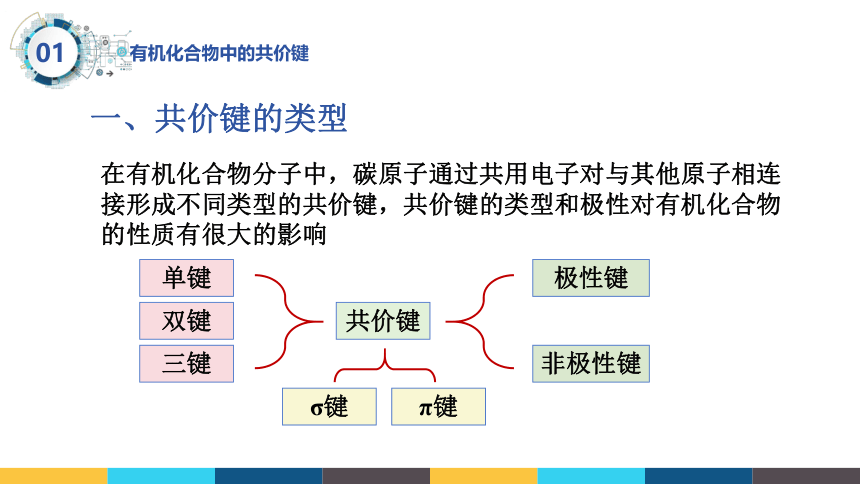
一、共价键的类型
在有机化合物分子中,碳原子通过共用电子对与其他原子相连接形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大的影响
共价键
双键
单键
三键
极性键
非极性键
σ键
π键
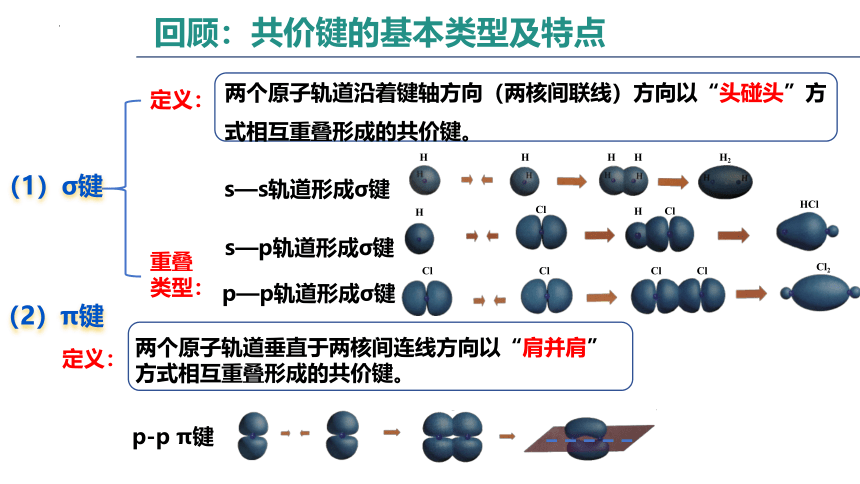
回顾:共价键的基本类型及特点
两个原子轨道沿着键轴方向(两核间联线)方向以“头碰头”方式相互重叠形成的共价键。
重叠类型:
s—s轨道形成σ键
s—p轨道形成σ键
p—p轨道形成σ键
(1)σ键
定义:
H
H
H
H
H2
Cl
H
Cl
H
HCl
Cl
Cl
Cl
Cl
Cl2
(2)π键
定义:
两个原子轨道垂直于两核间连线方向以“肩并肩”方式相互重叠形成的共价键。
p-p π键
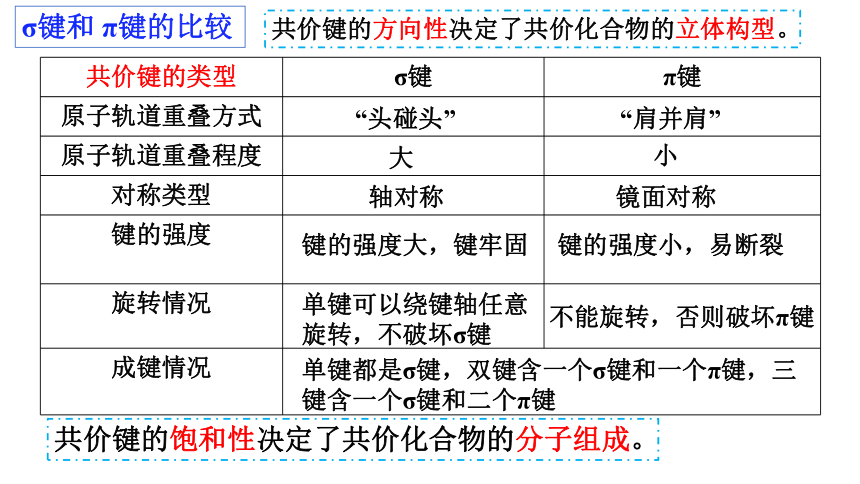
共价键的类型 σ键 π键
原子轨道重叠方式
原子轨道重叠程度
对称类型
键的强度
旋转情况
成键情况 “头碰头”
“肩并肩”
大
小
轴对称
镜面对称
键的强度大,键牢固
键的强度小,易断裂
单键可以绕键轴任意旋转,不破坏σ键
不能旋转,否则破坏π键
单键都是σ键,双键含一个σ键和一个π键,三键含一个σ键和二个π键
σ键和 π键的比较
共价键的饱和性决定了共价化合物的分子组成。
共价键的方向性决定了共价化合物的立体构型。
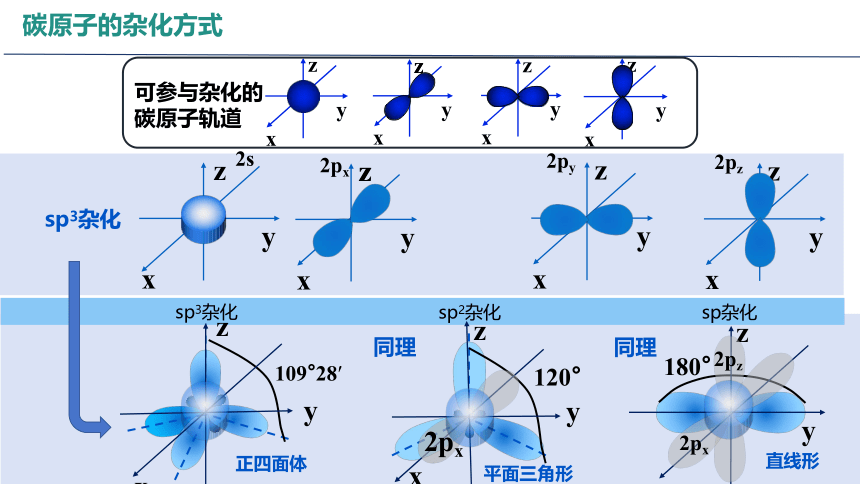
碳原子的杂化方式
sp3杂化
109°28′
x
y
z
正四面体
sp2杂化
120°
x
y
z
2px
平面三角形
sp杂化
180°
x
y
z
直线形
2px
2pz
x
y
z
x
y
z
z
x
y
z
x
y
z
sp3杂化
同理
同理
x
y
z
x
y
z
z
x
y
z
x
y
z
2s
2px
2py
2pz
可参与杂化的
碳原子轨道
3、共价键的极性与有机反应
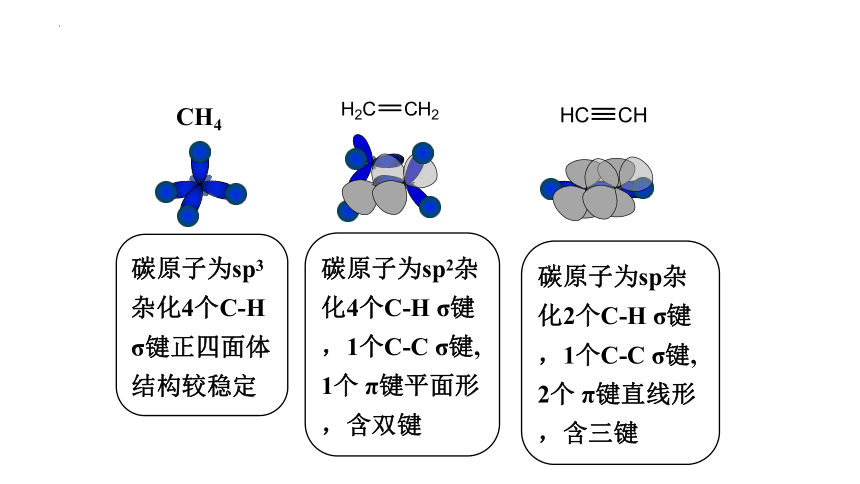
碳原子为sp杂化2个C-H σ键,1个C-C σ键, 2个 π键直线形,含三键
CH4
碳原子为sp3杂化4个C-H σ键正四面体结构较稳定
碳原子为sp2杂化4个C-H σ键,1个C-C σ键, 1个 π键平面形,含双键
02
有机化合物中的共价键
一、σ、π键与有机反应类型
有机物中的π键能发生加成反应,如乙烯和乙炔分子的双键和三键中含有π键,能发生加成反应。
②π键
有机物中的σ键能发生取代反应,如甲烷分子中含有C—H σ键,能发生取代反应。
①σ键
思考与讨论
共价键的类型
有机物中共价键的类型与有机反应类型的关系
单键 双键 三键
1个σ键 1个σ键 1个π键 1个σ键 2个π键
取代反应 加成反应 加成反应
02
有机化合物中的共价键
二、共价键的极性与有机反应
由于不同的成键原子间电负性的差异,共用电子对会发生偏移。
偏移的程度越大,共价键极性越强,在反应中越容易发生断裂。
有机化合物的官能团及其邻位的化学键往往是发生化学反应的活性部位。
【实验1-1】钠与乙醇、水反应的对比
水
乙醇
【实验探究】:
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度 2Na+2H2O=2NaOH + H2↑
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
剧烈程度:H2O>CH3CH2OH
受乙基的影响,乙醇分子中氢氧键的极性比水分子氢氧键的极性弱,乙醇比水更难电离出氢离子
(1) 乙醇与钠反应
2 + 2Na 2 + H2
【问题1】乙醇为什么能和金属钠反应?
乙醇分子中的氢氧键极性较强,能够发生断裂。
水分子结构 乙醇分子结构
共价键的极性与有机反应的关系
【问题2】为什么乙醇与钠反应不如水与钠反应剧烈?
氢氧键的极性:
水 > 乙醇
基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
共价键的断裂需要吸收能量,相对无机反应,有机反应一般速率较小。
乙基
共价键的极性与有机反应的关系
O─H的极性减弱
烃基推电子效应
O─H不易断裂
补充知识:吸电子基团与推电子基团(给电子基团)
键的极性对化学性质的影响
卤素—X(F、CI、Br、I)
如硝基(-NO2)
羧基(-COOH)
醛基(-CHO)
对于一个基团-RX:
(1)如果R的电负性大于X,那么它就是推电子基团(给电子基团)
如烷基(-CH3)
羟基(-OH)
烷氧基(-OCH3)
氨基(-NH2)
(2)如果R的电负性小于X,那么它就是吸电子基团
若分子连有吸电子基团,键的极性越强,越易断裂
物质酸性就越强
如酸性:F-COOH H-COOH
若分子连有推电子基团,键的极性越弱,越不易断裂
(推电子基团越多)物质酸性就越弱
如酸性:H-CH2COOH CH3-CH2COOH
>
>
___________________使得官能团中化学键的______发生变化,从而影响官能团和物质的性质
基团之间的相互影响
极性
推电子基团:—R(烷基)、—OR(烷氧基)、—OH、—NH2
吸电子基团:—X(卤代基)、—NO2(硝基)、—CN、
—CHO、—COOH
三、共价键的极性与有机反应
共价键的极性与有机反应的关系
物质 结构式 与钠反应现象 现象分析
水
乙醇
乙酸
“浮、游、熔、响”
反应剧烈
“沉、气、静”
没有钠与水反应剧烈
水中的O—H极性
较强
乙醇中的O—H极性
比水中的O—H弱
乙酸中的O—H极性比水中的O—H强
“浮、游、熔、响”
比钠与水反应更剧烈
【问题3】推测钠与乙酸溶液反应的现象,并简述理由
O─H的极性增强
羰基吸电子效应
O─H更易断裂
【思考与讨论】
依据上述所讲,分析乙醇与HBr反应
由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,反应中乙醇分子中断裂的键是碳氧单键 。
Δ
+
+
H2O
【任务】分析在这个反应中乙醇的断键位置
有机化合物分子中共价键断裂的位置存在多种可能。
相对无机反应,有机反应一般副反应较多,产物比较复杂。
C2H5OH + HBr C2H5Br + H2O
(2) 乙醇与氢溴酸反应
+ H-Br
+ H2O
课堂练习
1、判断正误(正确的打“√”,错误的打“×”)
(1)有机物分子中均有σ键和π键。( )
(2)含有π键的有机物一般容易发生加成反应。( )
(3)甲烷分子中只有C—H σ键,只能发生取代反应。( )
(4)乙烯分子中含有π键,所以化学性质比甲烷活泼。( )
√
×
×
√
答案
解析
1
2
3
2.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图。下列有关该物质的说法不正确的是( )
A.分子式为C3H4O3
B.分子中σ键与π键个数之比为10∶1
C.分子中既有极性键也有非极性键
D.分子中碳原子的杂化方式全部为sp2杂化
D
答案
解析
1
2
3
3.丙烯颜料是一种非常方便使用的手绘颜料。下列关于丙烯(CH3—CH=CH2)的说法正确的是( )
A.丙烯分子中3个碳原子在同一直线上
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子中不存在非极性键
D.一个丙烯分子中有8个σ键、1个π键
D
答案
解析
1
2
3
4、锅炉水添加剂中某种成分的结构式如下图所示
(1)该物质的分子式为______________。
(2)该分子中的碳原子形成了__________个σ键和__________个π键。
(3)该分子中碳原子的杂化方式为__________ ,─NH2中氮原子的杂化方式为______。
CH6N4O
3
1
sp2
sp3
5.多位化学家用简单的偶联反应合成了如下这个有趣的“纳米小人”分子。有关该分子的结构说法不正确的是( )
A.该分子中的C原子采取的杂化方式有:sp、sp2、sp3
B.该分子中的O原子采取sp3杂化
C.“纳米小人”头部的所有原子不能在同一平面内
D.“纳米小人”手、脚部位的碳原子不杂化
D
有机化合物几种图式的比较
拓 展
空间填充模型
1、写出下列有机物的键线式:
CH3 – CH – C = CH – CHO
OH
CH2CH3
CH3 – CH – C≡C – CH3
CH3
CH3CH2COOH
CH3COOCH2CH3
2、写出下列有机物的结构简式:
Cl
O
O
=
有机物分子组成和结构的表示方法
分子式
最简式
电子式
结构式
结构简式
键线式
碳骨架式
球棍模型
空间填充模型
只表示分子的组成,不能反映物质的结构.
只表示分子的部分组成,不能反映物质的结构.
既能表示分子的组成,
又能反映物质的结构.
但书写麻烦!
既能表示分子的组成,
又能反映物质的结构.
只能表示碳原子的连接方式,不能表示分子组成!
既能表示分子的组成,
又能反映物质的结构.
一般只用于题目分析,正规的书写表达时不用!
小结
常用
第一节 有机化合物的结构特点
第一章 有机化合物的结构特点与研究方法
第2课时 有机化合物中的共价键
1
认识有机化合物分子结构中碳原子的成键特点、共价键的类型和共价键的极性。
能初步根据有机化合物分子的结构特点对其化学性质和有机 反应规律进行分析预测
2
通过分析共价键的极性对有机化合物性质的影响,深化对“结构决定性质”的理解。
3
一、 有机化合物中的共价键类型
在有机化合物的分子中,碳原子通过共用电子对与其它原子形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大影响。
1.为什么甲烷的空间构型为正四面体,乙烯为平面形,而乙炔为直线形?
2.乙烯、乙炔的化学性质同乙烷相比,存在较大差异的原因?
思考与交流
01
有机化合物中的共价键
一、共价键的类型
在有机化合物分子中,碳原子通过共用电子对与其他原子相连接形成不同类型的共价键,共价键的类型和极性对有机化合物的性质有很大的影响
共价键
双键
单键
三键
极性键
非极性键
σ键
π键
回顾:共价键的基本类型及特点
两个原子轨道沿着键轴方向(两核间联线)方向以“头碰头”方式相互重叠形成的共价键。
重叠类型:
s—s轨道形成σ键
s—p轨道形成σ键
p—p轨道形成σ键
(1)σ键
定义:
H
H
H
H
H2
Cl
H
Cl
H
HCl
Cl
Cl
Cl
Cl
Cl2
(2)π键
定义:
两个原子轨道垂直于两核间连线方向以“肩并肩”方式相互重叠形成的共价键。
p-p π键
共价键的类型 σ键 π键
原子轨道重叠方式
原子轨道重叠程度
对称类型
键的强度
旋转情况
成键情况 “头碰头”
“肩并肩”
大
小
轴对称
镜面对称
键的强度大,键牢固
键的强度小,易断裂
单键可以绕键轴任意旋转,不破坏σ键
不能旋转,否则破坏π键
单键都是σ键,双键含一个σ键和一个π键,三键含一个σ键和二个π键
σ键和 π键的比较
共价键的饱和性决定了共价化合物的分子组成。
共价键的方向性决定了共价化合物的立体构型。
碳原子的杂化方式
sp3杂化
109°28′
x
y
z
正四面体
sp2杂化
120°
x
y
z
2px
平面三角形
sp杂化
180°
x
y
z
直线形
2px
2pz
x
y
z
x
y
z
z
x
y
z
x
y
z
sp3杂化
同理
同理
x
y
z
x
y
z
z
x
y
z
x
y
z
2s
2px
2py
2pz
可参与杂化的
碳原子轨道
3、共价键的极性与有机反应
碳原子为sp杂化2个C-H σ键,1个C-C σ键, 2个 π键直线形,含三键
CH4
碳原子为sp3杂化4个C-H σ键正四面体结构较稳定
碳原子为sp2杂化4个C-H σ键,1个C-C σ键, 1个 π键平面形,含双键
02
有机化合物中的共价键
一、σ、π键与有机反应类型
有机物中的π键能发生加成反应,如乙烯和乙炔分子的双键和三键中含有π键,能发生加成反应。
②π键
有机物中的σ键能发生取代反应,如甲烷分子中含有C—H σ键,能发生取代反应。
①σ键
思考与讨论
共价键的类型
有机物中共价键的类型与有机反应类型的关系
单键 双键 三键
1个σ键 1个σ键 1个π键 1个σ键 2个π键
取代反应 加成反应 加成反应
02
有机化合物中的共价键
二、共价键的极性与有机反应
由于不同的成键原子间电负性的差异,共用电子对会发生偏移。
偏移的程度越大,共价键极性越强,在反应中越容易发生断裂。
有机化合物的官能团及其邻位的化学键往往是发生化学反应的活性部位。
【实验1-1】钠与乙醇、水反应的对比
水
乙醇
【实验探究】:
向两只分别盛有蒸馏水和无水乙醇的烧杯中各加入同样大小的钠(约绿豆大),观察现象。
水和钠 无水乙醇和钠
实验原理
实验现象
剧烈程度 2Na+2H2O=2NaOH + H2↑
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
浮、熔、游、响、红
钠沉入底部,有气体产生,最终钠粒消失,液体仍为无色透明。
剧烈程度:H2O>CH3CH2OH
受乙基的影响,乙醇分子中氢氧键的极性比水分子氢氧键的极性弱,乙醇比水更难电离出氢离子
(1) 乙醇与钠反应
2 + 2Na 2 + H2
【问题1】乙醇为什么能和金属钠反应?
乙醇分子中的氢氧键极性较强,能够发生断裂。
水分子结构 乙醇分子结构
共价键的极性与有机反应的关系
【问题2】为什么乙醇与钠反应不如水与钠反应剧烈?
氢氧键的极性:
水 > 乙醇
基团之间的相互影响使官能团中化学键的极性发生变化,从而影响官能团和物质的性质。
共价键的断裂需要吸收能量,相对无机反应,有机反应一般速率较小。
乙基
共价键的极性与有机反应的关系
O─H的极性减弱
烃基推电子效应
O─H不易断裂
补充知识:吸电子基团与推电子基团(给电子基团)
键的极性对化学性质的影响
卤素—X(F、CI、Br、I)
如硝基(-NO2)
羧基(-COOH)
醛基(-CHO)
对于一个基团-RX:
(1)如果R的电负性大于X,那么它就是推电子基团(给电子基团)
如烷基(-CH3)
羟基(-OH)
烷氧基(-OCH3)
氨基(-NH2)
(2)如果R的电负性小于X,那么它就是吸电子基团
若分子连有吸电子基团,键的极性越强,越易断裂
物质酸性就越强
如酸性:F-COOH H-COOH
若分子连有推电子基团,键的极性越弱,越不易断裂
(推电子基团越多)物质酸性就越弱
如酸性:H-CH2COOH CH3-CH2COOH
>
>
___________________使得官能团中化学键的______发生变化,从而影响官能团和物质的性质
基团之间的相互影响
极性
推电子基团:—R(烷基)、—OR(烷氧基)、—OH、—NH2
吸电子基团:—X(卤代基)、—NO2(硝基)、—CN、
—CHO、—COOH
三、共价键的极性与有机反应
共价键的极性与有机反应的关系
物质 结构式 与钠反应现象 现象分析
水
乙醇
乙酸
“浮、游、熔、响”
反应剧烈
“沉、气、静”
没有钠与水反应剧烈
水中的O—H极性
较强
乙醇中的O—H极性
比水中的O—H弱
乙酸中的O—H极性比水中的O—H强
“浮、游、熔、响”
比钠与水反应更剧烈
【问题3】推测钠与乙酸溶液反应的现象,并简述理由
O─H的极性增强
羰基吸电子效应
O─H更易断裂
【思考与讨论】
依据上述所讲,分析乙醇与HBr反应
由于羟基中氧原子的电负性较大,乙醇分子中的碳氧键极性也较强,反应中乙醇分子中断裂的键是碳氧单键 。
Δ
+
+
H2O
【任务】分析在这个反应中乙醇的断键位置
有机化合物分子中共价键断裂的位置存在多种可能。
相对无机反应,有机反应一般副反应较多,产物比较复杂。
C2H5OH + HBr C2H5Br + H2O
(2) 乙醇与氢溴酸反应
+ H-Br
+ H2O
课堂练习
1、判断正误(正确的打“√”,错误的打“×”)
(1)有机物分子中均有σ键和π键。( )
(2)含有π键的有机物一般容易发生加成反应。( )
(3)甲烷分子中只有C—H σ键,只能发生取代反应。( )
(4)乙烯分子中含有π键,所以化学性质比甲烷活泼。( )
√
×
×
√
答案
解析
1
2
3
2.碳酸亚乙酯是锂离子电池低温电解液的重要添加剂,其结构如图。下列有关该物质的说法不正确的是( )
A.分子式为C3H4O3
B.分子中σ键与π键个数之比为10∶1
C.分子中既有极性键也有非极性键
D.分子中碳原子的杂化方式全部为sp2杂化
D
答案
解析
1
2
3
3.丙烯颜料是一种非常方便使用的手绘颜料。下列关于丙烯(CH3—CH=CH2)的说法正确的是( )
A.丙烯分子中3个碳原子在同一直线上
B.丙烯分子中3个碳原子都是sp3杂化
C.丙烯分子中不存在非极性键
D.一个丙烯分子中有8个σ键、1个π键
D
答案
解析
1
2
3
4、锅炉水添加剂中某种成分的结构式如下图所示
(1)该物质的分子式为______________。
(2)该分子中的碳原子形成了__________个σ键和__________个π键。
(3)该分子中碳原子的杂化方式为__________ ,─NH2中氮原子的杂化方式为______。
CH6N4O
3
1
sp2
sp3
5.多位化学家用简单的偶联反应合成了如下这个有趣的“纳米小人”分子。有关该分子的结构说法不正确的是( )
A.该分子中的C原子采取的杂化方式有:sp、sp2、sp3
B.该分子中的O原子采取sp3杂化
C.“纳米小人”头部的所有原子不能在同一平面内
D.“纳米小人”手、脚部位的碳原子不杂化
D
有机化合物几种图式的比较
拓 展
空间填充模型
1、写出下列有机物的键线式:
CH3 – CH – C = CH – CHO
OH
CH2CH3
CH3 – CH – C≡C – CH3
CH3
CH3CH2COOH
CH3COOCH2CH3
2、写出下列有机物的结构简式:
Cl
O
O
=
有机物分子组成和结构的表示方法
分子式
最简式
电子式
结构式
结构简式
键线式
碳骨架式
球棍模型
空间填充模型
只表示分子的组成,不能反映物质的结构.
只表示分子的部分组成,不能反映物质的结构.
既能表示分子的组成,
又能反映物质的结构.
但书写麻烦!
既能表示分子的组成,
又能反映物质的结构.
只能表示碳原子的连接方式,不能表示分子组成!
既能表示分子的组成,
又能反映物质的结构.
一般只用于题目分析,正规的书写表达时不用!
小结
常用
