人教版九年级化学上册第三单元物质构成的奥秘单元复习题(含解析)
文档属性
| 名称 | 人教版九年级化学上册第三单元物质构成的奥秘单元复习题(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 65.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-28 00:00:00 | ||
图片预览




文档简介
人教版九年级化学上册第三单元物质构成的奥秘单元复习题
一、单选题
1.据报道广东紫金县违规排污事件造成的铅(Pb)污染已导致45人血铅超标。则“Pb”不能表示( )
A.铅元素 B.金属铅 C.一个铅分子 D.一个铅原子
2.缺钙会发生骨质疏松,这里“钙”指的是( )
A.元素 B.原子 C.单质 D.分子
3.下列事实与相应的解释不一致的是( )
选项 事实 解释
A 50mL水和50mL酒精混合后的体积小于100mL 分子间有间隔
B 氧气和臭氧(O3)性质不完全相同 组成物质的元素不同
C 稀有气体的化学性质稳定 原子的最外层电子达到稳定结构
D 铜块在空气中不燃烧,镁条在空气中能燃烧 物质的种类决定反应能否进行
A.A B.B C.C D.D
4.青少年正处于身高猛增时期,这时要多补钙,这里的“钙”是指( )
A.钙原子 B.钙离子 C.钙元素 D.金属钙
5.不同种元素间最本质的区别是( )
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
6.如图是五种微粒的结构示意图,下列说法正确的是( )
A.①④属于金属元素 B.②的微粒符号是Al3+
C.②③⑤属于阳离子 D.②③属于同种元素
7.下列物质由离子构成的是( )
A.铁 B.水 C.氨气 D.氯化钠
8.干冰升华过程中发生改变的是( )
A.分子种类 B.分子间隔 C.分子数目 D.分子大小
9.用微粒观点对下列事例解释不正确的是( )
A.两个表面光滑的铅块相互压紧后会粘在一起——分子间有引力
B.过氧化氢的化学性质——由氢分子和氧分子保持
C.“飞沫”传播新冠病毒——分子在不断运动
D.空气压缩为液态空气——分子间间隔变小
10.从分子角度分析,对下列现象或操作解释不正确的是( )
事 实 解 释
A 某同学将洗好的校服晾晒在阳台上,第二天校服就干了 分子在不断地运动
B H2O和H2O2的化学性质不同 构成物质的分子种类不同
C 电解水得到氢气和氧气 化学变化中,分子可以再分
D 温度计中的酒精热胀冷缩 分子的体积随温度改变而改变
A.A B.B C.C D.D
11.下列对于分子、原子、离子的认识中,正确的是( )
A.原子是一切变化中的最小粒子,不可再分
B.化学变化中分子不改变
C.在含有多个电子的原子里,电子是分层排布的
D.钠原子和钠离子的化学性质相同
12.银是导电性最好的一种金属。下图是银在元素周期表中的信息,有关银元素说法错误的是( )
A.属于非金属元素 B.一个银原子核外有47个电子
C.相对原子质量为107.9 D.原子序数是47
二、非选择题
13.阅读下列短文并回答问题。
臭氧是氧气的“亲兄弟”。在紫外线照射下,一个氧分子可分解为两个氧原子,其中一个氧原子和其余的氧分子再次结合成臭氧分子。近地面的空气若含有较高浓度的臭氧会危害人体健康。目前臭氧已成为仅次于PM2.5的影响现代城市空气质量的重要因素。
某兴趣小组选择2间同样大小的教室,研究紫外线消毒教室时室内臭氧含量变化情况。1号教室为水泥大理石地面,无桌椅;2号教室为PVC地胶地面,有24套塑料桌椅。两室实验同时进行:先开紫外线灯对室内空气进行照射,每半小时测一次臭氧浓度,5.5小时后关紫外线灯,开门窗通风,每5分钟测一次臭氧浓度,得“臭氧浓度-时间”图如下。
(1)下列物质,不属于空气污染物的是___________。(填编号)
A.氧气 B.臭氧 C.PM2.5 D.稀有气体
E.二氧化氮
(2)如图是氧原子的结构示意图,图中a= 。反应中氧原子倾向于 (填“失去”或“得到”)电子形成相对稳定结构。
(3)臭氧的相对分子质量为 。1个臭氧分子和1个氧分子的质量比为 。请用化学方程式表示上文中发生的化学反应: 。
(4)对比分析实验结果,能得到的研究结论是 。
14.在“宏观一微观一符号”之间建立联系,是化学特有的思维方式。
(1)下图是四种粒子结构示意图.
①中的x= ,C粒子的符号为 。
②A,B,C,D中属于同种元素的粒子是 (填序号)。
③A和B两种粒子的 相同,所以它们具有相似的化学性质。
④具有相对稳定结构的粒子是 。
(2)用化学符号填空:
①2个镁原子 ② 2个氢分子 ③3个亚铁离子
④+5价的氮元素 ⑤氧化铝
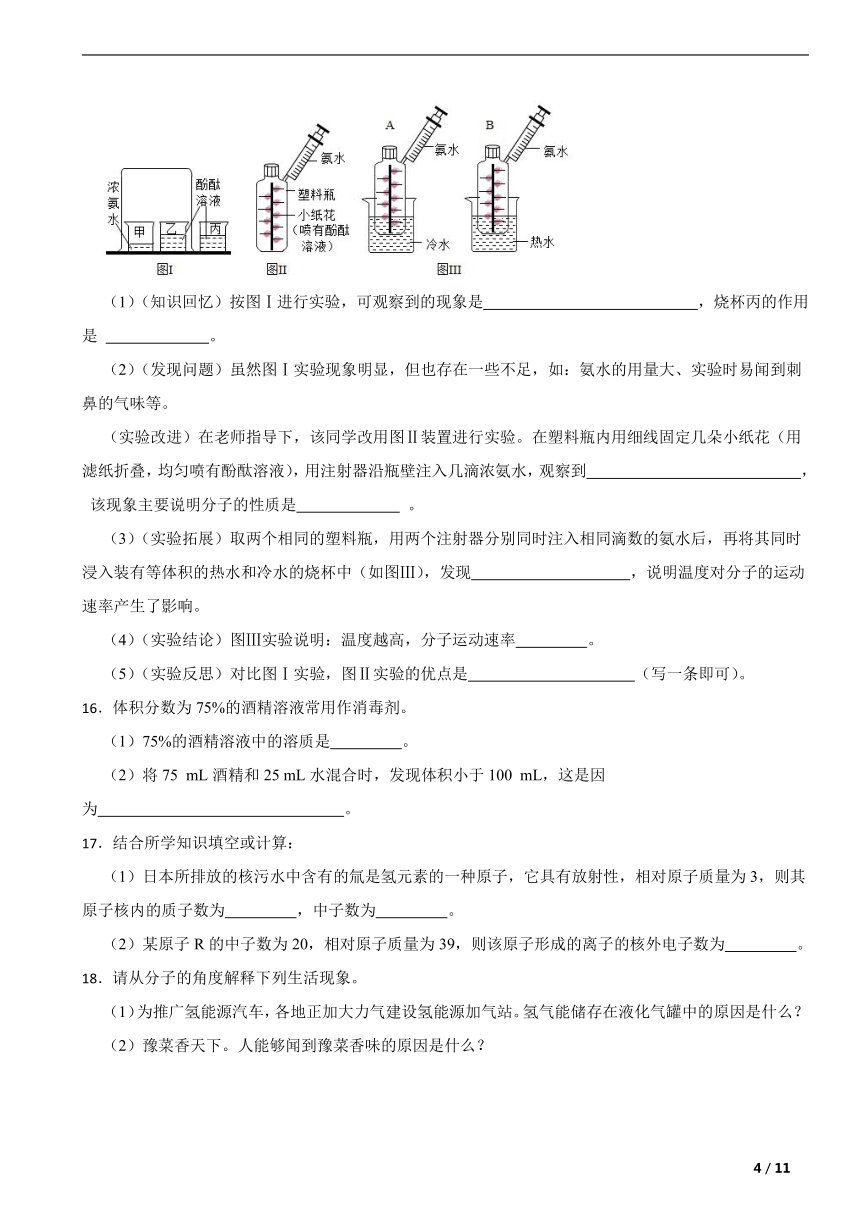
15.某同学设计如图实验装置探究“分子的性质”。
(1)(知识回忆)按图Ⅰ进行实验,可观察到的现象是 ,烧杯丙的作用是 。
(2)(发现问题)虽然图Ⅰ实验现象明显,但也存在一些不足,如:氨水的用量大、实验时易闻到刺鼻的气味等。
(实验改进)在老师指导下,该同学改用图Ⅱ装置进行实验。在塑料瓶内用细线固定几朵小纸花(用滤纸折叠,均匀喷有酚酞溶液),用注射器沿瓶壁注入几滴浓氨水,观察到 ,
该现象主要说明分子的性质是 。
(3)(实验拓展)取两个相同的塑料瓶,用两个注射器分别同时注入相同滴数的氨水后,再将其同时浸入装有等体积的热水和冷水的烧杯中(如图Ⅲ),发现 ,说明温度对分子的运动速率产生了影响。
(4)(实验结论)图Ⅲ实验说明:温度越高,分子运动速率 。
(5)(实验反思)对比图Ⅰ实验,图Ⅱ实验的优点是 (写一条即可)。
16.体积分数为75%的酒精溶液常用作消毒剂。
(1)75%的酒精溶液中的溶质是 。
(2)将75
mL酒精和25 mL水混合时,发现体积小于100
mL,这是因为 。
17.结合所学知识填空或计算:
(1)日本所排放的核污水中含有的氚是氢元素的一种原子,它具有放射性,相对原子质量为3,则其原子核内的质子数为 ,中子数为 。
(2)某原子R的中子数为20,相对原子质量为39,则该原子形成的离子的核外电子数为 。
18.请从分子的角度解释下列生活现象。
(1)为推广氢能源汽车,各地正加大力气建设氢能源加气站。氢气能储存在液化气罐中的原因是什么?
(2)豫菜香天下。人能够闻到豫菜香味的原因是什么?
答案解析部分
1.【答案】C
【解析】【解答】A. 铅是金属单质,符号“Pb”表示铅元素,故A不符合题意;
B. 符号“Pb”表示金属铅,故B不符合题意;
C. 符号“Pb”表示一个铅原子,故C符合题意;
D. 符号“Pb”表示一个铅原子,故D不符合题意。
故答案为:C。
【分析】元素符号,在宏观上表示一种元素,在微观上,表示一个该原子。
2.【答案】A
【解析】【解答】物质中的“钙”等不能以单质、分子、原子形式存在,而是指元素。通常用元素及其所占质量(质量分数)来描述的。
故答案为:A。
【分析】宏观上,元素组成物质。
3.【答案】B
【解析】【解答】A、50mL水和50mL酒精混合后的体积小于100mL,是因为分子间有间隔,A符合题意;
B决定物质性质的是组成和结构,氧气和臭氧(O3)性质不完全相同,是因为其组成物质的元素相同,但分子的构成不同,B符合题意;
C稀有气体的化学性质稳定,原子的最外层电子达到稳定结构,不易得失电子,不易发生化学变化,C不符合题意;
D铜块在空气中不燃烧,镁条在空气中能燃烧,是因为物质的种类决定决定其化学性质(金属活动性),种类不同,活动性不同,与氧气反应时的难易程度不同。
故答案为:B。
【分析】微粒的性质:1、存在空隙,2、在运动、3、比较小;物质的性质由结构决定。性质决定用途。
4.【答案】C
【解析】【解答】青少年正处于生长发育期,应在医生指导下适当补钙,这里的“钙”指的是不是以单质、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关。
故答案为:C。
【分析】宏观上,元素组成物质。
5.【答案】A
【解析】【解答】不同种元素的本质区别是质子数不同。
故答案为:A。
【分析】根据元素的种类由质子数决定分析。
6.【答案】B
【解析】【解答】A、金属元素的原子最外层电子数一般少于4个, ①的原子 最外层电子数为7,属于非金属元素,故A错误;
B、 ②的微粒核内质子数是13,核外电子总数为2+8=10,说明失去了最外层的3个电子,质子数>核外电子数,形成了阳离子,其离子符号为 Al3+ ,故B正确;
C、 ②③ 微粒的核内质子数>核外电子数,属于阳离子, ⑤ 微粒的核内质子数=核外电子数,属于原子,故C错误;
D、元素的种类由核内质子数决定,圆圈里面的数字表示核内质子数, ②的核内质子数是13,③的核内质子数是12,两者核内质子数不相等,属于不同种类的元素,故D错误;
故答案为:B.
【分析】A、根据金属元素最外层电子数一般少于4个进行分析解答;
B、根据原子失去电子形成阳离子进行分析解答;
C、根据阳离子核内质子数>核外电子数进行分析解答;
D、根据元素种类由核内质子数决定分析解答。
7.【答案】D
【解析】【解答】A、铁由铁原子构成,不符合题意;
B、水由水分子构成,不符合题意;
C、氨气由氨分子构成,不符合题意;
D、氯化钠由钠离子和氯离子构成,符合题意。
故答案为:D。
【分析】根据盐类物质由离子构成,金属类由原子构成,水、氨气等由分子构成分析。
8.【答案】B
【解析】【解答】干冰升华是干冰由固态直接变为气态,没有新物质生成,是物理变化,在物理变化过程中分子种类、分子数目和分子大小都是不变的。气态物质的分子间间隔比固态和液态的都大,所以干冰升华只是分子间间隔变大了,
故答案为:B。
【分析】根据分子间有间隔,进行分析。
9.【答案】B
【解析】【解答】A、两个表面光滑的铅块相互压紧后会粘在一起,是因为分子间有引力,不符合题意;
B、过氧化氢是由过氧化氢分子构成的,其化学性质由过氧化氢分子保持,符合题意;
C、“飞沫”传播新冠病毒,是因为分子是在不断的运动的,不符合题意;
D、空气压缩为液态空气,是因为分子间有间隔,气体受压后,分子间的间隔变小,不符合题意。
故答案为:B。
【分析】A、根据分子的特性进行分析:分子的质量和体积都很小,分子是不断运动的,分子之间有间隔。
10.【答案】D
【解析】【解答】解:A、某同学将洗好的校服晾晒在阳台上,第二天校服就干了,是因为水分子是在不断的运动的,运动到空气中去了,故选项解释正确.
B、H2O和H2O2的化学性质不同,是因为它们分子的构成不同,不同种的分子性质不同,故选项解释正确.
C、电解水得到氢气和氧气,是因为水分子分裂成了氢原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子,大量的氢分子、氧分子分别聚集成氢气、氧气,该事实说明分子是可以再分的,故选项解释正确.
D、温度计中的酒精热胀冷缩,是因为分子的间隔随温度改变而改变,故选项解释错误.
故选:D.
【分析】根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
11.【答案】C
【解析】【解答】A、原子是化学变化中的最小微粒,不再化学变化中,可以再分,故不符合题意;
B、化学变化中分子一定改变,原子不变,故不符合题意;
C、在含有多个电子的原子里,电子是分层排布的,故符合题意;
D、钠原子最外层有1个电子,很活泼,钠离子最外层有8个电子,比较稳定;钠原子和钠离子的化学性质不相同,故不符合题意。
故答案为:C。
【分析】A、根据原子的概念分析
B、根据化学变化中分子分裂成原子分析
C、根据核外电子的排布方式分析
D、根据决定元素化学性质的是最外层电子数分析
12.【答案】A
【解析】【解答】A、该元素的名称是银,带“钅”字旁,属于金属元素,故A符合题意;
B、在原子中,原子序数=核外电子数,左上角的数字为47,该元素的原子序数为47,一个银原子核外有47个电子,故B不符合题意;
C、汉字下面的数字表示相对原子质量,该元素的相对原子质量为107.9,相对原子质量单位是“1”,不是“克”,故C不符合题意;
D、左上角的数字为47,该元素的原子序数为47,故D不符合题意。
故答案为:A。
【分析】根据元素周期表一格的信息进行分析
13.【答案】(1)A;D
(2)6;得到
(3)48;3:2;
(4)相同条件下,在紫外线照射下,塑料越多,产生的臭氧越多
【解析】【解答】(1)A、氧气是空气的主要成分,不属于空气污染物,故正确;
B、臭氧属于空气污染物,故不正确;
C、PM2.5是可吸入颗粒物,属于空气污染物,故不正确;
D、稀有气体是空气的成分,不属于空气污染物,故正确;
E、二氧化氮属于空气污染物,故不正确;
故答案为:AD;
(2)核内质子数等于核外电子数,属于原子,氧原子的结构示意图,图中a=8-2=6,氧原子最外层有6个电子,大于4,容易得到2个电子,形成相对稳定结构;
(3)臭氧的相对分子质量为16×3=48,1个臭氧分子和1个氧分子的质量比为(16×3):(16×2)=3:2,氧气在紫外线照射的条件下生成臭氧,反应的化学方程式为: ;
(4)对比分析实验结果,能得到的研究结论是相同条件下,在紫外线照射下,塑料越多,产生的臭氧越多。
【分析】(1)根据大气成分不污染空气进行分析
(2)根据最外层电子数大于4得到电子进行分析
(3)根据相对分子质量的计算方法及方程式的书写方法进行分析
14.【答案】(1)8;Cl-;B和C;最外层电子数;CD
(2)2Mg;2H2;3Fe2+;;Al2O3
【解析】【解答】(1)①根据图示可知,在原子中,质子数=核外电子数,则18=2+8+x,x=8;C粒子质子数=17,核外电子数=18,质子数<核外电子数,为带1个单位负电荷的氯离子,其离子符号为:Cl-;②元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,B、C的质子数相同,属于同种元素;③元素的化学性质主要由原子的最外层电子数决定,A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质;
④最外层电子数为8(只有一层电子数为2)是稳定的结构,所以具有相对稳定结构的粒子是C、D;(2)①原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,在其元素符号前加上相应的数字。所以2个镁原子,就可表示为2Mg;②分子的表示方法是正确书写物质的化学式,表示多个该分子,在其化学式前加上相应的数字,因此2个氢分子表示为:2H2;③离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,3个亚铁离子可表示为:3Fe2+;④化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故+5价的氮元素可表示为: ;⑤在氧化铝中氧元素显-2价,铝元素显+3价,根据化合物中各元素的化合价的代数和为零,氧化铝的化学式是Al2O3。
【分析】(1)在原子结构示意图中,原子序数=核内质子数=核外电子数;当最外层电子数为8时达到稳定结构;原子的化学性质主要取决于原子的最外层电子数。
(2)离子表示方法:在表示该离子的元素符号右上角,标出该离子所带正负电荷数,数字在前,正负号在后,带一个电荷时,1要省略。若表示几个离子,在离子前面加上数字。
化合价表示方法:写出物质的化学式,计算要求元素的化合价,在化学式中该元素正上面写上数字和正负号,正负号在前,数字在后。
分子式表示方法:写出分子的化学式,有几个分子就在化学式前面写上相应的数字。
原子表示方法:用元素符号表示,表示多和该原子,在元素符号前面写上相应的数字。
15.【答案】(1)乙中的酚酞溶液逐渐变红;对照实验
(2)小纸花至下而上慢慢变红;不断运动
(3)B中小纸花先变红
(4)越快
(5)节约药品或更环保
【解析】【解答】知识回忆:按图Ⅰ进行实验,氨水显碱性,能使无色酚酞变红,可观察到的现象是乙中的酚酞溶液逐渐变红,烧杯丙的作用是与图甲形成对比,做对照实验;
实验改进:用注射器沿瓶壁注入几滴浓氨水,观察到小纸花至下而上慢慢变红,该现象主要说明分子的性质是分子在不断运动;
实验拓展:温度越高,分子运动速率越快,B中小纸花先变红,说明温度对分子的运动速率产生了影响;
实验结论:图Ⅲ实验说明:温度越高,分子运动速率越快;
实验反思:对比图Ⅰ实验,图Ⅱ实验的优点是节约药品或更环保。
【分析】(1)根据对比实验的相关知识进行分析
(2)根据氨气的密度比空气小分析
(3)根据温度越高分子运动越快分析
(4)根据装置的特点进行分析
16.【答案】(1)酒精
(2)水分子、酒精分子之间有间隔
【解析】【解答】(1)75%的酒精溶液中,溶剂是水,溶质是酒精;(2)将75 mL酒精和25 mL水混合时,发现体积小于100 mL,这是因为水分子、酒精分子之间有间隔,混合后总体积变小;
【分析】(1)根据只要有水的溶液溶剂都是水分析;
(2)根据分子间存在间隔分析。
17.【答案】(1)1;2
(2)18
【解析】【解答】(1)氚是氢元素的一种原子,其原子核内的质子数为1;中子数=相对原子质量-质子数=3-1=2;
(2)某原子R的中子数为20,相对原子质量为39,相对原子质量=质子数+中子数,该原子的质子数=39-20=19,原子里核内质子数等于核外电子数,其核外电子数为19,最外层电子数为1,容易失去电子形成的离子,该原子形成的离子的核外电子数为18。
【分析】(1)根据相对原子质量等于质子数加中子数分析;
(2)根据相对原子质量等于质子数加中子数,原子里核内质子数等于核外电子数,可分析该原子的核外电子数为19,形成的离子核外电子数为18。
18.【答案】(1)分子之间存在间隔,受压后,分子之间的间隔变小
(2)分子在不断运动
【解析】【解答】(1)分子之间存在间隔,受压后,分子之间的间隔变小,故氢气能储存在液化气罐中;
(2)人能够闻到豫菜香味的原因是分子在不断运动,引起香味的分子四处扩散。
【分析】根据分子的基本性质分析。
1 / 1
一、单选题
1.据报道广东紫金县违规排污事件造成的铅(Pb)污染已导致45人血铅超标。则“Pb”不能表示( )
A.铅元素 B.金属铅 C.一个铅分子 D.一个铅原子
2.缺钙会发生骨质疏松,这里“钙”指的是( )
A.元素 B.原子 C.单质 D.分子
3.下列事实与相应的解释不一致的是( )
选项 事实 解释
A 50mL水和50mL酒精混合后的体积小于100mL 分子间有间隔
B 氧气和臭氧(O3)性质不完全相同 组成物质的元素不同
C 稀有气体的化学性质稳定 原子的最外层电子达到稳定结构
D 铜块在空气中不燃烧,镁条在空气中能燃烧 物质的种类决定反应能否进行
A.A B.B C.C D.D
4.青少年正处于身高猛增时期,这时要多补钙,这里的“钙”是指( )
A.钙原子 B.钙离子 C.钙元素 D.金属钙
5.不同种元素间最本质的区别是( )
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
6.如图是五种微粒的结构示意图,下列说法正确的是( )
A.①④属于金属元素 B.②的微粒符号是Al3+
C.②③⑤属于阳离子 D.②③属于同种元素
7.下列物质由离子构成的是( )
A.铁 B.水 C.氨气 D.氯化钠
8.干冰升华过程中发生改变的是( )
A.分子种类 B.分子间隔 C.分子数目 D.分子大小
9.用微粒观点对下列事例解释不正确的是( )
A.两个表面光滑的铅块相互压紧后会粘在一起——分子间有引力
B.过氧化氢的化学性质——由氢分子和氧分子保持
C.“飞沫”传播新冠病毒——分子在不断运动
D.空气压缩为液态空气——分子间间隔变小
10.从分子角度分析,对下列现象或操作解释不正确的是( )
事 实 解 释
A 某同学将洗好的校服晾晒在阳台上,第二天校服就干了 分子在不断地运动
B H2O和H2O2的化学性质不同 构成物质的分子种类不同
C 电解水得到氢气和氧气 化学变化中,分子可以再分
D 温度计中的酒精热胀冷缩 分子的体积随温度改变而改变
A.A B.B C.C D.D
11.下列对于分子、原子、离子的认识中,正确的是( )
A.原子是一切变化中的最小粒子,不可再分
B.化学变化中分子不改变
C.在含有多个电子的原子里,电子是分层排布的
D.钠原子和钠离子的化学性质相同
12.银是导电性最好的一种金属。下图是银在元素周期表中的信息,有关银元素说法错误的是( )
A.属于非金属元素 B.一个银原子核外有47个电子
C.相对原子质量为107.9 D.原子序数是47
二、非选择题
13.阅读下列短文并回答问题。
臭氧是氧气的“亲兄弟”。在紫外线照射下,一个氧分子可分解为两个氧原子,其中一个氧原子和其余的氧分子再次结合成臭氧分子。近地面的空气若含有较高浓度的臭氧会危害人体健康。目前臭氧已成为仅次于PM2.5的影响现代城市空气质量的重要因素。
某兴趣小组选择2间同样大小的教室,研究紫外线消毒教室时室内臭氧含量变化情况。1号教室为水泥大理石地面,无桌椅;2号教室为PVC地胶地面,有24套塑料桌椅。两室实验同时进行:先开紫外线灯对室内空气进行照射,每半小时测一次臭氧浓度,5.5小时后关紫外线灯,开门窗通风,每5分钟测一次臭氧浓度,得“臭氧浓度-时间”图如下。
(1)下列物质,不属于空气污染物的是___________。(填编号)
A.氧气 B.臭氧 C.PM2.5 D.稀有气体
E.二氧化氮
(2)如图是氧原子的结构示意图,图中a= 。反应中氧原子倾向于 (填“失去”或“得到”)电子形成相对稳定结构。
(3)臭氧的相对分子质量为 。1个臭氧分子和1个氧分子的质量比为 。请用化学方程式表示上文中发生的化学反应: 。
(4)对比分析实验结果,能得到的研究结论是 。
14.在“宏观一微观一符号”之间建立联系,是化学特有的思维方式。
(1)下图是四种粒子结构示意图.
①中的x= ,C粒子的符号为 。
②A,B,C,D中属于同种元素的粒子是 (填序号)。
③A和B两种粒子的 相同,所以它们具有相似的化学性质。
④具有相对稳定结构的粒子是 。
(2)用化学符号填空:
①2个镁原子 ② 2个氢分子 ③3个亚铁离子
④+5价的氮元素 ⑤氧化铝
15.某同学设计如图实验装置探究“分子的性质”。
(1)(知识回忆)按图Ⅰ进行实验,可观察到的现象是 ,烧杯丙的作用是 。
(2)(发现问题)虽然图Ⅰ实验现象明显,但也存在一些不足,如:氨水的用量大、实验时易闻到刺鼻的气味等。
(实验改进)在老师指导下,该同学改用图Ⅱ装置进行实验。在塑料瓶内用细线固定几朵小纸花(用滤纸折叠,均匀喷有酚酞溶液),用注射器沿瓶壁注入几滴浓氨水,观察到 ,
该现象主要说明分子的性质是 。
(3)(实验拓展)取两个相同的塑料瓶,用两个注射器分别同时注入相同滴数的氨水后,再将其同时浸入装有等体积的热水和冷水的烧杯中(如图Ⅲ),发现 ,说明温度对分子的运动速率产生了影响。
(4)(实验结论)图Ⅲ实验说明:温度越高,分子运动速率 。
(5)(实验反思)对比图Ⅰ实验,图Ⅱ实验的优点是 (写一条即可)。
16.体积分数为75%的酒精溶液常用作消毒剂。
(1)75%的酒精溶液中的溶质是 。
(2)将75
mL酒精和25 mL水混合时,发现体积小于100
mL,这是因为 。
17.结合所学知识填空或计算:
(1)日本所排放的核污水中含有的氚是氢元素的一种原子,它具有放射性,相对原子质量为3,则其原子核内的质子数为 ,中子数为 。
(2)某原子R的中子数为20,相对原子质量为39,则该原子形成的离子的核外电子数为 。
18.请从分子的角度解释下列生活现象。
(1)为推广氢能源汽车,各地正加大力气建设氢能源加气站。氢气能储存在液化气罐中的原因是什么?
(2)豫菜香天下。人能够闻到豫菜香味的原因是什么?
答案解析部分
1.【答案】C
【解析】【解答】A. 铅是金属单质,符号“Pb”表示铅元素,故A不符合题意;
B. 符号“Pb”表示金属铅,故B不符合题意;
C. 符号“Pb”表示一个铅原子,故C符合题意;
D. 符号“Pb”表示一个铅原子,故D不符合题意。
故答案为:C。
【分析】元素符号,在宏观上表示一种元素,在微观上,表示一个该原子。
2.【答案】A
【解析】【解答】物质中的“钙”等不能以单质、分子、原子形式存在,而是指元素。通常用元素及其所占质量(质量分数)来描述的。
故答案为:A。
【分析】宏观上,元素组成物质。
3.【答案】B
【解析】【解答】A、50mL水和50mL酒精混合后的体积小于100mL,是因为分子间有间隔,A符合题意;
B决定物质性质的是组成和结构,氧气和臭氧(O3)性质不完全相同,是因为其组成物质的元素相同,但分子的构成不同,B符合题意;
C稀有气体的化学性质稳定,原子的最外层电子达到稳定结构,不易得失电子,不易发生化学变化,C不符合题意;
D铜块在空气中不燃烧,镁条在空气中能燃烧,是因为物质的种类决定决定其化学性质(金属活动性),种类不同,活动性不同,与氧气反应时的难易程度不同。
故答案为:B。
【分析】微粒的性质:1、存在空隙,2、在运动、3、比较小;物质的性质由结构决定。性质决定用途。
4.【答案】C
【解析】【解答】青少年正处于生长发育期,应在医生指导下适当补钙,这里的“钙”指的是不是以单质、分子、原子等形式存在,这里所指的“钙”是强调存在的元素,与具体形态无关。
故答案为:C。
【分析】宏观上,元素组成物质。
5.【答案】A
【解析】【解答】不同种元素的本质区别是质子数不同。
故答案为:A。
【分析】根据元素的种类由质子数决定分析。
6.【答案】B
【解析】【解答】A、金属元素的原子最外层电子数一般少于4个, ①的原子 最外层电子数为7,属于非金属元素,故A错误;
B、 ②的微粒核内质子数是13,核外电子总数为2+8=10,说明失去了最外层的3个电子,质子数>核外电子数,形成了阳离子,其离子符号为 Al3+ ,故B正确;
C、 ②③ 微粒的核内质子数>核外电子数,属于阳离子, ⑤ 微粒的核内质子数=核外电子数,属于原子,故C错误;
D、元素的种类由核内质子数决定,圆圈里面的数字表示核内质子数, ②的核内质子数是13,③的核内质子数是12,两者核内质子数不相等,属于不同种类的元素,故D错误;
故答案为:B.
【分析】A、根据金属元素最外层电子数一般少于4个进行分析解答;
B、根据原子失去电子形成阳离子进行分析解答;
C、根据阳离子核内质子数>核外电子数进行分析解答;
D、根据元素种类由核内质子数决定分析解答。
7.【答案】D
【解析】【解答】A、铁由铁原子构成,不符合题意;
B、水由水分子构成,不符合题意;
C、氨气由氨分子构成,不符合题意;
D、氯化钠由钠离子和氯离子构成,符合题意。
故答案为:D。
【分析】根据盐类物质由离子构成,金属类由原子构成,水、氨气等由分子构成分析。
8.【答案】B
【解析】【解答】干冰升华是干冰由固态直接变为气态,没有新物质生成,是物理变化,在物理变化过程中分子种类、分子数目和分子大小都是不变的。气态物质的分子间间隔比固态和液态的都大,所以干冰升华只是分子间间隔变大了,
故答案为:B。
【分析】根据分子间有间隔,进行分析。
9.【答案】B
【解析】【解答】A、两个表面光滑的铅块相互压紧后会粘在一起,是因为分子间有引力,不符合题意;
B、过氧化氢是由过氧化氢分子构成的,其化学性质由过氧化氢分子保持,符合题意;
C、“飞沫”传播新冠病毒,是因为分子是在不断的运动的,不符合题意;
D、空气压缩为液态空气,是因为分子间有间隔,气体受压后,分子间的间隔变小,不符合题意。
故答案为:B。
【分析】A、根据分子的特性进行分析:分子的质量和体积都很小,分子是不断运动的,分子之间有间隔。
10.【答案】D
【解析】【解答】解:A、某同学将洗好的校服晾晒在阳台上,第二天校服就干了,是因为水分子是在不断的运动的,运动到空气中去了,故选项解释正确.
B、H2O和H2O2的化学性质不同,是因为它们分子的构成不同,不同种的分子性质不同,故选项解释正确.
C、电解水得到氢气和氧气,是因为水分子分裂成了氢原子和氧原子,然后氢原子、氧原子分别重新组合形成氢分子、氧分子,大量的氢分子、氧分子分别聚集成氢气、氧气,该事实说明分子是可以再分的,故选项解释正确.
D、温度计中的酒精热胀冷缩,是因为分子的间隔随温度改变而改变,故选项解释错误.
故选:D.
【分析】根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
11.【答案】C
【解析】【解答】A、原子是化学变化中的最小微粒,不再化学变化中,可以再分,故不符合题意;
B、化学变化中分子一定改变,原子不变,故不符合题意;
C、在含有多个电子的原子里,电子是分层排布的,故符合题意;
D、钠原子最外层有1个电子,很活泼,钠离子最外层有8个电子,比较稳定;钠原子和钠离子的化学性质不相同,故不符合题意。
故答案为:C。
【分析】A、根据原子的概念分析
B、根据化学变化中分子分裂成原子分析
C、根据核外电子的排布方式分析
D、根据决定元素化学性质的是最外层电子数分析
12.【答案】A
【解析】【解答】A、该元素的名称是银,带“钅”字旁,属于金属元素,故A符合题意;
B、在原子中,原子序数=核外电子数,左上角的数字为47,该元素的原子序数为47,一个银原子核外有47个电子,故B不符合题意;
C、汉字下面的数字表示相对原子质量,该元素的相对原子质量为107.9,相对原子质量单位是“1”,不是“克”,故C不符合题意;
D、左上角的数字为47,该元素的原子序数为47,故D不符合题意。
故答案为:A。
【分析】根据元素周期表一格的信息进行分析
13.【答案】(1)A;D
(2)6;得到
(3)48;3:2;
(4)相同条件下,在紫外线照射下,塑料越多,产生的臭氧越多
【解析】【解答】(1)A、氧气是空气的主要成分,不属于空气污染物,故正确;
B、臭氧属于空气污染物,故不正确;
C、PM2.5是可吸入颗粒物,属于空气污染物,故不正确;
D、稀有气体是空气的成分,不属于空气污染物,故正确;
E、二氧化氮属于空气污染物,故不正确;
故答案为:AD;
(2)核内质子数等于核外电子数,属于原子,氧原子的结构示意图,图中a=8-2=6,氧原子最外层有6个电子,大于4,容易得到2个电子,形成相对稳定结构;
(3)臭氧的相对分子质量为16×3=48,1个臭氧分子和1个氧分子的质量比为(16×3):(16×2)=3:2,氧气在紫外线照射的条件下生成臭氧,反应的化学方程式为: ;
(4)对比分析实验结果,能得到的研究结论是相同条件下,在紫外线照射下,塑料越多,产生的臭氧越多。
【分析】(1)根据大气成分不污染空气进行分析
(2)根据最外层电子数大于4得到电子进行分析
(3)根据相对分子质量的计算方法及方程式的书写方法进行分析
14.【答案】(1)8;Cl-;B和C;最外层电子数;CD
(2)2Mg;2H2;3Fe2+;;Al2O3
【解析】【解答】(1)①根据图示可知,在原子中,质子数=核外电子数,则18=2+8+x,x=8;C粒子质子数=17,核外电子数=18,质子数<核外电子数,为带1个单位负电荷的氯离子,其离子符号为:Cl-;②元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),同种元素的粒子是质子数相同,B、C的质子数相同,属于同种元素;③元素的化学性质主要由原子的最外层电子数决定,A和B两种粒子的最外层电子数相同,所以它们具有相似的化学性质;
④最外层电子数为8(只有一层电子数为2)是稳定的结构,所以具有相对稳定结构的粒子是C、D;(2)①原子的表示方法就是用元素符号来表示一个原子,表示多个该原子,在其元素符号前加上相应的数字。所以2个镁原子,就可表示为2Mg;②分子的表示方法是正确书写物质的化学式,表示多个该分子,在其化学式前加上相应的数字,因此2个氢分子表示为:2H2;③离子的表示方法是在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,3个亚铁离子可表示为:3Fe2+;④化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故+5价的氮元素可表示为: ;⑤在氧化铝中氧元素显-2价,铝元素显+3价,根据化合物中各元素的化合价的代数和为零,氧化铝的化学式是Al2O3。
【分析】(1)在原子结构示意图中,原子序数=核内质子数=核外电子数;当最外层电子数为8时达到稳定结构;原子的化学性质主要取决于原子的最外层电子数。
(2)离子表示方法:在表示该离子的元素符号右上角,标出该离子所带正负电荷数,数字在前,正负号在后,带一个电荷时,1要省略。若表示几个离子,在离子前面加上数字。
化合价表示方法:写出物质的化学式,计算要求元素的化合价,在化学式中该元素正上面写上数字和正负号,正负号在前,数字在后。
分子式表示方法:写出分子的化学式,有几个分子就在化学式前面写上相应的数字。
原子表示方法:用元素符号表示,表示多和该原子,在元素符号前面写上相应的数字。
15.【答案】(1)乙中的酚酞溶液逐渐变红;对照实验
(2)小纸花至下而上慢慢变红;不断运动
(3)B中小纸花先变红
(4)越快
(5)节约药品或更环保
【解析】【解答】知识回忆:按图Ⅰ进行实验,氨水显碱性,能使无色酚酞变红,可观察到的现象是乙中的酚酞溶液逐渐变红,烧杯丙的作用是与图甲形成对比,做对照实验;
实验改进:用注射器沿瓶壁注入几滴浓氨水,观察到小纸花至下而上慢慢变红,该现象主要说明分子的性质是分子在不断运动;
实验拓展:温度越高,分子运动速率越快,B中小纸花先变红,说明温度对分子的运动速率产生了影响;
实验结论:图Ⅲ实验说明:温度越高,分子运动速率越快;
实验反思:对比图Ⅰ实验,图Ⅱ实验的优点是节约药品或更环保。
【分析】(1)根据对比实验的相关知识进行分析
(2)根据氨气的密度比空气小分析
(3)根据温度越高分子运动越快分析
(4)根据装置的特点进行分析
16.【答案】(1)酒精
(2)水分子、酒精分子之间有间隔
【解析】【解答】(1)75%的酒精溶液中,溶剂是水,溶质是酒精;(2)将75 mL酒精和25 mL水混合时,发现体积小于100 mL,这是因为水分子、酒精分子之间有间隔,混合后总体积变小;
【分析】(1)根据只要有水的溶液溶剂都是水分析;
(2)根据分子间存在间隔分析。
17.【答案】(1)1;2
(2)18
【解析】【解答】(1)氚是氢元素的一种原子,其原子核内的质子数为1;中子数=相对原子质量-质子数=3-1=2;
(2)某原子R的中子数为20,相对原子质量为39,相对原子质量=质子数+中子数,该原子的质子数=39-20=19,原子里核内质子数等于核外电子数,其核外电子数为19,最外层电子数为1,容易失去电子形成的离子,该原子形成的离子的核外电子数为18。
【分析】(1)根据相对原子质量等于质子数加中子数分析;
(2)根据相对原子质量等于质子数加中子数,原子里核内质子数等于核外电子数,可分析该原子的核外电子数为19,形成的离子核外电子数为18。
18.【答案】(1)分子之间存在间隔,受压后,分子之间的间隔变小
(2)分子在不断运动
【解析】【解答】(1)分子之间存在间隔,受压后,分子之间的间隔变小,故氢气能储存在液化气罐中;
(2)人能够闻到豫菜香味的原因是分子在不断运动,引起香味的分子四处扩散。
【分析】根据分子的基本性质分析。
1 / 1
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
