人教版九年级化学上册第六单元碳和碳的氧化物单元复习题(含解析)
文档属性
| 名称 | 人教版九年级化学上册第六单元碳和碳的氧化物单元复习题(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 131.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-28 00:00:00 | ||
图片预览


文档简介
人教版九年级化学上册第六单元碳和碳的氧化物单元复习题
一、单选题
1.短时间内储存一瓶氧气,正确的方法是( )
A.瓶口朝下,不盖玻璃片 B.瓶口朝上,盖玻璃片
C.瓶口朝上,不盖玻璃片 D.瓶口朝下,盖玻璃片
2.如图所示,某同学为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水,发现石灰水没有变化.据此,你认为该同学应该( )
A.得出空气中没有二氧化碳的结论
B.得出空气中含有少量二氧化碳的结论
C.继续用大针筒向澄清石灰水压入空气
D.撤去大针筒,用嘴向澄清石灰水吹气
3.某物质经分析知道只含有一种元素,则该物质不可能是( )
A.单质 B.化合物 C.纯净物 D.混合物
4.“吸烟有害健康”,香烟的烟气中含有上百种有毒物质,其中一种物质极易与血红蛋白结合.该物质是( )
A.SO2 B.CO C.CO2 D.NO2
5.下列物质的用途,主要利用其化学性质的是( )
A.金刚石用于切割玻璃 B.用铝制作导线
C.石墨制铅笔芯 D.用煤炭作燃料
6.防毒面具的滤毒罐中用来吸附毒气的物质是( )
A.炭黑 B.活性炭 C.金刚石 D.石墨
7.康康同学欲在实验室收集气体X,他查询的信息与选择收集方法无关的是()
A.X的气味 B.X在水中的溶解性
C.是否与空气和水反应 D.X的密度
8.对比是学习化学的重要方法,下列关于二氧化碳和一氧化碳的比较,完全正确的是( )
A.组成:CO2、CO均由碳元素和氧元素组成
B.性质:CO2、CO都有可燃性
C.用途:CO2可用于灭火;CO可用于人工降雨
D.危害:CO2会导致酸雨;CO会引起中毒
9.碳与碳的氧化物与人类关系密切,在生活中应用广泛。下列有关说法正确的是( )
A.石墨、金刚石、C60的物理性质和化学性质都相似
B.室内放一盆水能防止一氧化碳中毒
C.地球上二氧化碳含量上升的主要原因是植物的呼吸作用
D.CO、CO2都是没有颜色、没有气味的气体
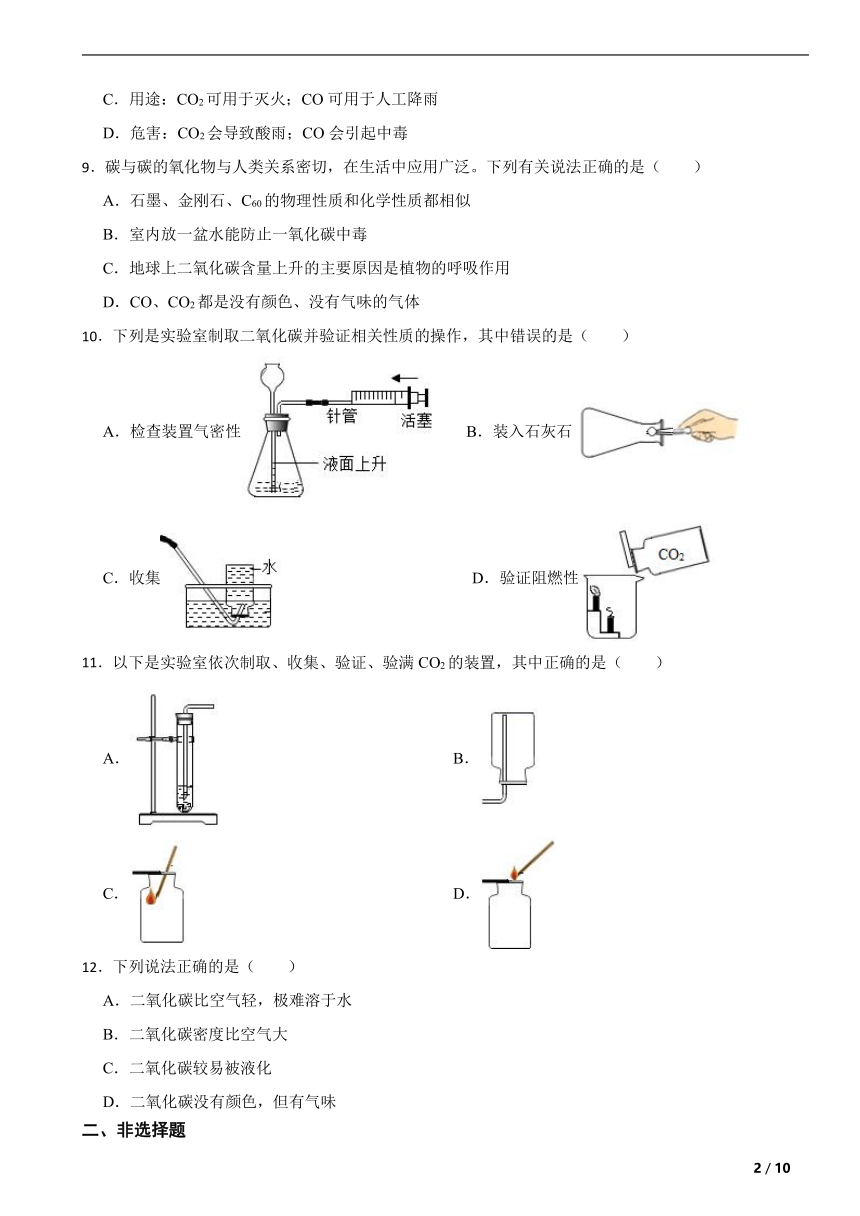
10.下列是实验室制取二氧化碳并验证相关性质的操作,其中错误的是( )
A.检查装置气密性 B.装入石灰石
C.收集 D.验证阻燃性
11.以下是实验室依次制取、收集、验证、验满CO2的装置,其中正确的是( )
A. B.
C. D.
12.下列说法正确的是( )
A.二氧化碳比空气轻,极难溶于水
B.二氧化碳密度比空气大
C.二氧化碳较易被液化
D.二氧化碳没有颜色,但有气味
二、非选择题
13.阅读下列科技短文并回答问题。
钻石由金刚石精加工而成,金刚石是天然存在的最硬的物质。据媒体报道,英国已成功研发出利用大气中的二氧化碳制造钻石的技术,并成功创造出“世界上第一颗零污染钻石”。创造过程中,首先将“钻石种子”放入一个密封容器中,容器内部充满富含碳元素的甲烷气体,随后将这个容器加热到800℃,其间碳元素会逐渐与“钻石种子”结合,在数周时间内形成一颗钻石——“空气钻石”,其性质与由金刚石加工而成的钻石完全相同。
研究表明,由金刚石制成一克拉的天然钻石需要消耗大量的资源,并产生大量二氧化碳,而“空气钻石”所用的二氧化碳可从空气中提取。
(1)用大气中的二氧化碳制造钻石是因为二氧化碳中含有 元素。
(2)用二氧化碳制造钻石过程中发生的是 (选填“物理”或“化学”)变化。
(3)下列说法错误的是____(填字母)。
A.“空气钻石”的硬度很大
B.“空气钻石”一定不能燃烧
C.“空气钻石”中碳原子仍在不断运动
D.制造“空气钻石”比开采天然钻石环保
(4)科学家利用金属钠与二氧化碳反应得到金刚石和另一种物质X,其化学方程式为 ,则X的化学式是 。
(5)金刚石除了精加工成钻石用作装饰品,还可用于 (写出1条即可)。
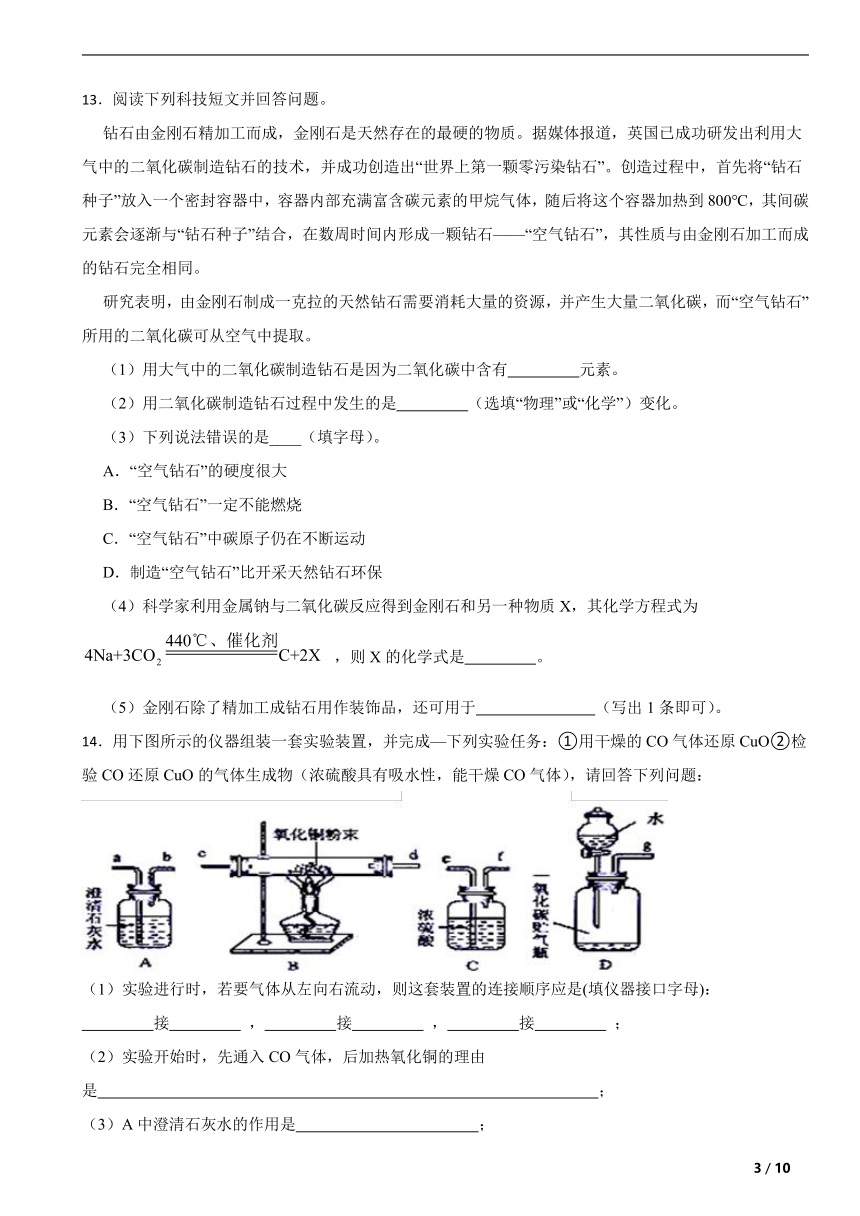
14.用下图所示的仪器组装一套实验装置,并完成—下列实验任务:①用干燥的CO气体还原CuO②检验CO还原CuO的气体生成物(浓硫酸具有吸水性,能干燥CO气体),请回答下列问题:
(1)实验进行时,若要气体从左向右流动,则这套装置的连接顺序应是(填仪器接口字母):
接 , 接 , 接 ;
(2)实验开始时,先通入CO气体,后加热氧化铜的理由是 ;
(3)A中澄清石灰水的作用是 ;
(4)该套实验装置从环境保护的角度考虑可能存在的不足是 ,
你提出的合理处理建议是 。
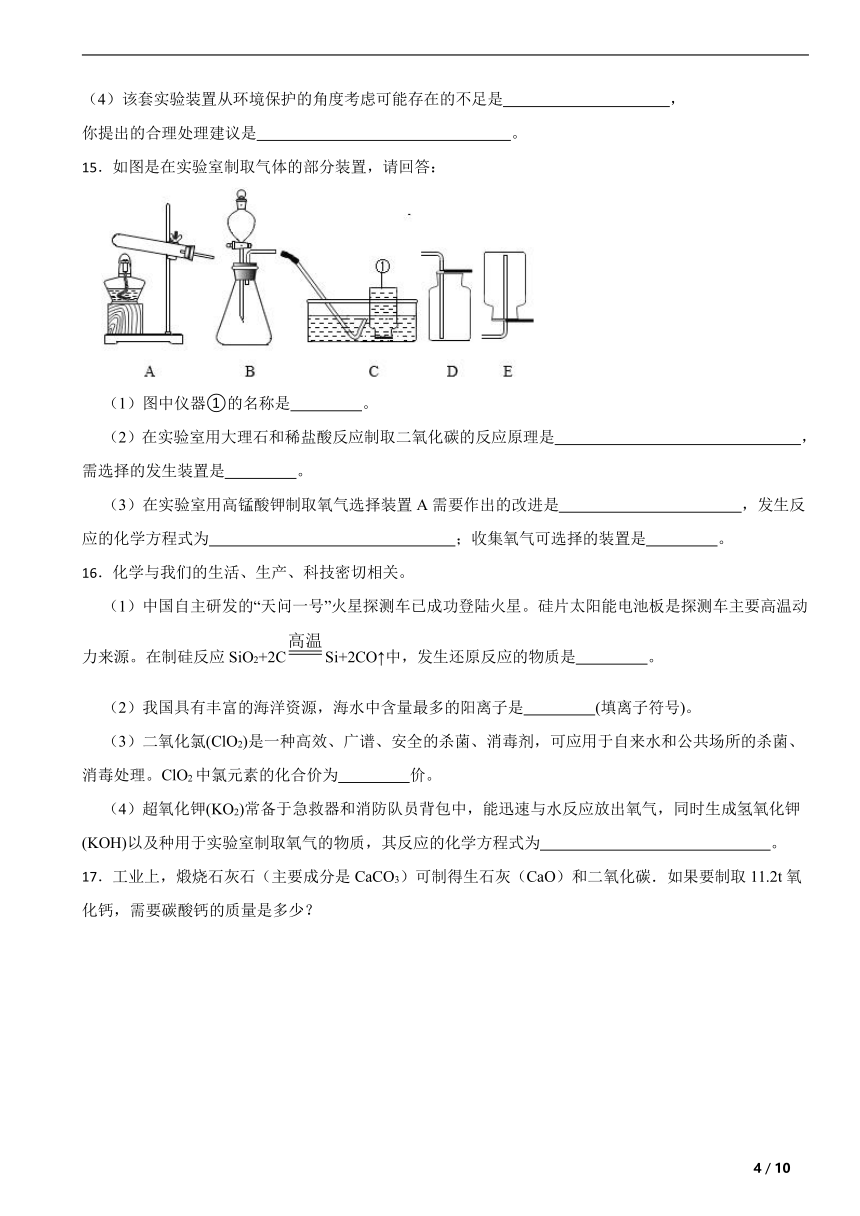
15.如图是在实验室制取气体的部分装置,请回答:
(1)图中仪器①的名称是 。
(2)在实验室用大理石和稀盐酸反应制取二氧化碳的反应原理是 ,需选择的发生装置是 。
(3)在实验室用高锰酸钾制取氧气选择装置A需要作出的改进是 ,发生反应的化学方程式为 ;收集氧气可选择的装置是 。
16.化学与我们的生活、生产、科技密切相关。
(1)中国自主研发的“天问一号”火星探测车已成功登陆火星。硅片太阳能电池板是探测车主要高温动力来源。在制硅反应SiO2+2CSi+2CO↑中,发生还原反应的物质是 。
(2)我国具有丰富的海洋资源,海水中含量最多的阳离子是 (填离子符号)。
(3)二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂,可应用于自来水和公共场所的杀菌、消毒处理。ClO2中氯元素的化合价为 价。
(4)超氧化钾(KO2)常备于急救器和消防队员背包中,能迅速与水反应放出氧气,同时生成氢氧化钾(KOH)以及种用于实验室制取氧气的物质,其反应的化学方程式为 。
17.工业上,煅烧石灰石(主要成分是CaCO3)可制得生石灰(CaO)和二氧化碳.如果要制取11.2t氧化钙,需要碳酸钙的质量是多少?
答案解析部分
1.【答案】B
【解析】【解答】短时间储存气体时可将气体储存在集气瓶中,瓶好玻璃片,如气体密度比空气大,可将集气瓶瓶口向上正放,如气体密度比空气小,可将集气瓶瓶口向下倒放,氧气密度比空气大,所以要瓶口向上正放在桌上,
故答案为:B。
【分析】实验室短时间内储存氧气一般选用集气瓶,由于氧气密度大,要选择瓶口朝上放置。
2.【答案】C
【解析】【解答】A、验证性实验是已经知道实验结果的,当实验现象与已知的结果不相符时,应该思考实验过程中存在的问题,不能贸然得出空气中没有二氧化碳的结论,A不符合题意;
B、实验中澄清石灰水没有变浑浊,不能得出空气中含有少量二氧化碳的结论,B不符合题意;
C、验证性实验是已经知道实验结果的,当实验现象与已知的结果不相符时,应该思考实验过程中存在的问题;空气中二氧化碳的量太少,通少量空气现象不明显,为了使实验现象更明显,所以应该继续通空气,直到现象明显为止,C符合题意;
D、人体呼吸作用会产生较多的二氧化碳,违背实验目的(验证空气中含有少量二氧化碳),D不符合题意。
故答案为:C。
【分析】由于空气中二氧化碳含量较少,故需要多次通入空气。
3.【答案】B
【解析】【解答】解:A、单质是由一种元素组成的纯净物,因此只含有一种元素可能是单质,故A不选;
B、化合物是指由两种或两种以上元素组成的纯净物,至少有两种元素,所以只含有一种元素一定不是化合物,故B选;
C、只含有一种元素的物质可能是单质,单质属于纯净物,故C不选;
D、只含有一种元素可能属于混合物,如氧气和臭氧的混合物都只含氧元素,故D不选.
故选B.
【分析】根据纯净物、混合物、单质、化合物的定义来回答本题,只含有一种元素不一定是纯净物.
4.【答案】B
【解析】【解答】解:烟草在燃烧过程中,产生了许多有害物质,如尼古丁、烟焦油、一氧化碳等,其中一氧化碳有毒,它能与血液中的血红蛋白结合,从而导致体内组织器官严重缺氧而中毒死亡.
故选B.
【分析】根据香烟烟气的成分和一氧化碳中毒的原理判断,一氧化碳等物质能和血液中的血红蛋白结合,从而使氧气失去和血红蛋白结合的机会,能够使人中毒.
5.【答案】D
【解析】【解答】A、金刚石用于切割玻璃是利用金刚石的硬度大,硬度属于物理性质,不符合题意;
B、用铝制作导线是利用铝的导电性,导电性属于物理性质,不符合题意;
C、用石墨制铅笔芯是利用石墨质软且呈黑色,质软且呈黑色属于物理性质,不符合题意;
D、用煤炭作燃料是利用煤炭的可燃性,可燃性属于化学性质,符合题意。
故答案为:D。
【分析】化学性质是指物质在化学变化中表现出来的性质,主要包括可燃性、助燃性、氧化性、还原性、酸碱性、稳定性、腐蚀性等。
6.【答案】B
【解析】【解答】解:活性炭具有吸附作用,能吸附色素和有毒的物质,常常用来吸附有毒的物质.观察选项,故选B.
答案:B
【分析】可以根据物质的性质和用途等方面的知识进行分析、考虑,从而得出正确的结论.
7.【答案】A
【解析】【分析】根据气体收集方法的选择方法:气体的溶解性和密度来回答本题.排水法要考虑气体的溶解性和是否与水反应;排空气法要考虑气体的密度及是否与空气反应.
【解答】收集方法的选择是根据:难溶于水或不易溶于水且不与水发生化学反应的气体用排水法收集,密度比空气大且不与空气中的物质反应的气体用向上排空气法收集,密度比空气小且不与空气中的物质反应的气体用向下排空气法收集.与气体的气味无关.
故选A。
【点评】实验室选择气体的制取装置和收集装置,是中考实验题中经常出现的题型.同学们只要抓住关键点,制取装置要考虑反应物的状态,收集装置要考虑气体的密度和溶解性,问题就会迎刃而解
8.【答案】A
【解析】【解答】A、一氧化碳和二氧化碳都是由碳元素和氧元素组成的,A符合题意;
B、二氧化碳不能燃烧,一氧化碳具有可燃性,B不符合题意;
C、二氧化碳的固体干冰升华吸热,可用于人工降雨;一氧化碳可用作气体燃料、冶炼金属的还原剂等,但不能用于人工降雨,C不符合题意;
D、二氧化碳会造成“温室效应”,导致酸雨的是二氧化硫,D不符合题意;
故答案为:A。
【分析】本考点考查了二氧化碳、一氧化碳的组成、性质和用途,一氧化碳和二氧化碳也是中考中的重要考点,二氧化碳的特性是能使澄清的石灰水变浑浊。
9.【答案】D
【解析】【解答】A、石墨、金刚石、C60的物理性质差异很大,因为它们中碳原子的排列方式不同,它们的组成元素都是碳元素,化学性质都相似,不符合题意;
B、一氧化碳难溶于水,室内放一盆水不能防止一氧化碳中毒,不符合题意;
C、地球上二氧化碳含量上升的主要原因是化石燃料的燃烧,不符合题意;
D、CO、CO2都是没有颜色、没有气味的气体,符合题意。
故答案为:D。
【分析】A、根据物质的结构决定物质的性质分析
B、根据一氧化碳的性质分析
C、根据化石燃料的燃烧对二氧化碳含量的影响分析
D、根据二氧化碳和一氧化碳的性质分析
10.【答案】C
【解析】【解答】A、如图,推动针管的活塞,若装置不漏气,则在气压差的作用下,长颈漏斗下方管体内出现水柱且不会落,选项不符合题意;
B、如图,装入块状药品将锥形瓶横放然后将药品放入再缓慢竖起,滑到底部,选项不符合题意;
C、如图,二氧化碳溶于水,因此不能用排水法收集,选项符合题意;
D、如图,下层蜡烛先熄灭上层蜡烛后熄灭,说明二氧化碳密度比空气大且不燃烧也不支持燃烧,选项不符合题意;
故答案为:C。
【分析】A.推动针管的活塞,若装置不漏气,长颈漏斗下方管体内出现一段稳定的水柱;
B.装入块状药品时,应将锥形瓶横放然后将药品放入再缓慢竖起;
C.二氧化碳能溶于水,也能与水反应,不能用排水法收集;
D.二氧化碳密度比空气大、不燃烧、也不支持燃烧。
11.【答案】D
【解析】【解答】A、实验室制取二氧化碳的原理是CaCO3+2HCl=CaCl2+H2O+CO2↑,反应物是固体和液体,在常温下进行反应,但A中装置导管伸入试管内液面以下,无法导出气体,A不符合题意;
B、二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,B装置是向下排空气法,B不符合题意;
C、二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳,不能用燃着的木条检验,C不符合题意;
D、二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;D符合题意。
故答案为:D。
【分析】A、根据反应物的状态和反应条件确定发生装置分析
B、根据二氧化碳的密度进行分析
C、根据检验二氧化碳利用澄清石灰水进行分析
D、根据验满气体在瓶口进行分析
12.【答案】B
【解析】【解答】解:A、二氧化碳密度比空气大,可溶于水.故A说法不正确;
B、二氧化碳密度比空气大.故B说法正确;
C、二氧化碳在加压、降温时可以转变为液体.故C说法不正确;
D、二氧化碳是一种没有颜色没有气味气体.故D说法不正确.
故选B.
【分析】根据二氧化碳的物理性质分析判断.二氧化碳是一种没有颜色没有气味气体,密度比空气大,可溶于水,不易被液化.
13.【答案】(1)碳
(2)化学
(3)B
(4)Na2CO3
(5)制作玻璃刀
【解析】【解答】(1)根据质量守恒定律化学反应前后元素种类不变可知:二氧化碳能制造钻石是因为二氧化碳中含有碳元素;
(2)有新物质生成的变化是化学变化,故用二氧化碳制造钻石过程中发生的是化学变化;
(3)A、“空气钻石”,其性质与由金刚石加工而成的钻石完全相同,金刚石的硬度大,故“空气钻石”的硬度也很大,说法正确;
B、“空气钻石”就是碳单质,具有可燃性,一定能燃烧,说法不正确;
C、微粒都是不断运动的,“空气钻石”中碳原子仍在不断运动,说法正确;
D、分析材料可知:由金刚石制成一克拉的天然钻石需要消耗大量的资源,并产生大量二氧化碳,而“空气钻石”所用的二氧化碳可从空气中提取,故制造“空气钻石”比开采天然钻石环保,说法正确;
故答案为:B;
(4)根据质量守恒定律化学反应前后原子的种类和个数都不变可推测出X的化学式是Na2CO3;
(5)金刚石硬度较大,可作玻璃刀。
【分析】(1)根据化学反应前后元素种类不变分析;
(2)根据化学变化有新物质生成分析;
(3)根据“空气钻石”是碳单质,结合碳的性质分析;
(4)根据化学反应前后原子种类和个数不变分析;
(5)根据金刚石硬度大分析。
14.【答案】g;e;f;c;d;a;排出玻璃管内的空气,防止加热一氧化碳与空气的混合物引起爆炸;检验生成的二氧化碳;没有进行尾气处理;在导管b处加一个燃着的酒精灯
【解析】【解答】(1)该实验中,先用浓硫酸 干燥一氧化碳,在还原氧化铜用澄清的石灰水验证二氧化碳气体。故链接顺序是ge,fc,da;
(2)实验开始时,要先通入CO气体,后加热,目的是排出玻璃管内的空气,防止加热一氧化碳与空气的混合物引起爆炸;
(3) A中澄清石灰水的作用是检验生成的二氧化碳;
(4)由于一氧化碳有毒,不能直接排放到空气中以免污染空气,故要添加尾气处理装置。
【分析】一氧化碳还原氧化铜实验
15.【答案】(1)集气瓶
(2);B
(3)在试管口放一团棉花;;C或D
【解析】【解答】(1)图中仪器①的名称是集气瓶;
(2)实验室用大理石和稀盐酸反应,该反应生成氯化钙、二氧化碳和水,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应中反应物为固体和液体,不需要加热,故需选择的发生装置是B;
(3)实验室用高锰酸钾制取氧气时,要在试管口放一团棉花,防止粉末进入导管导致导管堵塞,该反应的化学方程式为
;由于氧气不易溶于水并不与水反应,氧气的密度大于空气的密度,故可用排水法和向上排空气法收集氧气,故收集氧气可选择的装置是C或D。
【分析】
16.【答案】(1)SiO2
(2)Na+
(3)+4
(4)2KO2+2H2O=2KOH+H2O2+O2↑
【解析】【解答】(1)由 可知,碳夺取了二氧化硅中的氧,具有还原性,作还原剂;二氧化硅失去了氧,发生了还原反应,故填:SiO2;
(2)我国具有丰富的海洋资源,海水中的盐类物质中氯化钠含量最高,因此含量最多的阳离子是Na+,故填:Na+。
(3)ClO2中氧元素化合价是﹣2,根据化合物中元素化合价代数和为零可知,氯元素的化合价为+4价,故填:+4。
(4)超氧化钾(KO2)能迅速与水反应放出氧气,同时生成氢氧化钾(KOH)以及种用于实验室制取氧气的物质,实验室制取氧气的物质是过氧化氢,其反应的化学方程式为:2KO2+2H2O=2KOH+H2O2+O2↑。
【分析】(1)根据失氧物质发生还原反应分析;
(2)根据海水中钠离子含量最高分析;
(3)根据化合物中元素化合价代数和为0分析;
(4)根据超氧化钾与水反应生成氧气、氢氧化钾、过氧化氢分析。
17.【答案】解:设需要碳酸钙的质量为x.
CaCO3 CaO+ CO2↑
100
56
x
11.2t
= ,x=20t
答:需要碳酸钙的质量为20t
【解析】【分析】由氧化钙的质量根据碳酸钙分解的化学方程式可以计算出碳酸钙的质量.
1 / 1
一、单选题
1.短时间内储存一瓶氧气,正确的方法是( )
A.瓶口朝下,不盖玻璃片 B.瓶口朝上,盖玻璃片
C.瓶口朝上,不盖玻璃片 D.瓶口朝下,盖玻璃片
2.如图所示,某同学为验证空气中含有少量二氧化碳,将大针筒内的空气一次性压入新制的澄清石灰水,发现石灰水没有变化.据此,你认为该同学应该( )
A.得出空气中没有二氧化碳的结论
B.得出空气中含有少量二氧化碳的结论
C.继续用大针筒向澄清石灰水压入空气
D.撤去大针筒,用嘴向澄清石灰水吹气
3.某物质经分析知道只含有一种元素,则该物质不可能是( )
A.单质 B.化合物 C.纯净物 D.混合物
4.“吸烟有害健康”,香烟的烟气中含有上百种有毒物质,其中一种物质极易与血红蛋白结合.该物质是( )
A.SO2 B.CO C.CO2 D.NO2
5.下列物质的用途,主要利用其化学性质的是( )
A.金刚石用于切割玻璃 B.用铝制作导线
C.石墨制铅笔芯 D.用煤炭作燃料
6.防毒面具的滤毒罐中用来吸附毒气的物质是( )
A.炭黑 B.活性炭 C.金刚石 D.石墨
7.康康同学欲在实验室收集气体X,他查询的信息与选择收集方法无关的是()
A.X的气味 B.X在水中的溶解性
C.是否与空气和水反应 D.X的密度
8.对比是学习化学的重要方法,下列关于二氧化碳和一氧化碳的比较,完全正确的是( )
A.组成:CO2、CO均由碳元素和氧元素组成
B.性质:CO2、CO都有可燃性
C.用途:CO2可用于灭火;CO可用于人工降雨
D.危害:CO2会导致酸雨;CO会引起中毒
9.碳与碳的氧化物与人类关系密切,在生活中应用广泛。下列有关说法正确的是( )
A.石墨、金刚石、C60的物理性质和化学性质都相似
B.室内放一盆水能防止一氧化碳中毒
C.地球上二氧化碳含量上升的主要原因是植物的呼吸作用
D.CO、CO2都是没有颜色、没有气味的气体
10.下列是实验室制取二氧化碳并验证相关性质的操作,其中错误的是( )
A.检查装置气密性 B.装入石灰石
C.收集 D.验证阻燃性
11.以下是实验室依次制取、收集、验证、验满CO2的装置,其中正确的是( )
A. B.
C. D.
12.下列说法正确的是( )
A.二氧化碳比空气轻,极难溶于水
B.二氧化碳密度比空气大
C.二氧化碳较易被液化
D.二氧化碳没有颜色,但有气味
二、非选择题
13.阅读下列科技短文并回答问题。
钻石由金刚石精加工而成,金刚石是天然存在的最硬的物质。据媒体报道,英国已成功研发出利用大气中的二氧化碳制造钻石的技术,并成功创造出“世界上第一颗零污染钻石”。创造过程中,首先将“钻石种子”放入一个密封容器中,容器内部充满富含碳元素的甲烷气体,随后将这个容器加热到800℃,其间碳元素会逐渐与“钻石种子”结合,在数周时间内形成一颗钻石——“空气钻石”,其性质与由金刚石加工而成的钻石完全相同。
研究表明,由金刚石制成一克拉的天然钻石需要消耗大量的资源,并产生大量二氧化碳,而“空气钻石”所用的二氧化碳可从空气中提取。
(1)用大气中的二氧化碳制造钻石是因为二氧化碳中含有 元素。
(2)用二氧化碳制造钻石过程中发生的是 (选填“物理”或“化学”)变化。
(3)下列说法错误的是____(填字母)。
A.“空气钻石”的硬度很大
B.“空气钻石”一定不能燃烧
C.“空气钻石”中碳原子仍在不断运动
D.制造“空气钻石”比开采天然钻石环保
(4)科学家利用金属钠与二氧化碳反应得到金刚石和另一种物质X,其化学方程式为 ,则X的化学式是 。
(5)金刚石除了精加工成钻石用作装饰品,还可用于 (写出1条即可)。
14.用下图所示的仪器组装一套实验装置,并完成—下列实验任务:①用干燥的CO气体还原CuO②检验CO还原CuO的气体生成物(浓硫酸具有吸水性,能干燥CO气体),请回答下列问题:
(1)实验进行时,若要气体从左向右流动,则这套装置的连接顺序应是(填仪器接口字母):
接 , 接 , 接 ;
(2)实验开始时,先通入CO气体,后加热氧化铜的理由是 ;
(3)A中澄清石灰水的作用是 ;
(4)该套实验装置从环境保护的角度考虑可能存在的不足是 ,
你提出的合理处理建议是 。
15.如图是在实验室制取气体的部分装置,请回答:
(1)图中仪器①的名称是 。
(2)在实验室用大理石和稀盐酸反应制取二氧化碳的反应原理是 ,需选择的发生装置是 。
(3)在实验室用高锰酸钾制取氧气选择装置A需要作出的改进是 ,发生反应的化学方程式为 ;收集氧气可选择的装置是 。
16.化学与我们的生活、生产、科技密切相关。
(1)中国自主研发的“天问一号”火星探测车已成功登陆火星。硅片太阳能电池板是探测车主要高温动力来源。在制硅反应SiO2+2CSi+2CO↑中,发生还原反应的物质是 。
(2)我国具有丰富的海洋资源,海水中含量最多的阳离子是 (填离子符号)。
(3)二氧化氯(ClO2)是一种高效、广谱、安全的杀菌、消毒剂,可应用于自来水和公共场所的杀菌、消毒处理。ClO2中氯元素的化合价为 价。
(4)超氧化钾(KO2)常备于急救器和消防队员背包中,能迅速与水反应放出氧气,同时生成氢氧化钾(KOH)以及种用于实验室制取氧气的物质,其反应的化学方程式为 。
17.工业上,煅烧石灰石(主要成分是CaCO3)可制得生石灰(CaO)和二氧化碳.如果要制取11.2t氧化钙,需要碳酸钙的质量是多少?
答案解析部分
1.【答案】B
【解析】【解答】短时间储存气体时可将气体储存在集气瓶中,瓶好玻璃片,如气体密度比空气大,可将集气瓶瓶口向上正放,如气体密度比空气小,可将集气瓶瓶口向下倒放,氧气密度比空气大,所以要瓶口向上正放在桌上,
故答案为:B。
【分析】实验室短时间内储存氧气一般选用集气瓶,由于氧气密度大,要选择瓶口朝上放置。
2.【答案】C
【解析】【解答】A、验证性实验是已经知道实验结果的,当实验现象与已知的结果不相符时,应该思考实验过程中存在的问题,不能贸然得出空气中没有二氧化碳的结论,A不符合题意;
B、实验中澄清石灰水没有变浑浊,不能得出空气中含有少量二氧化碳的结论,B不符合题意;
C、验证性实验是已经知道实验结果的,当实验现象与已知的结果不相符时,应该思考实验过程中存在的问题;空气中二氧化碳的量太少,通少量空气现象不明显,为了使实验现象更明显,所以应该继续通空气,直到现象明显为止,C符合题意;
D、人体呼吸作用会产生较多的二氧化碳,违背实验目的(验证空气中含有少量二氧化碳),D不符合题意。
故答案为:C。
【分析】由于空气中二氧化碳含量较少,故需要多次通入空气。
3.【答案】B
【解析】【解答】解:A、单质是由一种元素组成的纯净物,因此只含有一种元素可能是单质,故A不选;
B、化合物是指由两种或两种以上元素组成的纯净物,至少有两种元素,所以只含有一种元素一定不是化合物,故B选;
C、只含有一种元素的物质可能是单质,单质属于纯净物,故C不选;
D、只含有一种元素可能属于混合物,如氧气和臭氧的混合物都只含氧元素,故D不选.
故选B.
【分析】根据纯净物、混合物、单质、化合物的定义来回答本题,只含有一种元素不一定是纯净物.
4.【答案】B
【解析】【解答】解:烟草在燃烧过程中,产生了许多有害物质,如尼古丁、烟焦油、一氧化碳等,其中一氧化碳有毒,它能与血液中的血红蛋白结合,从而导致体内组织器官严重缺氧而中毒死亡.
故选B.
【分析】根据香烟烟气的成分和一氧化碳中毒的原理判断,一氧化碳等物质能和血液中的血红蛋白结合,从而使氧气失去和血红蛋白结合的机会,能够使人中毒.
5.【答案】D
【解析】【解答】A、金刚石用于切割玻璃是利用金刚石的硬度大,硬度属于物理性质,不符合题意;
B、用铝制作导线是利用铝的导电性,导电性属于物理性质,不符合题意;
C、用石墨制铅笔芯是利用石墨质软且呈黑色,质软且呈黑色属于物理性质,不符合题意;
D、用煤炭作燃料是利用煤炭的可燃性,可燃性属于化学性质,符合题意。
故答案为:D。
【分析】化学性质是指物质在化学变化中表现出来的性质,主要包括可燃性、助燃性、氧化性、还原性、酸碱性、稳定性、腐蚀性等。
6.【答案】B
【解析】【解答】解:活性炭具有吸附作用,能吸附色素和有毒的物质,常常用来吸附有毒的物质.观察选项,故选B.
答案:B
【分析】可以根据物质的性质和用途等方面的知识进行分析、考虑,从而得出正确的结论.
7.【答案】A
【解析】【分析】根据气体收集方法的选择方法:气体的溶解性和密度来回答本题.排水法要考虑气体的溶解性和是否与水反应;排空气法要考虑气体的密度及是否与空气反应.
【解答】收集方法的选择是根据:难溶于水或不易溶于水且不与水发生化学反应的气体用排水法收集,密度比空气大且不与空气中的物质反应的气体用向上排空气法收集,密度比空气小且不与空气中的物质反应的气体用向下排空气法收集.与气体的气味无关.
故选A。
【点评】实验室选择气体的制取装置和收集装置,是中考实验题中经常出现的题型.同学们只要抓住关键点,制取装置要考虑反应物的状态,收集装置要考虑气体的密度和溶解性,问题就会迎刃而解
8.【答案】A
【解析】【解答】A、一氧化碳和二氧化碳都是由碳元素和氧元素组成的,A符合题意;
B、二氧化碳不能燃烧,一氧化碳具有可燃性,B不符合题意;
C、二氧化碳的固体干冰升华吸热,可用于人工降雨;一氧化碳可用作气体燃料、冶炼金属的还原剂等,但不能用于人工降雨,C不符合题意;
D、二氧化碳会造成“温室效应”,导致酸雨的是二氧化硫,D不符合题意;
故答案为:A。
【分析】本考点考查了二氧化碳、一氧化碳的组成、性质和用途,一氧化碳和二氧化碳也是中考中的重要考点,二氧化碳的特性是能使澄清的石灰水变浑浊。
9.【答案】D
【解析】【解答】A、石墨、金刚石、C60的物理性质差异很大,因为它们中碳原子的排列方式不同,它们的组成元素都是碳元素,化学性质都相似,不符合题意;
B、一氧化碳难溶于水,室内放一盆水不能防止一氧化碳中毒,不符合题意;
C、地球上二氧化碳含量上升的主要原因是化石燃料的燃烧,不符合题意;
D、CO、CO2都是没有颜色、没有气味的气体,符合题意。
故答案为:D。
【分析】A、根据物质的结构决定物质的性质分析
B、根据一氧化碳的性质分析
C、根据化石燃料的燃烧对二氧化碳含量的影响分析
D、根据二氧化碳和一氧化碳的性质分析
10.【答案】C
【解析】【解答】A、如图,推动针管的活塞,若装置不漏气,则在气压差的作用下,长颈漏斗下方管体内出现水柱且不会落,选项不符合题意;
B、如图,装入块状药品将锥形瓶横放然后将药品放入再缓慢竖起,滑到底部,选项不符合题意;
C、如图,二氧化碳溶于水,因此不能用排水法收集,选项符合题意;
D、如图,下层蜡烛先熄灭上层蜡烛后熄灭,说明二氧化碳密度比空气大且不燃烧也不支持燃烧,选项不符合题意;
故答案为:C。
【分析】A.推动针管的活塞,若装置不漏气,长颈漏斗下方管体内出现一段稳定的水柱;
B.装入块状药品时,应将锥形瓶横放然后将药品放入再缓慢竖起;
C.二氧化碳能溶于水,也能与水反应,不能用排水法收集;
D.二氧化碳密度比空气大、不燃烧、也不支持燃烧。
11.【答案】D
【解析】【解答】A、实验室制取二氧化碳的原理是CaCO3+2HCl=CaCl2+H2O+CO2↑,反应物是固体和液体,在常温下进行反应,但A中装置导管伸入试管内液面以下,无法导出气体,A不符合题意;
B、二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,B装置是向下排空气法,B不符合题意;
C、二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊,就证明是二氧化碳,不能用燃着的木条检验,C不符合题意;
D、二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;D符合题意。
故答案为:D。
【分析】A、根据反应物的状态和反应条件确定发生装置分析
B、根据二氧化碳的密度进行分析
C、根据检验二氧化碳利用澄清石灰水进行分析
D、根据验满气体在瓶口进行分析
12.【答案】B
【解析】【解答】解:A、二氧化碳密度比空气大,可溶于水.故A说法不正确;
B、二氧化碳密度比空气大.故B说法正确;
C、二氧化碳在加压、降温时可以转变为液体.故C说法不正确;
D、二氧化碳是一种没有颜色没有气味气体.故D说法不正确.
故选B.
【分析】根据二氧化碳的物理性质分析判断.二氧化碳是一种没有颜色没有气味气体,密度比空气大,可溶于水,不易被液化.
13.【答案】(1)碳
(2)化学
(3)B
(4)Na2CO3
(5)制作玻璃刀
【解析】【解答】(1)根据质量守恒定律化学反应前后元素种类不变可知:二氧化碳能制造钻石是因为二氧化碳中含有碳元素;
(2)有新物质生成的变化是化学变化,故用二氧化碳制造钻石过程中发生的是化学变化;
(3)A、“空气钻石”,其性质与由金刚石加工而成的钻石完全相同,金刚石的硬度大,故“空气钻石”的硬度也很大,说法正确;
B、“空气钻石”就是碳单质,具有可燃性,一定能燃烧,说法不正确;
C、微粒都是不断运动的,“空气钻石”中碳原子仍在不断运动,说法正确;
D、分析材料可知:由金刚石制成一克拉的天然钻石需要消耗大量的资源,并产生大量二氧化碳,而“空气钻石”所用的二氧化碳可从空气中提取,故制造“空气钻石”比开采天然钻石环保,说法正确;
故答案为:B;
(4)根据质量守恒定律化学反应前后原子的种类和个数都不变可推测出X的化学式是Na2CO3;
(5)金刚石硬度较大,可作玻璃刀。
【分析】(1)根据化学反应前后元素种类不变分析;
(2)根据化学变化有新物质生成分析;
(3)根据“空气钻石”是碳单质,结合碳的性质分析;
(4)根据化学反应前后原子种类和个数不变分析;
(5)根据金刚石硬度大分析。
14.【答案】g;e;f;c;d;a;排出玻璃管内的空气,防止加热一氧化碳与空气的混合物引起爆炸;检验生成的二氧化碳;没有进行尾气处理;在导管b处加一个燃着的酒精灯
【解析】【解答】(1)该实验中,先用浓硫酸 干燥一氧化碳,在还原氧化铜用澄清的石灰水验证二氧化碳气体。故链接顺序是ge,fc,da;
(2)实验开始时,要先通入CO气体,后加热,目的是排出玻璃管内的空气,防止加热一氧化碳与空气的混合物引起爆炸;
(3) A中澄清石灰水的作用是检验生成的二氧化碳;
(4)由于一氧化碳有毒,不能直接排放到空气中以免污染空气,故要添加尾气处理装置。
【分析】一氧化碳还原氧化铜实验
15.【答案】(1)集气瓶
(2);B
(3)在试管口放一团棉花;;C或D
【解析】【解答】(1)图中仪器①的名称是集气瓶;
(2)实验室用大理石和稀盐酸反应,该反应生成氯化钙、二氧化碳和水,方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应中反应物为固体和液体,不需要加热,故需选择的发生装置是B;
(3)实验室用高锰酸钾制取氧气时,要在试管口放一团棉花,防止粉末进入导管导致导管堵塞,该反应的化学方程式为
;由于氧气不易溶于水并不与水反应,氧气的密度大于空气的密度,故可用排水法和向上排空气法收集氧气,故收集氧气可选择的装置是C或D。
【分析】
16.【答案】(1)SiO2
(2)Na+
(3)+4
(4)2KO2+2H2O=2KOH+H2O2+O2↑
【解析】【解答】(1)由 可知,碳夺取了二氧化硅中的氧,具有还原性,作还原剂;二氧化硅失去了氧,发生了还原反应,故填:SiO2;
(2)我国具有丰富的海洋资源,海水中的盐类物质中氯化钠含量最高,因此含量最多的阳离子是Na+,故填:Na+。
(3)ClO2中氧元素化合价是﹣2,根据化合物中元素化合价代数和为零可知,氯元素的化合价为+4价,故填:+4。
(4)超氧化钾(KO2)能迅速与水反应放出氧气,同时生成氢氧化钾(KOH)以及种用于实验室制取氧气的物质,实验室制取氧气的物质是过氧化氢,其反应的化学方程式为:2KO2+2H2O=2KOH+H2O2+O2↑。
【分析】(1)根据失氧物质发生还原反应分析;
(2)根据海水中钠离子含量最高分析;
(3)根据化合物中元素化合价代数和为0分析;
(4)根据超氧化钾与水反应生成氧气、氢氧化钾、过氧化氢分析。
17.【答案】解:设需要碳酸钙的质量为x.
CaCO3 CaO+ CO2↑
100
56
x
11.2t
= ,x=20t
答:需要碳酸钙的质量为20t
【解析】【分析】由氧化钙的质量根据碳酸钙分解的化学方程式可以计算出碳酸钙的质量.
1 / 1
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
