河南省中牟县第二高级中学高中化学鲁科版选修四3-2-5弱电解质的电离,盐类的水解课件(共12张PPT)
文档属性
| 名称 | 河南省中牟县第二高级中学高中化学鲁科版选修四3-2-5弱电解质的电离,盐类的水解课件(共12张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 282.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-09-29 00:00:00 | ||
图片预览




文档简介
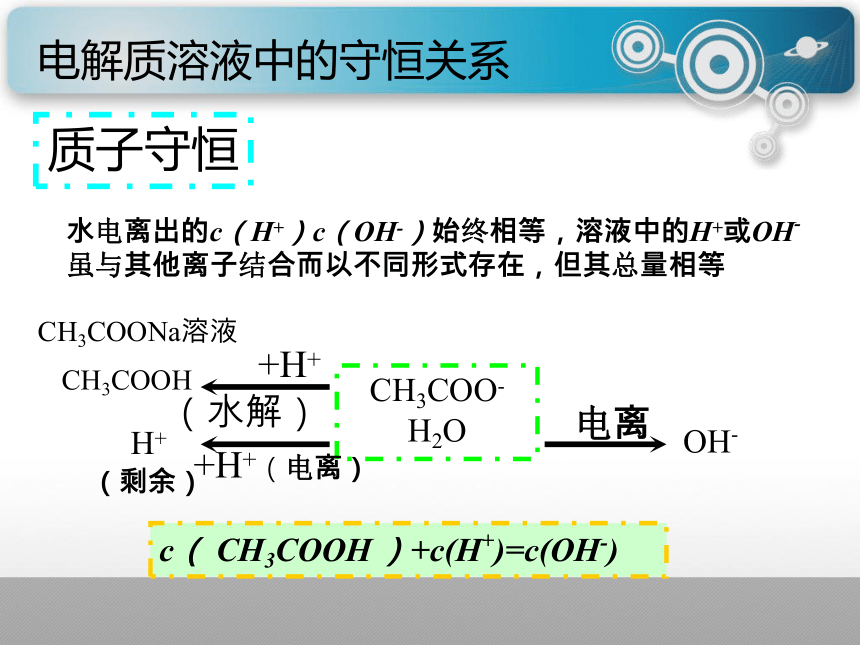
课件12张PPT。四、电解质溶液中的守恒关系电荷守恒物料守恒(原子守恒)三个守恒质子守恒电解质溶液中的守恒关系电荷守恒电解质溶液中,阳离子所带电荷总数一定等于阴离子所带电荷总数。NaHCO3溶液c(Na+)+c(H+)=c(HCO-3)+c(OH-)+2c(CO32-)K2S溶液c(K+)+c(H+)=c(HS-)+c(OH-)+2c(S2-)金太阳新课标资源网课件大赛参赛课件 电解质溶液中的守恒关系物料守恒在电解质溶液中,由于某些离子能够水解,离子种类变多,但是其中所含原子的总数始终不变。NaHCO3溶液c(Na+)=c(HCO-3)+c(H2CO3)+c(CO32-)K2S溶液c(K+)=2[c(HS-)+c(H2S)+c(S2-)]n(Na)=n(C)n(K)=2n(S)金太阳新课标资源网课件大赛参赛课件 电解质溶液中的守恒关系质子守恒水电离出的c(H+)c(OH-)始终相等,溶液中的H+或OH-虽与其他离子结合而以不同形式存在,但其总量相等CH3COONa溶液CH3COO-
H2O+H+(水解)CH3COOH+H+(电离)H+(剩余)电离OH-c( CH3COOH )+c(H+)=c(OH-)电解质溶液中的守恒关系质子守恒水电离出的c(H+)c(OH-)始终相等,溶液中的H+或OH-虽与其他离子结合而以不同形式存在,但其总量相等K2S溶液S2-(水解)
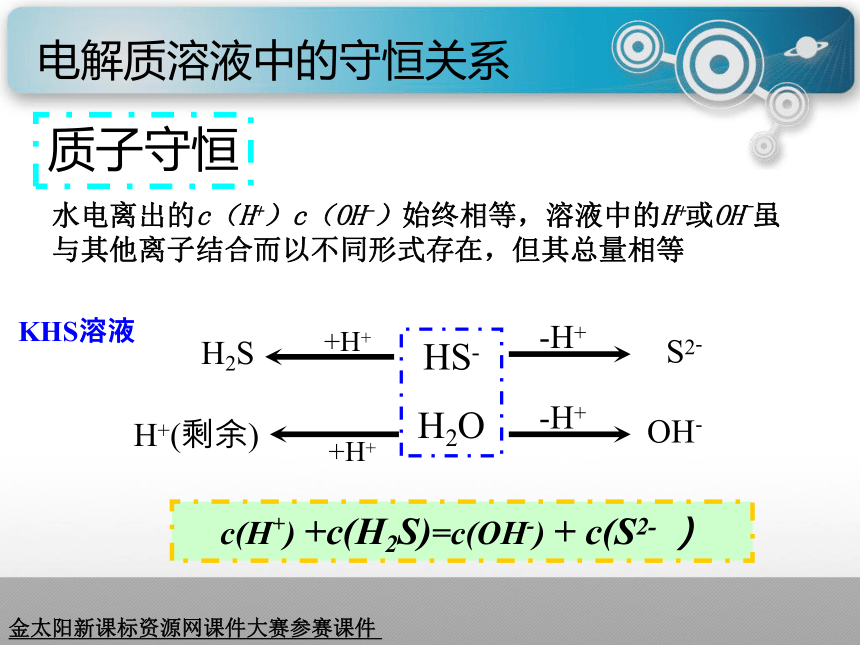
H2O(电离)+H+HS-+H+H+(剩余)电离OH-+2H+H2Sc(HS- )+c(H+) +2c(H2S)=c(OH-)金太阳新课标资源网课件大赛参赛课件 电解质溶液中的守恒关系质子守恒水电离出的c(H+)c(OH-)始终相等,溶液中的H+或OH-虽与其他离子结合而以不同形式存在,但其总量相等KHS溶液HS-
H2O+H+H+(剩余)-H+OH-+H+H2S-H+S2-c(H+) +c(H2S)=c(OH-) + c(S2- )金太阳新课标资源网课件大赛参赛课件 电解质溶液中的守恒关系质子守恒通过联立电荷守恒和原子守恒,消去与得到和给出质子无关的粒子K2S溶液联立,消去K+得c(HS- )+c(H+) +2c(H2S)=c(OH-)电解质溶液中的守恒关系质子守恒通过联立电荷守恒和原子守恒,消去与得到和给出质子无关的粒子NaHS溶液联立,消去Na+得c(H+) +c(H2S)=c(OH-) + c(S2- )五、比较盐溶液中的离子浓度大小如:氯化铵溶液中C(Cl-)>C(NH4+)>C(H+)>C(OH-)注意: 盐溶液中离子种类多少的判断,需考虑到盐类的水解如:Na2S溶液中离子浓度比较:
KAl(SO4)2 溶液中离子浓度比较:C(Na+)>C(S2-)>C(OH-)>C(HS-)>C(H+)
C(SO42-)>C(K+)>C(Al3+)>C(H+)>C(OH-)Na2CO3溶液中,各离子浓度大小顺序为______________________学以致用NaHCO3溶液中,各离子浓度大小顺序为______________________金太阳新课标资源网课件大赛参赛课件 谢谢关注!!金太阳新课标资源网课件大赛参赛课件
H2O+H+(水解)CH3COOH+H+(电离)H+(剩余)电离OH-c( CH3COOH )+c(H+)=c(OH-)电解质溶液中的守恒关系质子守恒水电离出的c(H+)c(OH-)始终相等,溶液中的H+或OH-虽与其他离子结合而以不同形式存在,但其总量相等K2S溶液S2-(水解)
H2O(电离)+H+HS-+H+H+(剩余)电离OH-+2H+H2Sc(HS- )+c(H+) +2c(H2S)=c(OH-)金太阳新课标资源网课件大赛参赛课件 电解质溶液中的守恒关系质子守恒水电离出的c(H+)c(OH-)始终相等,溶液中的H+或OH-虽与其他离子结合而以不同形式存在,但其总量相等KHS溶液HS-
H2O+H+H+(剩余)-H+OH-+H+H2S-H+S2-c(H+) +c(H2S)=c(OH-) + c(S2- )金太阳新课标资源网课件大赛参赛课件 电解质溶液中的守恒关系质子守恒通过联立电荷守恒和原子守恒,消去与得到和给出质子无关的粒子K2S溶液联立,消去K+得c(HS- )+c(H+) +2c(H2S)=c(OH-)电解质溶液中的守恒关系质子守恒通过联立电荷守恒和原子守恒,消去与得到和给出质子无关的粒子NaHS溶液联立,消去Na+得c(H+) +c(H2S)=c(OH-) + c(S2- )五、比较盐溶液中的离子浓度大小如:氯化铵溶液中C(Cl-)>C(NH4+)>C(H+)>C(OH-)注意: 盐溶液中离子种类多少的判断,需考虑到盐类的水解如:Na2S溶液中离子浓度比较:
KAl(SO4)2 溶液中离子浓度比较:C(Na+)>C(S2-)>C(OH-)>C(HS-)>C(H+)
C(SO42-)>C(K+)>C(Al3+)>C(H+)>C(OH-)Na2CO3溶液中,各离子浓度大小顺序为______________________学以致用NaHCO3溶液中,各离子浓度大小顺序为______________________金太阳新课标资源网课件大赛参赛课件 谢谢关注!!金太阳新课标资源网课件大赛参赛课件
