课题4 化学式与化合价(30张PPT)
文档属性
| 名称 | 课题4 化学式与化合价(30张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 137.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-09-29 00:00:00 | ||
图片预览










文档简介
课件30张PPT。
化学式与化合价大公中学 张晓华开始学习-化合价: 注意点:
1、化合价有正价和负价
(1)氧元素通常显-2价,氢元素通常显+1价
(2)金属元素显正价,非金属元素显负价-- “金正, 非金属负”
(3)一些元素在不同的物质里有不同的化合价
2、在化合物里正负化合物的代数和为0
3、单质里,元素的化合价为0元素的化合价是元素的原子在形成 化合物时表现出来的一种化学性质顺口溜:
一价钠钾银氢;二价镁钙铜锌钡;
三铝四硅记在心;
单质都为0; 永远也不变。二三铁(正二价叫亚铁)
二四碳,二四六硫要记全。
氯负一.氧硫负二最常见。说明:
?按谐音记:
那家迎亲
没盖红新被 ?在氯化物
和硫化物中
氯和硫分别
显负一价和
负二价。思考二、什么是化学式 注意:每种纯净物的组成是固定不变的。
所以表示每种物质组成的化学式只有一个这种用元素符号表示物质组成的式子。化学式的意义:
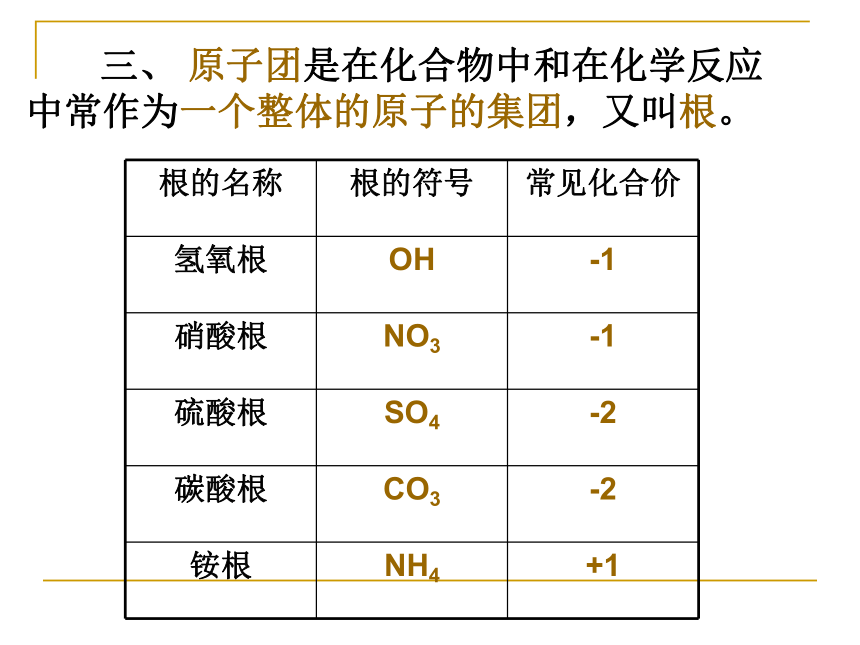
以H2O为例,它表示了几种意义?1、表示这种物质2、表示水由氢元素和氧元素组成3、表示一个水分子4、表示一个水分子中含一个氧原子和两个氢原子H2O思考:一个H2O中分子含有一个H分子和一个O原子。这句话是否正确,为什么?讨论: H、2H、 H2、2H2O各具有什么意义? 三、 原子团是在化合物中和在化学反应中常作为一个整体的原子的集团,又叫根。三、化学式的写法1、单质的写法: 稀有气体和金属是由原子直接构成,及常温下为固态的大多数非金属,单质直接由元素 符号来表示 .如:He,Ne, Fe,Cu,S,P
2、化合物的写法 (1)这种物质由那些元素 组成 (2)化学式时元素 排列顺序的规定 “金左,非 右” “氧在后” 。 (3)化学元素式中各元素的原子个数比是多少(4)表示原子数的“小写数字”的书写部位四、化学式的读法:
一般从右向左读作“某化某”有时还要读出化学式中各种元素的原子个数
(1) 氧化物:如HgO、SO2 、Fe3O4,读作“氧化某”,.有时还要读出化学式中各种元素的原子个数,如Fe3O4读作四氧化三铁 “几氧化几某” 。
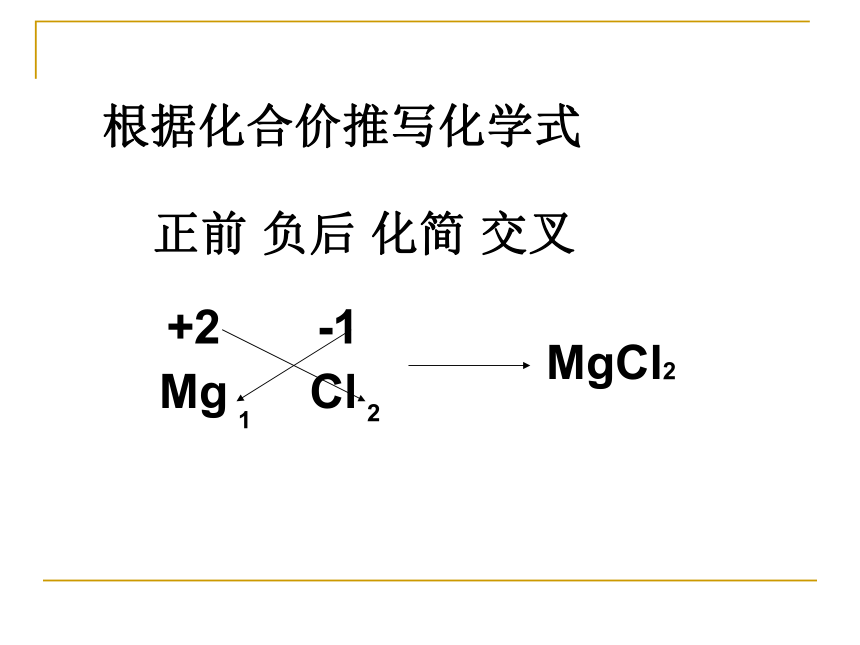
(2) 金属与非金属组成 的化合物如:如NaCl 、 KCl 、 ZnS 读作“某化某” 如ZnS读作硫化锌。(3) 其它如: P2O5 读作五氧化二磷, BaCl2读作氯化钡 ,H2O2读作过氧化氢 , KClO3读作氯酸钾根据化合价推写化学式正前 负后 化简 交叉Mg+2Cl-121MgCl2化学式的书写 (1)化合物的化学式 例1 写出氧化铝的化学式
(1)定位:确定元素或原子团的顺序。正左负右Al O(2)标价:正确地在各元素或原子团的
上方标出化合价。Al O+3 -2(3)交叉约简:将化合价的绝对值交叉写
在对方元素或原子团的右下方 。+3 -2
Al O 23交叉约简:将化合价的绝对值交叉写在对方元素或原子团的右下方,
能约简的要约为最简约数。原子或原子团的个数为1时,通常1省去不写。原子团在2个或2个以上时,应加上括号。
例2? 已知铁的化合价为+3,O的化合价为-2价,求氧化铁的化学式。 (1)定位:正左负右Fe O(2)标价+3 -2(3)交叉23(4)根据化合物中各元素的化合价的
代数和为零的原则,检查所写的化
学式是否正确。+3×2+(-2) ×3=0正确试一试 标出下列物质中划线
元素的化合价O2 H2O NaCl H2S 0 -2 +1 -2KClO3 H2SO4 KMnO4 +5 +6 +7 Ca(OH)2 +2练一练: 标出下列划线元素的化合价Na 2O BaCO3 Al2O3
H2SO4 Cu(OH)2 KNO3
NH4NO3 Fe2(SO4)3 +1 +4 +3
+6 +2 +5
-3 +5 +3(一)、根据化学式确定元素的化合价: 1、标出化学式中各元素的化合价例1、标出下列物质中各元素的化合价:
氯化锌 金属锌 氢氧化钠 ZnCl2 Zn NaOH+2-10+1-2+1注意:化合价标在相应元素符号的正上方课堂练习:标出下列物质中各元素的化合价:
(1)MgO (2)K20 (3) H20 (4)Ca(OH)2+2 -2+1-2+1-2+2 -2+1六、化合价的运用:(二)确定物质中某元素的化合价例2、试确定氯酸钾中氯元素的化合价【思路】先写出化学式KClO3设未知数解:设KClO3中Cl的化合价为X列等式(正负总价和为0)+1+X+(-2)×3=0解答 X=+5
答:氯酸钾中氯元素的化合价为+5+ 5六、化合价的运用:(三)、根据化合价确定元素的化学式:例3、已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式【思路】(1)先写元素符号(正前负后)(2)标出各元素的化合价(正上)(3)把化合价数值化为最简(4)把化简后的数字交叉写出
(求最小公倍数)P OP O+ 3 -2P OP2O 3P OP O+ 5 -2P O+ 5 -2P2O5省略+ 3 -2+ 3 -2P2O3P2O 5+ 5 -21、说出下列物质中硫元素的化合价
H2S S H2SO3 H2SO4
2、试确定下列化合物中原子团的化合价
KOH Mg(NO3)2 BaSO4 Na2CO3 Na3PO4-20+4+6-1-1-2-2-3想一想原子团的化合价都是负价吗?不是,如 NH4+13、填空:
下列化学式如有错误请改在横线上:
氧化钙Ca2O2 ______, 氯化铁 FeCl2 ______,
氯化锌 ZnCl ______, 硫化铝 Al3S2 ______,
氢氧化铜CuOH _____, 氯化钠ClNa ______,CaOFeCl3ZnCl2Al2S3Cu(OH)2NaCl1、已知在H3RO4中,氢元素为+1价,氧为-2价,则其中R的化合价为( )
A、+3 B、+4 C、+5 D、+6
2、下列化合物中,氮元素为+5价的是( )
A、N0 B、NO2 C、HNO2 D、KNO3
3、元素R的氧化物的化学式为R2O3,则R元素与OH-组成的物质的化学式为( )
A、ROH B、R(OH)2 C、R(OH)3 D、R(OH)4CDC六. 化合价的运用1. 根据元素化合价推出实际存在的物质的化学式(1). 排列元素 符号------正价在前负价在后(2). 确定原子个数-------求两种元素正负化合价绝对值的最小公倍数(3). 写出化学式----------把原子个数写在各元素 符号的右下方(4). 检查化学式----------依据: 化合价代数和为0 例.写出氧化铝的化学式2. 根据化学式判断元素的化合价 求 MnO2, FeO,Fe2O3, NH4NO3中 Mn , Fe , N 三种元素的
化合价 依据 :化合物里正负化合价代数和为0结论:1.同种元素 在不同的化合物里有不同的化合价
2.同一化合物里同种元素 也可能有不同的化合价
化学式与化合价开始学习 相对分子质量的有关计算八、相对分子质量思考:原子的质量很小,故我们采用相对原子质量,那么由原子构成的分子,质量仍然很小,又如何表示呢?
化学式中各原子的相对原子质量的总和,就是相对分子质量 (符号为Mr) 相对分子的运用:
1、根据化学式计算相对分子质量
例1、 求 O2、 H2O、 KMnO4的相对分子质量
练习1、求Fe3O4、CO(NH2)2的相对分子质量相对分子质量的运用2、计算物质组成元素的质量 比
各元素之间的质量比=各原子的相对原子质量总和之比
例2、MnO2中锰元素和氧元素的质量比等于
练习2:
1、 H2O2、 Cu(OH)2中各元素的质量比?
2、NH4NO3中各元素的质量比?
3.求物质中某元素的质量 分数练习3、计算化肥硝酸铵中(NH4NO3)中氮元素的质量分数例3、H2O2中氢元素的质量分数? 4、一定量的某物质中含有某元素的质量
元素的质量=某物质的质量×某元素的质量分数
例4、求18gH2O中氢元素的质量?
练习4、某农田里的作物需N施含35kg的氮肥,如果施用的氮肥是尿素( CO(NH2)2 ),则需要多少kg
课堂练习
1. 说明下列化学元素用语各表示
(1)H (2)2H (3)H2 (4)2H2 (5)H2O (6)2H2O 2、海洛因是政府明令禁止的毒品,其化学式C21H23NO5,它由 种元素组成 ,每个海洛因中共有________个原子C.H.O.N共4种共有503.某化合物的化学式为HnROm,其中R的化合价为( )
A 、+(m-n) B 、+(2m-n)
C 、+(n-m) D、+(2n-m)B 例8、燃放爆竹产生一种污染物,其元素的质量比为l:1,该污染物是( ) ?? A、 H2S? B、CO?
C、S02 D、N02 例9、甲醛(化学式为CH2O)是室内装潢时的主要污染物之一,下列说法正确的是( ) A. 甲醛是由碳、氢、氧三种元素组成 B. 甲醛是由碳原子和水分子构成 C.甲醛分子是由 碳原子、氢气分子、氧原子构成 D. 甲醛是由一个碳元素、二个氢元素、一个氧元素 组成 CA4、综合应用:某物质的化学式为HnRO2n-1,它的相对分子质量为M,则该化合物中R 元素的化合价为________,R 元素的相对原子质量为_________ (O-16 H-1)+(3n-2)M-33n+16【解法 】:解:(1)设R的化合价为x
(+1) ·n+x+(-2) ·(2n-1)=0
x=+(3n-2)
(2)M-1×n-16×(2n-1)
=M-33n+16
化学式与化合价大公中学 张晓华开始学习-化合价: 注意点:
1、化合价有正价和负价
(1)氧元素通常显-2价,氢元素通常显+1价
(2)金属元素显正价,非金属元素显负价-- “金正, 非金属负”
(3)一些元素在不同的物质里有不同的化合价
2、在化合物里正负化合物的代数和为0
3、单质里,元素的化合价为0元素的化合价是元素的原子在形成 化合物时表现出来的一种化学性质顺口溜:
一价钠钾银氢;二价镁钙铜锌钡;
三铝四硅记在心;
单质都为0; 永远也不变。二三铁(正二价叫亚铁)
二四碳,二四六硫要记全。
氯负一.氧硫负二最常见。说明:
?按谐音记:
那家迎亲
没盖红新被 ?在氯化物
和硫化物中
氯和硫分别
显负一价和
负二价。思考二、什么是化学式 注意:每种纯净物的组成是固定不变的。
所以表示每种物质组成的化学式只有一个这种用元素符号表示物质组成的式子。化学式的意义:
以H2O为例,它表示了几种意义?1、表示这种物质2、表示水由氢元素和氧元素组成3、表示一个水分子4、表示一个水分子中含一个氧原子和两个氢原子H2O思考:一个H2O中分子含有一个H分子和一个O原子。这句话是否正确,为什么?讨论: H、2H、 H2、2H2O各具有什么意义? 三、 原子团是在化合物中和在化学反应中常作为一个整体的原子的集团,又叫根。三、化学式的写法1、单质的写法: 稀有气体和金属是由原子直接构成,及常温下为固态的大多数非金属,单质直接由元素 符号来表示 .如:He,Ne, Fe,Cu,S,P
2、化合物的写法 (1)这种物质由那些元素 组成 (2)化学式时元素 排列顺序的规定 “金左,非 右” “氧在后” 。 (3)化学元素式中各元素的原子个数比是多少(4)表示原子数的“小写数字”的书写部位四、化学式的读法:
一般从右向左读作“某化某”有时还要读出化学式中各种元素的原子个数
(1) 氧化物:如HgO、SO2 、Fe3O4,读作“氧化某”,.有时还要读出化学式中各种元素的原子个数,如Fe3O4读作四氧化三铁 “几氧化几某” 。
(2) 金属与非金属组成 的化合物如:如NaCl 、 KCl 、 ZnS 读作“某化某” 如ZnS读作硫化锌。(3) 其它如: P2O5 读作五氧化二磷, BaCl2读作氯化钡 ,H2O2读作过氧化氢 , KClO3读作氯酸钾根据化合价推写化学式正前 负后 化简 交叉Mg+2Cl-121MgCl2化学式的书写 (1)化合物的化学式 例1 写出氧化铝的化学式
(1)定位:确定元素或原子团的顺序。正左负右Al O(2)标价:正确地在各元素或原子团的
上方标出化合价。Al O+3 -2(3)交叉约简:将化合价的绝对值交叉写
在对方元素或原子团的右下方 。+3 -2
Al O 23交叉约简:将化合价的绝对值交叉写在对方元素或原子团的右下方,
能约简的要约为最简约数。原子或原子团的个数为1时,通常1省去不写。原子团在2个或2个以上时,应加上括号。
例2? 已知铁的化合价为+3,O的化合价为-2价,求氧化铁的化学式。 (1)定位:正左负右Fe O(2)标价+3 -2(3)交叉23(4)根据化合物中各元素的化合价的
代数和为零的原则,检查所写的化
学式是否正确。+3×2+(-2) ×3=0正确试一试 标出下列物质中划线
元素的化合价O2 H2O NaCl H2S 0 -2 +1 -2KClO3 H2SO4 KMnO4 +5 +6 +7 Ca(OH)2 +2练一练: 标出下列划线元素的化合价Na 2O BaCO3 Al2O3
H2SO4 Cu(OH)2 KNO3
NH4NO3 Fe2(SO4)3 +1 +4 +3
+6 +2 +5
-3 +5 +3(一)、根据化学式确定元素的化合价: 1、标出化学式中各元素的化合价例1、标出下列物质中各元素的化合价:
氯化锌 金属锌 氢氧化钠 ZnCl2 Zn NaOH+2-10+1-2+1注意:化合价标在相应元素符号的正上方课堂练习:标出下列物质中各元素的化合价:
(1)MgO (2)K20 (3) H20 (4)Ca(OH)2+2 -2+1-2+1-2+2 -2+1六、化合价的运用:(二)确定物质中某元素的化合价例2、试确定氯酸钾中氯元素的化合价【思路】先写出化学式KClO3设未知数解:设KClO3中Cl的化合价为X列等式(正负总价和为0)+1+X+(-2)×3=0解答 X=+5
答:氯酸钾中氯元素的化合价为+5+ 5六、化合价的运用:(三)、根据化合价确定元素的化学式:例3、已知磷元素有两种氧化物,其中磷的化合价分别为+3和+5,写出这两种磷的氧化物的化学式【思路】(1)先写元素符号(正前负后)(2)标出各元素的化合价(正上)(3)把化合价数值化为最简(4)把化简后的数字交叉写出
(求最小公倍数)P OP O+ 3 -2P OP2O 3P OP O+ 5 -2P O+ 5 -2P2O5省略+ 3 -2+ 3 -2P2O3P2O 5+ 5 -21、说出下列物质中硫元素的化合价
H2S S H2SO3 H2SO4
2、试确定下列化合物中原子团的化合价
KOH Mg(NO3)2 BaSO4 Na2CO3 Na3PO4-20+4+6-1-1-2-2-3想一想原子团的化合价都是负价吗?不是,如 NH4+13、填空:
下列化学式如有错误请改在横线上:
氧化钙Ca2O2 ______, 氯化铁 FeCl2 ______,
氯化锌 ZnCl ______, 硫化铝 Al3S2 ______,
氢氧化铜CuOH _____, 氯化钠ClNa ______,CaOFeCl3ZnCl2Al2S3Cu(OH)2NaCl1、已知在H3RO4中,氢元素为+1价,氧为-2价,则其中R的化合价为( )
A、+3 B、+4 C、+5 D、+6
2、下列化合物中,氮元素为+5价的是( )
A、N0 B、NO2 C、HNO2 D、KNO3
3、元素R的氧化物的化学式为R2O3,则R元素与OH-组成的物质的化学式为( )
A、ROH B、R(OH)2 C、R(OH)3 D、R(OH)4CDC六. 化合价的运用1. 根据元素化合价推出实际存在的物质的化学式(1). 排列元素 符号------正价在前负价在后(2). 确定原子个数-------求两种元素正负化合价绝对值的最小公倍数(3). 写出化学式----------把原子个数写在各元素 符号的右下方(4). 检查化学式----------依据: 化合价代数和为0 例.写出氧化铝的化学式2. 根据化学式判断元素的化合价 求 MnO2, FeO,Fe2O3, NH4NO3中 Mn , Fe , N 三种元素的
化合价 依据 :化合物里正负化合价代数和为0结论:1.同种元素 在不同的化合物里有不同的化合价
2.同一化合物里同种元素 也可能有不同的化合价
化学式与化合价开始学习 相对分子质量的有关计算八、相对分子质量思考:原子的质量很小,故我们采用相对原子质量,那么由原子构成的分子,质量仍然很小,又如何表示呢?
化学式中各原子的相对原子质量的总和,就是相对分子质量 (符号为Mr) 相对分子的运用:
1、根据化学式计算相对分子质量
例1、 求 O2、 H2O、 KMnO4的相对分子质量
练习1、求Fe3O4、CO(NH2)2的相对分子质量相对分子质量的运用2、计算物质组成元素的质量 比
各元素之间的质量比=各原子的相对原子质量总和之比
例2、MnO2中锰元素和氧元素的质量比等于
练习2:
1、 H2O2、 Cu(OH)2中各元素的质量比?
2、NH4NO3中各元素的质量比?
3.求物质中某元素的质量 分数练习3、计算化肥硝酸铵中(NH4NO3)中氮元素的质量分数例3、H2O2中氢元素的质量分数? 4、一定量的某物质中含有某元素的质量
元素的质量=某物质的质量×某元素的质量分数
例4、求18gH2O中氢元素的质量?
练习4、某农田里的作物需N施含35kg的氮肥,如果施用的氮肥是尿素( CO(NH2)2 ),则需要多少kg
课堂练习
1. 说明下列化学元素用语各表示
(1)H (2)2H (3)H2 (4)2H2 (5)H2O (6)2H2O 2、海洛因是政府明令禁止的毒品,其化学式C21H23NO5,它由 种元素组成 ,每个海洛因中共有________个原子C.H.O.N共4种共有503.某化合物的化学式为HnROm,其中R的化合价为( )
A 、+(m-n) B 、+(2m-n)
C 、+(n-m) D、+(2n-m)B 例8、燃放爆竹产生一种污染物,其元素的质量比为l:1,该污染物是( ) ?? A、 H2S? B、CO?
C、S02 D、N02 例9、甲醛(化学式为CH2O)是室内装潢时的主要污染物之一,下列说法正确的是( ) A. 甲醛是由碳、氢、氧三种元素组成 B. 甲醛是由碳原子和水分子构成 C.甲醛分子是由 碳原子、氢气分子、氧原子构成 D. 甲醛是由一个碳元素、二个氢元素、一个氧元素 组成 CA4、综合应用:某物质的化学式为HnRO2n-1,它的相对分子质量为M,则该化合物中R 元素的化合价为________,R 元素的相对原子质量为_________ (O-16 H-1)+(3n-2)M-33n+16【解法 】:解:(1)设R的化合价为x
(+1) ·n+x+(-2) ·(2n-1)=0
x=+(3n-2)
(2)M-1×n-16×(2n-1)
=M-33n+16
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
