从“定量”的视角再看—碳酸钠和碳酸氢钠 课件 (共15张PPT)2024届高考二轮专题复习
文档属性
| 名称 | 从“定量”的视角再看—碳酸钠和碳酸氢钠 课件 (共15张PPT)2024届高考二轮专题复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 52.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-29 00:00:00 | ||
图片预览





文档简介
(共15张PPT)
从“定量”的视角再看
Na2CO3、NaHCO3
小苏打洗洁精
小苏打牙膏
干粉灭火器
制试剂
制肥皂
制玻璃
软水剂
造纸
苏氏兄弟
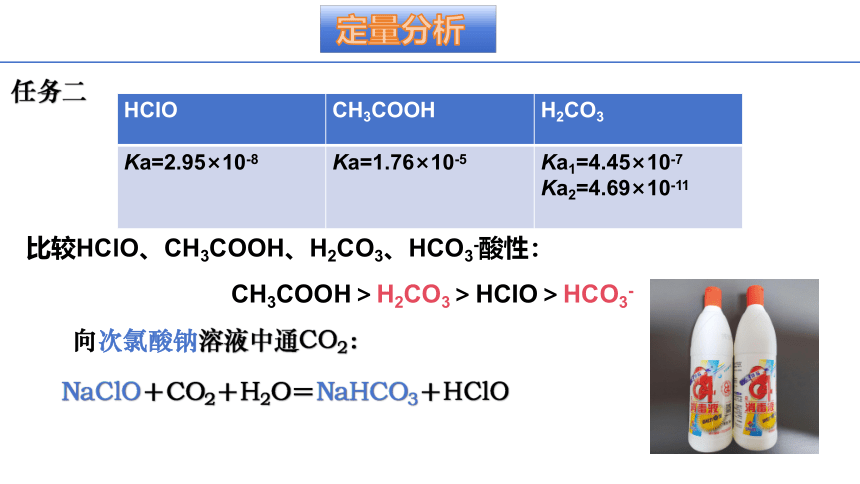
HCIO CH3COOH H2CO3
Ka=2.95×10-8 Ka=1.76×10-5 Ka1=4.45×10-7
Ka2=4.69×10-11
比较HClO、CH3COOH、H2CO3、HCO3-酸性:
CH3COOH>H2CO3>HCIO>HCO3-
向次氯酸钠溶液中通CO2:
NaClO+CO2+H2O=NaHCO3+HClO
任务二
定量分析
Ksp(CaCO3)= 2.8×10-9
Ka(HClO)=2.95×10-8
Ka1(H2CO3)=4.45×10-7 Ka2(H2CO3)=4.69×10-11
Ca(ClO)2+CO2+H2O=2HClO+CaCO3
Ca(ClO)2+2CO2+2H2O=2HClO+Ca(HCO3)2
通过计算比较两个反应K值的大小。
向次氯酸钙溶液中通CO2:
定量分析
HCO3-和Ca2+能共存吗?
探究实验1:向NaHCO3中滴加CaCl2溶液,观察实验现象。
NaHCO3 2ml 1mol·L-1
CaCl2 4~5滴 1mol·L-1
实验现象
NaHCO3 2ml 1mol·L-1
CaCI2 4~5滴 1mol·L-1
实验现象 白色沉淀并有气体产生
分析原因:
1、产生的沉淀可能是什么?为什么?
Ksp(Ca(OH)2)= c(Ca2+)c2(OH-)≈10-6
c(Ca2+)≈0.1mol·L-1
定性分析
若要形成沉淀,则c(OH-)≥10-2.5,pH≥11.5。
饱和碳酸氢钠的pH为8.32。因此不会有氢氧化钙沉淀产生。
产生的气体应该是什么?
写出碳酸氢钠与氯化钙反应的离子方程式。
HCO3-+H+ H2O+CO2↑
分析原因:
NaHCO3 2ml 1mol·L-1
CaCI2 4~5滴 1mol·L-1
实验现象 白色沉淀并有气体产生
定性分析
根据相关平衡常数,写出该反应的化学平衡常数表达式K并计算数量级。
Ksp(CaCO3)= 2.8×10-9 Ka1(H2CO3)=4.45×10-7 Ka2(H2CO3)=4.69×10-11
K
定量分析
1、 将FeSO4与NaHCO3溶液混合发生“除铁”反应的离子方程式为
_________________________。
2、以FeSO4溶液与NaCO3溶液制备FeCO3沉淀,反应物的滴加顺序较合理的是 ( )
A. 将FeSO4溶液滴加到NaCO3溶液中
B. 将NaCO3溶液滴加到FeSO4溶液中
破题模型:与量有关的滴加顺序问题
应用体验
HCO3-沉淀金属阳离子的通式:
金属阳离子+HCO3-=难溶碳酸盐↓+H2O+CO2↑
★ 归纳总结
提出问题,定性分析
查找资料,收集数据
定量分析,解决问题
Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀。
(1)下列关于步骤④的说法正确的是_____(填字母)。
A.过滤后的滤液中仍含有较多Ce3+,需要将滤液循环以提高产率
B.可以用Na2CO3溶液代替NH4HCO3溶液,不影响产品纯度
C.过滤时选择减压过滤能够大大提高过滤效率
D.该步骤发生的反应是2Ce3++6HCO3-=Ce2(CO3)3↓+3CO2↑+3H2O
CD
1、
2、(2023江苏高考真题)室温下,用含少量 Mg2+的 MnSO4溶液制备 MnCO3的过程如题图所示。已知Ksp(MgF2)=5.2×10-11,Ka(HF)=6.3×10-4。下列说法正确的是( )
C
3、空气中CO2含量的控制和CO2资源利用具有重要意义。
4、
BD
从“定量”的视角再看
Na2CO3、NaHCO3
小苏打洗洁精
小苏打牙膏
干粉灭火器
制试剂
制肥皂
制玻璃
软水剂
造纸
苏氏兄弟
HCIO CH3COOH H2CO3
Ka=2.95×10-8 Ka=1.76×10-5 Ka1=4.45×10-7
Ka2=4.69×10-11
比较HClO、CH3COOH、H2CO3、HCO3-酸性:
CH3COOH>H2CO3>HCIO>HCO3-
向次氯酸钠溶液中通CO2:
NaClO+CO2+H2O=NaHCO3+HClO
任务二
定量分析
Ksp(CaCO3)= 2.8×10-9
Ka(HClO)=2.95×10-8
Ka1(H2CO3)=4.45×10-7 Ka2(H2CO3)=4.69×10-11
Ca(ClO)2+CO2+H2O=2HClO+CaCO3
Ca(ClO)2+2CO2+2H2O=2HClO+Ca(HCO3)2
通过计算比较两个反应K值的大小。
向次氯酸钙溶液中通CO2:
定量分析
HCO3-和Ca2+能共存吗?
探究实验1:向NaHCO3中滴加CaCl2溶液,观察实验现象。
NaHCO3 2ml 1mol·L-1
CaCl2 4~5滴 1mol·L-1
实验现象
NaHCO3 2ml 1mol·L-1
CaCI2 4~5滴 1mol·L-1
实验现象 白色沉淀并有气体产生
分析原因:
1、产生的沉淀可能是什么?为什么?
Ksp(Ca(OH)2)= c(Ca2+)c2(OH-)≈10-6
c(Ca2+)≈0.1mol·L-1
定性分析
若要形成沉淀,则c(OH-)≥10-2.5,pH≥11.5。
饱和碳酸氢钠的pH为8.32。因此不会有氢氧化钙沉淀产生。
产生的气体应该是什么?
写出碳酸氢钠与氯化钙反应的离子方程式。
HCO3-+H+ H2O+CO2↑
分析原因:
NaHCO3 2ml 1mol·L-1
CaCI2 4~5滴 1mol·L-1
实验现象 白色沉淀并有气体产生
定性分析
根据相关平衡常数,写出该反应的化学平衡常数表达式K并计算数量级。
Ksp(CaCO3)= 2.8×10-9 Ka1(H2CO3)=4.45×10-7 Ka2(H2CO3)=4.69×10-11
K
定量分析
1、 将FeSO4与NaHCO3溶液混合发生“除铁”反应的离子方程式为
_________________________。
2、以FeSO4溶液与NaCO3溶液制备FeCO3沉淀,反应物的滴加顺序较合理的是 ( )
A. 将FeSO4溶液滴加到NaCO3溶液中
B. 将NaCO3溶液滴加到FeSO4溶液中
破题模型:与量有关的滴加顺序问题
应用体验
HCO3-沉淀金属阳离子的通式:
金属阳离子+HCO3-=难溶碳酸盐↓+H2O+CO2↑
★ 归纳总结
提出问题,定性分析
查找资料,收集数据
定量分析,解决问题
Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀。
(1)下列关于步骤④的说法正确的是_____(填字母)。
A.过滤后的滤液中仍含有较多Ce3+,需要将滤液循环以提高产率
B.可以用Na2CO3溶液代替NH4HCO3溶液,不影响产品纯度
C.过滤时选择减压过滤能够大大提高过滤效率
D.该步骤发生的反应是2Ce3++6HCO3-=Ce2(CO3)3↓+3CO2↑+3H2O
CD
1、
2、(2023江苏高考真题)室温下,用含少量 Mg2+的 MnSO4溶液制备 MnCO3的过程如题图所示。已知Ksp(MgF2)=5.2×10-11,Ka(HF)=6.3×10-4。下列说法正确的是( )
C
3、空气中CO2含量的控制和CO2资源利用具有重要意义。
4、
BD
同课章节目录
