化学人教版(2019)选择性必修3 3.4.2羧酸衍生物(共23张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.4.2羧酸衍生物(共23张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-29 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
1、认识羧酸衍生物(酯、油脂、酰胺)和胺的结构特点及应用。
2、通过探究乙酸乙酯的水解,熟悉控制变量法的应用,体验科学探究的一般过程。
羧酸衍生物的结构特点和主要化学性质。
羧酸衍生物的结构特点和主要化学性质。
丁酸乙酯
戊酸戊酯
生活中的酯
CH3(CH2)3 ─ CO ─(CH2)4CH3
O
CH3(CH2)2 ─ CO ─ CH2CH3
O
邻氨基苯甲酸甲酯
─ COCH
─ NH2
O
1、羧酸衍生物:
3、酯的结构通式:
R1:只能是烃基
R(H) ─ C ─ O ─ R1
O
4、饱和一元酯的分子通式为:
CnH2nO2 (n≥2)
一、酯
官能团:酯基
─ C ─ O ─
O
简写为─ COO ─
与饱和一元羧酸互为同分异构体
2、酯:
羧酸分子羧基中的 ─ OH被其他原子或原子团取代后的产物。
酯是羧酸分子羧基中的 ─ OH被 ─ OR′取代后的产物。
5、酯的命名——根据反应物称为“某酸某酯”
丙酸乙酯
CH3CH2COCH2CH3
O
乙酸乙酯
CH3COCH2CH3
O
COOCH2CH3
COOCH2CH3
乙二酸二乙酯
如:
一、酯
酸 + 醇 = 酯 + 水
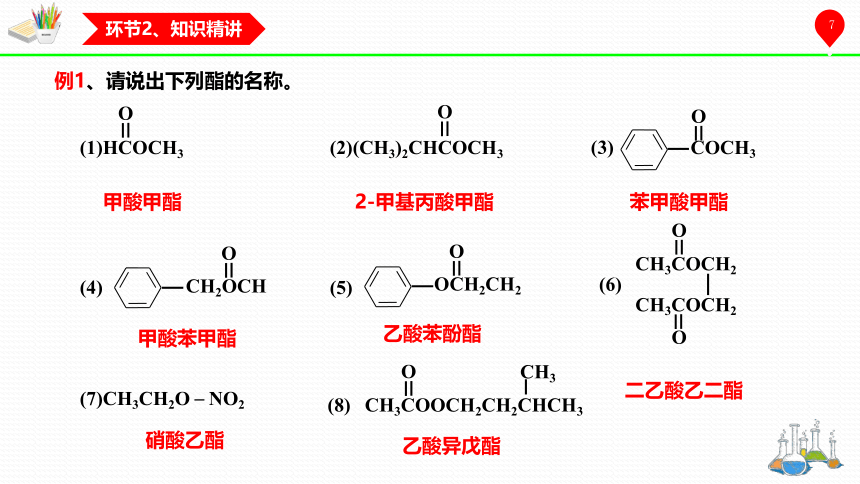
2-甲基丙酸甲酯
(7)CH3CH2O ─ NO2
硝酸乙酯
苯甲酸甲酯
甲酸苯甲酯
例1、请说出下列酯的名称。
甲酸甲酯
二乙酸乙二酯
乙酸苯酚酯
(1)HCOCH3
O
(2)(CH3)2CHCOCH3
O
CH3COCH2
CH3COCH2
(6)
O
O
COCH3
(3)
O
CH2OCH
(4)
O
OCH2CH2
(5)
O
CH3COOCH2CH2CHCH3
CH3
(8)
O
乙酸异戊酯
6、酯的物理性质
①低级酯是具有芳香气味的液体。
②密度比水小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。
7、酯的存在和用途
广泛存在于自然界,如苹果里含有戊酸戊酯,菠萝里含有丁酸乙酯、香蕉里含有乙酸异戊酯等。日常生活中的饮料、糖果和糕点等常使用酯类香料。
一、酯
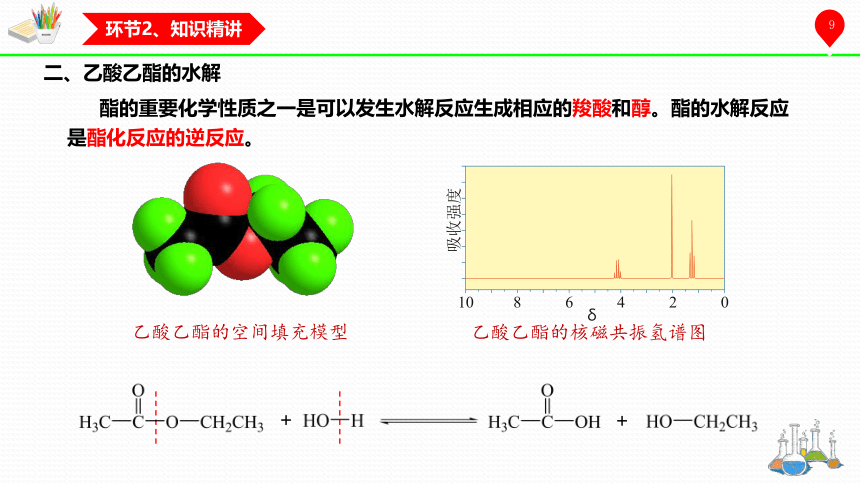
二、乙酸乙酯的水解
+
酯的重要化学性质之一是可以发生水解反应生成相应的羧酸和醇。酯的水解反应是酯化反应的逆反应。
10
8
6
4
2
0
吸收强度
δ
乙酸乙酯的核磁共振氢谱图
乙酸乙酯的空间填充模型
+
思考与讨论
乙酸乙酯水解的速率与与哪些条件有关?
溶液的酸碱性、温度、催化剂等
实验探究
1、在中性、酸性和碱性条件下酯的水解速率的比较?
2、在不同温度下水解速率的比较?
酯层消失的时间差异
如何判断乙酸乙酯在不同条件下水解速率的差别?
实验探究
实验现象
含有石蕊的 稀硫酸
含有石蕊的 蒸馏水
含有 石蕊的NaOH溶液
分层,酯层无明显变化
酯层消失最快,溶液整体变成蓝色
酯层消失较慢,溶液整体成红色
1、在中性、酸性和碱性条件下酯的水解速率的比较?
酯在碱性条件下水解速率最快,酸性、中性条件下几乎不水解;在强碱的溶液中酯水解趋于完全。
实验探究
含有 石蕊的稀硫酸 常温
水浴 加热
实验现象
2、在不同温度下水解速率的比较?
酯层消失一部分
酯层几乎消失
温度越高,酯水解程度越大。
思考与讨论
根据平衡移动原理,解释乙酸乙酯在碱性条件下发生的水解反应是不可逆的?乙酸乙酯在酸性和碱性条件下的水解有什么不同?
+
+
稀H2SO4
△
NaOH
+
H2O
+
+
+
△
NaOH
乙酸
乙醇
乙酸钠
乙醇
HCOOCH3 +H2O
①
CH3OH+HCOOH
稀硫酸
△
HCOOCH3 +NaOH
△
CH3OH+HCOONa
CH3COOCH3 +NaOH
CH3COOCH3 +H2O
②
CH3OH+CH3COONa
△
例2、写出下列酯在酸性和碱性条件下的水解方程式。
稀硫酸
△
CH3OH+CH3COOH
例2、写出下列酯在酸性和碱性条件下的水解方程式。
+
2
稀H2SO4
△
+
2
+
2
NaOH
△
+
2
③
例2、写出下列酯在酸性和碱性条件下的水解方程式。
+
2
稀H2SO4
△
+
2
+
2
NaOH
△
+
2
④
三、油脂
油脂是重要的营养物质,主要成分是高级脂肪酸和甘油形成的酯。
R、R’和R”代表高级脂肪酸的烃基。
硬脂酸:C17H35COOH
软脂酸:C15H31COOH
油 酸:C17H33COOH
亚油酸:C17H31COOH
饱和
不饱和
液态,烃基不饱和
固态,烃基饱和
三、油脂
1、水解反应
+
3NaOH
△
3
+
硬脂酸甘油酯
甘油
硬脂酸钠
皂化反应
在酸、碱等催化剂的作用下,油脂可以发生水解反应。在碱性条件下,油脂水解生成甘油和高级脂肪酸盐。
三、油脂
2、油脂的氢化
不饱和程度较高、熔点较低的液态油,通过催化回拨以可提高饱和度,转变成半固态的脂肪,这个过程称为油脂的氢化,也称油脂的硬化。由此制得的油脂叫人造脂肪,又称硬化油。
+
3H2
催化剂
△
硬脂酸甘油酯
油酸甘油酯
四、胺
烃基取代氨分子中的氢原子而形成的化合物叫做胺,一般可写作R-NH2。胺也可以看作是烃分子中的氢原子被氨基所替代得到的化合物。
CH3-NH2
CH3CH2-NH2
NH2
甲胺
乙胺
苯胺
NH2
+
HCl
NH3Cl
苯胺
苯胺盐酸盐
R-NH2
胺
氨基中的氮原子有一个孤电子对,H+则有空轨道,可以形成配位键,故胺具有碱性。
五、酰胺
酰胺是羧酸分子中羟基被氨基所替代得到的化合物。其结构一般表示为 。
酰基
酰胺基
乙酰胺
苯甲酰胺
N,N-二甲基甲酰胺
五、酰胺
酰胺在酸或碱存在并加热的条件下可以发生水解。如果水解时加入碱,生成的酸变会变成盐,同时有氨气逸出。
+
+
△
+
+ NH4Cl
△
+ HCl
+ NaOH
+ ↑
△
物质 氨 胺 酰胺 铵盐
组成元素
结构特点
化学性质
用途
N、H
C、N、H
C、O、N、H
N、H及其它元素
三角锥形分子
含有氨基
R-NH2
含有酰胺基
含有铵根离子
具有碱性,与酸反应生成铵盐
具有碱性,与酸反应生成盐
在酸或碱存在并加热的条件下可以发生水解反应
受热易分解,与碱共热产生氨气
制冷剂,生产硝酸和尿素
合成医药,农药和染料
溶剂和化工原料
生产化肥和炸药
思考与讨论
氨、胺、酰胺和铵盐的对比
1、认识羧酸衍生物(酯、油脂、酰胺)和胺的结构特点及应用。
2、通过探究乙酸乙酯的水解,熟悉控制变量法的应用,体验科学探究的一般过程。
羧酸衍生物的结构特点和主要化学性质。
羧酸衍生物的结构特点和主要化学性质。
丁酸乙酯
戊酸戊酯
生活中的酯
CH3(CH2)3 ─ CO ─(CH2)4CH3
O
CH3(CH2)2 ─ CO ─ CH2CH3
O
邻氨基苯甲酸甲酯
─ COCH
─ NH2
O
1、羧酸衍生物:
3、酯的结构通式:
R1:只能是烃基
R(H) ─ C ─ O ─ R1
O
4、饱和一元酯的分子通式为:
CnH2nO2 (n≥2)
一、酯
官能团:酯基
─ C ─ O ─
O
简写为─ COO ─
与饱和一元羧酸互为同分异构体
2、酯:
羧酸分子羧基中的 ─ OH被其他原子或原子团取代后的产物。
酯是羧酸分子羧基中的 ─ OH被 ─ OR′取代后的产物。
5、酯的命名——根据反应物称为“某酸某酯”
丙酸乙酯
CH3CH2COCH2CH3
O
乙酸乙酯
CH3COCH2CH3
O
COOCH2CH3
COOCH2CH3
乙二酸二乙酯
如:
一、酯
酸 + 醇 = 酯 + 水
2-甲基丙酸甲酯
(7)CH3CH2O ─ NO2
硝酸乙酯
苯甲酸甲酯
甲酸苯甲酯
例1、请说出下列酯的名称。
甲酸甲酯
二乙酸乙二酯
乙酸苯酚酯
(1)HCOCH3
O
(2)(CH3)2CHCOCH3
O
CH3COCH2
CH3COCH2
(6)
O
O
COCH3
(3)
O
CH2OCH
(4)
O
OCH2CH2
(5)
O
CH3COOCH2CH2CHCH3
CH3
(8)
O
乙酸异戊酯
6、酯的物理性质
①低级酯是具有芳香气味的液体。
②密度比水小。
③难溶于水,易溶于乙醇和乙醚等有机溶剂。
7、酯的存在和用途
广泛存在于自然界,如苹果里含有戊酸戊酯,菠萝里含有丁酸乙酯、香蕉里含有乙酸异戊酯等。日常生活中的饮料、糖果和糕点等常使用酯类香料。
一、酯
二、乙酸乙酯的水解
+
酯的重要化学性质之一是可以发生水解反应生成相应的羧酸和醇。酯的水解反应是酯化反应的逆反应。
10
8
6
4
2
0
吸收强度
δ
乙酸乙酯的核磁共振氢谱图
乙酸乙酯的空间填充模型
+
思考与讨论
乙酸乙酯水解的速率与与哪些条件有关?
溶液的酸碱性、温度、催化剂等
实验探究
1、在中性、酸性和碱性条件下酯的水解速率的比较?
2、在不同温度下水解速率的比较?
酯层消失的时间差异
如何判断乙酸乙酯在不同条件下水解速率的差别?
实验探究
实验现象
含有石蕊的 稀硫酸
含有石蕊的 蒸馏水
含有 石蕊的NaOH溶液
分层,酯层无明显变化
酯层消失最快,溶液整体变成蓝色
酯层消失较慢,溶液整体成红色
1、在中性、酸性和碱性条件下酯的水解速率的比较?
酯在碱性条件下水解速率最快,酸性、中性条件下几乎不水解;在强碱的溶液中酯水解趋于完全。
实验探究
含有 石蕊的稀硫酸 常温
水浴 加热
实验现象
2、在不同温度下水解速率的比较?
酯层消失一部分
酯层几乎消失
温度越高,酯水解程度越大。
思考与讨论
根据平衡移动原理,解释乙酸乙酯在碱性条件下发生的水解反应是不可逆的?乙酸乙酯在酸性和碱性条件下的水解有什么不同?
+
+
稀H2SO4
△
NaOH
+
H2O
+
+
+
△
NaOH
乙酸
乙醇
乙酸钠
乙醇
HCOOCH3 +H2O
①
CH3OH+HCOOH
稀硫酸
△
HCOOCH3 +NaOH
△
CH3OH+HCOONa
CH3COOCH3 +NaOH
CH3COOCH3 +H2O
②
CH3OH+CH3COONa
△
例2、写出下列酯在酸性和碱性条件下的水解方程式。
稀硫酸
△
CH3OH+CH3COOH
例2、写出下列酯在酸性和碱性条件下的水解方程式。
+
2
稀H2SO4
△
+
2
+
2
NaOH
△
+
2
③
例2、写出下列酯在酸性和碱性条件下的水解方程式。
+
2
稀H2SO4
△
+
2
+
2
NaOH
△
+
2
④
三、油脂
油脂是重要的营养物质,主要成分是高级脂肪酸和甘油形成的酯。
R、R’和R”代表高级脂肪酸的烃基。
硬脂酸:C17H35COOH
软脂酸:C15H31COOH
油 酸:C17H33COOH
亚油酸:C17H31COOH
饱和
不饱和
液态,烃基不饱和
固态,烃基饱和
三、油脂
1、水解反应
+
3NaOH
△
3
+
硬脂酸甘油酯
甘油
硬脂酸钠
皂化反应
在酸、碱等催化剂的作用下,油脂可以发生水解反应。在碱性条件下,油脂水解生成甘油和高级脂肪酸盐。
三、油脂
2、油脂的氢化
不饱和程度较高、熔点较低的液态油,通过催化回拨以可提高饱和度,转变成半固态的脂肪,这个过程称为油脂的氢化,也称油脂的硬化。由此制得的油脂叫人造脂肪,又称硬化油。
+
3H2
催化剂
△
硬脂酸甘油酯
油酸甘油酯
四、胺
烃基取代氨分子中的氢原子而形成的化合物叫做胺,一般可写作R-NH2。胺也可以看作是烃分子中的氢原子被氨基所替代得到的化合物。
CH3-NH2
CH3CH2-NH2
NH2
甲胺
乙胺
苯胺
NH2
+
HCl
NH3Cl
苯胺
苯胺盐酸盐
R-NH2
胺
氨基中的氮原子有一个孤电子对,H+则有空轨道,可以形成配位键,故胺具有碱性。
五、酰胺
酰胺是羧酸分子中羟基被氨基所替代得到的化合物。其结构一般表示为 。
酰基
酰胺基
乙酰胺
苯甲酰胺
N,N-二甲基甲酰胺
五、酰胺
酰胺在酸或碱存在并加热的条件下可以发生水解。如果水解时加入碱,生成的酸变会变成盐,同时有氨气逸出。
+
+
△
+
+ NH4Cl
△
+ HCl
+ NaOH
+ ↑
△
物质 氨 胺 酰胺 铵盐
组成元素
结构特点
化学性质
用途
N、H
C、N、H
C、O、N、H
N、H及其它元素
三角锥形分子
含有氨基
R-NH2
含有酰胺基
含有铵根离子
具有碱性,与酸反应生成铵盐
具有碱性,与酸反应生成盐
在酸或碱存在并加热的条件下可以发生水解反应
受热易分解,与碱共热产生氨气
制冷剂,生产硝酸和尿素
合成医药,农药和染料
溶剂和化工原料
生产化肥和炸药
思考与讨论
氨、胺、酰胺和铵盐的对比
