河南省濮阳市第一高级中学2023-2024学年高二下学期3月第一次质量检测化学(B)试题(含答案)
文档属性
| 名称 | 河南省濮阳市第一高级中学2023-2024学年高二下学期3月第一次质量检测化学(B)试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 569.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-03-31 00:00:00 | ||
图片预览



文档简介
濮阳市第一高级中学2023-2024学年高二下学期3月第一次质量检测
化学试题(B)
2024.03
注意事项:
1.本试卷共9页,满分100分,考试时间75分钟。
2.试题卷上不要答题,请用0.5毫米黑色签字笔直接把答案写在答题卡上对应的答题区域内。答在试题卷上的答案无效。
可能用到的相对原子质量:H-1、C-12、N-14、O-16、Ge-73
第Ⅰ卷(共45分)
一、选择题(每小题只有一个选项符合要求,每小题3分,共45分。)
1.化学与生活、科研紧密相关,下列说法错误的是( )
A.在日常装修中,溶解油漆一般用有机溶剂(如乙酸乙酯等)而不用水
B.液晶可应用于手机、电脑和电视的显示器
C.在实验室,常用酒精萃取碘水中的碘单质
D.日常生活中的焰火和霓虹灯光,都与原子核外电子跃迁释放能量有关
2.可用作白色颜料和阻燃剂,在实验室中可利用的水解反应制取,总反应可表示为。下列化学用语表示正确的是( )
A.和互为同分异构体
B.基态O原子价层电子排布图:
C.基态的核外电子排布式:
D.的VSEPR模型:
3.侯德榜联合制碱法的原理之一是,下列关于该原理涉及到的物质说法正确的是( )
A.晶体中只存在离子键 B.分子中存在非极性共价键
C.分子中碳原子采取杂化 D.分子的空间结构是三角锥形
4.我国古代四大发明之一黑火药的爆炸反应为:。设为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L 含有的原子数为 B.0.1 mol 晶体中含离子数目为
C.28g ()含的π键数目为 D.1 L 0.1 mol L 溶液中含数目为
5.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是( )
选项 性质差异 结构因素
A 酸性:三氟乙酸>三氯乙酸 电负性差异
B 熔点:干冰 晶体类型差异
C 溶解性:在中的溶解度大于在水中的溶解度 相似相溶
D 稳定性:的分解温度(3000℃)远大于(900℃) 有无氢键
6.工业上电解熔融和冰晶石()的混合物可制得铝。下列说法正确的( )
A.半径大小: B.电负性大小:
C.第一电离能大小: D.碱性强弱:
7.短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列判断正确的是( )
A.Z位于元素周期表的p区 B.简单氢化物沸点:X>Y
C.Z与W形成的化合物是离子化合物 D.的空间构型与VSEPR构型一致
8.下列有关说法错误的是( )
A.、石墨和金刚石晶体类型相同
B.DNA双螺旋的两个螺旋链是通过氢键结合的
C.AgCl溶于氨水,由于AgCl与反应生成了可溶性配合物
D.冠醚(18-冠-6)的空穴与尺寸适配,两者能通过弱相互作用形成超分子
9.硫酸铜溶于过量氨水中形成深蓝色溶液。下列有关说法不正确的( )
A.与之间形成的化学键称为配位键
B.提供孤电子对
C.提供空轨道
D.阴离子的空间结构为三角锥形
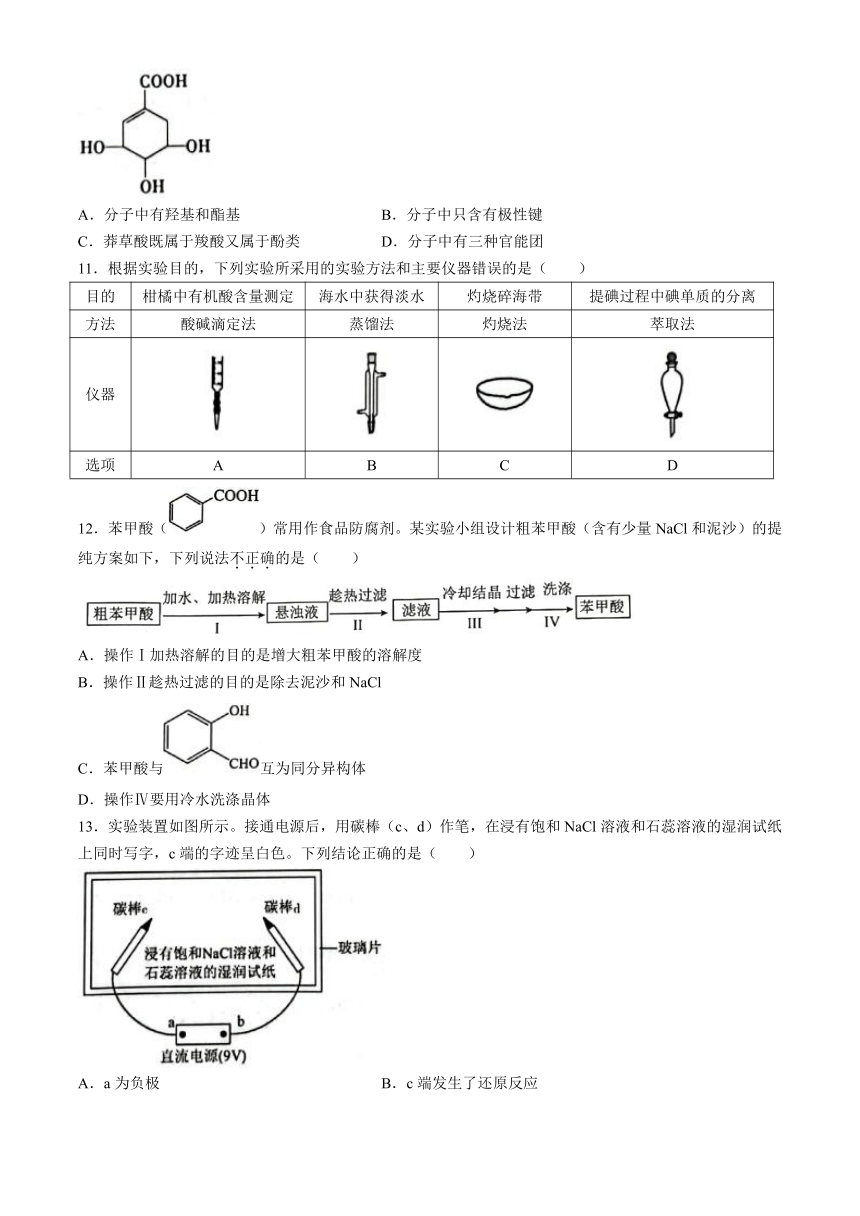
10.莽草酸可用于合成药物达菲,其结构简式如图。下列关于莽草酸的说法正确的( )
A.分子中有羟基和酯基 B.分子中只含有极性键
C.莽草酸既属于羧酸又属于酚类 D.分子中有三种官能团
11.根据实验目的,下列实验所采用的实验方法和主要仪器错误的是( )
目的 柑橘中有机酸含量测定 海水中获得淡水 灼烧碎海带 提碘过程中碘单质的分离
方法 酸碱滴定法 蒸馏法 灼烧法 萃取法
仪器
选项 A B C D
12.苯甲酸()常用作食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下,下列说法不正确的是( )
A.操作Ⅰ加热溶解的目的是增大粗苯甲酸的溶解度
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.苯甲酸与互为同分异构体
D.操作Ⅳ要用冷水洗涤晶体
13.实验装置如图所示。接通电源后,用碳棒(c、d)作笔,在浸有饱和NaCl溶液和石蕊溶液的湿润试纸上同时写字,c端的字迹呈白色。下列结论正确的是( )
A.a为负极 B.c端发生了还原反应
C.d端的字迹呈蓝色 D.电子流向为:b→d→c→a
14.常温下,下列说法正确的是( )
A.的氯化铵溶液,由水电离的mol/L
B.AgCl在同浓度的和NaCl溶液中的溶解度相同
C.等浓度等体积的溶液和NaOH溶液混合后,溶液显中性
D.将的醋酸溶液加水稀释100倍,pH变为5
15.萤石()晶胞结构如图所示,下列说法不正确的是( )
A.该晶胞中黑球代表 B.该晶胞中含有的数目为8
C.该晶胞中与的数目之比为1∶2 D.该晶胞中与等距且最近的数目为4
第Ⅱ卷(共55分)
16.(12分)高铁酸钠()是一种新型绿色消毒剂,主要用于饮用水处理。制备高铁酸钠的反应原理为:。某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C)制备高铁酸钠的主要流程如下。
(1)Fe在元素周期表中的位置______,中铁的化合价为______。
(2)“碱浸”过程中发生的离子反应方程式为__________________。
(3)“酸浸”时适当升温的目的是____________。
(4)“滤渣”的主要成分为______。
(5)“操作Ⅰ”中通入空气的目的是____________。
(6)常温下,加入NaOH溶液调节溶液______时,溶液中mol/L(已知:常温下,的溶度积常数为)。
17.(13分)由H、C、O、N、Cu、Fe、Al、Ge等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价层电子轨道表示式______。
(2)早期发现的一种天然准晶颗粒由三种Al、Cu、Fe元素组成,准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过______方法区分晶体、准晶体和非晶体。
(3)离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
①基态碳原子的成对电子数与未成对电子数之比为______,基态碳原子核外电子占据的最高能级的电子云轮廓图为______形。
②碳和氢形成的最简单碳正离子,该阳离子的空间构型为______。
③化合物能溶于水的原因是____________。
(4)下图为Ge单晶晶胞。原子坐标参数A为;B为;C为,则D原子的坐标参数为______。
18.(14分)环己烯是重要的化工原料,其实验室制备流程如下。
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)环己醇的官能团名称为______。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
①仪器A的名称为______。
②该装置中冷凝水应从______(填“a”或“b”)口通入。
(3)操作2的名称是______,用到的玻璃仪器有______。
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和碎瓷片,______,弃去前馏分,收集83℃的馏分。
A.先通冷凝水,再加热 B.先加热,再通冷凝水
Ⅱ.环己烯的性质
(5)下列有关环己烯的说法正确的是______。
A.属于芳香族化合物 B.环己烯和环己醇可用红外光谱鉴别
C.与乙烯互为同系物 D.能使溴水褪色
(6)环己烯的核磁共振氢谱图共显示______组峰。
(7)环己醇沸点高于环己烯的原因是______。
19.(16分)氢气是一种清洁高效能源,如何经济实用制取氢气成为重要课题。
Ⅰ.氨气中氢含量高,是一种优质的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法一:氨热分解法制氢气
相关化学键的键能数据如表所示:
化学键
键能E/(kJ/mol) 946 436 391
(1)反应 ______kJ/mol。
(2)该反应的_____0(填“大于”、“小于”或“等于”)。
(3)298 K时,1 g H2燃烧生成放热121 kJ,1 mol蒸发吸热44 kJ,表示燃烧热的热化学方程式为____________。
方法二:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示:
(4)电极b与电源______相连(填“正极”或“负极”)。
(5)电解过程中的移动方向为______(填“从左往右”或“从右往左”)。
(6)阳极的电极反应式为______。
Ⅱ.可用于高效制取氢气,发生的反应为。
若起始时容器中只有,平衡时三种物质的物质的量与裂解温度关系如图。
(7)图中曲线Z表示的物质是______(填化学式)。
(8)C点时的转化率为______%(保留一位小数)。
化学试题答案
2024.03
一、选择题(本小题共15小题,每题3分,共45分。每题只有一个正确选项。)
题号 1 2 3 4 5 6 7 8
答案 C C D B D A C A
题号 9 10 11 12 13 14 15
答案 D D C B C A D
二、非选择题(本小题共4小题,共55分。)
16.(除标注外,每空2分,共12分)
(1)第四周期Ⅷ族(1分) (1分)
(2)或
(3)提高浸出速率
(4)C(5)将氧化为(6)3
17.(除标注外,每空2分,共13分)
(1)(2)X射线衍射(1分)
(3)①2∶1 哑铃形②平面三角形
③与水分子之间形成了氢键
(4)
18.(除标注外,每空2分,共14分)
(1)羟基(1分)
(2)①圆底烧瓶(1分)②b(1分)
(3)分液(1分) 分液漏斗、烧杯
(4)①A(5)BD(6)3
(6)环己醇分子间形成了分子间氢键,环己烯分子间只存在范德华力
19.(每空2分,共16分)
(1)(2)大于
3) kJ mol
(4)负极(5)从右往左(6)
(7)(8)66.7
化学试题(B)
2024.03
注意事项:
1.本试卷共9页,满分100分,考试时间75分钟。
2.试题卷上不要答题,请用0.5毫米黑色签字笔直接把答案写在答题卡上对应的答题区域内。答在试题卷上的答案无效。
可能用到的相对原子质量:H-1、C-12、N-14、O-16、Ge-73
第Ⅰ卷(共45分)
一、选择题(每小题只有一个选项符合要求,每小题3分,共45分。)
1.化学与生活、科研紧密相关,下列说法错误的是( )
A.在日常装修中,溶解油漆一般用有机溶剂(如乙酸乙酯等)而不用水
B.液晶可应用于手机、电脑和电视的显示器
C.在实验室,常用酒精萃取碘水中的碘单质
D.日常生活中的焰火和霓虹灯光,都与原子核外电子跃迁释放能量有关
2.可用作白色颜料和阻燃剂,在实验室中可利用的水解反应制取,总反应可表示为。下列化学用语表示正确的是( )
A.和互为同分异构体
B.基态O原子价层电子排布图:
C.基态的核外电子排布式:
D.的VSEPR模型:
3.侯德榜联合制碱法的原理之一是,下列关于该原理涉及到的物质说法正确的是( )
A.晶体中只存在离子键 B.分子中存在非极性共价键
C.分子中碳原子采取杂化 D.分子的空间结构是三角锥形
4.我国古代四大发明之一黑火药的爆炸反应为:。设为阿伏加德罗常数的值,下列说法正确的是( )
A.11.2 L 含有的原子数为 B.0.1 mol 晶体中含离子数目为
C.28g ()含的π键数目为 D.1 L 0.1 mol L 溶液中含数目为
5.物质结构决定物质性质。下列性质差异与结构因素匹配错误的是( )
选项 性质差异 结构因素
A 酸性:三氟乙酸>三氯乙酸 电负性差异
B 熔点:干冰 晶体类型差异
C 溶解性:在中的溶解度大于在水中的溶解度 相似相溶
D 稳定性:的分解温度(3000℃)远大于(900℃) 有无氢键
6.工业上电解熔融和冰晶石()的混合物可制得铝。下列说法正确的( )
A.半径大小: B.电负性大小:
C.第一电离能大小: D.碱性强弱:
7.短周期主族元素X、Y、Z、W的原子序数依次增大,X、Y同周期并相邻,Y是组成水的元素之一,Z在同周期主族元素中金属性最强,W原子在同周期主族元素中原子半径最小,下列判断正确的是( )
A.Z位于元素周期表的p区 B.简单氢化物沸点:X>Y
C.Z与W形成的化合物是离子化合物 D.的空间构型与VSEPR构型一致
8.下列有关说法错误的是( )
A.、石墨和金刚石晶体类型相同
B.DNA双螺旋的两个螺旋链是通过氢键结合的
C.AgCl溶于氨水,由于AgCl与反应生成了可溶性配合物
D.冠醚(18-冠-6)的空穴与尺寸适配,两者能通过弱相互作用形成超分子
9.硫酸铜溶于过量氨水中形成深蓝色溶液。下列有关说法不正确的( )
A.与之间形成的化学键称为配位键
B.提供孤电子对
C.提供空轨道
D.阴离子的空间结构为三角锥形
10.莽草酸可用于合成药物达菲,其结构简式如图。下列关于莽草酸的说法正确的( )
A.分子中有羟基和酯基 B.分子中只含有极性键
C.莽草酸既属于羧酸又属于酚类 D.分子中有三种官能团
11.根据实验目的,下列实验所采用的实验方法和主要仪器错误的是( )
目的 柑橘中有机酸含量测定 海水中获得淡水 灼烧碎海带 提碘过程中碘单质的分离
方法 酸碱滴定法 蒸馏法 灼烧法 萃取法
仪器
选项 A B C D
12.苯甲酸()常用作食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下,下列说法不正确的是( )
A.操作Ⅰ加热溶解的目的是增大粗苯甲酸的溶解度
B.操作Ⅱ趁热过滤的目的是除去泥沙和NaCl
C.苯甲酸与互为同分异构体
D.操作Ⅳ要用冷水洗涤晶体
13.实验装置如图所示。接通电源后,用碳棒(c、d)作笔,在浸有饱和NaCl溶液和石蕊溶液的湿润试纸上同时写字,c端的字迹呈白色。下列结论正确的是( )
A.a为负极 B.c端发生了还原反应
C.d端的字迹呈蓝色 D.电子流向为:b→d→c→a
14.常温下,下列说法正确的是( )
A.的氯化铵溶液,由水电离的mol/L
B.AgCl在同浓度的和NaCl溶液中的溶解度相同
C.等浓度等体积的溶液和NaOH溶液混合后,溶液显中性
D.将的醋酸溶液加水稀释100倍,pH变为5
15.萤石()晶胞结构如图所示,下列说法不正确的是( )
A.该晶胞中黑球代表 B.该晶胞中含有的数目为8
C.该晶胞中与的数目之比为1∶2 D.该晶胞中与等距且最近的数目为4
第Ⅱ卷(共55分)
16.(12分)高铁酸钠()是一种新型绿色消毒剂,主要用于饮用水处理。制备高铁酸钠的反应原理为:。某化学兴趣小组用废铁屑(主要成分为Fe,杂质有Al、C)制备高铁酸钠的主要流程如下。
(1)Fe在元素周期表中的位置______,中铁的化合价为______。
(2)“碱浸”过程中发生的离子反应方程式为__________________。
(3)“酸浸”时适当升温的目的是____________。
(4)“滤渣”的主要成分为______。
(5)“操作Ⅰ”中通入空气的目的是____________。
(6)常温下,加入NaOH溶液调节溶液______时,溶液中mol/L(已知:常温下,的溶度积常数为)。
17.(13分)由H、C、O、N、Cu、Fe、Al、Ge等元素能形成多种物质。这些物质有许多用途。请回答下列问题:
(1)基态Cu原子的价层电子轨道表示式______。
(2)早期发现的一种天然准晶颗粒由三种Al、Cu、Fe元素组成,准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过______方法区分晶体、准晶体和非晶体。
(3)离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的离子由H、C、N三种元素组成,结构如图所示。回答下列问题:
①基态碳原子的成对电子数与未成对电子数之比为______,基态碳原子核外电子占据的最高能级的电子云轮廓图为______形。
②碳和氢形成的最简单碳正离子,该阳离子的空间构型为______。
③化合物能溶于水的原因是____________。
(4)下图为Ge单晶晶胞。原子坐标参数A为;B为;C为,则D原子的坐标参数为______。
18.(14分)环己烯是重要的化工原料,其实验室制备流程如下。
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)环己醇的官能团名称为______。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
①仪器A的名称为______。
②该装置中冷凝水应从______(填“a”或“b”)口通入。
(3)操作2的名称是______,用到的玻璃仪器有______。
(4)将操作3(蒸馏)的步骤补齐:安装蒸馏装置,加入待蒸馏的物质和碎瓷片,______,弃去前馏分,收集83℃的馏分。
A.先通冷凝水,再加热 B.先加热,再通冷凝水
Ⅱ.环己烯的性质
(5)下列有关环己烯的说法正确的是______。
A.属于芳香族化合物 B.环己烯和环己醇可用红外光谱鉴别
C.与乙烯互为同系物 D.能使溴水褪色
(6)环己烯的核磁共振氢谱图共显示______组峰。
(7)环己醇沸点高于环己烯的原因是______。
19.(16分)氢气是一种清洁高效能源,如何经济实用制取氢气成为重要课题。
Ⅰ.氨气中氢含量高,是一种优质的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法一:氨热分解法制氢气
相关化学键的键能数据如表所示:
化学键
键能E/(kJ/mol) 946 436 391
(1)反应 ______kJ/mol。
(2)该反应的_____0(填“大于”、“小于”或“等于”)。
(3)298 K时,1 g H2燃烧生成放热121 kJ,1 mol蒸发吸热44 kJ,表示燃烧热的热化学方程式为____________。
方法二:氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图所示:
(4)电极b与电源______相连(填“正极”或“负极”)。
(5)电解过程中的移动方向为______(填“从左往右”或“从右往左”)。
(6)阳极的电极反应式为______。
Ⅱ.可用于高效制取氢气,发生的反应为。
若起始时容器中只有,平衡时三种物质的物质的量与裂解温度关系如图。
(7)图中曲线Z表示的物质是______(填化学式)。
(8)C点时的转化率为______%(保留一位小数)。
化学试题答案
2024.03
一、选择题(本小题共15小题,每题3分,共45分。每题只有一个正确选项。)
题号 1 2 3 4 5 6 7 8
答案 C C D B D A C A
题号 9 10 11 12 13 14 15
答案 D D C B C A D
二、非选择题(本小题共4小题,共55分。)
16.(除标注外,每空2分,共12分)
(1)第四周期Ⅷ族(1分) (1分)
(2)或
(3)提高浸出速率
(4)C(5)将氧化为(6)3
17.(除标注外,每空2分,共13分)
(1)(2)X射线衍射(1分)
(3)①2∶1 哑铃形②平面三角形
③与水分子之间形成了氢键
(4)
18.(除标注外,每空2分,共14分)
(1)羟基(1分)
(2)①圆底烧瓶(1分)②b(1分)
(3)分液(1分) 分液漏斗、烧杯
(4)①A(5)BD(6)3
(6)环己醇分子间形成了分子间氢键,环己烯分子间只存在范德华力
19.(每空2分,共16分)
(1)(2)大于
3) kJ mol
(4)负极(5)从右往左(6)
(7)(8)66.7
同课章节目录
