黑龙江省齐齐哈尔市第八中学校2023-2024学年高一下学期3月月考化学试题(含答案)
文档属性
| 名称 | 黑龙江省齐齐哈尔市第八中学校2023-2024学年高一下学期3月月考化学试题(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 581.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-01 20:10:33 | ||
图片预览




文档简介
齐齐哈尔市第八中学校2023-2024学年高一下学期3月月考
化学试题
可能用到的近似相对原子质量:
第I卷(选择题45分)
一、选择题:本题共15小题,每小题3分,共45分。每小题有一个选项符合题意。
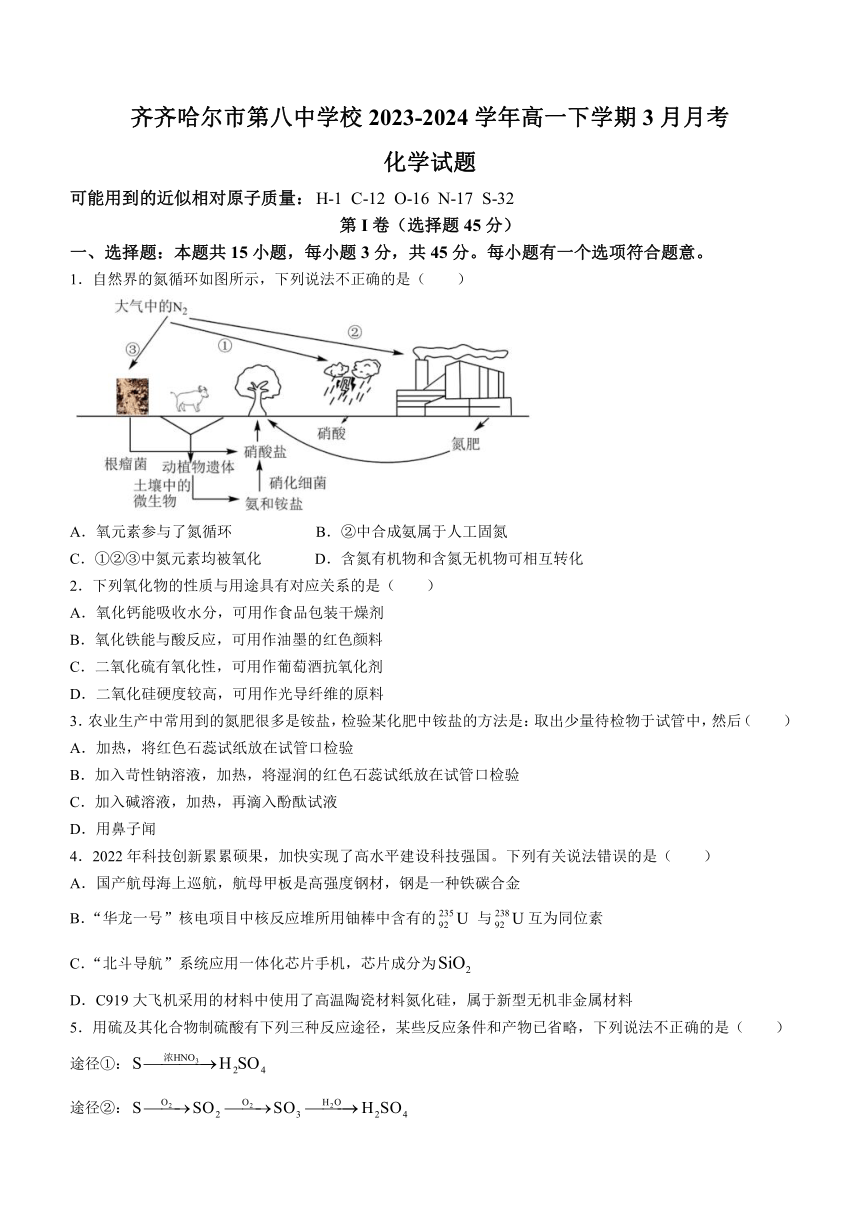
1.自然界的氮循环如图所示,下列说法不正确的是( )
A.氧元素参与了氮循环 B.②中合成氨属于人工固氮
C.①②③中氮元素均被氧化 D.含氮有机物和含氮无机物可相互转化
2.下列氧化物的性质与用途具有对应关系的是( )
A.氧化钙能吸收水分,可用作食品包装干燥剂
B.氧化铁能与酸反应,可用作油墨的红色颜料
C.二氧化硫有氧化性,可用作葡萄酒抗氧化剂
D.二氧化硅硬度较高,可用作光导纤维的原料
3.农业生产中常用到的氮肥很多是铵盐,检验某化肥中铵盐的方法是:取出少量待检物于试管中,然后( )
A.加热,将红色石蕊试纸放在试管口检验
B.加入苛性钠溶液,加热,将湿润的红色石蕊试纸放在试管口检验
C.加入碱溶液,加热,再滴入酚酞试液
D.用鼻子闻
4.2022年科技创新累累硕果,加快实现了高水平建设科技强国。下列有关说法错误的是( )
A.国产航母海上巡航,航母甲板是高强度钢材,钢是一种铁碳合金
B.“华龙一号”核电项目中核反应堆所用铀棒中含有的与互为同位素
C.“北斗导航”系统应用一体化芯片手机,芯片成分为
D.C919大飞机采用的材料中使用了高温陶瓷材料氮化硅,属于新型无机非金属材料
5.用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物已省略,下列说法不正确的是( )
途径①:
途径②:
途径③:
A.途径①的反应中体现了浓的强氧化性
B.途径②、③的第二步反应在实际生产中可以通过增大的浓度来降低成本
C.由途径①、②、③分别制取,理论上各消耗,各转移
D.途径②、③比途径①污染相对小且原子利用率高,更能体现“绿色化学”的理念
6.学科思想方法是学好化学的关键,下列有关学科思想方法的理解不正确的是( )
A.物质的结构与性质关联,根据物质的结构可以分析其性质。例如氮分子中存在叁键,断开它需要较多的能量,所以N,的化学性质稳定
B.基于物质的类别与化合价,可以预测物质的性质。例如从硫的化合价角度分析,既有氧化性又有还原性
C.类比是研究物质性质的常用方法之一,可预测许多物质的性质。例如铝与稀硫酸反应生成氢气,则铝与稀硝酸反应生成氢气
D.模型在科学认识中具有描述、解释和预测等功能,例如电离模型很好地解释了酸、碱、盐的某些性质
7.下列情况会对人体健康造成较大危害的是( )
A.用漂白食品 B.用食醋清洗热水瓶胆内壁附着的水垢
C.自来水中通入少量进行消毒杀菌 D.用小苏打发酵面团制作馒头
8.常温下,下列各组离子在指定条件下能大量共存的是( )
A.溶液:
B.使酚酞变红色的溶液:
C.某无色溶液:
D.的溶液:
9.设为阿伏伽德罗常数的值。下列说法正确的是( )
A.分子中所含的数目为
B.的溶液中所含的数目为
C.与足量S充分反应,转移电子数为
D.与足量反应,生成的分子数小于
10.某实验小组在培养皿中设计了如下微型实验:向亚硫酸钠固体上滴加几滴的浓硫酸,立即用表面皿盖住培养皿。下列说法正确的是( )
A.b处溶液紫色褪去,证明具有漂白性
B.c处出现黄色浑浊,表明具有氧化性
C.d处发生反应:
D.e处紫色石蕊溶液由紫色变为红色,后又逐渐褪色
11.某小组同学进行铜与浓硫酸反应时,发现有黑色物质产生。该小组同学猜测,黑色物质中可能含有和。针对产生的黑色物质,该小组同学继续进行实验探究,获得数据如下表所示。
硫酸浓度 黑色物质出现的温度 黑色物质消失的温度
15 约150 约236
16 约140 约250
18 约120 不消失
下列推测不合理的是( )
A.硫酸浓度越大,黑色物质越易出现、越难消失
B.黑色物质消失过程中伴随大量生成
C.硫酸浓度为时,若先升温至以上,再将铜丝与浓硫酸接触,可以避免黑色物质产生
D.若取黑色物质洗涤、干燥后,加稀硫酸,固体质量不变,说明黑色物质中不含
12.下列离子方程式正确的是( )
A.向溶液中滴加盐酸:
B.向溶液中通入足量
C.向溶液中通入足量:
D.用热溶液洗涤试管内壁的硫黄:
13.足量的铜与一定体积的浓硝酸充分反应后生成硝酸铜以及和的混合气体,若将所得到的气体与标准状况下氧气混合后充入足量水中,气体恰好完全反应得到硝酸。则向反应后的溶液中加入的氢氧化钠溶液使其中的铜离子恰好完全沉淀,需要消耗氢氧化钠的溶液的体积是( )
A. B. C. D.
14.将标准状况下和的混合气体通过灼热的三氧化二铬(催化剂),氨全部被氧化。将反应后气体全部通入水中,无气体剩余,制得100L溶液,则该溶液的浓度为( )
A. B. C. D.
15.把含的混合溶液分成两等份,一份用烧碱刚好把全部赶出,另一份与溶液完全反应消耗,则原溶液中为( )
A. B. C. D.
第Ⅱ卷(非选择题55分)
二、非选择题:本题共4小题,共55分
16.完成下列化学方程式(是离子反应的写离子方程式):
(1)等物质的量二氧化硫和氯气通入水中
(2)二氧化硫通入酸性高锰酸钾溶液中
(3)高温煅烧黄铁矿
(4)炭与浓硫酸加热
(5)硫与浓硫酸加热
(6)铜和浓硫酸加热
(7)铜和浓硝酸(实验室制)
(8)铜和稀硝酸(实验室制)
(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中
(10)二氧化氮通入苛性钠溶液中
17.S02是常见的大气污染物,燃煤是产生的主要原因。工业上有多种方法可以减少的排放。
(1)往煤中添加一些生石灰,可使燃煤过程中产生的转化成硫酸钙。该反应的化学方程式为______________________________。
(2)可用多种溶液做燃煤烟气中的吸收液。
①分别用等物质的量浓度的溶液和溶液做吸收液,当生成等物质的量时,两种吸收液体积比__________。
②溶液吸收了足量的后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使溶液再生,再生过程的化学方程式为______________________________。
(3)甲同学认为溶液可以做的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
已知:反应开始后,A中固体表面有气泡产生同时有白雾生成;B中有白色沉淀。
甲认为B中白色沉淀是与溶液反应生成的,所以溶液可做吸收液。
乙同学认为B中的白色沉淀是,产生的原因可能是
①A中产生的白雾是浓硫酸的酸雾,进入B中与溶液反应生成沉淀。
②________________________________________
为证明与溶液不能得到沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
反应开始后,A中固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现象;D中红色褪去。
③试管B中试剂是溶液__________;滴加浓硫酸之前的操作是____________________。
④通过甲乙两位同学的实验,得出的结论是______________________________。
18.硝酸是一种重要的化工原料,氨氧化法是工业生产中制取硝酸的主要途径,某兴趣小组在实验室模拟氨氧化法制硝酸,实验装置如图所示,回答下列问题:
(注:氯化钙可以与反应生成八氨合氯化钙。)
(1)仪器a的名称为__________,其中加的试剂为__________。
(2)实验时先点燃C中的酒精灯,当催化剂由暗绿色变为微红时通入空气,后出现暗红色,移去酒精灯,能保持红热状态的原因是____________________,装置C中发生反应的总反应化学方程式为______________________________。
(3)装置D的作用是____________________,装置G的作用是____________________。
(4)反应开始后,在装置E中看到的现象是______________________________。
(5)实验结束后,证明有生成的操作是______________________________。
19.一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。
试回答下列问题:
(1)写出下列物质化学式:A____________________;C____________________;
(2)写出F的电子式:______________________________;
(3)写出溶液E与共热反应的离子方程式:______________________________;
(4)写出A和新制氯水反应的离子方程式:______________________________。
参考答案:
一、选择题:本题共15小题,每小题3分,共45分。每小题有一个选项符合题意。
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
C A B C C C A D D B B D C B B
二、非选择题:本题共4小题,共55分.
16.(20分)完成下列离子方程式:
二氧化硫和氯气等物质的量通入水中
二氧化硫通入酸性高锰酸钾溶液中
高温煅烧黄铁刊
炭与浓硫酸加热
硫与浓硫酸加热
铜和浓硫酸加热
铜和浓硝酸
(实验室制)
铜和稀硝酸
(实验室制)
二氧化氮和一氧化氮混合气体通入苛性钠溶液
17.(14分)(1)
(2)
(3)A中产生的与装置内空气中的进入B中与溶液反应生成沉淀饱和
打开弹簧夹,通入,一段时间后关闭弹簧夹
不能用溶液做吸收的吸收液(或与溶液不能得到沉淀)
18.(11分)(1)球形干燥管 碱石灰
(2)该反应为放热反应
(3)除去氨气和水蒸气 吸收尾气
(4)气体变为红棕色
(5)取少量F中的液体于试管中,滴加几滴紫色石蕊试液,溶液变红,证明有生成
19.(10分)
化学试题
可能用到的近似相对原子质量:
第I卷(选择题45分)
一、选择题:本题共15小题,每小题3分,共45分。每小题有一个选项符合题意。
1.自然界的氮循环如图所示,下列说法不正确的是( )
A.氧元素参与了氮循环 B.②中合成氨属于人工固氮
C.①②③中氮元素均被氧化 D.含氮有机物和含氮无机物可相互转化
2.下列氧化物的性质与用途具有对应关系的是( )
A.氧化钙能吸收水分,可用作食品包装干燥剂
B.氧化铁能与酸反应,可用作油墨的红色颜料
C.二氧化硫有氧化性,可用作葡萄酒抗氧化剂
D.二氧化硅硬度较高,可用作光导纤维的原料
3.农业生产中常用到的氮肥很多是铵盐,检验某化肥中铵盐的方法是:取出少量待检物于试管中,然后( )
A.加热,将红色石蕊试纸放在试管口检验
B.加入苛性钠溶液,加热,将湿润的红色石蕊试纸放在试管口检验
C.加入碱溶液,加热,再滴入酚酞试液
D.用鼻子闻
4.2022年科技创新累累硕果,加快实现了高水平建设科技强国。下列有关说法错误的是( )
A.国产航母海上巡航,航母甲板是高强度钢材,钢是一种铁碳合金
B.“华龙一号”核电项目中核反应堆所用铀棒中含有的与互为同位素
C.“北斗导航”系统应用一体化芯片手机,芯片成分为
D.C919大飞机采用的材料中使用了高温陶瓷材料氮化硅,属于新型无机非金属材料
5.用硫及其化合物制硫酸有下列三种反应途径,某些反应条件和产物已省略,下列说法不正确的是( )
途径①:
途径②:
途径③:
A.途径①的反应中体现了浓的强氧化性
B.途径②、③的第二步反应在实际生产中可以通过增大的浓度来降低成本
C.由途径①、②、③分别制取,理论上各消耗,各转移
D.途径②、③比途径①污染相对小且原子利用率高,更能体现“绿色化学”的理念
6.学科思想方法是学好化学的关键,下列有关学科思想方法的理解不正确的是( )
A.物质的结构与性质关联,根据物质的结构可以分析其性质。例如氮分子中存在叁键,断开它需要较多的能量,所以N,的化学性质稳定
B.基于物质的类别与化合价,可以预测物质的性质。例如从硫的化合价角度分析,既有氧化性又有还原性
C.类比是研究物质性质的常用方法之一,可预测许多物质的性质。例如铝与稀硫酸反应生成氢气,则铝与稀硝酸反应生成氢气
D.模型在科学认识中具有描述、解释和预测等功能,例如电离模型很好地解释了酸、碱、盐的某些性质
7.下列情况会对人体健康造成较大危害的是( )
A.用漂白食品 B.用食醋清洗热水瓶胆内壁附着的水垢
C.自来水中通入少量进行消毒杀菌 D.用小苏打发酵面团制作馒头
8.常温下,下列各组离子在指定条件下能大量共存的是( )
A.溶液:
B.使酚酞变红色的溶液:
C.某无色溶液:
D.的溶液:
9.设为阿伏伽德罗常数的值。下列说法正确的是( )
A.分子中所含的数目为
B.的溶液中所含的数目为
C.与足量S充分反应,转移电子数为
D.与足量反应,生成的分子数小于
10.某实验小组在培养皿中设计了如下微型实验:向亚硫酸钠固体上滴加几滴的浓硫酸,立即用表面皿盖住培养皿。下列说法正确的是( )
A.b处溶液紫色褪去,证明具有漂白性
B.c处出现黄色浑浊,表明具有氧化性
C.d处发生反应:
D.e处紫色石蕊溶液由紫色变为红色,后又逐渐褪色
11.某小组同学进行铜与浓硫酸反应时,发现有黑色物质产生。该小组同学猜测,黑色物质中可能含有和。针对产生的黑色物质,该小组同学继续进行实验探究,获得数据如下表所示。
硫酸浓度 黑色物质出现的温度 黑色物质消失的温度
15 约150 约236
16 约140 约250
18 约120 不消失
下列推测不合理的是( )
A.硫酸浓度越大,黑色物质越易出现、越难消失
B.黑色物质消失过程中伴随大量生成
C.硫酸浓度为时,若先升温至以上,再将铜丝与浓硫酸接触,可以避免黑色物质产生
D.若取黑色物质洗涤、干燥后,加稀硫酸,固体质量不变,说明黑色物质中不含
12.下列离子方程式正确的是( )
A.向溶液中滴加盐酸:
B.向溶液中通入足量
C.向溶液中通入足量:
D.用热溶液洗涤试管内壁的硫黄:
13.足量的铜与一定体积的浓硝酸充分反应后生成硝酸铜以及和的混合气体,若将所得到的气体与标准状况下氧气混合后充入足量水中,气体恰好完全反应得到硝酸。则向反应后的溶液中加入的氢氧化钠溶液使其中的铜离子恰好完全沉淀,需要消耗氢氧化钠的溶液的体积是( )
A. B. C. D.
14.将标准状况下和的混合气体通过灼热的三氧化二铬(催化剂),氨全部被氧化。将反应后气体全部通入水中,无气体剩余,制得100L溶液,则该溶液的浓度为( )
A. B. C. D.
15.把含的混合溶液分成两等份,一份用烧碱刚好把全部赶出,另一份与溶液完全反应消耗,则原溶液中为( )
A. B. C. D.
第Ⅱ卷(非选择题55分)
二、非选择题:本题共4小题,共55分
16.完成下列化学方程式(是离子反应的写离子方程式):
(1)等物质的量二氧化硫和氯气通入水中
(2)二氧化硫通入酸性高锰酸钾溶液中
(3)高温煅烧黄铁矿
(4)炭与浓硫酸加热
(5)硫与浓硫酸加热
(6)铜和浓硫酸加热
(7)铜和浓硝酸(实验室制)
(8)铜和稀硝酸(实验室制)
(9)二氧化氮和一氧化氮混合气体通入苛性钠溶液中
(10)二氧化氮通入苛性钠溶液中
17.S02是常见的大气污染物,燃煤是产生的主要原因。工业上有多种方法可以减少的排放。
(1)往煤中添加一些生石灰,可使燃煤过程中产生的转化成硫酸钙。该反应的化学方程式为______________________________。
(2)可用多种溶液做燃煤烟气中的吸收液。
①分别用等物质的量浓度的溶液和溶液做吸收液,当生成等物质的量时,两种吸收液体积比__________。
②溶液吸收了足量的后会失效,可将这种失效的溶液与一定量的石灰水溶液充分反应后过滤,使溶液再生,再生过程的化学方程式为______________________________。
(3)甲同学认为溶液可以做的吸收液。为此甲同学设计如图实验(夹持装置和加热装置略,气密性已检验):
已知:反应开始后,A中固体表面有气泡产生同时有白雾生成;B中有白色沉淀。
甲认为B中白色沉淀是与溶液反应生成的,所以溶液可做吸收液。
乙同学认为B中的白色沉淀是,产生的原因可能是
①A中产生的白雾是浓硫酸的酸雾,进入B中与溶液反应生成沉淀。
②________________________________________
为证明与溶液不能得到沉淀,乙同学对甲同学的实验装置做了如图改动并实验(夹持装置和加热装置略,气密性已检验):
反应开始后,A中固体表面有气泡产生同时有白雾生成;B、C试管中除了有气泡外,未见其他现象;D中红色褪去。
③试管B中试剂是溶液__________;滴加浓硫酸之前的操作是____________________。
④通过甲乙两位同学的实验,得出的结论是______________________________。
18.硝酸是一种重要的化工原料,氨氧化法是工业生产中制取硝酸的主要途径,某兴趣小组在实验室模拟氨氧化法制硝酸,实验装置如图所示,回答下列问题:
(注:氯化钙可以与反应生成八氨合氯化钙。)
(1)仪器a的名称为__________,其中加的试剂为__________。
(2)实验时先点燃C中的酒精灯,当催化剂由暗绿色变为微红时通入空气,后出现暗红色,移去酒精灯,能保持红热状态的原因是____________________,装置C中发生反应的总反应化学方程式为______________________________。
(3)装置D的作用是____________________,装置G的作用是____________________。
(4)反应开始后,在装置E中看到的现象是______________________________。
(5)实验结束后,证明有生成的操作是______________________________。
19.一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。
试回答下列问题:
(1)写出下列物质化学式:A____________________;C____________________;
(2)写出F的电子式:______________________________;
(3)写出溶液E与共热反应的离子方程式:______________________________;
(4)写出A和新制氯水反应的离子方程式:______________________________。
参考答案:
一、选择题:本题共15小题,每小题3分,共45分。每小题有一个选项符合题意。
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
C A B C C C A D D B B D C B B
二、非选择题:本题共4小题,共55分.
16.(20分)完成下列离子方程式:
二氧化硫和氯气等物质的量通入水中
二氧化硫通入酸性高锰酸钾溶液中
高温煅烧黄铁刊
炭与浓硫酸加热
硫与浓硫酸加热
铜和浓硫酸加热
铜和浓硝酸
(实验室制)
铜和稀硝酸
(实验室制)
二氧化氮和一氧化氮混合气体通入苛性钠溶液
17.(14分)(1)
(2)
(3)A中产生的与装置内空气中的进入B中与溶液反应生成沉淀饱和
打开弹簧夹,通入,一段时间后关闭弹簧夹
不能用溶液做吸收的吸收液(或与溶液不能得到沉淀)
18.(11分)(1)球形干燥管 碱石灰
(2)该反应为放热反应
(3)除去氨气和水蒸气 吸收尾气
(4)气体变为红棕色
(5)取少量F中的液体于试管中,滴加几滴紫色石蕊试液,溶液变红,证明有生成
19.(10分)
同课章节目录
