2024年化学 中考 第3讲 碳和碳的氧化物(含答案)
文档属性
| 名称 | 2024年化学 中考 第3讲 碳和碳的氧化物(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 908.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-02 00:00:00 | ||
图片预览



文档简介
第3讲 碳和碳的氧化物
命题点1 碳单质的性质和用途
1.下列有关碳的性质和用途,对应不合理的是( )
A.金刚石切割玻璃——硬度大
B.焦炭冶炼金属——还原性
C.活性炭除色素——吸附性
D.石墨作电极——质软
2.(易错易混)下列说法正确的是( )
A.金刚石、石墨、C60均为由原子构成的物质
B.木炭、活性炭、焦炭、炭黑都属于碳单质
C.石墨转化为金刚石属于化学变化
D.金刚石和石墨物理性质和化学性质均相同
[知识逐点过]
1.碳单质的物理性质及用途
名称 金刚石 石墨 C60
物理性质 天然存在的最____的物质 质软,具有优良的____性,有滑腻感
用途 作钻头、裁玻璃、制装饰品等 制作铅笔芯、石墨电极、润滑剂等 可能用于超导、催化等领域
说明 由于金刚石、石墨中碳原子的________不同,因此它们的物理性质存在较大差异
【知识补充】活性炭、木炭等主要成分为碳单质
2.碳单质的化学性质及用途
化学性质 结论或化学方程式 用途
稳定性 常温下,碳的化学性质______ 用墨书写字画
可燃性 a.氧气充足:________________(写化学方程式,下同) b.氧气不足:__________________ 作燃料
还原性 a.与二氧化碳反应:__________________(吸热反应) b.与氧化铜反应:________________; 现象:_____________________________ c.与氧化铁反应:__________________________; 现象:_____________________________
冶炼金属
真题演练
1.判断说法的正误:金刚石、石墨、活性炭性质相同(2018.4B)( )
2.焙烧硅藻土、活性炭都有________的结构,能起到吸附作用。
3.画作用水墨打底,保存千年而不变色,说明常温下碳的化学性质_____________。
[拓展训练]
4.[中华优秀传统文化]中国古籍文房四宝指的是“笔、墨、纸、砚”,其中“墨”的主要成分是炭黑。炭黑的下列性质属于化学性质的是( )
A.可燃性 B.常温下呈固态 C.难溶于水 D.熔点高
5.金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是( )
A.构成金刚石和石墨的原子大小不同 B.金刚石和石墨中原子排列方式相同
C.1 g金刚石和1 g石墨所含原子数相同 D.金刚石和石墨在氧气中都不能燃烧
6.石墨、活性炭和木炭在生产生活中有着广泛的应用。
(1)石墨的用途可以是________(选一个即可,填标号)。
A.用于制铅笔芯 B.用作电极 C.用于切割大理石
(2)活性炭作冰箱除味剂,是利用其________(填“物理”或“化学”)性质。
(3)木炭可用作燃料。木炭充分燃烧的化学方程式为________________________。
命题点2 一氧化碳和二氧化碳
1.(易错易混)下列有关CO和CO2的说法正确的是( )
A.CO和CO2组成元素相同,二者化学性质相似
B.CO和CO2都能与水反应,都能使紫色石蕊溶液变红
C.CO和CO2都能用于冶炼金属
D.CO和CO2在一定条件下可相互转化
2.根据下列实验回答问题。
(1)实验1中,①②为用紫色石蕊溶液润湿的纸花。能说明CO2密度大于空气的现象是_____________。欲证明CO2能与水反应,还需补充的实验是____________________。
【教材改编维度】 第2(1)题:关联整合教材实验 将教材上倾倒二氧化碳及二氧化碳与水反应的实验进行整合,用一个装置进行两个实验的分析探究。
(2)分别用等量水和NaOH溶液进行实验2,验证CO2能与NaOH反应。实验中加入等量水的目的是________,实验中可观察到的现象是____________________________。
[知识逐点过]
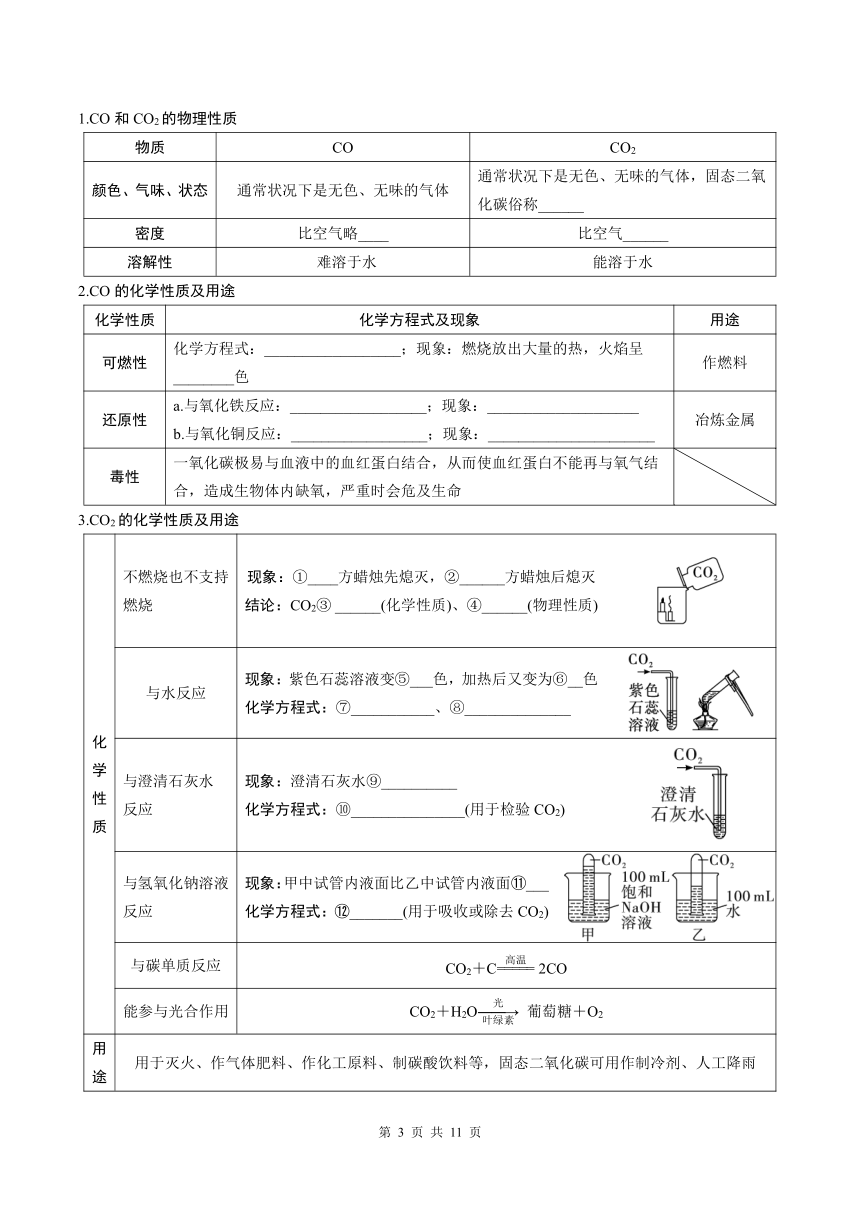
1.CO和CO2的物理性质
物质 CO CO2
颜色、气味、状态 通常状况下是无色、无味的气体 通常状况下是无色、无味的气体,固态二氧化碳俗称______
密度 比空气略____ 比空气______
溶解性 难溶于水 能溶于水
2.CO的化学性质及用途
化学性质 化学方程式及现象 用途
可燃性 化学方程式:__________________;现象:燃烧放出大量的热,火焰呈________色 作燃料
还原性 a.与氧化铁反应:__________________;现象:____________________ b.与氧化铜反应:__________________;现象:______________________ 冶炼金属
毒性 一氧化碳极易与血液中的血红蛋白结合,从而使血红蛋白不能再与氧气结合,造成生物体内缺氧,严重时会危及生命
3.CO2的化学性质及用途
化学性质 不燃烧也不支持燃烧 现象:①____方蜡烛先熄灭,②______方蜡烛后熄灭 结论:CO2③ ______(化学性质)、④______(物理性质)
与水反应 现象:紫色石蕊溶液变⑤___色,加热后又变为⑥__色 化学方程式:⑦___________、⑧______________
与澄清石灰水 反应 现象:澄清石灰水⑨__________ 化学方程式:⑩_______________(用于检验CO2)
与氢氧化钠溶液反应 现象:甲中试管内液面比乙中试管内液面 ___ 化学方程式: _______(用于吸收或除去CO2)
与碳单质反应 CO2+C 2CO
能参与光合作用 CO2+H2O 葡萄糖+O2
用途 用于灭火、作气体肥料、作化工原料、制碳酸饮料等,固态二氧化碳可用作制冷剂、人工降雨
4.CO2的制取
5.温室效应与低碳生活
自然界中的碳氧循环
温室效应加剧 原因 大气中________含量过高
缓解加剧的措施 a.控制排放——减少化石燃料的使用,使用清洁能源 b.增强吸收——大力植树造林,严禁乱砍滥伐
低碳生活 概念 所谓“低碳”,就是较低的________的排放
日常做法 减少使用一次性筷子和塑料袋,步行或乘坐公共交通工具出行等
6.CO和CO2的鉴别及除杂
鉴别 与碱反应 通入澄清石灰水中,变浑浊的是①________(填化学式,下同)
与指示剂作用 通入紫色石蕊溶液中,变红的是②________
与金属氧化物反应 通过灼热的氧化铜,有红色固体生成的是③________
与氧气反应 能燃烧的是④________
除杂(括号内为杂质) CO2(CO) 通过足量灼热的⑤________
CO(CO2) 依次通过足量的⑥________溶液、浓硫酸
通过足量灼热的炭粉
[构建物质网络]
1.请写出下列物质的化学式
甲____________ 乙____________
2.请写出图中对应标号的化学方程式
④________________________________________________________________________;
⑤________________________________________________________________________;
⑦________________________________________________________________________;
⑧________________________________________________________________________。
真题演练
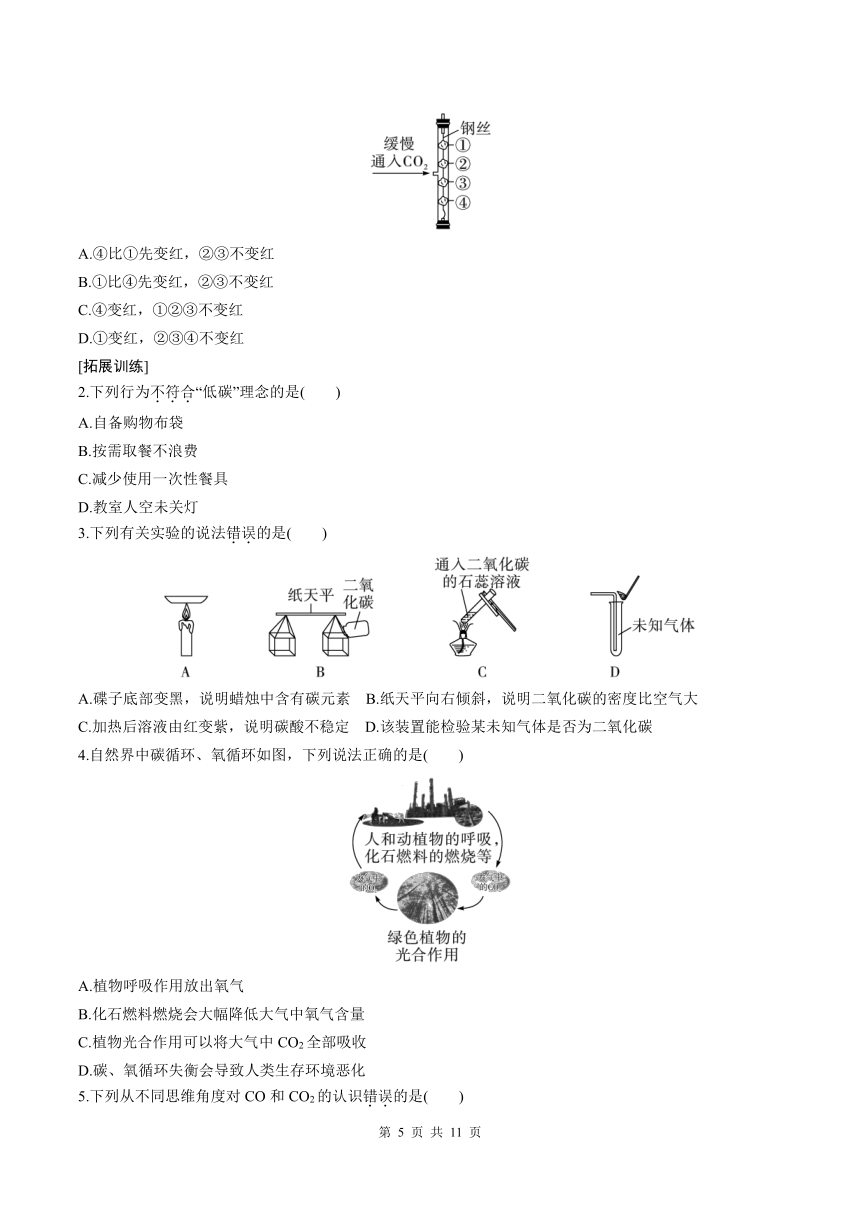
1.如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。下列能准确描述实现现象的是( )
A.④比①先变红,②③不变红
B.①比④先变红,②③不变红
C.④变红,①②③不变红
D.①变红,②③④不变红
[拓展训练]
2.下列行为不符合“低碳”理念的是( )
A.自备购物布袋
B.按需取餐不浪费
C.减少使用一次性餐具
D.教室人空未关灯
3.下列有关实验的说法错误的是( )
A.碟子底部变黑,说明蜡烛中含有碳元素 B.纸天平向右倾斜,说明二氧化碳的密度比空气大
C.加热后溶液由红变紫,说明碳酸不稳定 D.该装置能检验某未知气体是否为二氧化碳
4.自然界中碳循环、氧循环如图,下列说法正确的是( )
A.植物呼吸作用放出氧气
B.化石燃料燃烧会大幅降低大气中氧气含量
C.植物光合作用可以将大气中CO2全部吸收
D.碳、氧循环失衡会导致人类生存环境恶化
5.下列从不同思维角度对CO和CO2的认识错误的是( )
A.构成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子
B.性质:通常情况下,CO2不支持燃烧;CO支持燃烧
C.用途:固态CO2可用于人工降雨;CO可作燃料
D.危害:CO2无毒;CO易与血液中的血红蛋白结合引起中毒
6.生活中含碳物质种类繁多、应用广泛。根据如图回答问题。
(1)图1中的物质类别未包括________(填字母)。
a.酸 b.碱 c.盐 d.有机物
(2)写出图1中属于分解反应的化学方程式________________________(写一个即可)。
(3)写出图1中可用于鉴别一氧化碳和二氧化碳的反应是________(填序号)。
(4)上述转化⑦的一个用途是________________。
(5)小明按如图2进行趣味实验,将U形管开口端放入烧杯内,观察到溶液进入U形管并流入另一端。
①烧杯内溶液呈________色。
②U形管开口端放入烧杯后,管内气体压强_____(填“增大”“不变”或“减小”),溶液在管内上升并流入另一端。
7.已知草酸钙(CaC2O4)加热易分解:CaC2O4 CaO+CO↑+CO2↑。为验证分解产物中既有CO又有CO2,小明设计如下实验装置。回答下列问题。
(1)B中实验现象是______________。
(2)Fe2O3中铁元素化合价为________,写出其在D中发生反应的化学方程式_________________________。
(3)小华认为,在D装置后再增加装置B才能验证CO的存在,小明认为不加装置B就可验证,小明的理由是______________________________________________________。
(4)从环保的角度考虑,该实验装置的不足之处是________________________________。
第3讲 碳和碳的氧化物
[基础训练]
1.下列关于碳单质的说法中正确的是( )
A.硬度都很大
B.都可用于制造铅笔芯
C.都是黑色固体
D.常温下化学性质都不活泼
2.关于碳及其化合物的说法正确的是( )
A.一氧化碳有还原性、毒性
B.二氧化碳是一种污染性气体
C.含碳化合物属于有机物
D.活性炭具有吸附性,木炭没有吸附性
3.下列实验操作不能达到目的的是 ( )
选项 A B C D
目的及操作 鉴别CO2、CO 鉴别CO2、CO 除去CO2 除去CO
【易错剖析】 第3D题 易错点:只根据CO能与O2在点燃条件生成CO2的性质判断方案是否正确,忽略了CO2中含有少量CO时,CO不能被点燃。 避错指南:除杂时,不仅要考虑需除去的物质,还要考虑待保留的物质,需结合两者的性质设计方案,确保需除去的物质被转化且待保留的物质不受影响。由此,此题可设计“将气体通入灼热的氧化铜”等方法除去CO2中的CO。
4.碳元素是组成物质种类最多的元素,许多含碳元素的物质都与生活息息相关。
(1)金刚石、石墨、C60均是由碳元素组成的单质,其中由分子构成的是________。
(2)CO可作燃料,其完全燃烧的化学方程式为__________________________。
(3)明代《天工开物》中,提到有关墨的制作方法:凡墨,烧烟凝质而为之。“烟”最可能是________ (填“木炭”“炭黑”或“石墨”)。
(4)二氧化碳可用于灭火是利用其具有________________________________的性质。
(5)生活中可减少二氧化碳排放的做法有________________________________。
5.根据如图实验装置,回答问题:
图1
(1)图1中标有①的仪器名称为________。
(2)实验室用石灰石和稀盐酸制取纯净、干燥的二氧化碳,反应的化学方程式为________________________,请从图1中选择所需装置,所选装置接口字母连接顺序为________。
(3)不使用块状石灰石和稀硫酸制取二氧化碳的原因是______________________________________________。
(4)[新考法][创新装置]同学们利用制取的二氧化碳进行图2所示的二氧化碳性质探究实验。
图2
①可证明 CO2能与水反应的现象是________________,密度比空气大的现象是____________。
②燃着的木条熄灭,由此可得出CO2具有的性质是____________________。
6.减少CO2排放、实现碳中和已成为全球共识,碳封存、碳捕集、碳循环是实现碳中和的主要途径。
探究一:碳封存。将 CO2注入油气层起到驱油作用,既提高油的采收率,又实现碳封存。
图1
(1)用图1装置模拟油气田封存 CO2。连接 A、B装置,将 CO2从______端(填“a”或 “b”)通入装有油的广口瓶中封存,油被压入烧杯中。
探究二:碳捕集。小组同学探究酸、碱和盐的性质及 CO2的捕集。
【设计与实验】甲同学设计如图2装置(夹持仪器已省略),检查装置气密性,装入药品如图所示,关闭 k1、k2、k3。打开 k1,向装满 CO2的烧瓶 C中注入 50 mLNaOH溶液,再关闭 k1;打开 k2,观察到D中部分液体进入 C中,有白色沉淀产生,再关闭 k2。
图2
【实验结论】 CO2能与 NaOH反应。
【交流与讨论】(2)乙同学认为甲同学得出结论的证据不足,理由是________________。
(3)[新考法][过程开放]在甲同学实验后,乙同学取 C中物质进行了补充实验,经分析判断,证明了 CO2能与 NaOH反应。则乙同学的方案是________________________(写出实验操作和现象)。
(4)用 NaOH溶液“捕集 CO2”的化学方程式为________________________。
【实验拓展】(5)打开k3,观察到E中稀盐酸进入D中,溶液变为无色。
①D中发生反应的化学方程式为______________________________。
②为确定E中稀盐酸进入 D中反应后的溶质成分(酚酞除外),下列药品可选用的有________(填字母序号)。
a.石蕊溶液 b.CuSO4溶液 c.AgNO3溶液 d.Fe2O3固体
(6)通过探究二,可归纳出碱的化学性质有____________________________。
【解题有策略】 第6题探究二 排除含干扰物的物质检验方法 解题对策如下: 第1步:找出需检验的物质和干扰物质:如本题的实质是检验C中是否存在Na2CO3,干扰的物质可能是NaOH或CO2。 第2步:分2种方案说明:①选择和需检验的物质、干扰物质的现象不同的试剂,(2)中进入C中的试剂为Ca(OH)2溶液,与Na2CO3和CO2反应的现象均为产生白色沉淀,故得出结论的证据不足。而(3)中设计方案时则可取C中的溶液,选取与Na2CO3和NaOH混合现象不同的BaCl2溶液等验证CO2能与NaOH反应。②先除去干扰离子,再证明需检验的离子,注意此过程不能引入需检验的离子,如碱变质程度的验证中可利用氯化钙等先除去CO,再检验OH-是否存在。
探究三:碳循环。利用 CO2与 H2反应,产生有应用价值的液体有机物,属于碳中和技术。
(7)利用 CO2与 H2在一定条件下反应生成甲醇(CH3OH)和水,反应的化学方程式为__________________。
[综合提升]
7.碳及其化合物存在如下转化关系:C→CO CO2 X(“→”表示一种物质会一步转化成另一种物质)。下列有关说法错误的是( )
A.由 C转化为 CO2的过程中碳元素的化合价依次升高
B.CO只能通过与 O2反应转化为 CO2
C.CO2可通过与 C反应转化为 CO,化学方程式为 C+CO2 2CO
D.X可能是酸或盐
【教材改编维度】 第7题 变转化图呈现方式:改变教材习题中物质间的转化关系图的呈现方式,且部分物质未给出。
第3讲
命题点1
1.D 2.C
知识逐点过
1.硬 导电 排列方式
2.不活泼(或稳定) C+O2 CO2 2C+O2 2CO
C+CO2 2CO C+2CuO 2Cu+CO2↑
黑色固体逐渐变红 3C+2Fe2O3 4Fe+3CO2↑
红棕色固体逐渐变黑
真题演练
1.×
2.疏松多孔
3.不活泼(或稳定)
4.A 5.C
6.(1)A(或B) (2)物理 (3)C+O2 CO2
命题点2
1.D
2.(1)通入CO2后,②处纸花先变红,①处纸花后变红 将二氧化碳倾倒在干燥的紫色石蕊纸花上(合理即可)
(2)作对照实验 气球均变大,且注入氢氧化钠溶液时的气球比注入水时变得更大
知识逐点过
1.干冰 小 大
2.2CO+O2 2CO2 蓝 3CO+Fe2O3 2Fe+3CO2
红棕色固体逐渐变黑 CO+CuO Cu+CO2 黑色固体逐渐变红
3.①下 ②上 ③不燃烧也不支持燃烧 ④密度比空气大 ⑤红 ⑥紫
⑦H2O+CO2=== H2CO3 ⑧H2CO3 H2O+CO2↑ ⑨变浑浊 ⑩Ca(OH)2+CO2===CaCO3↓+H2O
高
CO2+2NaOH===Na2CO3+H2O
5.二氧化碳(或CO2) 二氧化碳(或CO2)
6.①CO2 ②CO2 ③CO ④CO ⑤CuO(合理即可) ⑥NaOH
构建物质网络
1.Na2CO3 CO
2.④2HCl+Na2CO3=== 2NaCl+H2O+CO2↑(合理即可)
⑤CaCl2+Na2CO3=== 2NaCl+CaCO3↓(合理即可)
⑦C2H5OH+3O2 2CO2+3H2O
⑧CO2+Ca(OH)2=== CaCO3↓+H2O
真题演练
1.A 2.D 3.D 4.D 5.B
6.(1)b (2)CaCO3 CaO+CO2↑(或H2CO3 === H2O+CO2↑) (3)⑤ (4)制碳酸饮料(合理即可)
(5)①红 ②减小
7.(1)澄清石灰水变浑浊 (2)+3 3CO+Fe2O3 2Fe+3CO2
(3)D中玻璃管内观察到红棕色粉末变黑,即可证明有CO存在(合理即可) (4)缺少尾气处理装置(合理即可)
命题点1 碳单质的性质和用途
1.下列有关碳的性质和用途,对应不合理的是( )
A.金刚石切割玻璃——硬度大
B.焦炭冶炼金属——还原性
C.活性炭除色素——吸附性
D.石墨作电极——质软
2.(易错易混)下列说法正确的是( )
A.金刚石、石墨、C60均为由原子构成的物质
B.木炭、活性炭、焦炭、炭黑都属于碳单质
C.石墨转化为金刚石属于化学变化
D.金刚石和石墨物理性质和化学性质均相同
[知识逐点过]
1.碳单质的物理性质及用途
名称 金刚石 石墨 C60
物理性质 天然存在的最____的物质 质软,具有优良的____性,有滑腻感
用途 作钻头、裁玻璃、制装饰品等 制作铅笔芯、石墨电极、润滑剂等 可能用于超导、催化等领域
说明 由于金刚石、石墨中碳原子的________不同,因此它们的物理性质存在较大差异
【知识补充】活性炭、木炭等主要成分为碳单质
2.碳单质的化学性质及用途
化学性质 结论或化学方程式 用途
稳定性 常温下,碳的化学性质______ 用墨书写字画
可燃性 a.氧气充足:________________(写化学方程式,下同) b.氧气不足:__________________ 作燃料
还原性 a.与二氧化碳反应:__________________(吸热反应) b.与氧化铜反应:________________; 现象:_____________________________ c.与氧化铁反应:__________________________; 现象:_____________________________
冶炼金属
真题演练
1.判断说法的正误:金刚石、石墨、活性炭性质相同(2018.4B)( )
2.焙烧硅藻土、活性炭都有________的结构,能起到吸附作用。
3.画作用水墨打底,保存千年而不变色,说明常温下碳的化学性质_____________。
[拓展训练]
4.[中华优秀传统文化]中国古籍文房四宝指的是“笔、墨、纸、砚”,其中“墨”的主要成分是炭黑。炭黑的下列性质属于化学性质的是( )
A.可燃性 B.常温下呈固态 C.难溶于水 D.熔点高
5.金刚石和石墨是常见的碳单质,其结构如图所示。下列说法正确的是( )
A.构成金刚石和石墨的原子大小不同 B.金刚石和石墨中原子排列方式相同
C.1 g金刚石和1 g石墨所含原子数相同 D.金刚石和石墨在氧气中都不能燃烧
6.石墨、活性炭和木炭在生产生活中有着广泛的应用。
(1)石墨的用途可以是________(选一个即可,填标号)。
A.用于制铅笔芯 B.用作电极 C.用于切割大理石
(2)活性炭作冰箱除味剂,是利用其________(填“物理”或“化学”)性质。
(3)木炭可用作燃料。木炭充分燃烧的化学方程式为________________________。
命题点2 一氧化碳和二氧化碳
1.(易错易混)下列有关CO和CO2的说法正确的是( )
A.CO和CO2组成元素相同,二者化学性质相似
B.CO和CO2都能与水反应,都能使紫色石蕊溶液变红
C.CO和CO2都能用于冶炼金属
D.CO和CO2在一定条件下可相互转化
2.根据下列实验回答问题。
(1)实验1中,①②为用紫色石蕊溶液润湿的纸花。能说明CO2密度大于空气的现象是_____________。欲证明CO2能与水反应,还需补充的实验是____________________。
【教材改编维度】 第2(1)题:关联整合教材实验 将教材上倾倒二氧化碳及二氧化碳与水反应的实验进行整合,用一个装置进行两个实验的分析探究。
(2)分别用等量水和NaOH溶液进行实验2,验证CO2能与NaOH反应。实验中加入等量水的目的是________,实验中可观察到的现象是____________________________。
[知识逐点过]
1.CO和CO2的物理性质
物质 CO CO2
颜色、气味、状态 通常状况下是无色、无味的气体 通常状况下是无色、无味的气体,固态二氧化碳俗称______
密度 比空气略____ 比空气______
溶解性 难溶于水 能溶于水
2.CO的化学性质及用途
化学性质 化学方程式及现象 用途
可燃性 化学方程式:__________________;现象:燃烧放出大量的热,火焰呈________色 作燃料
还原性 a.与氧化铁反应:__________________;现象:____________________ b.与氧化铜反应:__________________;现象:______________________ 冶炼金属
毒性 一氧化碳极易与血液中的血红蛋白结合,从而使血红蛋白不能再与氧气结合,造成生物体内缺氧,严重时会危及生命
3.CO2的化学性质及用途
化学性质 不燃烧也不支持燃烧 现象:①____方蜡烛先熄灭,②______方蜡烛后熄灭 结论:CO2③ ______(化学性质)、④______(物理性质)
与水反应 现象:紫色石蕊溶液变⑤___色,加热后又变为⑥__色 化学方程式:⑦___________、⑧______________
与澄清石灰水 反应 现象:澄清石灰水⑨__________ 化学方程式:⑩_______________(用于检验CO2)
与氢氧化钠溶液反应 现象:甲中试管内液面比乙中试管内液面 ___ 化学方程式: _______(用于吸收或除去CO2)
与碳单质反应 CO2+C 2CO
能参与光合作用 CO2+H2O 葡萄糖+O2
用途 用于灭火、作气体肥料、作化工原料、制碳酸饮料等,固态二氧化碳可用作制冷剂、人工降雨
4.CO2的制取
5.温室效应与低碳生活
自然界中的碳氧循环
温室效应加剧 原因 大气中________含量过高
缓解加剧的措施 a.控制排放——减少化石燃料的使用,使用清洁能源 b.增强吸收——大力植树造林,严禁乱砍滥伐
低碳生活 概念 所谓“低碳”,就是较低的________的排放
日常做法 减少使用一次性筷子和塑料袋,步行或乘坐公共交通工具出行等
6.CO和CO2的鉴别及除杂
鉴别 与碱反应 通入澄清石灰水中,变浑浊的是①________(填化学式,下同)
与指示剂作用 通入紫色石蕊溶液中,变红的是②________
与金属氧化物反应 通过灼热的氧化铜,有红色固体生成的是③________
与氧气反应 能燃烧的是④________
除杂(括号内为杂质) CO2(CO) 通过足量灼热的⑤________
CO(CO2) 依次通过足量的⑥________溶液、浓硫酸
通过足量灼热的炭粉
[构建物质网络]
1.请写出下列物质的化学式
甲____________ 乙____________
2.请写出图中对应标号的化学方程式
④________________________________________________________________________;
⑤________________________________________________________________________;
⑦________________________________________________________________________;
⑧________________________________________________________________________。
真题演练
1.如图所示实验中,①④为用紫色石蕊溶液润湿的棉球,②③为浸过紫色石蕊溶液的干燥棉球。下列能准确描述实现现象的是( )
A.④比①先变红,②③不变红
B.①比④先变红,②③不变红
C.④变红,①②③不变红
D.①变红,②③④不变红
[拓展训练]
2.下列行为不符合“低碳”理念的是( )
A.自备购物布袋
B.按需取餐不浪费
C.减少使用一次性餐具
D.教室人空未关灯
3.下列有关实验的说法错误的是( )
A.碟子底部变黑,说明蜡烛中含有碳元素 B.纸天平向右倾斜,说明二氧化碳的密度比空气大
C.加热后溶液由红变紫,说明碳酸不稳定 D.该装置能检验某未知气体是否为二氧化碳
4.自然界中碳循环、氧循环如图,下列说法正确的是( )
A.植物呼吸作用放出氧气
B.化石燃料燃烧会大幅降低大气中氧气含量
C.植物光合作用可以将大气中CO2全部吸收
D.碳、氧循环失衡会导致人类生存环境恶化
5.下列从不同思维角度对CO和CO2的认识错误的是( )
A.构成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子
B.性质:通常情况下,CO2不支持燃烧;CO支持燃烧
C.用途:固态CO2可用于人工降雨;CO可作燃料
D.危害:CO2无毒;CO易与血液中的血红蛋白结合引起中毒
6.生活中含碳物质种类繁多、应用广泛。根据如图回答问题。
(1)图1中的物质类别未包括________(填字母)。
a.酸 b.碱 c.盐 d.有机物
(2)写出图1中属于分解反应的化学方程式________________________(写一个即可)。
(3)写出图1中可用于鉴别一氧化碳和二氧化碳的反应是________(填序号)。
(4)上述转化⑦的一个用途是________________。
(5)小明按如图2进行趣味实验,将U形管开口端放入烧杯内,观察到溶液进入U形管并流入另一端。
①烧杯内溶液呈________色。
②U形管开口端放入烧杯后,管内气体压强_____(填“增大”“不变”或“减小”),溶液在管内上升并流入另一端。
7.已知草酸钙(CaC2O4)加热易分解:CaC2O4 CaO+CO↑+CO2↑。为验证分解产物中既有CO又有CO2,小明设计如下实验装置。回答下列问题。
(1)B中实验现象是______________。
(2)Fe2O3中铁元素化合价为________,写出其在D中发生反应的化学方程式_________________________。
(3)小华认为,在D装置后再增加装置B才能验证CO的存在,小明认为不加装置B就可验证,小明的理由是______________________________________________________。
(4)从环保的角度考虑,该实验装置的不足之处是________________________________。
第3讲 碳和碳的氧化物
[基础训练]
1.下列关于碳单质的说法中正确的是( )
A.硬度都很大
B.都可用于制造铅笔芯
C.都是黑色固体
D.常温下化学性质都不活泼
2.关于碳及其化合物的说法正确的是( )
A.一氧化碳有还原性、毒性
B.二氧化碳是一种污染性气体
C.含碳化合物属于有机物
D.活性炭具有吸附性,木炭没有吸附性
3.下列实验操作不能达到目的的是 ( )
选项 A B C D
目的及操作 鉴别CO2、CO 鉴别CO2、CO 除去CO2 除去CO
【易错剖析】 第3D题 易错点:只根据CO能与O2在点燃条件生成CO2的性质判断方案是否正确,忽略了CO2中含有少量CO时,CO不能被点燃。 避错指南:除杂时,不仅要考虑需除去的物质,还要考虑待保留的物质,需结合两者的性质设计方案,确保需除去的物质被转化且待保留的物质不受影响。由此,此题可设计“将气体通入灼热的氧化铜”等方法除去CO2中的CO。
4.碳元素是组成物质种类最多的元素,许多含碳元素的物质都与生活息息相关。
(1)金刚石、石墨、C60均是由碳元素组成的单质,其中由分子构成的是________。
(2)CO可作燃料,其完全燃烧的化学方程式为__________________________。
(3)明代《天工开物》中,提到有关墨的制作方法:凡墨,烧烟凝质而为之。“烟”最可能是________ (填“木炭”“炭黑”或“石墨”)。
(4)二氧化碳可用于灭火是利用其具有________________________________的性质。
(5)生活中可减少二氧化碳排放的做法有________________________________。
5.根据如图实验装置,回答问题:
图1
(1)图1中标有①的仪器名称为________。
(2)实验室用石灰石和稀盐酸制取纯净、干燥的二氧化碳,反应的化学方程式为________________________,请从图1中选择所需装置,所选装置接口字母连接顺序为________。
(3)不使用块状石灰石和稀硫酸制取二氧化碳的原因是______________________________________________。
(4)[新考法][创新装置]同学们利用制取的二氧化碳进行图2所示的二氧化碳性质探究实验。
图2
①可证明 CO2能与水反应的现象是________________,密度比空气大的现象是____________。
②燃着的木条熄灭,由此可得出CO2具有的性质是____________________。
6.减少CO2排放、实现碳中和已成为全球共识,碳封存、碳捕集、碳循环是实现碳中和的主要途径。
探究一:碳封存。将 CO2注入油气层起到驱油作用,既提高油的采收率,又实现碳封存。
图1
(1)用图1装置模拟油气田封存 CO2。连接 A、B装置,将 CO2从______端(填“a”或 “b”)通入装有油的广口瓶中封存,油被压入烧杯中。
探究二:碳捕集。小组同学探究酸、碱和盐的性质及 CO2的捕集。
【设计与实验】甲同学设计如图2装置(夹持仪器已省略),检查装置气密性,装入药品如图所示,关闭 k1、k2、k3。打开 k1,向装满 CO2的烧瓶 C中注入 50 mLNaOH溶液,再关闭 k1;打开 k2,观察到D中部分液体进入 C中,有白色沉淀产生,再关闭 k2。
图2
【实验结论】 CO2能与 NaOH反应。
【交流与讨论】(2)乙同学认为甲同学得出结论的证据不足,理由是________________。
(3)[新考法][过程开放]在甲同学实验后,乙同学取 C中物质进行了补充实验,经分析判断,证明了 CO2能与 NaOH反应。则乙同学的方案是________________________(写出实验操作和现象)。
(4)用 NaOH溶液“捕集 CO2”的化学方程式为________________________。
【实验拓展】(5)打开k3,观察到E中稀盐酸进入D中,溶液变为无色。
①D中发生反应的化学方程式为______________________________。
②为确定E中稀盐酸进入 D中反应后的溶质成分(酚酞除外),下列药品可选用的有________(填字母序号)。
a.石蕊溶液 b.CuSO4溶液 c.AgNO3溶液 d.Fe2O3固体
(6)通过探究二,可归纳出碱的化学性质有____________________________。
【解题有策略】 第6题探究二 排除含干扰物的物质检验方法 解题对策如下: 第1步:找出需检验的物质和干扰物质:如本题的实质是检验C中是否存在Na2CO3,干扰的物质可能是NaOH或CO2。 第2步:分2种方案说明:①选择和需检验的物质、干扰物质的现象不同的试剂,(2)中进入C中的试剂为Ca(OH)2溶液,与Na2CO3和CO2反应的现象均为产生白色沉淀,故得出结论的证据不足。而(3)中设计方案时则可取C中的溶液,选取与Na2CO3和NaOH混合现象不同的BaCl2溶液等验证CO2能与NaOH反应。②先除去干扰离子,再证明需检验的离子,注意此过程不能引入需检验的离子,如碱变质程度的验证中可利用氯化钙等先除去CO,再检验OH-是否存在。
探究三:碳循环。利用 CO2与 H2反应,产生有应用价值的液体有机物,属于碳中和技术。
(7)利用 CO2与 H2在一定条件下反应生成甲醇(CH3OH)和水,反应的化学方程式为__________________。
[综合提升]
7.碳及其化合物存在如下转化关系:C→CO CO2 X(“→”表示一种物质会一步转化成另一种物质)。下列有关说法错误的是( )
A.由 C转化为 CO2的过程中碳元素的化合价依次升高
B.CO只能通过与 O2反应转化为 CO2
C.CO2可通过与 C反应转化为 CO,化学方程式为 C+CO2 2CO
D.X可能是酸或盐
【教材改编维度】 第7题 变转化图呈现方式:改变教材习题中物质间的转化关系图的呈现方式,且部分物质未给出。
第3讲
命题点1
1.D 2.C
知识逐点过
1.硬 导电 排列方式
2.不活泼(或稳定) C+O2 CO2 2C+O2 2CO
C+CO2 2CO C+2CuO 2Cu+CO2↑
黑色固体逐渐变红 3C+2Fe2O3 4Fe+3CO2↑
红棕色固体逐渐变黑
真题演练
1.×
2.疏松多孔
3.不活泼(或稳定)
4.A 5.C
6.(1)A(或B) (2)物理 (3)C+O2 CO2
命题点2
1.D
2.(1)通入CO2后,②处纸花先变红,①处纸花后变红 将二氧化碳倾倒在干燥的紫色石蕊纸花上(合理即可)
(2)作对照实验 气球均变大,且注入氢氧化钠溶液时的气球比注入水时变得更大
知识逐点过
1.干冰 小 大
2.2CO+O2 2CO2 蓝 3CO+Fe2O3 2Fe+3CO2
红棕色固体逐渐变黑 CO+CuO Cu+CO2 黑色固体逐渐变红
3.①下 ②上 ③不燃烧也不支持燃烧 ④密度比空气大 ⑤红 ⑥紫
⑦H2O+CO2=== H2CO3 ⑧H2CO3 H2O+CO2↑ ⑨变浑浊 ⑩Ca(OH)2+CO2===CaCO3↓+H2O
高
CO2+2NaOH===Na2CO3+H2O
5.二氧化碳(或CO2) 二氧化碳(或CO2)
6.①CO2 ②CO2 ③CO ④CO ⑤CuO(合理即可) ⑥NaOH
构建物质网络
1.Na2CO3 CO
2.④2HCl+Na2CO3=== 2NaCl+H2O+CO2↑(合理即可)
⑤CaCl2+Na2CO3=== 2NaCl+CaCO3↓(合理即可)
⑦C2H5OH+3O2 2CO2+3H2O
⑧CO2+Ca(OH)2=== CaCO3↓+H2O
真题演练
1.A 2.D 3.D 4.D 5.B
6.(1)b (2)CaCO3 CaO+CO2↑(或H2CO3 === H2O+CO2↑) (3)⑤ (4)制碳酸饮料(合理即可)
(5)①红 ②减小
7.(1)澄清石灰水变浑浊 (2)+3 3CO+Fe2O3 2Fe+3CO2
(3)D中玻璃管内观察到红棕色粉末变黑,即可证明有CO存在(合理即可) (4)缺少尾气处理装置(合理即可)
同课章节目录
