化学人教版(2019)必修第二册7.3.3官能团与有机物的分类及性质(共35张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第二册7.3.3官能团与有机物的分类及性质(共35张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 14.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-03 13:51:25 | ||
图片预览








文档简介
(共35张PPT)
第三节 乙醇与乙酸
第3课时:官能团与有机物的分类及性质
第七章 有机化合物
有机物的官能团与物质类别的关系
01
常见官能团与有机物性质的关系
02
学习目标
1.通过旧知回顾、讨论交流,能结合实例认识有机物常见官能团,能从官能团类别的角度辨识各类有机化合物,深化“结构决定性质”的观念。
2.通过典例剖析、原理分析,了解官能团之间转化与物质类别和性质的关系,进一步理解氧化反应、取代反应、加成反应等常见有机反应类型。
3.通过归纳总结、整理提升,初步形成从烯烃(乙烯)到醇(乙醇)、醛(乙醛)、羧酸(乙酸)、酯(乙酸乙酯)的转化关系,认识多官能团有机物性质分析的基本方法。
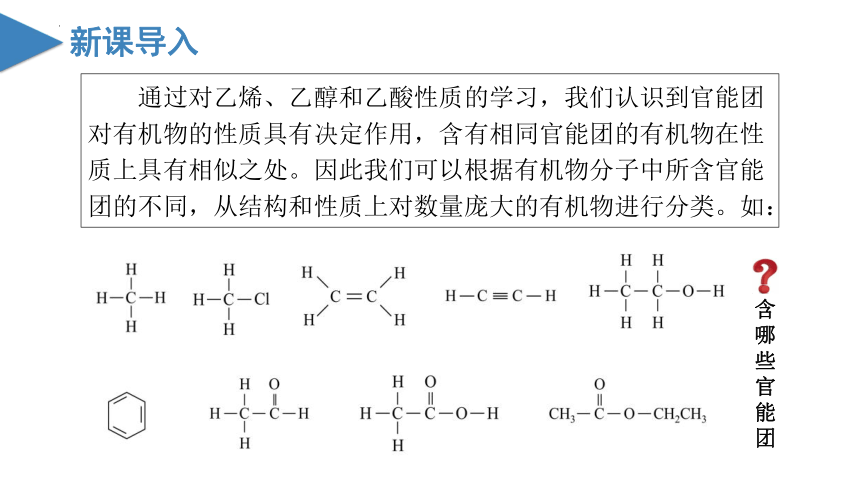
通过对乙烯、乙醇和乙酸性质的学习,我们认识到官能团对有机物的性质具有决定作用,含有相同官能团的有机物在性质上具有相似之处。因此我们可以根据有机物分子中所含官能团的不同,从结构和性质上对数量庞大的有机物进行分类。如:
含哪些官能团
有机物的官能团与物质类别的关系
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动1:阅读教材P81页内容,结合表7-2,思考常见有机物的类别
与官能团的关系,填写表格内容。
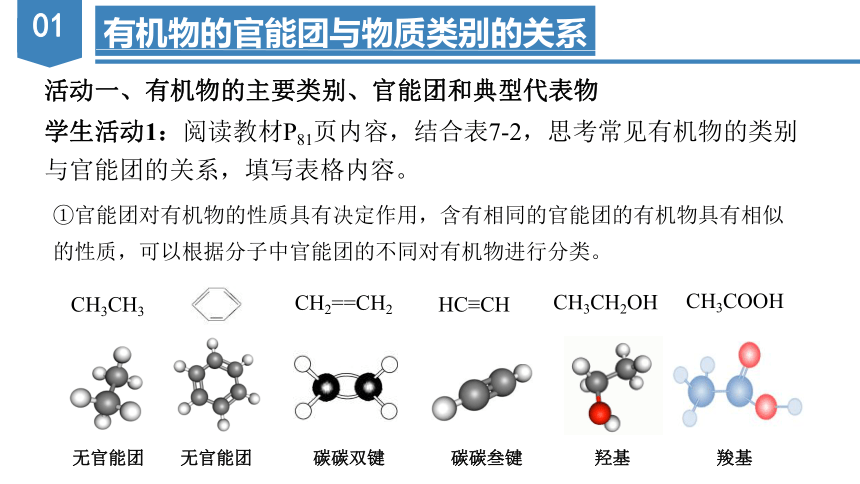
①官能团对有机物的性质具有决定作用,含有相同的官能团的有机物具有相似的性质,可以根据分子中官能团的不同对有机物进行分类。
HC≡CH
CH2==CH2
CH3CH3
CH3CH2OH
CH3COOH
无官能团
无官能团
碳碳双键
碳碳叁键
羟基
羧基
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
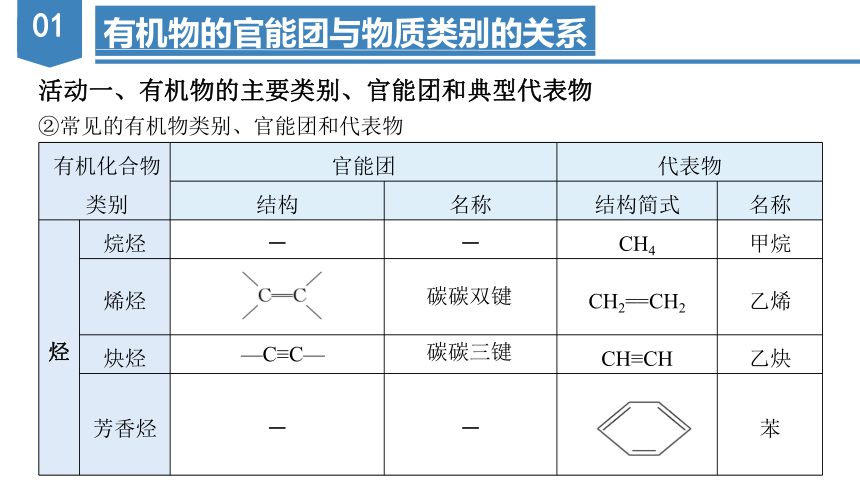
②常见的有机物类别、官能团和代表物
有机化合物类别 官能团 代表物 结构 名称 结构简式 名称
烃 烷烃 - - CH4 甲烷
烯烃 CH2==CH2 乙烯
炔烃 CH≡CH 乙炔
芳香烃 - - 苯
碳碳双键
碳碳三键
—C≡C—
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
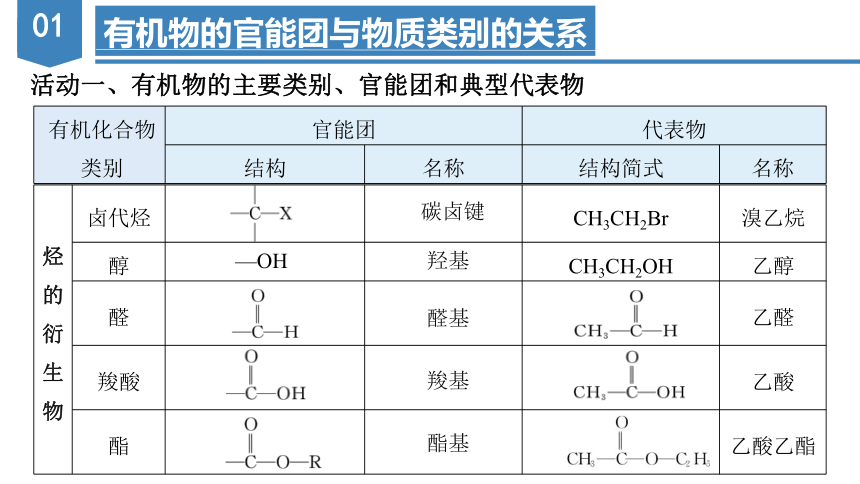
烃的衍生物 卤代烃 CH3CH2Br 溴乙烷
醇 CH3CH2OH 乙醇
醛 乙醛
羧酸 乙酸
酯 乙酸乙酯
碳卤键
羟基
醛基
羧基
酯基
有机化合物类别 官能团 代表物 结构 名称 结构简式 名称
—OH
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动2:探究书写烃的衍生物同分异构体顺序基本思维模型是什么?
①烃的衍生物同分异构体有三种具备类型:类别(官能团)异构、碳链异构、位置(官能团)异构。
②书写烃的衍生物基本思维模型
根据有机物的分子组成判定其可能的类别异构
根据类别异构写出各类别异构的可能的碳链结构(先写最长的碳链,依次写出少一个碳原子的碳链,把余下的碳原子连到相应的碳链上去。
第一步:判类别
第二步:写碳链
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动2:探究书写烃的衍生物同分异构体顺序基本思维模型是什么?
②书写烃的衍生物基本思维模型(举例略)
一般是先写不带官能团的烃的同分异构体,再在各碳链上依次移动官能团的位置,有两个或两个以上的官能团时,先连一个官能团,再连第二个官能团,依此类推。
按“碳四键”的原理,碳原子剩余的价键用氢原子去填充饱和,就可得所有同分异构体的结构简式。
第三步:移官位
第四步:氢饱和
对应训练
【典例1】下列物质中含有两种官能团的烃的衍生物为( )
A.CH3CH2NO2 B.CH2=CHBr
C.CH2Cl2 D.
B
【解析】A.该有机物含有-NO2一种官能团,故A错误;B.该有机物存在碳碳双键、-Br两种官能团,故B正确;C.该有机物存在-Cl一种官能团,故C错误;D.该有机物存在-Br一种官能团,故D错误。故选B。
对应训练
【典例2】下列关于官能团的判断中说法错误的是( )
A.醇的官能团是羟基(—OH) B.羧酸的官能团是羟基(—OH)
C.酯的官能团是酯基( ) D.烯烃的官能团是碳碳双键( )
B
【解析】醇类的官能团为羟基(—OH),A项正确;羧酸的官能团为羧基(—COOH),且羧基是个整体,不能分开,B项错误;酯的官能团是酯基( ),C项正确;烯烃的官能团是碳碳双键( ),D项正
确。故选B。
有机物的官能团与物质类别的关系
活动二、几种重要有机物组成、结构及类别
学生活动1:结合已有知识,思考几种常见烃、乙醇、乙酸、乙酸乙酯
的分子组成和结构有何特点?填写表格内容。
物质 甲烷 乙烯 乙炔 乙醇 乙酸 乙酸乙酯
分子式
电子式 —— —— ——
结构式
H-C≡C-H
CH4
C2H4
C2H2
C2H6O
C2H4O2
C4H8O2
有机物的官能团与物质类别的关系
活动二、几种重要有机物组成、结构及类别
物质 甲烷 乙烯 乙炔 乙醇 乙酸 乙酸乙酯
结构简式
球棍模型
空间填充模型
官能团 ——
类别
烷烃
烯烃
炔烃
醇
羧酸
酯
CH4
CH2=CH2
HC≡CH
CH3CH2OH或C2H5OH
CH3COOH
CH3COOCH2CH3
-C≡C-
—OH
有机物的官能团与物质类别的关系
活动二、几种重要有机物组成、结构及类别
学生活动2:结合教材P81页“方法引导”栏目,思考认识有机化合物的
一般思路是什么?
有机物结构
官能团种类
有机物性质
官能团性质
分析
联想
结论
【温馨提示】认识一种有机物,可先从结构入手,分析其碳骨架和官能团,了解其所属的类别;再结合该类有机物的一般性质推测其可能具有的性质,并通过实验进行验证;在此基础上了解该有机物的用途,即“结构决定性质,性质决定用途”
对应训练
【典例1】某种食品防腐剂的结构简式如图所示,下列关于该物质
的说法正确的是( )
A.分子式为
B.是一种有机高分子化合物
C.分子中含有三种含氧官能团
D.1mol该物质能与3mol NaOH反应
A
【解析】A.由结构简式可知该物质的分子式为:C7H10O5,故A正确;B.该物质分子式C7H10O5,相对分子质量较小,不属于高分子化合物,故B错误;C.由结构简式可知该物质含有碳碳双键,羟基,羧基三种官能团,其中含氧官能团只有羟基和羧基两种,故C错误;D.该物质中只有羧基能与NaOH反应,1mol该物质含有2mol羧基能与2molNaOH反应,故D错误;故选:A。
对应训练
A
【典例2】有机物M、N、Q之间的转化关系为 ,下列说法正确的是( )
A.M的同分异构体有3种(不考虑立体异构)
B.N分子中所有原子共平面
C.Q的名称为异丙烷 D.M、N、Q均能与溴水反应
【解析】M、N、Q分别为 、 、 。求M的同分异构体可以转化为求丁烷的一氯代物,丁烷有2种同分异构体:CH3CH2CH2CH3、 一氯代物均有2种,故共有4种,除M外,还有3种,A项正确;N分子中所有原子不可能共平面,B项错误;Q的名称是异丁烷,C项错误;M、Q不能与溴水反应,N分子中含有碳碳双键,能与Br2发生加成反应,D项错误。
常见官能团与有机物性质的关系
常见官能团与有机物性质的关系
活动一、常见几种官能团的性质探究
学生活动1:结合下表,归纳总结常见几种官能团分别具有哪些主要的
化学性质?填写表格内容。
官能团 主要化学性质
(碳碳双键) —C≡C—(碳碳三键)
①加成反应:与X2(制二卤代烃)、H2(制烷烃)、HX(制一卤代烃)、H2O(制一元醇)等。
②加聚反应:制高分子化合物。
③氧化反应:燃烧、强氧化剂(酸性高锰酸钾溶液褪色)氧化。
常见官能团与有机物性质的关系
活动一、常见几种官能团的性质探究
官能团 主要化学性质
—OH (醇羟基)
—COOH(羧基)
(酯基)
①弱酸性:R—COOH R—COO-+H+(R—烃基)
②酯化(取代)反应:与醇反应生成酯,可逆。
①置换反应:与活泼金属(如钠)反应生成氢气
②催化氧化:Cu或Ag作催化剂,加热,生成醛或酮
③酯化(取代)反应:与酸反应生成酯,可逆。
水解(取代)反应:酸性条件,可逆,生成羧酸和醇;
碱性条件,不可逆,生成羧酸钠和醇,且1mol消耗1molNaOH
常见官能团与有机物性质的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动2:结合已有知识,比较水、乙醇、碳酸、乙酸四种含有羟基
的物质性质的异同,可得出什么结论?填写表格内容。
乙醇 水 碳酸 乙酸
电离程度
酸碱性
与Na
与NaOH
与NaHCO3
结论 不电离
(非电解质)
微弱电离
(极弱电解质)
部分电离(弱电解质)
部分电离
(弱电解质)
中性
中性
弱酸性
弱酸性
反应
反应
反应
反应
反应
反应
反应
不反应
不反应
不反应
不反应
不反应
羟基中氢原子的活泼性:乙醇<水<碳酸<乙酸
对应训练
【典例1】下列有关酒和酒精的说法正确的是( )
A.检验乙醇中是否含水,可加入少量的金属钠,若生成气体则含水
B.酒精结构中含有—OH,可推测乙醇溶液呈碱性
C.获取无水乙醇的方法是先加入熟石灰,然后再蒸馏
D.酒精是一种很好的溶剂,能溶解许多无机物和有机化合物,人们
用白酒浸泡中药制成药酒就是利用了这一性质
D
【解析】金属钠和水及乙醇都可以反应生成H2,A错误;酒精的结构简式为C2H5OH,分子在溶液中不能发生电离,溶液呈中性,B错误;熟石灰[Ca(OH)2]不能吸水,故无法彻底去除乙醇中的水,C错误;酒精能溶解许多无机物和有机物,故白酒可以浸泡中药制药酒,D正确。
对应训练
【典例2】我国本土药学家屠呦呦因为发现青蒿素而获得2015年的诺贝
尔生理学或医学奖。已知二羟甲戊酸()是生物合成青蒿素的原料之一,
下列关于二羟甲戊酸的说法正确的是( )
A.与乙醇发生酯化反应生成产物的分子式为C8H18O4
B.能发生加成反应,不能发生取代反应
C.在铜催化下可以与氧气发生反应
D.标准状况下,1 mol该有机物可以与足量金属钠反应产生22.4 L H2
C
【解析】二羟甲戊酸结构中含一个—COOH,与乙醇发生酯化反应生成物中有一个酯基,其分子式为C8H16O4,A错误;不能发生加成反应,B错误;该物质含—CH2OH,在铜催化下能与氧气发生反应,C正确;1 mol该有机物与足量金属钠反应可生成1.5 mol氢气,标准状况下为33.6 L,D错误。
常见官能团与有机物性质的关系
活动二、认识常见有机反应类型及反应条件
学生活动1:结合已有知识,思考有机反应中的氧化、还原反应有何特
点和规律?
(1)氧化反应
①定义:有机物分子中失去氢原子或加入氧原子的反应。即有机物“去氢”或“得氧”的反应称为氧化反应。
②类型:a.醇的氧化反应:羟基的O—H键断裂,与羟基相连的碳原子的C—H键断裂,形成C=O键。与羟基相连的碳原子上无氢原子时,醇不能被催化氧化。
【温馨提示】乙醇在人体内的转化:乙醇 乙醛 乙酸 CO2
常见官能团与有机物性质的关系
活动二、认识常见有机反应类型及反应条件
学生活动1:结合已有知识,思考有机反应中的氧化、还原反应有何特
点和规律?
b. 醛的氧化反应:醛基的C—H键断裂,醛基被氧化成羧基。
c. 有机物的燃烧、不饱和烃和苯的同系物使酸性KMnO4溶液褪色等。
(2)还原反应
①定义:有机物分子中加入氢原子或失去氧原子的反应。即有机物“加氢”或“去氧”的反应称为还原反应。
②类型:醛、酮、烯烃、炔烃、苯及其同系物、酚等的催化加氢反应。
常见官能团与有机物性质的关系
活动二、认识常见有机反应类型及反应条件
学生活动2:有机反应条件与反应类型有何关系?
①在NaOH水溶液中能发生酯的水解反应。
②在光照、X2(表示卤素单质,下同)条件下发生烷基上的取代反应;在铁粉、X2
条件下发生苯环上的取代反应。
③在浓H2SO4和加热条件下,能发生酯化反应或酯的水解反应等。
④与溴水或溴的CCl4溶液反应,可能发生的是烯烃的加成反应。
⑤与H2在催化剂作用下发生反应,则发生的是烯烃、芳香烃加成反应或还原反应。
⑥在O2、Cu(或Ag)、加热或CuO、加热条件下,发生醇的催化氧化反应。
对应训练
【典例1】某有机物的结构简式为 ,它在一定条件下可发生
的反应为 ( )
①酯化反应 ②氧化反应 ③加聚反应 ④取代反应
A.②③④ B.①②③
C.①②④ D.③④
C
【解析】该物质含有羟基、羧基和酯基,能发生酯化反应、氧化反应和取代反应,但不含碳碳双键或碳碳三键,不能发生加聚反应,故C正确。
对应训练
【典例2】分枝酸可用于生化研究。其结构简式如图。下列关于分枝
酸的叙述正确的是( )
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分枝酸最多可与3 mol NaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
B
【解析】分子中含有4种官能团:羧基、羟基、碳碳双键、醚键,故错误;B项,均为酯化反应,故正确;C项,1 mol分枝酸最多可与2 mol NaOH中和,故错误;D项,前者为加成反应,后者为氧化反应,故错误。
1.下列物质中含有两种官能团的是( )
A.氯乙烯(CH2==CHCl) B.苯乙烯( )
C.丙三醇( ) D.甲苯( )
A
【解析】决定有机化合物特性的原子或原子团叫做官能团。氯乙烯中含有 和碳氯键两种官能团;苯乙烯中含 有一种官能团;丙三醇中含有—OH一种官能团;甲苯中没有官能团。
2.下列说法正确的是( )
A.羟基与氢氧根有相同的化学式和电子式
B.乙醇是含—OH的化合物
C.常温下,1 mol乙醇可与足量的Na反应生成11.2 L H2
D.已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键
为②③
B
【解析】羟基的化学式是—OH,电子式是 ,氢氧根的化学式是OH-,电子式是 ,A项错误;1 mol乙醇与足量的Na反应可以生成0.5 mol H2,在标准状况下是11.2 L,C项错误;乙醇发生催化氧化时断裂的化学键应为①③,D项错误。
3.柠檬酸的结构简式如图,下列说法正确的是( )
A.1 mol柠檬酸可与4 mol NaOH发生中和反应
B.柠檬酸中能发生酯化反应的官能团有2种
C.1 mol柠檬酸与足量金属Na反应生成1.5 mol H2
D.柠檬酸与O2在Cu作催化剂、加热的条件下发生催化氧化反应
B
【解析】柠檬酸分子中有三个羧基,故1 mol柠檬酸可与3 mol氢氧化钠发生中和反应,A错误;柠檬酸分子中含有羧基和羟基两种官能团,二者均能发生酯化反应,B正确;羟基和羧基均可与钠反应生成H2,所以1 mol柠檬酸和足量金属钠反应生成2 mol H2,C错误;柠檬酸分子中与羟基直接相连的碳原子上没有氢原子,无法发生催化氧化反应,D错误。
C
4.已知:决定有机化合物化学性质的原子或原子团叫官能团,常
见的官能团有碳碳双键( )羟基( —OH)、羧基(—COOH)、酯基
(—COO—)等,具有相同官能团的有机物具有相似的化学性质。某
有机物的结构为 ,该有机物不可能具有的性质是( )
A.该有机物可以和反应
B.分子中所有碳原子可能共面,所有原子不可能共面
C.既能发生取代反应,也能发生加成反应和水解反应
D.标准状况下,22.4 L该有机物与足量的反应,生成氢气的质量
大于2 g
【解析】A.该有机物有苯环和碳碳双键,所以1 mol该有机物可以和4 mol H2反应,A正确;B.苯环、碳碳双键为平面结构,烷基为空间结构,碳碳单键可以旋转,所以分子中所有碳原子可能共面,所有原子不可能共面,B正确;C.有机物中有—OH可以发生酯化反应(取代反应),有碳碳双键可以发生加成反应,不能发生水解反应,C错误;D.—COOH、—OH均与Na反应生成氢气,1mol该有机物与足量Na反应生成1mol氢气,其质量为2g,而标准状况下,22.4L该有机物(液体)的物质的量大于1mol,则生成氢气的质量大于2g,D正确;故选C。
延时符
碳碳双键、碳碳三键、碳卤键、羟基、羧基、酯基
结构、类别、性质、验证、用途
官能团
种类
认识有机物一般思路
官能团
性质
不同官能团有不同性质(官能团决定性质)
多种官能团的化合物具有各个官能团的性质
多种官能团之间相互影响,可表现出特殊性
官能团与有机物的分类
第3课时 官能团与有机物的
分类及性质
第三节 乙醇与乙酸
第3课时:官能团与有机物的分类及性质
第七章 有机化合物
有机物的官能团与物质类别的关系
01
常见官能团与有机物性质的关系
02
学习目标
1.通过旧知回顾、讨论交流,能结合实例认识有机物常见官能团,能从官能团类别的角度辨识各类有机化合物,深化“结构决定性质”的观念。
2.通过典例剖析、原理分析,了解官能团之间转化与物质类别和性质的关系,进一步理解氧化反应、取代反应、加成反应等常见有机反应类型。
3.通过归纳总结、整理提升,初步形成从烯烃(乙烯)到醇(乙醇)、醛(乙醛)、羧酸(乙酸)、酯(乙酸乙酯)的转化关系,认识多官能团有机物性质分析的基本方法。
通过对乙烯、乙醇和乙酸性质的学习,我们认识到官能团对有机物的性质具有决定作用,含有相同官能团的有机物在性质上具有相似之处。因此我们可以根据有机物分子中所含官能团的不同,从结构和性质上对数量庞大的有机物进行分类。如:
含哪些官能团
有机物的官能团与物质类别的关系
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动1:阅读教材P81页内容,结合表7-2,思考常见有机物的类别
与官能团的关系,填写表格内容。
①官能团对有机物的性质具有决定作用,含有相同的官能团的有机物具有相似的性质,可以根据分子中官能团的不同对有机物进行分类。
HC≡CH
CH2==CH2
CH3CH3
CH3CH2OH
CH3COOH
无官能团
无官能团
碳碳双键
碳碳叁键
羟基
羧基
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
②常见的有机物类别、官能团和代表物
有机化合物类别 官能团 代表物 结构 名称 结构简式 名称
烃 烷烃 - - CH4 甲烷
烯烃 CH2==CH2 乙烯
炔烃 CH≡CH 乙炔
芳香烃 - - 苯
碳碳双键
碳碳三键
—C≡C—
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
烃的衍生物 卤代烃 CH3CH2Br 溴乙烷
醇 CH3CH2OH 乙醇
醛 乙醛
羧酸 乙酸
酯 乙酸乙酯
碳卤键
羟基
醛基
羧基
酯基
有机化合物类别 官能团 代表物 结构 名称 结构简式 名称
—OH
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动2:探究书写烃的衍生物同分异构体顺序基本思维模型是什么?
①烃的衍生物同分异构体有三种具备类型:类别(官能团)异构、碳链异构、位置(官能团)异构。
②书写烃的衍生物基本思维模型
根据有机物的分子组成判定其可能的类别异构
根据类别异构写出各类别异构的可能的碳链结构(先写最长的碳链,依次写出少一个碳原子的碳链,把余下的碳原子连到相应的碳链上去。
第一步:判类别
第二步:写碳链
有机物的官能团与物质类别的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动2:探究书写烃的衍生物同分异构体顺序基本思维模型是什么?
②书写烃的衍生物基本思维模型(举例略)
一般是先写不带官能团的烃的同分异构体,再在各碳链上依次移动官能团的位置,有两个或两个以上的官能团时,先连一个官能团,再连第二个官能团,依此类推。
按“碳四键”的原理,碳原子剩余的价键用氢原子去填充饱和,就可得所有同分异构体的结构简式。
第三步:移官位
第四步:氢饱和
对应训练
【典例1】下列物质中含有两种官能团的烃的衍生物为( )
A.CH3CH2NO2 B.CH2=CHBr
C.CH2Cl2 D.
B
【解析】A.该有机物含有-NO2一种官能团,故A错误;B.该有机物存在碳碳双键、-Br两种官能团,故B正确;C.该有机物存在-Cl一种官能团,故C错误;D.该有机物存在-Br一种官能团,故D错误。故选B。
对应训练
【典例2】下列关于官能团的判断中说法错误的是( )
A.醇的官能团是羟基(—OH) B.羧酸的官能团是羟基(—OH)
C.酯的官能团是酯基( ) D.烯烃的官能团是碳碳双键( )
B
【解析】醇类的官能团为羟基(—OH),A项正确;羧酸的官能团为羧基(—COOH),且羧基是个整体,不能分开,B项错误;酯的官能团是酯基( ),C项正确;烯烃的官能团是碳碳双键( ),D项正
确。故选B。
有机物的官能团与物质类别的关系
活动二、几种重要有机物组成、结构及类别
学生活动1:结合已有知识,思考几种常见烃、乙醇、乙酸、乙酸乙酯
的分子组成和结构有何特点?填写表格内容。
物质 甲烷 乙烯 乙炔 乙醇 乙酸 乙酸乙酯
分子式
电子式 —— —— ——
结构式
H-C≡C-H
CH4
C2H4
C2H2
C2H6O
C2H4O2
C4H8O2
有机物的官能团与物质类别的关系
活动二、几种重要有机物组成、结构及类别
物质 甲烷 乙烯 乙炔 乙醇 乙酸 乙酸乙酯
结构简式
球棍模型
空间填充模型
官能团 ——
类别
烷烃
烯烃
炔烃
醇
羧酸
酯
CH4
CH2=CH2
HC≡CH
CH3CH2OH或C2H5OH
CH3COOH
CH3COOCH2CH3
-C≡C-
—OH
有机物的官能团与物质类别的关系
活动二、几种重要有机物组成、结构及类别
学生活动2:结合教材P81页“方法引导”栏目,思考认识有机化合物的
一般思路是什么?
有机物结构
官能团种类
有机物性质
官能团性质
分析
联想
结论
【温馨提示】认识一种有机物,可先从结构入手,分析其碳骨架和官能团,了解其所属的类别;再结合该类有机物的一般性质推测其可能具有的性质,并通过实验进行验证;在此基础上了解该有机物的用途,即“结构决定性质,性质决定用途”
对应训练
【典例1】某种食品防腐剂的结构简式如图所示,下列关于该物质
的说法正确的是( )
A.分子式为
B.是一种有机高分子化合物
C.分子中含有三种含氧官能团
D.1mol该物质能与3mol NaOH反应
A
【解析】A.由结构简式可知该物质的分子式为:C7H10O5,故A正确;B.该物质分子式C7H10O5,相对分子质量较小,不属于高分子化合物,故B错误;C.由结构简式可知该物质含有碳碳双键,羟基,羧基三种官能团,其中含氧官能团只有羟基和羧基两种,故C错误;D.该物质中只有羧基能与NaOH反应,1mol该物质含有2mol羧基能与2molNaOH反应,故D错误;故选:A。
对应训练
A
【典例2】有机物M、N、Q之间的转化关系为 ,下列说法正确的是( )
A.M的同分异构体有3种(不考虑立体异构)
B.N分子中所有原子共平面
C.Q的名称为异丙烷 D.M、N、Q均能与溴水反应
【解析】M、N、Q分别为 、 、 。求M的同分异构体可以转化为求丁烷的一氯代物,丁烷有2种同分异构体:CH3CH2CH2CH3、 一氯代物均有2种,故共有4种,除M外,还有3种,A项正确;N分子中所有原子不可能共平面,B项错误;Q的名称是异丁烷,C项错误;M、Q不能与溴水反应,N分子中含有碳碳双键,能与Br2发生加成反应,D项错误。
常见官能团与有机物性质的关系
常见官能团与有机物性质的关系
活动一、常见几种官能团的性质探究
学生活动1:结合下表,归纳总结常见几种官能团分别具有哪些主要的
化学性质?填写表格内容。
官能团 主要化学性质
(碳碳双键) —C≡C—(碳碳三键)
①加成反应:与X2(制二卤代烃)、H2(制烷烃)、HX(制一卤代烃)、H2O(制一元醇)等。
②加聚反应:制高分子化合物。
③氧化反应:燃烧、强氧化剂(酸性高锰酸钾溶液褪色)氧化。
常见官能团与有机物性质的关系
活动一、常见几种官能团的性质探究
官能团 主要化学性质
—OH (醇羟基)
—COOH(羧基)
(酯基)
①弱酸性:R—COOH R—COO-+H+(R—烃基)
②酯化(取代)反应:与醇反应生成酯,可逆。
①置换反应:与活泼金属(如钠)反应生成氢气
②催化氧化:Cu或Ag作催化剂,加热,生成醛或酮
③酯化(取代)反应:与酸反应生成酯,可逆。
水解(取代)反应:酸性条件,可逆,生成羧酸和醇;
碱性条件,不可逆,生成羧酸钠和醇,且1mol消耗1molNaOH
常见官能团与有机物性质的关系
活动一、有机物的主要类别、官能团和典型代表物
学生活动2:结合已有知识,比较水、乙醇、碳酸、乙酸四种含有羟基
的物质性质的异同,可得出什么结论?填写表格内容。
乙醇 水 碳酸 乙酸
电离程度
酸碱性
与Na
与NaOH
与NaHCO3
结论 不电离
(非电解质)
微弱电离
(极弱电解质)
部分电离(弱电解质)
部分电离
(弱电解质)
中性
中性
弱酸性
弱酸性
反应
反应
反应
反应
反应
反应
反应
不反应
不反应
不反应
不反应
不反应
羟基中氢原子的活泼性:乙醇<水<碳酸<乙酸
对应训练
【典例1】下列有关酒和酒精的说法正确的是( )
A.检验乙醇中是否含水,可加入少量的金属钠,若生成气体则含水
B.酒精结构中含有—OH,可推测乙醇溶液呈碱性
C.获取无水乙醇的方法是先加入熟石灰,然后再蒸馏
D.酒精是一种很好的溶剂,能溶解许多无机物和有机化合物,人们
用白酒浸泡中药制成药酒就是利用了这一性质
D
【解析】金属钠和水及乙醇都可以反应生成H2,A错误;酒精的结构简式为C2H5OH,分子在溶液中不能发生电离,溶液呈中性,B错误;熟石灰[Ca(OH)2]不能吸水,故无法彻底去除乙醇中的水,C错误;酒精能溶解许多无机物和有机物,故白酒可以浸泡中药制药酒,D正确。
对应训练
【典例2】我国本土药学家屠呦呦因为发现青蒿素而获得2015年的诺贝
尔生理学或医学奖。已知二羟甲戊酸()是生物合成青蒿素的原料之一,
下列关于二羟甲戊酸的说法正确的是( )
A.与乙醇发生酯化反应生成产物的分子式为C8H18O4
B.能发生加成反应,不能发生取代反应
C.在铜催化下可以与氧气发生反应
D.标准状况下,1 mol该有机物可以与足量金属钠反应产生22.4 L H2
C
【解析】二羟甲戊酸结构中含一个—COOH,与乙醇发生酯化反应生成物中有一个酯基,其分子式为C8H16O4,A错误;不能发生加成反应,B错误;该物质含—CH2OH,在铜催化下能与氧气发生反应,C正确;1 mol该有机物与足量金属钠反应可生成1.5 mol氢气,标准状况下为33.6 L,D错误。
常见官能团与有机物性质的关系
活动二、认识常见有机反应类型及反应条件
学生活动1:结合已有知识,思考有机反应中的氧化、还原反应有何特
点和规律?
(1)氧化反应
①定义:有机物分子中失去氢原子或加入氧原子的反应。即有机物“去氢”或“得氧”的反应称为氧化反应。
②类型:a.醇的氧化反应:羟基的O—H键断裂,与羟基相连的碳原子的C—H键断裂,形成C=O键。与羟基相连的碳原子上无氢原子时,醇不能被催化氧化。
【温馨提示】乙醇在人体内的转化:乙醇 乙醛 乙酸 CO2
常见官能团与有机物性质的关系
活动二、认识常见有机反应类型及反应条件
学生活动1:结合已有知识,思考有机反应中的氧化、还原反应有何特
点和规律?
b. 醛的氧化反应:醛基的C—H键断裂,醛基被氧化成羧基。
c. 有机物的燃烧、不饱和烃和苯的同系物使酸性KMnO4溶液褪色等。
(2)还原反应
①定义:有机物分子中加入氢原子或失去氧原子的反应。即有机物“加氢”或“去氧”的反应称为还原反应。
②类型:醛、酮、烯烃、炔烃、苯及其同系物、酚等的催化加氢反应。
常见官能团与有机物性质的关系
活动二、认识常见有机反应类型及反应条件
学生活动2:有机反应条件与反应类型有何关系?
①在NaOH水溶液中能发生酯的水解反应。
②在光照、X2(表示卤素单质,下同)条件下发生烷基上的取代反应;在铁粉、X2
条件下发生苯环上的取代反应。
③在浓H2SO4和加热条件下,能发生酯化反应或酯的水解反应等。
④与溴水或溴的CCl4溶液反应,可能发生的是烯烃的加成反应。
⑤与H2在催化剂作用下发生反应,则发生的是烯烃、芳香烃加成反应或还原反应。
⑥在O2、Cu(或Ag)、加热或CuO、加热条件下,发生醇的催化氧化反应。
对应训练
【典例1】某有机物的结构简式为 ,它在一定条件下可发生
的反应为 ( )
①酯化反应 ②氧化反应 ③加聚反应 ④取代反应
A.②③④ B.①②③
C.①②④ D.③④
C
【解析】该物质含有羟基、羧基和酯基,能发生酯化反应、氧化反应和取代反应,但不含碳碳双键或碳碳三键,不能发生加聚反应,故C正确。
对应训练
【典例2】分枝酸可用于生化研究。其结构简式如图。下列关于分枝
酸的叙述正确的是( )
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分枝酸最多可与3 mol NaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
B
【解析】分子中含有4种官能团:羧基、羟基、碳碳双键、醚键,故错误;B项,均为酯化反应,故正确;C项,1 mol分枝酸最多可与2 mol NaOH中和,故错误;D项,前者为加成反应,后者为氧化反应,故错误。
1.下列物质中含有两种官能团的是( )
A.氯乙烯(CH2==CHCl) B.苯乙烯( )
C.丙三醇( ) D.甲苯( )
A
【解析】决定有机化合物特性的原子或原子团叫做官能团。氯乙烯中含有 和碳氯键两种官能团;苯乙烯中含 有一种官能团;丙三醇中含有—OH一种官能团;甲苯中没有官能团。
2.下列说法正确的是( )
A.羟基与氢氧根有相同的化学式和电子式
B.乙醇是含—OH的化合物
C.常温下,1 mol乙醇可与足量的Na反应生成11.2 L H2
D.已知乙醇的结构式如图所示,则乙醇催化氧化时断裂的化学键
为②③
B
【解析】羟基的化学式是—OH,电子式是 ,氢氧根的化学式是OH-,电子式是 ,A项错误;1 mol乙醇与足量的Na反应可以生成0.5 mol H2,在标准状况下是11.2 L,C项错误;乙醇发生催化氧化时断裂的化学键应为①③,D项错误。
3.柠檬酸的结构简式如图,下列说法正确的是( )
A.1 mol柠檬酸可与4 mol NaOH发生中和反应
B.柠檬酸中能发生酯化反应的官能团有2种
C.1 mol柠檬酸与足量金属Na反应生成1.5 mol H2
D.柠檬酸与O2在Cu作催化剂、加热的条件下发生催化氧化反应
B
【解析】柠檬酸分子中有三个羧基,故1 mol柠檬酸可与3 mol氢氧化钠发生中和反应,A错误;柠檬酸分子中含有羧基和羟基两种官能团,二者均能发生酯化反应,B正确;羟基和羧基均可与钠反应生成H2,所以1 mol柠檬酸和足量金属钠反应生成2 mol H2,C错误;柠檬酸分子中与羟基直接相连的碳原子上没有氢原子,无法发生催化氧化反应,D错误。
C
4.已知:决定有机化合物化学性质的原子或原子团叫官能团,常
见的官能团有碳碳双键( )羟基( —OH)、羧基(—COOH)、酯基
(—COO—)等,具有相同官能团的有机物具有相似的化学性质。某
有机物的结构为 ,该有机物不可能具有的性质是( )
A.该有机物可以和反应
B.分子中所有碳原子可能共面,所有原子不可能共面
C.既能发生取代反应,也能发生加成反应和水解反应
D.标准状况下,22.4 L该有机物与足量的反应,生成氢气的质量
大于2 g
【解析】A.该有机物有苯环和碳碳双键,所以1 mol该有机物可以和4 mol H2反应,A正确;B.苯环、碳碳双键为平面结构,烷基为空间结构,碳碳单键可以旋转,所以分子中所有碳原子可能共面,所有原子不可能共面,B正确;C.有机物中有—OH可以发生酯化反应(取代反应),有碳碳双键可以发生加成反应,不能发生水解反应,C错误;D.—COOH、—OH均与Na反应生成氢气,1mol该有机物与足量Na反应生成1mol氢气,其质量为2g,而标准状况下,22.4L该有机物(液体)的物质的量大于1mol,则生成氢气的质量大于2g,D正确;故选C。
延时符
碳碳双键、碳碳三键、碳卤键、羟基、羧基、酯基
结构、类别、性质、验证、用途
官能团
种类
认识有机物一般思路
官能团
性质
不同官能团有不同性质(官能团决定性质)
多种官能团的化合物具有各个官能团的性质
多种官能团之间相互影响,可表现出特殊性
官能团与有机物的分类
第3课时 官能团与有机物的
分类及性质
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
