化学人教版(2019)选择性必修3 1.1.2有机化合物中的共价键 同分异构现象(共23张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 1.1.2有机化合物中的共价键 同分异构现象(共23张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 120.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-05 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第一节 有机化合物的结构特点
第2课时 有机化合物中的共价键
有机化合物的同分异构现象
(1)按共用电子对数目
单键:如H-H键
双键:如C=C键
三键:如C≡C键
(2)按共用电子对是否偏移
非极性键
极性键
(3)按原子轨道的重叠方式
σ键
π键
[温故而知新】 共价键的分类
甲烷不能发生加成反应,乙烯、乙炔能发生加成反应,三者碳碳
共价键的类型有什么不同呢?
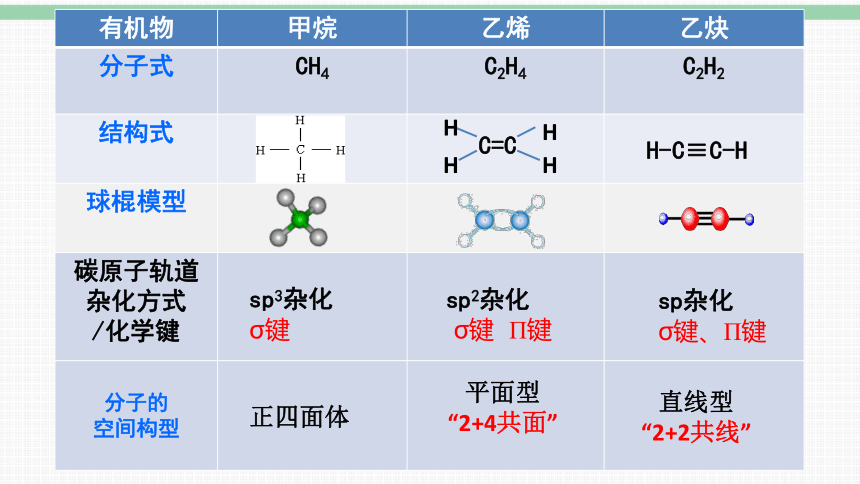
有机物 甲烷 乙烯 乙炔
分子式 CH4 C2H4 C2H2
结构式
球棍模型
碳原子轨道杂化方式 /化学键
分子的 空间构型
C=C
H
H
H
H
H-C≡C-H
正四面体
平面型
“2+4共面”
直线型
“2+2共线”
sp2杂化
σ键 Π键
sp3杂化
σ键
sp杂化
σ键、Π键
1.认识有机化合物分子中共价键的类型、极性与有机反应的关系。
2.理解有机化合物的同分异构现象,能判断、书写有机化合物的同分异构体。
学 习 目 标
知识点一 有机化合物中的共价键
1.共价键的类型
(1)根据原子轨道的重叠方式可分为σ键和π键
共价键 重叠方式 特点
σ键 沿两原子核间的键轴方向以“________”形式相互重叠 成键的原子或原子团____绕键轴旋转
π键 原子中未参与杂化的p轨道以“________”的形式从侧面重叠 成键的原子或原子团______绕键轴旋转
头碰头
可
肩并肩
不能
(3)共价键的类型与有机反应类型的关系
σ键轨道重叠程度较大,强度较大,不易断裂,能发生取代反应;
π键的轨道重叠程度比σ键的小,比较容易断裂,π键更活泼,能发生加成反应。
N2特殊,π键比σ键稳定。
2.共价键的极性与有机反应
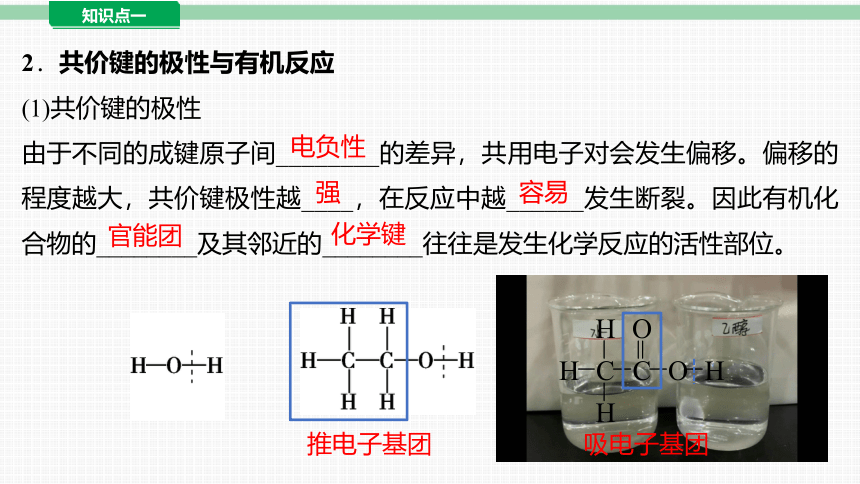
(1)共价键的极性
由于不同的成键原子间________的差异,共用电子对会发生偏移。偏移的程度越大,共价键极性越____,在反应中越______发生断裂。因此有机化合物的________及其邻近的________往往是发生化学反应的活性部位。
电负性
强
容易
官能团
化学键
推电子基团
吸电子基团
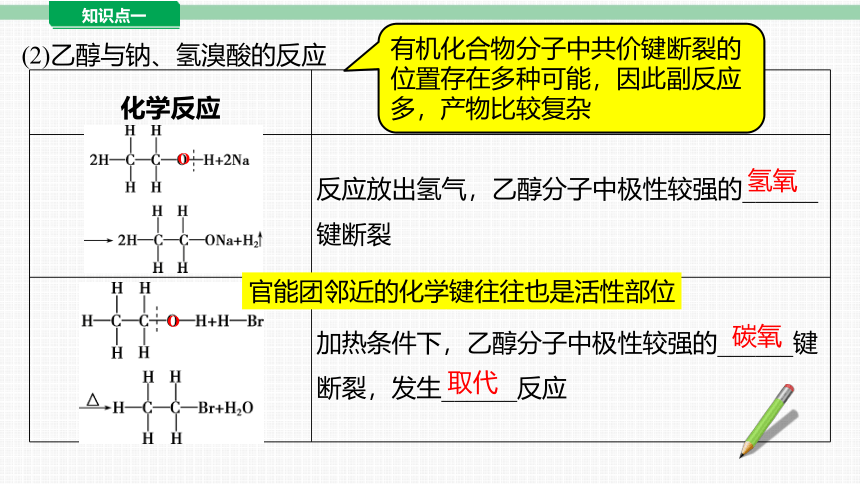
(2)乙醇与钠、氢溴酸的反应
化学反应 断键分析
反应放出氢气,乙醇分子中极性较强的______键断裂
加热条件下,乙醇分子中极性较强的______键断裂,发生______反应
氢氧
碳氧
取代
官能团邻近的化学键往往也是活性部位
有机化合物分子中共价键断裂的位置存在多种可能,因此副反应多,产物比较复杂
O
O
名称 正戊烷 异戊烷 新戊烷
结构简式 CH3(CH2)3CH3 CH3CH2CH(CH3)2 C(CH3)4
相同点 不同点 戊烷(C5H12)的三种结构,如下所示:
分子式都是C5H12 、 化学性质相似
分子结构不同,物理性质不同, 支链越多,沸点越低
写出C6H14所有有机物的结构简式:
CH3CH2CH2CH2CH2CH3
碳架异构:主链由长到短
支链由整到散
位置由心到边
支链不能比端基长
思考:C5H11Cl 有几种结构?
碳链异构 位置异构(烃基异构)
⑴等效氢法
①同一个C原子上的H原子等效。CH4
②处于对称位置C原子上的H原子等效。
③同一个C原子上所连—CH3上的H原子等效。
⑵应用
①烃基异构
②一卤代物异构
知识点二 有机化合物的同分异构现象
(烃基异构)—等效氢
3.有机化合物的构造异构(填结构简式)
异构类别 实例
碳架异构
C4H10:_____________________、___________________
位置异构
C4H8:______________________、__________________
异构类别 实例
位置 异构
C6H4Cl2:_____________、______________、______________
官能 团异构
C2H6O:______________________、__________________
例:写出分子式为C4H10O的同分异构体
定碳骨架
先定官能团种类
再排碳骨架
最后定官能团位置
定官能团
挪官能团
醇、醚
O
O
O
等效氢
总结
同分异构现象
构造异构
碳架异构
位置异构
官能团异构
共价键
有机反应类型
相邻基团
化学性质
类型
极性
有机化合物
烃的二氯代物同分异构体数目的判断
(1)先写出烃的同分异构体。碳链异构→位置异构
(2)然后再利用“定一移一”法,即先固定一个氯原子的位置,再移动另一个氯原子,以确定同分异构体的数目。
1.分子式为C3H6Cl2的有机物共有 种。
2.分子式为C4H8Cl2的有机物有 种。
3.分子式为C5H12的烷烃与氯气发生取代反应,生成物中含有两个氯原子且氯原子位于相邻碳原子上的结构有 种。
知识点三 多角度认识有机化合物的分子组成与结构
1.碳原子的成键特点
每个碳原子能形成4个共价键。碳碳之间可以形成单键、双键、三键,碳氧之间可形成单键、双键,碳氢之间只形成单键。
2.有机化合物的表示方法
种类 实例 含义
分子式 CH4 用元素符号和数字表示物质分子组成的式子
最简式 (实验式) 乙烷(C2H6)的 最简式为CH3 表示物质组成的各元素原子最简整数比的式子
种类 实例 含义
电子式 表示分子中各原子最外层电子成键情况的式子
结构式 表示分子中原子的结合或排列顺序的式子,但不表示空间结构
种类 实例 含义
结构简式 CH2==CHCH3 将结构式中的碳碳单键、碳氢键等短线省略后得到的式子
键线式 将结构式中碳、氢元素符号省略,只表示分子中键的连接情况和官能团,每个拐点或终点均表示有一个碳原子
种类 实例 含义
球棍模型 小球表示原子,短棍表示价键,用于表示分子的空间结构(立体形状)
空间填 充模型 表示分子中各原子的相对大小和结合顺序
谢谢观看
第一节 有机化合物的结构特点
第2课时 有机化合物中的共价键
有机化合物的同分异构现象
(1)按共用电子对数目
单键:如H-H键
双键:如C=C键
三键:如C≡C键
(2)按共用电子对是否偏移
非极性键
极性键
(3)按原子轨道的重叠方式
σ键
π键
[温故而知新】 共价键的分类
甲烷不能发生加成反应,乙烯、乙炔能发生加成反应,三者碳碳
共价键的类型有什么不同呢?
有机物 甲烷 乙烯 乙炔
分子式 CH4 C2H4 C2H2
结构式
球棍模型
碳原子轨道杂化方式 /化学键
分子的 空间构型
C=C
H
H
H
H
H-C≡C-H
正四面体
平面型
“2+4共面”
直线型
“2+2共线”
sp2杂化
σ键 Π键
sp3杂化
σ键
sp杂化
σ键、Π键
1.认识有机化合物分子中共价键的类型、极性与有机反应的关系。
2.理解有机化合物的同分异构现象,能判断、书写有机化合物的同分异构体。
学 习 目 标
知识点一 有机化合物中的共价键
1.共价键的类型
(1)根据原子轨道的重叠方式可分为σ键和π键
共价键 重叠方式 特点
σ键 沿两原子核间的键轴方向以“________”形式相互重叠 成键的原子或原子团____绕键轴旋转
π键 原子中未参与杂化的p轨道以“________”的形式从侧面重叠 成键的原子或原子团______绕键轴旋转
头碰头
可
肩并肩
不能
(3)共价键的类型与有机反应类型的关系
σ键轨道重叠程度较大,强度较大,不易断裂,能发生取代反应;
π键的轨道重叠程度比σ键的小,比较容易断裂,π键更活泼,能发生加成反应。
N2特殊,π键比σ键稳定。
2.共价键的极性与有机反应
(1)共价键的极性
由于不同的成键原子间________的差异,共用电子对会发生偏移。偏移的程度越大,共价键极性越____,在反应中越______发生断裂。因此有机化合物的________及其邻近的________往往是发生化学反应的活性部位。
电负性
强
容易
官能团
化学键
推电子基团
吸电子基团
(2)乙醇与钠、氢溴酸的反应
化学反应 断键分析
反应放出氢气,乙醇分子中极性较强的______键断裂
加热条件下,乙醇分子中极性较强的______键断裂,发生______反应
氢氧
碳氧
取代
官能团邻近的化学键往往也是活性部位
有机化合物分子中共价键断裂的位置存在多种可能,因此副反应多,产物比较复杂
O
O
名称 正戊烷 异戊烷 新戊烷
结构简式 CH3(CH2)3CH3 CH3CH2CH(CH3)2 C(CH3)4
相同点 不同点 戊烷(C5H12)的三种结构,如下所示:
分子式都是C5H12 、 化学性质相似
分子结构不同,物理性质不同, 支链越多,沸点越低
写出C6H14所有有机物的结构简式:
CH3CH2CH2CH2CH2CH3
碳架异构:主链由长到短
支链由整到散
位置由心到边
支链不能比端基长
思考:C5H11Cl 有几种结构?
碳链异构 位置异构(烃基异构)
⑴等效氢法
①同一个C原子上的H原子等效。CH4
②处于对称位置C原子上的H原子等效。
③同一个C原子上所连—CH3上的H原子等效。
⑵应用
①烃基异构
②一卤代物异构
知识点二 有机化合物的同分异构现象
(烃基异构)—等效氢
3.有机化合物的构造异构(填结构简式)
异构类别 实例
碳架异构
C4H10:_____________________、___________________
位置异构
C4H8:______________________、__________________
异构类别 实例
位置 异构
C6H4Cl2:_____________、______________、______________
官能 团异构
C2H6O:______________________、__________________
例:写出分子式为C4H10O的同分异构体
定碳骨架
先定官能团种类
再排碳骨架
最后定官能团位置
定官能团
挪官能团
醇、醚
O
O
O
等效氢
总结
同分异构现象
构造异构
碳架异构
位置异构
官能团异构
共价键
有机反应类型
相邻基团
化学性质
类型
极性
有机化合物
烃的二氯代物同分异构体数目的判断
(1)先写出烃的同分异构体。碳链异构→位置异构
(2)然后再利用“定一移一”法,即先固定一个氯原子的位置,再移动另一个氯原子,以确定同分异构体的数目。
1.分子式为C3H6Cl2的有机物共有 种。
2.分子式为C4H8Cl2的有机物有 种。
3.分子式为C5H12的烷烃与氯气发生取代反应,生成物中含有两个氯原子且氯原子位于相邻碳原子上的结构有 种。
知识点三 多角度认识有机化合物的分子组成与结构
1.碳原子的成键特点
每个碳原子能形成4个共价键。碳碳之间可以形成单键、双键、三键,碳氧之间可形成单键、双键,碳氢之间只形成单键。
2.有机化合物的表示方法
种类 实例 含义
分子式 CH4 用元素符号和数字表示物质分子组成的式子
最简式 (实验式) 乙烷(C2H6)的 最简式为CH3 表示物质组成的各元素原子最简整数比的式子
种类 实例 含义
电子式 表示分子中各原子最外层电子成键情况的式子
结构式 表示分子中原子的结合或排列顺序的式子,但不表示空间结构
种类 实例 含义
结构简式 CH2==CHCH3 将结构式中的碳碳单键、碳氢键等短线省略后得到的式子
键线式 将结构式中碳、氢元素符号省略,只表示分子中键的连接情况和官能团,每个拐点或终点均表示有一个碳原子
种类 实例 含义
球棍模型 小球表示原子,短棍表示价键,用于表示分子的空间结构(立体形状)
空间填 充模型 表示分子中各原子的相对大小和结合顺序
谢谢观看
