2024届高三化学二轮复习 备考 化学反应与能量课件(共28张PPT)
文档属性
| 名称 | 2024届高三化学二轮复习 备考 化学反应与能量课件(共28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-04 00:00:00 | ||
图片预览




文档简介
(共28张PPT)
化学反应与能量 (包括焓变、熵)
黄冈市2024届高三化学二轮复习备考
内容
摘要
二轮备考策略
学情考情分析
课程标准解读
1
3
4
黄冈市2024届高三化学二轮复习备考
高考试题研究
2
《普通高中化学课程标准(2017年版2020年修订)》 内容要求 学业要求
(1)认识化学键的断裂和形成是反应中物质变化的实质及能量变化的主要原因 (2)认识物质具有能量,认识吸热反应与放热反应,了解化学反应体系能量改变与化学键的断裂和形成有关。体会提高燃料的燃烧效率、开发高能清洁燃料和研制新型电池的重要性 (3)认识化学能可与热能、电能等其他形式能量之间相互转化,能量的转化遵循能量守恒定律。知道内能是体系内物质的各种能量的总和,受温度、压强、物质的聚集状态的影响 (4)恒温恒压下化学反应的反应热可用焓变表示,了解盖斯定律及简单应用 (5)知道化学反应有方向,知道化学反应的方向与反应的焓变和熵变有关 (1)能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质
(2)能进行反应焓变的简单计算,能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应
(3)能举例说明化学在解决能源危机中的重要作用,能分析能源的利用对自然环境和社会发展的影响。能综合考虑化学变化中的物质变化和能量变化来分析、解决实际问题,如煤炭的综合利用
学科素养 (1)能分析物质化学变化和伴随发生的能量转化与物质微观结构之间的关系,体现了宏观辨识与微观探析。 (2)能运用化学计量单位定量分析化学变化及其伴随发生的能量变化,体现了变化观念与平衡思想。 (3)具有“绿色化学”观念,能运用知识分析和探讨某些化学过程对人类健康、社会可持续发展可能带来的双重影响,并从多个方面评估这些影响;具有理论联系实际的观念,有将化学成果应用于生产、生活的意识,能依据实际条件并运用所学知识和方法解决生产、生活中简单的化学问题,体现了科学探究与创新意识及科学态度与社会责任。
1.1 高中化学课程标准
关键能力
必备知识
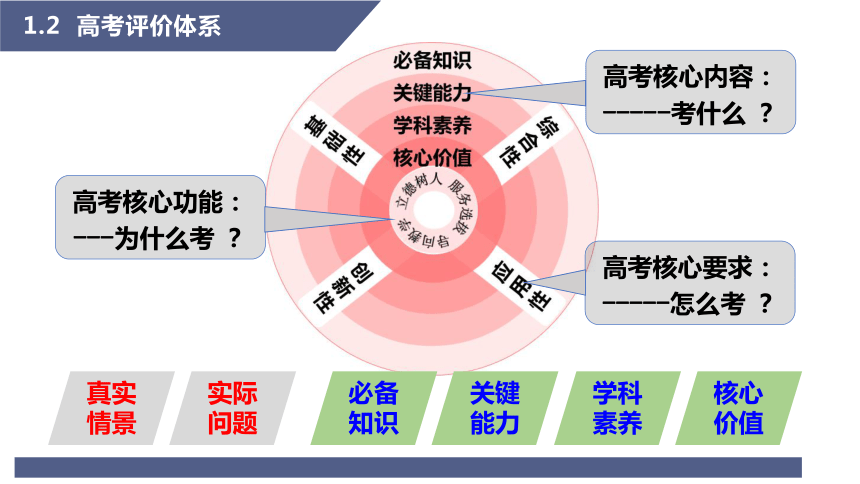
核心价值
学科素养
实际问题
真实情景
高考核心功能:
---为什么考 ?
高考核心要求:
-----怎么考 ?
高考核心内容:
-----考什么 ?
1.2 高考评价体系
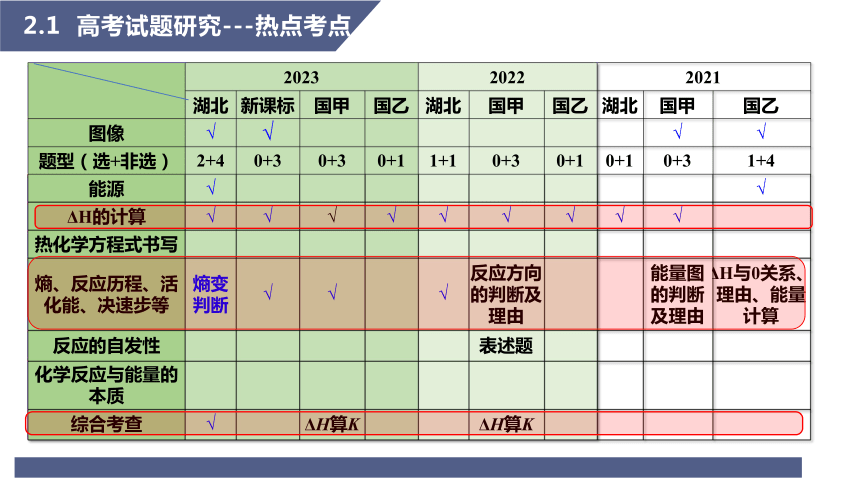
2.1 高考试题研究---热点考点
2023 2022 2021 湖北 新课标 国甲 国乙 湖北 国甲 国乙 湖北 国甲 国乙
图像 √ √ √ √
题型(选+非选) 2+4 0+3 0+3 0+1 1+1 0+3 0+1 0+1 0+3 1+4
能源 √ √
ΔH的计算 √ √ √ √ √ √ √ √ √
热化学方程式书写
熵、反应历程、活化能、决速步等 熵变判断 √ √ √ 反应方向的判断及理由 能量图的判断及理由 ΔH与0关系、理由、能量计算
反应的自发性 表述题
化学反应与能量的本质
综合考查 √ ΔH算K ΔH算K
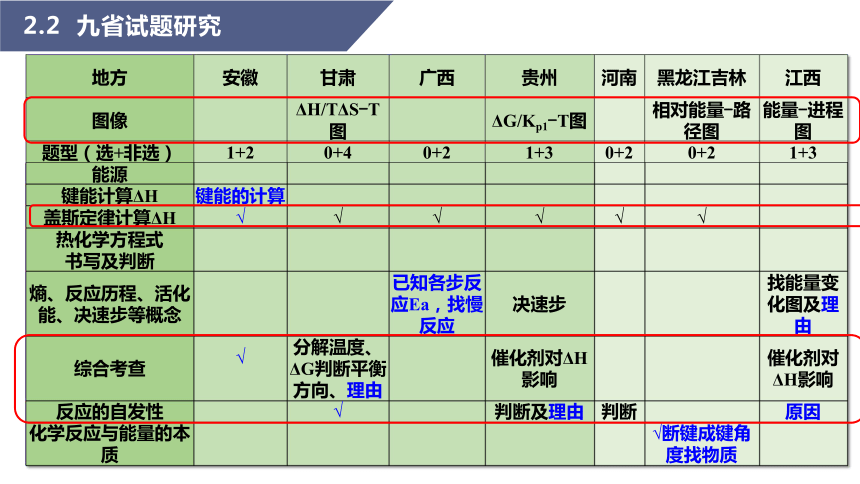
2.2 九省试题研究
情景素材:生产生活、铜锈
学科素养:证据推理与模型认知
关键能力:信息提取、逻辑推理能力
命题特点:考查了ΔG=ΔH-TΔS,即反
应的自发与方向
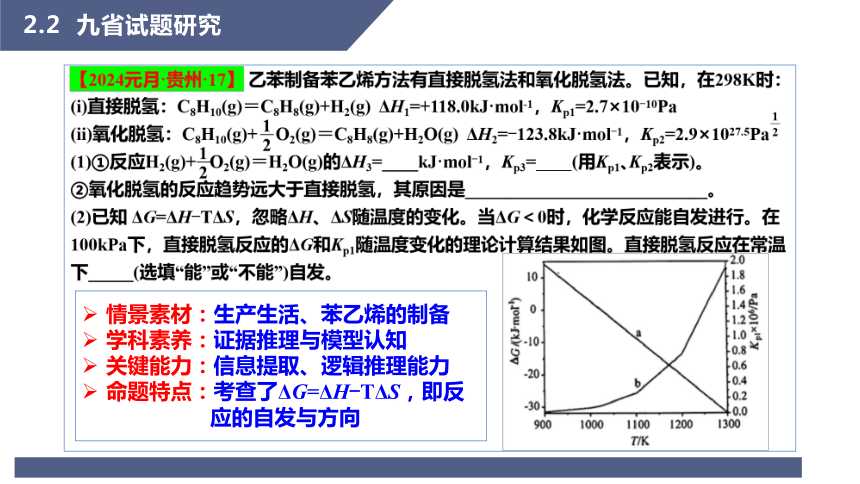
2.2 九省试题研究
情景素材:生产生活、苯乙烯的制备
学科素养:证据推理与模型认知
关键能力:信息提取、逻辑推理能力
命题特点:考查了ΔG=ΔH-TΔS,即反
应的自发与方向
地方 安徽 甘肃 广西 贵州 河南 黑龙江吉林 江西
图像 ΔH/TΔS-T图 ΔG/Kp1-T图 相对能量-路径图 能量-进程图
题型(选+非选) 1+2 0+4 0+2 1+3 0+2 0+2 1+3
能源
键能计算ΔH 键能的计算
盖斯定律计算ΔH √ √ √ √ √ √
热化学方程式 书写及判断
熵、反应历程、活化能、决速步等概念 已知各步反应Ea,找慢反应 决速步 找能量变化图及理由
综合考查 √ 分解温度、ΔG判断平衡方向、理由 催化剂对ΔH影响 催化剂对ΔH影响
反应的自发性 √ 判断及理由 判断 原因
化学反应与能量的本质 √断键成键角度找物质
2.2 九省试题研究
2.3 高考试题研究--近三年湖北
选择题 2021年未考查
2022年一道(T8),考查化学反应的熵变
2023年两道(T1、3),考查能源的选择、化学反应的熵变
非选择题 均考查了ΔH的计算
2023年新增了对基元反应、活化能进行考查
湖北考情分析
1. 近三年分值逐年递增
2. 仍以非选择题为主,出现在平衡大题前面几问中
3. 选择题近三年分别考查了0、1、2道
24年命题预测:
(1)湖北卷仍以非选择题考查形式为主,考查1~3个空;选择题至少一道。
(2)选择题沿用前沿背景:以环保材料、时事热点、教材素材等为素材。
(3)非选题延续高频考点(重点):ΔH的计算(键能、盖斯定律、活化能、相对能量、等效平衡等)
(4)非选题难点:图像的分析
(5)非选题热点:反应的自发性判断、基元反应、活化能等
(6)重视深挖教材:教材新增的素材(研究与实践、科学技术社会、探究、资料卡片等);新增概念(自发反应、熵、基元反应、活化能等);
2.3 高考试题研究--高考预测
【2023·湖北】 2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进入到高质量新阶段。下列不能作为火箭推进剂的是
A.液氮-液氢 B.液氧-液氢
C.液态NO2-肼 D.液氧-煤油
选择性必修一:P11
【选择性必修一P17练习与应用:T4】
4. 火箭发射时,可用肼(N2H4,液态)作燃料,NO2做氧化剂,二者反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)=2NO2(g) ΔH1=+664kJ/mol
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2(g)反应的热化学方程式。
2.4 高考试题研究与学法指导
考点:考查化学反应中能量的转化及应用
(1)从教材素材上挖掘考点
~~~~~~研究与实践~~~~~~
了解火箭推进剂
【研究目的】
火箭推进剂在航天和军事等领域具有广泛的应用。通过查阅资料,了解火箭推进剂的发展历史、现状及趋势,感受火箭推进剂的发展对人类社会进步的促进作用,体会化学反应中能量变化的重要价值。
【研究任务】
(1)了解火箭推进剂的发展历史
(2)了解我国目前常用的火箭推进剂的类型、成分和特点
(3)了解火箭推进剂的发展趋势
【结果与讨论】
(1)通过研究,你得到什么启示?
(2)撰写研究报告,并于同学讨论。
1、从教材上挖掘考点
情境素材:航天器的火箭推进剂
学科素养:证据推理与模型认知
关键能力:信息提取能力、理解与辨析能力
命题特点:考题突出考查了基础性、应用性
2.4 高考试题研究与学法指导
(2)从教材概念上挖掘考点
考点:两道题均考查了化学反应的熵变
1、从教材上挖掘考点
2.4 高考试题研究与学法指导
(2)从教材概念上挖掘考点
(2022年1月浙江)AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)+Bn-(aq),其焓变和熵变分别为ΔH和ΔS。下列说法正确的是( )
A. ΔH和ΔS均大于零
B. ΔH和ΔS均小于零
C. ΔH大于零或小于零,ΔS大于零
D. ΔH和ΔS均可能大于零或小于零
(2022年1月浙江)29. 工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得到满足不同需求的原料气。
(1)在C和O2的反应体系中:
反应1:C(s)+O2(g)=CO2(g) ΔH1=-394kJ·mol-1
反应2:2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
反应3:2C(s)+O2(g)=2CO(g) ΔH3。
①设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是___。
情景素材:科研成果、新材料---纳米碗
试题特色:图文简洁、思维量大
关键能力:信息获取与加工、逻辑推理与论证能力
必备知识:键能计算ΔH、基元反应、决速步、化学反应中能量变化的本质、范特霍夫方程的应用
1、从教材上挖掘考点
【2022·国甲·28】目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时的热化学方程式及平衡常数如下:
(ⅰ)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) H1= +172 kJ·mol-1,Kp1=1.0×10-2
(ⅱ)碳氯化:2C(s)+TiO2(s)+2Cl2(g)=TiCl4(g)+2CO(g) H2=-51 kJ·mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的 H=___kJ·mol-1。
②碳氯化的反应趋势远大于直接氯化,原因是___。
考点:三道题均考查了化学反应的方向(ΔH、ΔS)
学业要求1:能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质。
学业要求3:能举例说明化学在解决能源危机中的重要作用,能分析能源的利用对自然环境和社会发展的影响。能综合考虑化学变化中的物质变化和能量变化来分析、解决实际问题,如煤炭的综合利用。
内容要求5:知道化学反应是有方向的,知道化学反应的方向与反应的焓变和熵变有关。
学法指导一: 教材内容,依然是高考选题的重要来源,引导学生回归教材,重视新增概念(自发反应、熵、基元反应、活化能、快慢反应、环境、体系等),明确概念的内涵和外延;挖掘教材素材(教材习题、“研究与实践”“科学·技术·社会”“探究”“信息搜索”“资料卡片”“图片”等栏目),关注时事热点,精细备考,是解决高考中此类题型的突破口。
2.4 高考试题研究与学法指导
1、从教材上挖掘考点
2、从“屡换新颜”的图像上分析突破
2023年全国甲
(1)能量-反应历程图
2023年湖北卷
2021山东卷
2021全国甲卷
(2)相对能量-反应历程图
2021年重庆卷
2023年1月浙江卷
(3)能量转化图
2023年全国新课标卷
(4)K的对数-1/T图
2023年湖北卷
2021年全国乙卷
坡式
梯式
坡式
梯式
坡式
梯式
2.4 高考试题研究与学法指导
学法指导二:抓住各类图像的特点,识别信息,精准转化,关注反应机理、物质变化过程中的能量变化、过渡态理论、范特霍夫公式、活化能与反应速率的关系、有效碰撞、催化作用机理等。
学业要求1:能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质。
学业要求2:能进行反应焓变的简单计算,能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应。
2.4 高考试题研究与学法指导
3、透过“新”背景提取“旧”知识
2021湖北
(1)反应热的计算
与物质结构相联系,用键能计算反应热
2.4 高考试题研究与学法指导
盖斯定律计算反应热
(2021.山东卷)
活化能计算反应热
反应热计算K
A.用物质的相对能量计算反应热
B.键能的计算
D.活化能与速率的关系、热化学方程式的书写
(2022·山东卷)利用γ 丁内酯(BL)制备1,4 丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和1 丁醇(BuOH)的副反应,涉及反应如下:
已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压H2氛围下进行,故H2压强近似等于总压。回答下列问题:
(1)以5.0×10-3 mol BL或BD为初始原料,在493 K、3.0×103 kPa的高压H2氛围下,分别在恒压容器中进行反应。达平衡时,以BL为原料,体系向环境放热X kJ;以BD为原料,体系从环境吸热Y kJ。忽略副反应热效应,反应Ⅰ焓变ΔH(493 K,3.0×103 kPa)=-200(X+Y)kJ·mol-1。
平衡与ΔH的关系,等效平衡思想计算ΔH
3、透过“新”背景提取“旧”知识
(1)反应热的计算
2.4 高考试题研究与学法指导
3、透过“新”背景提取“旧”知识
(2)综合考查(热点)
范德霍夫公式与能量变化、化学键的关系综合考查
2021年全国乙卷
根据图像,对反应吸热放热的判断及理由;结合反应对吸收热量计算
2.4 高考试题研究与学法指导
学法指导三:微专题突破“新”信息中“旧”的高频薄弱考点
“新”中“旧”考点:
1.由键能、盖斯定律、活化能、相对能量计算反应热仍是重点;
2.结合化学平衡中能量变化来计算反应热是难点;
3.知识点的考查呈融合趋势,不再单一考查,与新概念(范德霍夫公式等)、物质的结构与性质、化学平衡等融合,综合考查是热点
学业要求1:能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质。
学业要求2:能进行反应焓变的简单计算,能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应。
2.4 高考试题研究与学法指导
题号 满分 均分 难度 区分度
19(1) 2 0.36 0.18 0.35
19(2) 2 0.96 0.52 0.29
19(3)① 2 0.68 0.34 0.36
19(3)② 2 0.5 0.25 0.43
19(3)③ 2 1.04 0.52 0.46
19(4) 4 0.55 0.14 0.31
对反应热的计算与22山东卷考法类似
错因:
不会运用化学平衡中等效平衡思想来计算ΔH;
对正负号没有注意。
错因:不会用热效应判断平衡状态、漏选D选项
3.1 学情考情分析-武汉二调
错因:燃烧热概念不熟,失分
题干特点:自由基反应+能量反应过程图
错因:
A:不能理解题意,分析不同燃料耗氧量多少
B、C:对题目所给基元反应分析不到位,学生理解新信息能力不足。
D:不能从能量历程图看出断键所需能量,错误的把基元反应的能量变化当成断键所需能量
题目 A卷(1164)
A B C D 空 正确率
XZ-4 887 98 (8.42%) 83 96 76.20%
题目 A卷(1164)
A B C D 空 正确率
XZ-10 109 645 169 240(20.62%) 1 55.41%
3.2 学情考情分析-黄冈三调
二轮复习备考策略
四
总课时:2课时
反应的自发性(ΔG)、化学平衡及范特霍夫方程的应用
ΔH与能量机理图、平衡的小综合
微专题一
微专题二
4.1 备考策略---课时安排
1. 关注教材,重视素材
关注新教材素材和新概念,深入挖掘
2. 整合资源,构建网络
整合归纳,构建网络,使知识系统化和条理化
3. 精选试题,考练结合
把握高考方向,精选试题,以练习促能力,以考试促进步
4.2 备考策略---复习策略
练 ----- 发现问题
讲 -----问题驱动,回归教材,引热点,构网络,建模型
练 -----精选试题,专项训练,一 一突破
评 -----评共性,评审题,评规范,评细节
练习题---基础
周测题---规范
高考题---能力
提炼
共性
问题
错题重做
温故知新
错题筛选
4.3 备考策略---复习模式
“反应的自发性(ΔG)、化学平衡及范特霍夫方程的应用”
环节一 环节二 环节三 环节四
回归教材:自由能与化学反应的方向资料卡片
真题整合:
精选真题,见识常考的题型和内容
模型构建:
1.ΔG的判断;2.原因解释题;3.解题步骤。
练习巩固:
变式训练,交流点评,课堂小结。
4.3 备考策略---复习模式
感谢聆听,敬请指正!
化学反应与能量 (包括焓变、熵)
黄冈市2024届高三化学二轮复习备考
内容
摘要
二轮备考策略
学情考情分析
课程标准解读
1
3
4
黄冈市2024届高三化学二轮复习备考
高考试题研究
2
《普通高中化学课程标准(2017年版2020年修订)》 内容要求 学业要求
(1)认识化学键的断裂和形成是反应中物质变化的实质及能量变化的主要原因 (2)认识物质具有能量,认识吸热反应与放热反应,了解化学反应体系能量改变与化学键的断裂和形成有关。体会提高燃料的燃烧效率、开发高能清洁燃料和研制新型电池的重要性 (3)认识化学能可与热能、电能等其他形式能量之间相互转化,能量的转化遵循能量守恒定律。知道内能是体系内物质的各种能量的总和,受温度、压强、物质的聚集状态的影响 (4)恒温恒压下化学反应的反应热可用焓变表示,了解盖斯定律及简单应用 (5)知道化学反应有方向,知道化学反应的方向与反应的焓变和熵变有关 (1)能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质
(2)能进行反应焓变的简单计算,能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应
(3)能举例说明化学在解决能源危机中的重要作用,能分析能源的利用对自然环境和社会发展的影响。能综合考虑化学变化中的物质变化和能量变化来分析、解决实际问题,如煤炭的综合利用
学科素养 (1)能分析物质化学变化和伴随发生的能量转化与物质微观结构之间的关系,体现了宏观辨识与微观探析。 (2)能运用化学计量单位定量分析化学变化及其伴随发生的能量变化,体现了变化观念与平衡思想。 (3)具有“绿色化学”观念,能运用知识分析和探讨某些化学过程对人类健康、社会可持续发展可能带来的双重影响,并从多个方面评估这些影响;具有理论联系实际的观念,有将化学成果应用于生产、生活的意识,能依据实际条件并运用所学知识和方法解决生产、生活中简单的化学问题,体现了科学探究与创新意识及科学态度与社会责任。
1.1 高中化学课程标准
关键能力
必备知识
核心价值
学科素养
实际问题
真实情景
高考核心功能:
---为什么考 ?
高考核心要求:
-----怎么考 ?
高考核心内容:
-----考什么 ?
1.2 高考评价体系
2.1 高考试题研究---热点考点
2023 2022 2021 湖北 新课标 国甲 国乙 湖北 国甲 国乙 湖北 国甲 国乙
图像 √ √ √ √
题型(选+非选) 2+4 0+3 0+3 0+1 1+1 0+3 0+1 0+1 0+3 1+4
能源 √ √
ΔH的计算 √ √ √ √ √ √ √ √ √
热化学方程式书写
熵、反应历程、活化能、决速步等 熵变判断 √ √ √ 反应方向的判断及理由 能量图的判断及理由 ΔH与0关系、理由、能量计算
反应的自发性 表述题
化学反应与能量的本质
综合考查 √ ΔH算K ΔH算K
2.2 九省试题研究
情景素材:生产生活、铜锈
学科素养:证据推理与模型认知
关键能力:信息提取、逻辑推理能力
命题特点:考查了ΔG=ΔH-TΔS,即反
应的自发与方向
2.2 九省试题研究
情景素材:生产生活、苯乙烯的制备
学科素养:证据推理与模型认知
关键能力:信息提取、逻辑推理能力
命题特点:考查了ΔG=ΔH-TΔS,即反
应的自发与方向
地方 安徽 甘肃 广西 贵州 河南 黑龙江吉林 江西
图像 ΔH/TΔS-T图 ΔG/Kp1-T图 相对能量-路径图 能量-进程图
题型(选+非选) 1+2 0+4 0+2 1+3 0+2 0+2 1+3
能源
键能计算ΔH 键能的计算
盖斯定律计算ΔH √ √ √ √ √ √
热化学方程式 书写及判断
熵、反应历程、活化能、决速步等概念 已知各步反应Ea,找慢反应 决速步 找能量变化图及理由
综合考查 √ 分解温度、ΔG判断平衡方向、理由 催化剂对ΔH影响 催化剂对ΔH影响
反应的自发性 √ 判断及理由 判断 原因
化学反应与能量的本质 √断键成键角度找物质
2.2 九省试题研究
2.3 高考试题研究--近三年湖北
选择题 2021年未考查
2022年一道(T8),考查化学反应的熵变
2023年两道(T1、3),考查能源的选择、化学反应的熵变
非选择题 均考查了ΔH的计算
2023年新增了对基元反应、活化能进行考查
湖北考情分析
1. 近三年分值逐年递增
2. 仍以非选择题为主,出现在平衡大题前面几问中
3. 选择题近三年分别考查了0、1、2道
24年命题预测:
(1)湖北卷仍以非选择题考查形式为主,考查1~3个空;选择题至少一道。
(2)选择题沿用前沿背景:以环保材料、时事热点、教材素材等为素材。
(3)非选题延续高频考点(重点):ΔH的计算(键能、盖斯定律、活化能、相对能量、等效平衡等)
(4)非选题难点:图像的分析
(5)非选题热点:反应的自发性判断、基元反应、活化能等
(6)重视深挖教材:教材新增的素材(研究与实践、科学技术社会、探究、资料卡片等);新增概念(自发反应、熵、基元反应、活化能等);
2.3 高考试题研究--高考预测
【2023·湖北】 2023年5月10日,天舟六号货运飞船成功发射,标志着我国航天事业进入到高质量新阶段。下列不能作为火箭推进剂的是
A.液氮-液氢 B.液氧-液氢
C.液态NO2-肼 D.液氧-煤油
选择性必修一:P11
【选择性必修一P17练习与应用:T4】
4. 火箭发射时,可用肼(N2H4,液态)作燃料,NO2做氧化剂,二者反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)=2NO2(g) ΔH1=+664kJ/mol
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=-534kJ/mol
请写出N2H4(l)与NO2(g)反应的热化学方程式。
2.4 高考试题研究与学法指导
考点:考查化学反应中能量的转化及应用
(1)从教材素材上挖掘考点
~~~~~~研究与实践~~~~~~
了解火箭推进剂
【研究目的】
火箭推进剂在航天和军事等领域具有广泛的应用。通过查阅资料,了解火箭推进剂的发展历史、现状及趋势,感受火箭推进剂的发展对人类社会进步的促进作用,体会化学反应中能量变化的重要价值。
【研究任务】
(1)了解火箭推进剂的发展历史
(2)了解我国目前常用的火箭推进剂的类型、成分和特点
(3)了解火箭推进剂的发展趋势
【结果与讨论】
(1)通过研究,你得到什么启示?
(2)撰写研究报告,并于同学讨论。
1、从教材上挖掘考点
情境素材:航天器的火箭推进剂
学科素养:证据推理与模型认知
关键能力:信息提取能力、理解与辨析能力
命题特点:考题突出考查了基础性、应用性
2.4 高考试题研究与学法指导
(2)从教材概念上挖掘考点
考点:两道题均考查了化学反应的熵变
1、从教材上挖掘考点
2.4 高考试题研究与学法指导
(2)从教材概念上挖掘考点
(2022年1月浙江)AB型强电解质在水中的溶解(可视作特殊的化学反应)表示为AB(s)=An+(aq)+Bn-(aq),其焓变和熵变分别为ΔH和ΔS。下列说法正确的是( )
A. ΔH和ΔS均大于零
B. ΔH和ΔS均小于零
C. ΔH大于零或小于零,ΔS大于零
D. ΔH和ΔS均可能大于零或小于零
(2022年1月浙江)29. 工业上,以煤炭为原料,通入一定比例的空气和水蒸气,经过系列反应可以得到满足不同需求的原料气。
(1)在C和O2的反应体系中:
反应1:C(s)+O2(g)=CO2(g) ΔH1=-394kJ·mol-1
反应2:2CO(g)+O2(g)=2CO2(g) ΔH2=-566kJ·mol-1
反应3:2C(s)+O2(g)=2CO(g) ΔH3。
①设y=ΔH-TΔS,反应1、2和3的y随温度的变化关系如图1所示。图中对应于反应3的线条是___。
情景素材:科研成果、新材料---纳米碗
试题特色:图文简洁、思维量大
关键能力:信息获取与加工、逻辑推理与论证能力
必备知识:键能计算ΔH、基元反应、决速步、化学反应中能量变化的本质、范特霍夫方程的应用
1、从教材上挖掘考点
【2022·国甲·28】目前生产钛的方法之一是将金红石(TiO2)转化为TiCl4,再进一步还原得到钛。
(1)TiO2转化为TiCl4有直接氯化法和碳氯化法。在1000℃时的热化学方程式及平衡常数如下:
(ⅰ)直接氯化:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g) H1= +172 kJ·mol-1,Kp1=1.0×10-2
(ⅱ)碳氯化:2C(s)+TiO2(s)+2Cl2(g)=TiCl4(g)+2CO(g) H2=-51 kJ·mol-1,Kp2=1.2×1012Pa
①反应2C(s)+O2(g)=2CO(g)的 H=___kJ·mol-1。
②碳氯化的反应趋势远大于直接氯化,原因是___。
考点:三道题均考查了化学反应的方向(ΔH、ΔS)
学业要求1:能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质。
学业要求3:能举例说明化学在解决能源危机中的重要作用,能分析能源的利用对自然环境和社会发展的影响。能综合考虑化学变化中的物质变化和能量变化来分析、解决实际问题,如煤炭的综合利用。
内容要求5:知道化学反应是有方向的,知道化学反应的方向与反应的焓变和熵变有关。
学法指导一: 教材内容,依然是高考选题的重要来源,引导学生回归教材,重视新增概念(自发反应、熵、基元反应、活化能、快慢反应、环境、体系等),明确概念的内涵和外延;挖掘教材素材(教材习题、“研究与实践”“科学·技术·社会”“探究”“信息搜索”“资料卡片”“图片”等栏目),关注时事热点,精细备考,是解决高考中此类题型的突破口。
2.4 高考试题研究与学法指导
1、从教材上挖掘考点
2、从“屡换新颜”的图像上分析突破
2023年全国甲
(1)能量-反应历程图
2023年湖北卷
2021山东卷
2021全国甲卷
(2)相对能量-反应历程图
2021年重庆卷
2023年1月浙江卷
(3)能量转化图
2023年全国新课标卷
(4)K的对数-1/T图
2023年湖北卷
2021年全国乙卷
坡式
梯式
坡式
梯式
坡式
梯式
2.4 高考试题研究与学法指导
学法指导二:抓住各类图像的特点,识别信息,精准转化,关注反应机理、物质变化过程中的能量变化、过渡态理论、范特霍夫公式、活化能与反应速率的关系、有效碰撞、催化作用机理等。
学业要求1:能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质。
学业要求2:能进行反应焓变的简单计算,能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应。
2.4 高考试题研究与学法指导
3、透过“新”背景提取“旧”知识
2021湖北
(1)反应热的计算
与物质结构相联系,用键能计算反应热
2.4 高考试题研究与学法指导
盖斯定律计算反应热
(2021.山东卷)
活化能计算反应热
反应热计算K
A.用物质的相对能量计算反应热
B.键能的计算
D.活化能与速率的关系、热化学方程式的书写
(2022·山东卷)利用γ 丁内酯(BL)制备1,4 丁二醇(BD),反应过程中伴有生成四氢呋喃(THF)和1 丁醇(BuOH)的副反应,涉及反应如下:
已知:①反应Ⅰ为快速平衡,可认为不受慢反应Ⅱ、Ⅲ的影响;②因反应Ⅰ在高压H2氛围下进行,故H2压强近似等于总压。回答下列问题:
(1)以5.0×10-3 mol BL或BD为初始原料,在493 K、3.0×103 kPa的高压H2氛围下,分别在恒压容器中进行反应。达平衡时,以BL为原料,体系向环境放热X kJ;以BD为原料,体系从环境吸热Y kJ。忽略副反应热效应,反应Ⅰ焓变ΔH(493 K,3.0×103 kPa)=-200(X+Y)kJ·mol-1。
平衡与ΔH的关系,等效平衡思想计算ΔH
3、透过“新”背景提取“旧”知识
(1)反应热的计算
2.4 高考试题研究与学法指导
3、透过“新”背景提取“旧”知识
(2)综合考查(热点)
范德霍夫公式与能量变化、化学键的关系综合考查
2021年全国乙卷
根据图像,对反应吸热放热的判断及理由;结合反应对吸收热量计算
2.4 高考试题研究与学法指导
学法指导三:微专题突破“新”信息中“旧”的高频薄弱考点
“新”中“旧”考点:
1.由键能、盖斯定律、活化能、相对能量计算反应热仍是重点;
2.结合化学平衡中能量变化来计算反应热是难点;
3.知识点的考查呈融合趋势,不再单一考查,与新概念(范德霍夫公式等)、物质的结构与性质、化学平衡等融合,综合考查是热点
学业要求1:能辨识化学反应中的能量转化形式,能解释化学反应中能量变化的本质。
学业要求2:能进行反应焓变的简单计算,能用热化学方程式表示反应中的能量变化,能运用反应焓变合理选择和利用化学反应。
2.4 高考试题研究与学法指导
题号 满分 均分 难度 区分度
19(1) 2 0.36 0.18 0.35
19(2) 2 0.96 0.52 0.29
19(3)① 2 0.68 0.34 0.36
19(3)② 2 0.5 0.25 0.43
19(3)③ 2 1.04 0.52 0.46
19(4) 4 0.55 0.14 0.31
对反应热的计算与22山东卷考法类似
错因:
不会运用化学平衡中等效平衡思想来计算ΔH;
对正负号没有注意。
错因:不会用热效应判断平衡状态、漏选D选项
3.1 学情考情分析-武汉二调
错因:燃烧热概念不熟,失分
题干特点:自由基反应+能量反应过程图
错因:
A:不能理解题意,分析不同燃料耗氧量多少
B、C:对题目所给基元反应分析不到位,学生理解新信息能力不足。
D:不能从能量历程图看出断键所需能量,错误的把基元反应的能量变化当成断键所需能量
题目 A卷(1164)
A B C D 空 正确率
XZ-4 887 98 (8.42%) 83 96 76.20%
题目 A卷(1164)
A B C D 空 正确率
XZ-10 109 645 169 240(20.62%) 1 55.41%
3.2 学情考情分析-黄冈三调
二轮复习备考策略
四
总课时:2课时
反应的自发性(ΔG)、化学平衡及范特霍夫方程的应用
ΔH与能量机理图、平衡的小综合
微专题一
微专题二
4.1 备考策略---课时安排
1. 关注教材,重视素材
关注新教材素材和新概念,深入挖掘
2. 整合资源,构建网络
整合归纳,构建网络,使知识系统化和条理化
3. 精选试题,考练结合
把握高考方向,精选试题,以练习促能力,以考试促进步
4.2 备考策略---复习策略
练 ----- 发现问题
讲 -----问题驱动,回归教材,引热点,构网络,建模型
练 -----精选试题,专项训练,一 一突破
评 -----评共性,评审题,评规范,评细节
练习题---基础
周测题---规范
高考题---能力
提炼
共性
问题
错题重做
温故知新
错题筛选
4.3 备考策略---复习模式
“反应的自发性(ΔG)、化学平衡及范特霍夫方程的应用”
环节一 环节二 环节三 环节四
回归教材:自由能与化学反应的方向资料卡片
真题整合:
精选真题,见识常考的题型和内容
模型构建:
1.ΔG的判断;2.原因解释题;3.解题步骤。
练习巩固:
变式训练,交流点评,课堂小结。
4.3 备考策略---复习模式
感谢聆听,敬请指正!
同课章节目录
