4.2蛋白质课件(共34张PPT) 人教版(2019)选择性必修3
文档属性
| 名称 | 4.2蛋白质课件(共34张PPT) 人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 115.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-06 01:03:59 | ||
图片预览








文档简介
(共34张PPT)
第四章 生物大分子
2019人教版选择性必修三
第二节 蛋白质
蛋白质
核心素养发展目标
1.知道氨基酸的组成、结构特点和主要化学性质,了解氨基酸、蛋白质与人体健康的关系。
2.了解蛋白质的组成、结构和性质,认识人工合成多肽、蛋白质等的意义。
3.知道酶催化的特点。
蛋白质
组成蛋白质的氨基酸主要是___________
ɑ-氨基酸
R CH COOH
NH2
ɑ
当R不是H时(即除甘氨酸外),ɑ-碳为手性碳原子
大部分ɑ-氨基酸具有对映异构
氨基酸
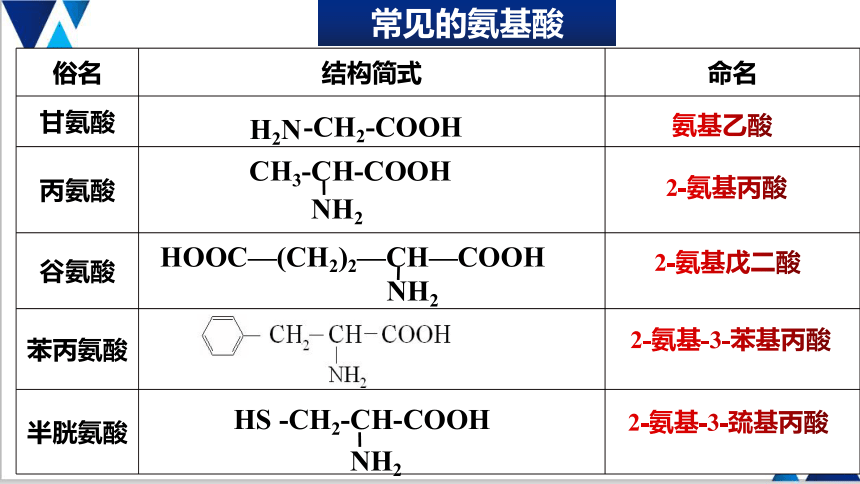
常见的氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
-CH2-COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3-CH-COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
HS -CH2-CH-COOH
NH2
天然氨基酸均为无色晶体,熔点较高,在200~3000C时熔化分解
1.物理性质
一般能溶于水而难溶于乙醇、乙醚等有机溶剂
氨基酸的性质
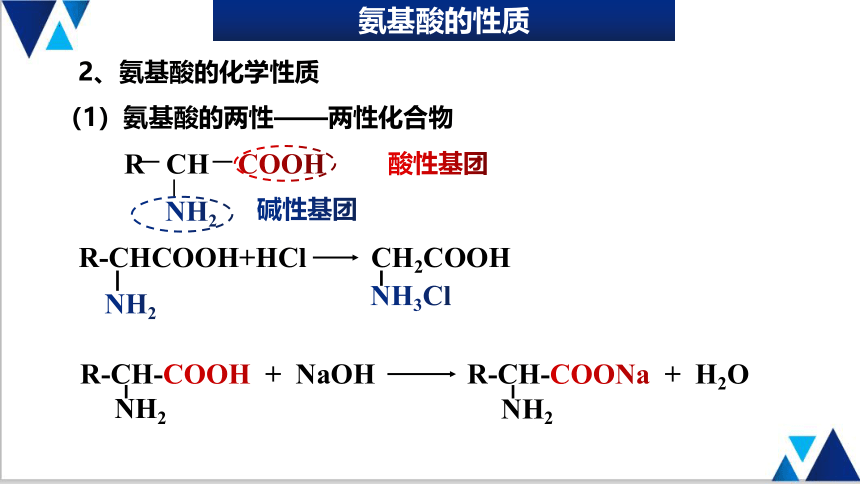
2、氨基酸的化学性质
(1)氨基酸的两性
——两性化合物
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
R-CHCOOH+HCl CH2COOH
NH2
NH3Cl
R CH COOH
NH2
氨基酸的性质
酸性基团
碱性基团
下列物质中既能与盐酸反应,又能与NaOH溶液反应的是 ( )
①NaHCO3 ; ②(NH4)2S ; ③Al(OH)3 ;
④NH4Cl; ⑤H2N-CH2-COOH ; ⑥CH3COOH
A.①②③ B.①②④⑤ C.⑤⑥ D.①②③⑤
小结:既能与酸反应又能与碱反应的物质
(1)多元弱酸的酸式盐; (2)弱酸的铵盐;
(3)具两性的物质; (4)氨基酸和蛋白质;
D
氨基酸
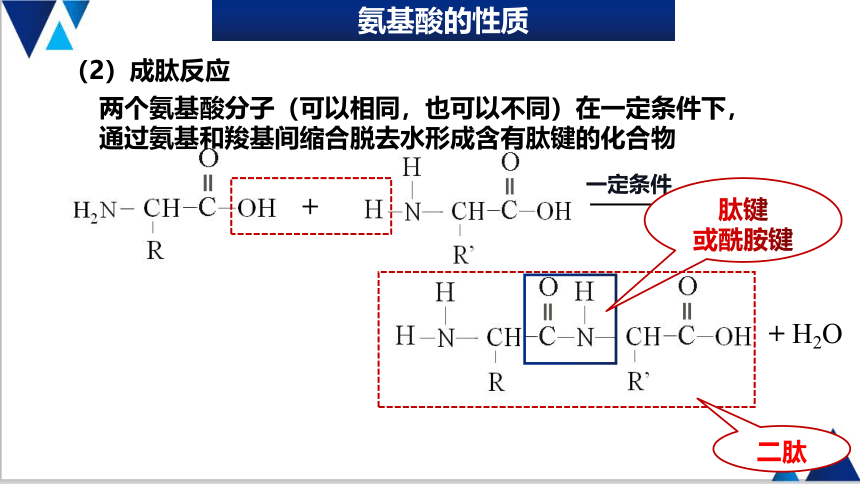
(2)成肽反应
一定条件
+
肽键
或酰胺键
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基和羧基间缩合脱去水形成含有肽键的化合物
+ H2O
二肽
氨基酸的性质
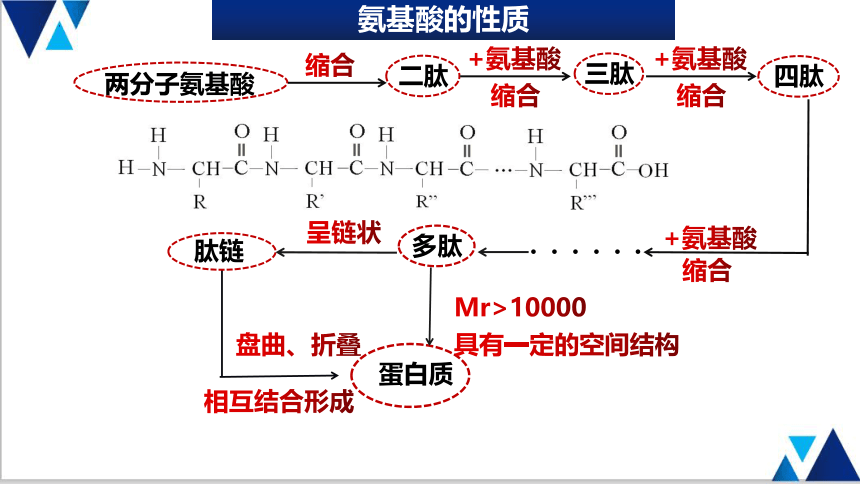
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · · · ·
相互结合形成
盘曲、折叠
蛋白质
Mr>10000
具有一定的空间结构
氨基酸的性质
呈链状
肽链
该过程实际是氨基酸分子缩聚成高分子化合物的过程——氨基酸的缩聚反应。由n个同种氨基酸分子发生成肽反应,生成一个肽链时,会生成(n-1)个水分子和(n-1)个肽键。
氨基酸的性质
写出苯丙氨酸与甘氨酸发生成肽反应生成多肽的化学方程式
小结:缩聚反应:由一种单体进行缩聚反应,生成的小分子物质的量一般为n-1;由两种单体进行缩聚反应,生成的小分子物质的量一般为2n-1。
n
蛋白质
1.定义:蛋白质是由多种氨基酸通过肽键等相互连接形成的一类生物大分子,是一般细胞中含量最多的有机分子。
蛋白质中主要含有C、H、O、N等元素,属于天然有机高分子化合物。
蛋白质含量的测定:由于生物组织中绝大部分氮元素来自蛋白质,而且各种来源不同的蛋白质的含氮量都比较接近,平均为16%。因此生物样品中的1g氮元素大致相当于6.25 g蛋白质,由此可以通过测定样品中氮元素的质量分数计算出其中蛋白质的含量。
多肽链的氨基酸
种类、数目及排列顺序
特定的空间结构
蛋白质的结构
各种蛋白质都有其特殊功能和活性
一级结构
二级结构
三级结构
四级结构
蛋白质的结构
例如,血红蛋白分子中的________会因遗传因素变成________,这一微小差别会导致红细胞的形态由正常的圆饼状变为异常的镰刀状,使人患镰状细胞贫血。
蛋白质分子中氨基酸单体的__________称为蛋白质的一级结构
排列顺序
一级结构是______________的基础,对蛋白质的___________起着决定性作用
蛋白质高级结构
性质和功能
谷氨酸
缬氨酸
蛋白质的结构
肽键中的氧原子与氢原子之间__________,会使肽链 ____________成特定的空间结构,形成蛋白质的二级结构。
存在氢键
盘绕或折叠
氢键
蛋白质的结构
肽链在二级结构基础上还会进一步盘曲折叠,形成更复杂的三级结构
多个具有特定三级结构的多肽链通过___________________(如氢键等)排列组装,形成蛋白质的四级结构。
非共价键相互作用
蛋白质的结构
(1)两性:蛋白质的结构中含有__________和____________两种官能团,因此既能与酸反应又能与碱反应,是两性分子。
—NH2
—COOH
酸、碱或酶
氨基酸
HO
H
O
H
H—N—CH2—C—
O
H
—N—CH2—C—OH
蛋白质的性质
(2)水解:蛋白质在______________的作用下,水解生成相对分子质量较小的多肽化合物,最终水解得到__________。天然蛋白质水解的最终产物都是α-氨基酸。
蛋白质的性质
(3)盐析
少量的某些可溶性盐(如硫酸铵、硫酸钠、氯化钠等)能促进蛋白质的溶解。但当这些盐在蛋白质溶液中达到一定浓度时,反而使蛋白质的溶解度降低而使其从溶液中析出,这种作用称为盐析。
蛋白质的性质
(3)盐析
特点与应用:蛋白质的盐析是一个可逆过程,利用多次盐析的方法可分离提纯蛋白质。
蛋白质的性质
(4)变性
概念
影响因素 物理
化学因素
特点
(4)变性
蛋白质的性质
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热、加压、搅拌、振荡、紫外线和放射线、超声波等
强酸、强碱、重金属盐、乙醇、甲醛、丙酮等
变性会使蛋白质的结构发生变化,使其失去原有的生理活性,在水中不能重新溶解,是不可逆过程
在日常生活中有时需要利用蛋白质变性,如食物加热、消毒等,有时防止蛋白质变性,如疫苗等生物制剂需低温保存等。
【思考】
2.为什么紫外线可用于环境和物品消毒,放射线可用于医疗器械灭菌?
误服重金属盐,可口服牛奶、蛋清或豆浆,其目的是使重金属盐与牛奶等发生变性作用,从而减少人体蛋白质变性。
紫外线用于环境和物品消毒,放射线用于医疗器械消毒,都是利用紫外线或放射线使细菌和病毒中的蛋白发生变性而使其死亡。
蛋白质的性质
1.因误服铅、汞等重金属盐中毒的患者在急救时,为什么可口服牛奶、蛋清或豆浆?
蛋白质的性质
(5)显色反应
向蛋白质溶液加入浓硝酸会有_____色沉淀产生,加热后沉淀变_____色。
——可用于蛋白质的分析检测
固体蛋白质如皮肤、指甲遇浓硝酸变______色。
白
含有苯环
黄
黄
其他一些试剂也可以与蛋白质作用,呈现特定颜色
(5)显色反应
蛋白质的性质
(6)燃烧产生烧焦羽毛的气味
用于区别合成纤维与蛋白质(如真丝、蚕丝、纯毛、毛线等)
中国科学院生物化学研究所、有机化学研究所和北京大学化学系等单位的多位科学家经过长期不懈努力,在1965年首先合成了结晶牛胰岛素。
科学史话
蛋白质的性质
酶
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
特点
具有高效催化作用
条件温和
具有高度的专一性
一般是普通催化剂的107倍
一般在接近体温和中性的条件下进行,此时酶的活性最高。超过适宜的温度时,酶将失去活性
酶是一类由细胞产生的、对生物体内的化学反应具有催化作用的有机物,其中大多数是蛋白质。
应用:蛋白酶用于医药、制革等工业;淀粉酶用于食品、发酵、纺织等工业;有的酶还可用于疾病的诊断。
(1)成肽反应的规律为—COOH脱—OH,—NH2脱—H ( )
(2)氨基酸分子、烃分子中的氢原子数均为偶数( )
(3)两个氨基酸分子脱水后形成的二肽中含有两个肽键( )
(4)向两份蛋白质溶液中分别加入饱和NaCl溶液和CuSO4溶液,均有固体析出,且两者的原理相同( )
(5)通常用酒精消毒,其原理是酒精使细菌中的蛋白质盐析而失去生理活性( )
1.正误判断
√
×
×
×
达标检测
×
达标检测
2.甘氨酸和丙氨酸混合,在一定条件下发生缩合反应生成二肽的化合物共有( )
A.4种 B.3种 C.2种 D.1种
A
同种氨基酸缩合反应生成二肽的化合物各有一种,甘氨酸和丙氨酸发生缩合反应生成二肽的化合物有两种。
A. B.
C.NH2—CH2—COOH D.
3.含有下列结构片段的蛋白质在胃液中水解,不可能产生的氨基酸是( )
达标检测
D
达标检测
4.某物质的结构简式如图所示,下列有关该物质的说法不正确的是( )
A.该物质的分子式为C13H16N2O5
B.该物质是由两分子不同的氨基酸经脱水缩合而得
C.该物质属于蛋白质
D.1 mol该物质最多可与2 mol NaHCO3反应
C
达标检测
5.下列物质中可以使蛋白质变性的是( )
①福尔马林 ②酒精 ③高锰酸钾溶液 ④硫酸铵溶液 ⑤硫酸铜 ⑥双氧水 ⑦硝酸
A.除④⑦外 B.除③⑥外
C.①②⑤ D.除④外
D
达标检测
C
6.下列关于蛋白质的叙述正确的是( )
A.加热能杀死流感病毒是因为病毒的蛋白质受热发生盐析
B.温度越高,对某些化学反应的催化效率越高
C.蛋白质水解的最终产物是氨基酸
D.任何结构的蛋白质遇到浓硝酸都会变成黄色
达标检测
A
7.下列关于酶的叙述中,不正确的是( )
A.酶是一种糖类物质
B.酶大多数是蛋白质
C.酶是生物体内产生的催化剂
D.酶受到高温或重金属盐作用时会变性
绝大多数酶是蛋白质,而不是糖类物质,具有蛋白质的性质,当受到高温或重金属盐作用时会变性;酶还是生物体内产生的高效催化剂,其催化作用具有条件温和、不需加热、高度专一、催化效率高等特点。
第四章 生物大分子
2019人教版选择性必修三
第二节 蛋白质
蛋白质
核心素养发展目标
1.知道氨基酸的组成、结构特点和主要化学性质,了解氨基酸、蛋白质与人体健康的关系。
2.了解蛋白质的组成、结构和性质,认识人工合成多肽、蛋白质等的意义。
3.知道酶催化的特点。
蛋白质
组成蛋白质的氨基酸主要是___________
ɑ-氨基酸
R CH COOH
NH2
ɑ
当R不是H时(即除甘氨酸外),ɑ-碳为手性碳原子
大部分ɑ-氨基酸具有对映异构
氨基酸
常见的氨基酸
俗名 结构简式 命名
甘氨酸
丙氨酸
谷氨酸
苯丙氨酸
半胱氨酸
-CH2-COOH
H2N
氨基乙酸
2-氨基丙酸
2-氨基戊二酸
2-氨基-3-苯基丙酸
2-氨基-3-巯基丙酸
CH3-CH-COOH
NH2
HOOC—(CH2)2—CH—COOH
NH2
HS -CH2-CH-COOH
NH2
天然氨基酸均为无色晶体,熔点较高,在200~3000C时熔化分解
1.物理性质
一般能溶于水而难溶于乙醇、乙醚等有机溶剂
氨基酸的性质
2、氨基酸的化学性质
(1)氨基酸的两性
——两性化合物
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
R-CHCOOH+HCl CH2COOH
NH2
NH3Cl
R CH COOH
NH2
氨基酸的性质
酸性基团
碱性基团
下列物质中既能与盐酸反应,又能与NaOH溶液反应的是 ( )
①NaHCO3 ; ②(NH4)2S ; ③Al(OH)3 ;
④NH4Cl; ⑤H2N-CH2-COOH ; ⑥CH3COOH
A.①②③ B.①②④⑤ C.⑤⑥ D.①②③⑤
小结:既能与酸反应又能与碱反应的物质
(1)多元弱酸的酸式盐; (2)弱酸的铵盐;
(3)具两性的物质; (4)氨基酸和蛋白质;
D
氨基酸
(2)成肽反应
一定条件
+
肽键
或酰胺键
两个氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基和羧基间缩合脱去水形成含有肽键的化合物
+ H2O
二肽
氨基酸的性质
两分子氨基酸
缩合
二肽
三肽
缩合
+氨基酸
缩合
+氨基酸
四肽
缩合
+氨基酸
多肽
· · · · · ·
相互结合形成
盘曲、折叠
蛋白质
Mr>10000
具有一定的空间结构
氨基酸的性质
呈链状
肽链
该过程实际是氨基酸分子缩聚成高分子化合物的过程——氨基酸的缩聚反应。由n个同种氨基酸分子发生成肽反应,生成一个肽链时,会生成(n-1)个水分子和(n-1)个肽键。
氨基酸的性质
写出苯丙氨酸与甘氨酸发生成肽反应生成多肽的化学方程式
小结:缩聚反应:由一种单体进行缩聚反应,生成的小分子物质的量一般为n-1;由两种单体进行缩聚反应,生成的小分子物质的量一般为2n-1。
n
蛋白质
1.定义:蛋白质是由多种氨基酸通过肽键等相互连接形成的一类生物大分子,是一般细胞中含量最多的有机分子。
蛋白质中主要含有C、H、O、N等元素,属于天然有机高分子化合物。
蛋白质含量的测定:由于生物组织中绝大部分氮元素来自蛋白质,而且各种来源不同的蛋白质的含氮量都比较接近,平均为16%。因此生物样品中的1g氮元素大致相当于6.25 g蛋白质,由此可以通过测定样品中氮元素的质量分数计算出其中蛋白质的含量。
多肽链的氨基酸
种类、数目及排列顺序
特定的空间结构
蛋白质的结构
各种蛋白质都有其特殊功能和活性
一级结构
二级结构
三级结构
四级结构
蛋白质的结构
例如,血红蛋白分子中的________会因遗传因素变成________,这一微小差别会导致红细胞的形态由正常的圆饼状变为异常的镰刀状,使人患镰状细胞贫血。
蛋白质分子中氨基酸单体的__________称为蛋白质的一级结构
排列顺序
一级结构是______________的基础,对蛋白质的___________起着决定性作用
蛋白质高级结构
性质和功能
谷氨酸
缬氨酸
蛋白质的结构
肽键中的氧原子与氢原子之间__________,会使肽链 ____________成特定的空间结构,形成蛋白质的二级结构。
存在氢键
盘绕或折叠
氢键
蛋白质的结构
肽链在二级结构基础上还会进一步盘曲折叠,形成更复杂的三级结构
多个具有特定三级结构的多肽链通过___________________(如氢键等)排列组装,形成蛋白质的四级结构。
非共价键相互作用
蛋白质的结构
(1)两性:蛋白质的结构中含有__________和____________两种官能团,因此既能与酸反应又能与碱反应,是两性分子。
—NH2
—COOH
酸、碱或酶
氨基酸
HO
H
O
H
H—N—CH2—C—
O
H
—N—CH2—C—OH
蛋白质的性质
(2)水解:蛋白质在______________的作用下,水解生成相对分子质量较小的多肽化合物,最终水解得到__________。天然蛋白质水解的最终产物都是α-氨基酸。
蛋白质的性质
(3)盐析
少量的某些可溶性盐(如硫酸铵、硫酸钠、氯化钠等)能促进蛋白质的溶解。但当这些盐在蛋白质溶液中达到一定浓度时,反而使蛋白质的溶解度降低而使其从溶液中析出,这种作用称为盐析。
蛋白质的性质
(3)盐析
特点与应用:蛋白质的盐析是一个可逆过程,利用多次盐析的方法可分离提纯蛋白质。
蛋白质的性质
(4)变性
概念
影响因素 物理
化学因素
特点
(4)变性
蛋白质的性质
在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象
加热、加压、搅拌、振荡、紫外线和放射线、超声波等
强酸、强碱、重金属盐、乙醇、甲醛、丙酮等
变性会使蛋白质的结构发生变化,使其失去原有的生理活性,在水中不能重新溶解,是不可逆过程
在日常生活中有时需要利用蛋白质变性,如食物加热、消毒等,有时防止蛋白质变性,如疫苗等生物制剂需低温保存等。
【思考】
2.为什么紫外线可用于环境和物品消毒,放射线可用于医疗器械灭菌?
误服重金属盐,可口服牛奶、蛋清或豆浆,其目的是使重金属盐与牛奶等发生变性作用,从而减少人体蛋白质变性。
紫外线用于环境和物品消毒,放射线用于医疗器械消毒,都是利用紫外线或放射线使细菌和病毒中的蛋白发生变性而使其死亡。
蛋白质的性质
1.因误服铅、汞等重金属盐中毒的患者在急救时,为什么可口服牛奶、蛋清或豆浆?
蛋白质的性质
(5)显色反应
向蛋白质溶液加入浓硝酸会有_____色沉淀产生,加热后沉淀变_____色。
——可用于蛋白质的分析检测
固体蛋白质如皮肤、指甲遇浓硝酸变______色。
白
含有苯环
黄
黄
其他一些试剂也可以与蛋白质作用,呈现特定颜色
(5)显色反应
蛋白质的性质
(6)燃烧产生烧焦羽毛的气味
用于区别合成纤维与蛋白质(如真丝、蚕丝、纯毛、毛线等)
中国科学院生物化学研究所、有机化学研究所和北京大学化学系等单位的多位科学家经过长期不懈努力,在1965年首先合成了结晶牛胰岛素。
科学史话
蛋白质的性质
酶
在酶的作用下,生物才能进行新陈代谢,完成消化、呼吸、运动、生长、发育、繁殖等生命活动。
特点
具有高效催化作用
条件温和
具有高度的专一性
一般是普通催化剂的107倍
一般在接近体温和中性的条件下进行,此时酶的活性最高。超过适宜的温度时,酶将失去活性
酶是一类由细胞产生的、对生物体内的化学反应具有催化作用的有机物,其中大多数是蛋白质。
应用:蛋白酶用于医药、制革等工业;淀粉酶用于食品、发酵、纺织等工业;有的酶还可用于疾病的诊断。
(1)成肽反应的规律为—COOH脱—OH,—NH2脱—H ( )
(2)氨基酸分子、烃分子中的氢原子数均为偶数( )
(3)两个氨基酸分子脱水后形成的二肽中含有两个肽键( )
(4)向两份蛋白质溶液中分别加入饱和NaCl溶液和CuSO4溶液,均有固体析出,且两者的原理相同( )
(5)通常用酒精消毒,其原理是酒精使细菌中的蛋白质盐析而失去生理活性( )
1.正误判断
√
×
×
×
达标检测
×
达标检测
2.甘氨酸和丙氨酸混合,在一定条件下发生缩合反应生成二肽的化合物共有( )
A.4种 B.3种 C.2种 D.1种
A
同种氨基酸缩合反应生成二肽的化合物各有一种,甘氨酸和丙氨酸发生缩合反应生成二肽的化合物有两种。
A. B.
C.NH2—CH2—COOH D.
3.含有下列结构片段的蛋白质在胃液中水解,不可能产生的氨基酸是( )
达标检测
D
达标检测
4.某物质的结构简式如图所示,下列有关该物质的说法不正确的是( )
A.该物质的分子式为C13H16N2O5
B.该物质是由两分子不同的氨基酸经脱水缩合而得
C.该物质属于蛋白质
D.1 mol该物质最多可与2 mol NaHCO3反应
C
达标检测
5.下列物质中可以使蛋白质变性的是( )
①福尔马林 ②酒精 ③高锰酸钾溶液 ④硫酸铵溶液 ⑤硫酸铜 ⑥双氧水 ⑦硝酸
A.除④⑦外 B.除③⑥外
C.①②⑤ D.除④外
D
达标检测
C
6.下列关于蛋白质的叙述正确的是( )
A.加热能杀死流感病毒是因为病毒的蛋白质受热发生盐析
B.温度越高,对某些化学反应的催化效率越高
C.蛋白质水解的最终产物是氨基酸
D.任何结构的蛋白质遇到浓硝酸都会变成黄色
达标检测
A
7.下列关于酶的叙述中,不正确的是( )
A.酶是一种糖类物质
B.酶大多数是蛋白质
C.酶是生物体内产生的催化剂
D.酶受到高温或重金属盐作用时会变性
绝大多数酶是蛋白质,而不是糖类物质,具有蛋白质的性质,当受到高温或重金属盐作用时会变性;酶还是生物体内产生的高效催化剂,其催化作用具有条件温和、不需加热、高度专一、催化效率高等特点。
