第3章 微项目 青蒿素分子的结构测定——晶体在分子结构测定中的应用 学案(含答案) 2023-2024学年高二化学鲁科版(2019)选择性必修2
文档属性
| 名称 | 第3章 微项目 青蒿素分子的结构测定——晶体在分子结构测定中的应用 学案(含答案) 2023-2024学年高二化学鲁科版(2019)选择性必修2 |

|
|
| 格式 | docx | ||
| 文件大小 | 289.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-23 00:00:00 | ||
图片预览


文档简介
微项目:青蒿素分子的结构测定——晶体在分子结构测定中的应用
【学习目标】
1.了解测定分子结构的一般思路与方法,认识晶体对于分子结构测定的独特意义。
2.知道利用晶体X射线衍射能够测定原子坐标进而确定分子的空间结构,是测定分子结构的重要手段。
3.体会分子结构测定对于建立与优化物质结构理论模型,认识、解释和预测物质性质具有重要价值。
【自主预习】
1.测定分子结构及组成的方法
(1)质谱法:用电场和磁场将运动的离子(带电荷的原子、分子或分子碎片,有分子离子、同位素离子、碎片离子、重排离子、多电荷离子、亚稳离子、负离子和离子-分子相互作用产生的离子)按它们的质荷比分离后进行检测的方法。可以进行相对分子质量的测定、化学式的确定及结构鉴定等。
(2)红外光谱法:将分子吸收红外光的情况用仪器记录就得到该试样的红外吸收光谱图,利用光谱图中吸收峰的波长、强度和形状来判断分子中的基团,对分子进行结构分析。
(3)核磁共振谱法:NMR是研究原子核对射频辐射的吸收,它是对各种有机物和无机物的成分、结构进行定性分析的最强有力的工具之一,有时亦可进行定量分析。
(4)X射线衍射法:使用X射线探测某些分子或晶体结构的科研方法。
2.分子空间结构的测定程序
分析图像→测定晶胞参数→推算原子坐标→计算原子距离→判断化学键及其类型→确定分子结构
3.借助晶体X射线衍射测定分子结构的基本思路
【合作探究】
项目活动1 了解利用晶体测定分子结构的意义
情境导入 我国研究人员从1973年初开始测定青蒿素的组成与结构。首先,研究人员利用高分辨质谱仪测定出青蒿素的相对分子质量为282.33。结合元素分析,确定其分子式为C15H22O5。然后,研究人员经过一系列复杂的氧化还原反应实验,推测青蒿素具有含过氧基团的倍半萜内酯结构。红外光谱实验结果表明,青蒿素分子中确实含有酯基和过氧基团。结合核磁共振氢谱图提供的关于碳、氢原子的种类和数量的信息,研究人员推定了青蒿素中甲基、过氧基团、带有酯基的六元环等部分结构片段。然而,单纯依靠这些研究方法还不能精确判断青蒿素分子中所有碳原子和氧原子以何种方式连接形成骨架。1975年,研究人员采用晶体X射线衍射的方法,确定了青蒿素的分子结构。
问题生成
1.假设一个实验样品尺寸的数量级为10-4 m,原子直径的数量级为10-10 m,请估算这个实验样品中的原子数目。
【答案】晶胞一般是立方体,原子为球体,忽略原子间隙,则该样品中的原子数目约为=×1018≈2×1018。
2.上述材料中用到了哪些方法测定青蒿素分子的组成和结构 这些方法主要有什么用途
【答案】探究青蒿素分子组成和结构的过程中,科研人员使用的测定方法:
测定方法 获得的分子组成和结构的信息
质谱仪 测定出青蒿素的相对分子质量为282.33
元素分析 确定其分子式为C15H22O5
复杂的氧化还 原反应实验 推测青蒿素具有过氧基团的倍半萜结构
红外光谱 确实含有酯基和过氧基团
核磁共振谱图 推断出青蒿素中甲基、过氧基团、带有酯基的六元环等部分结构片段
晶体X射线衍射 推断所有碳原子和氧原子的连接方式,确定了青蒿素的分子结构
3.测定青蒿素分子中各原子空间排列方式时,科研人员遇到了什么困难 为什么用一般的方法无法精确地测定青蒿素的分子结构
【答案】不论是常规的化学实验方法,还是质谱、红外光谱等仪器测定的手段,都只能帮助我们了解分子的官能团等结构特点,并借此推测分子的结构,但对于所含原子数较多的分子来说,难以对其空间结构进行精确推测。
4.晶体的X射线衍射法对测定分子空间结构有什么重要意义
【答案】利用数学和物理知识对衍射所得图像进行复杂处理,可以测定晶体的晶胞参数,推算得到晶胞中所有原子的坐标,从而计算出原子间的距离,判断哪些原子间存在化学键以及化学键的类型,确定分子的空间结构。
【迁移应用】
1.下列可用于判断某物质为晶体的方法是( )。
A.质谱法 B.红外光谱法 C.核磁共振谱法 D.X射线衍射法
【答案】D
【解析】质谱法用于测定有机物的相对分子质量,不能判断某物质是否为晶体;红外光谱仪能测定出有机物的官能团和化学键,不能判断某物质是否为晶体;核磁共振氢谱法用于测定有机物分子中碳氢原子的种类和数目比,不能判断某物质是否为晶体;晶体与非晶体最本质的区别是组成物质的微粒在微观空间是否有序排列,X射线衍射可以测定微观结构,可以鉴别晶体与非晶体。
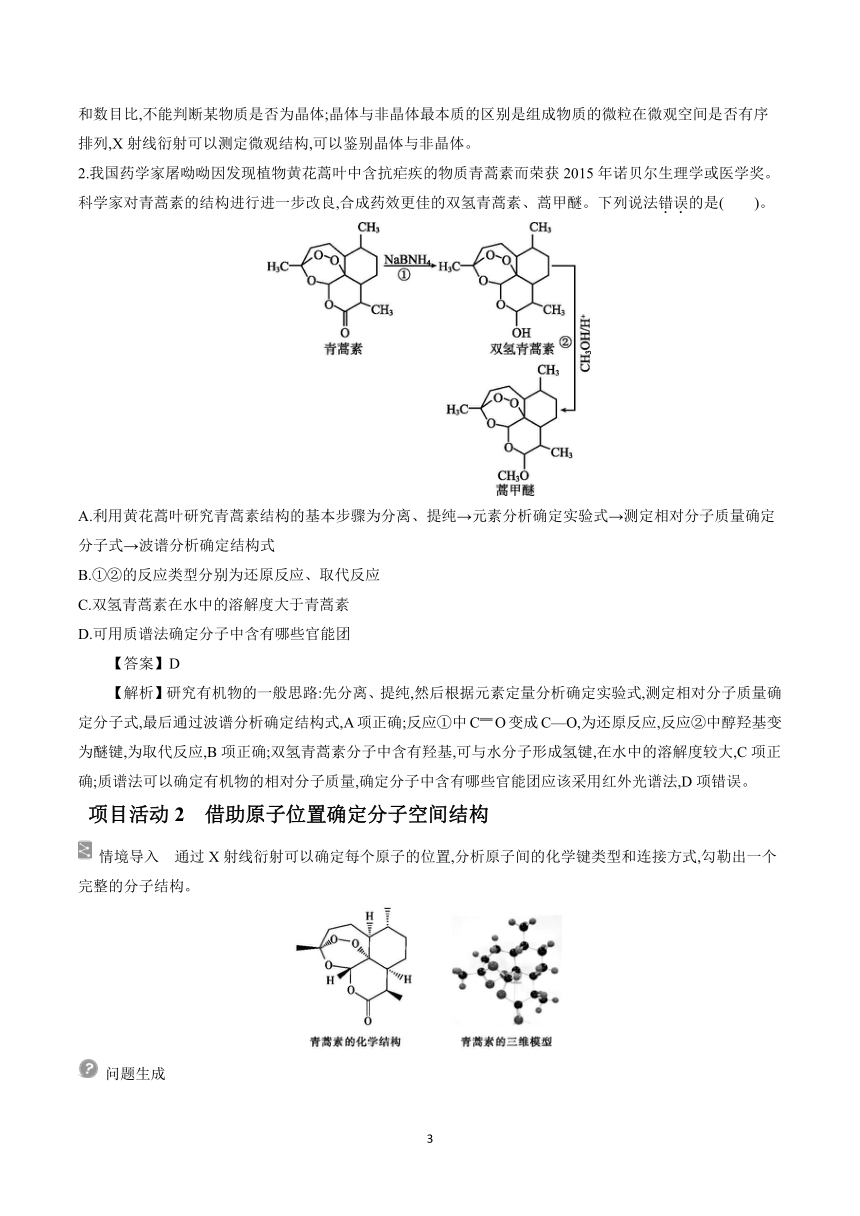
2.我国药学家屠呦呦因发现植物黄花蒿叶中含抗疟疾的物质青蒿素而荣获2015年诺贝尔生理学或医学奖。科学家对青蒿素的结构进行进一步改良,合成药效更佳的双氢青蒿素、蒿甲醚。下列说法错误的是( )。
A.利用黄花蒿叶研究青蒿素结构的基本步骤为分离、提纯→元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式
B.①②的反应类型分别为还原反应、取代反应
C.双氢青蒿素在水中的溶解度大于青蒿素
D.可用质谱法确定分子中含有哪些官能团
【答案】D
【解析】研究有机物的一般思路:先分离、提纯,然后根据元素定量分析确定实验式,测定相对分子质量确定分子式,最后通过波谱分析确定结构式,A项正确;反应①中CO变成C—O,为还原反应,反应②中醇羟基变为醚键,为取代反应,B项正确;双氢青蒿素分子中含有羟基,可与水分子形成氢键,在水中的溶解度较大,C项正确;质谱法可以确定有机物的相对分子质量,确定分子中含有哪些官能团应该采用红外光谱法,D项错误。
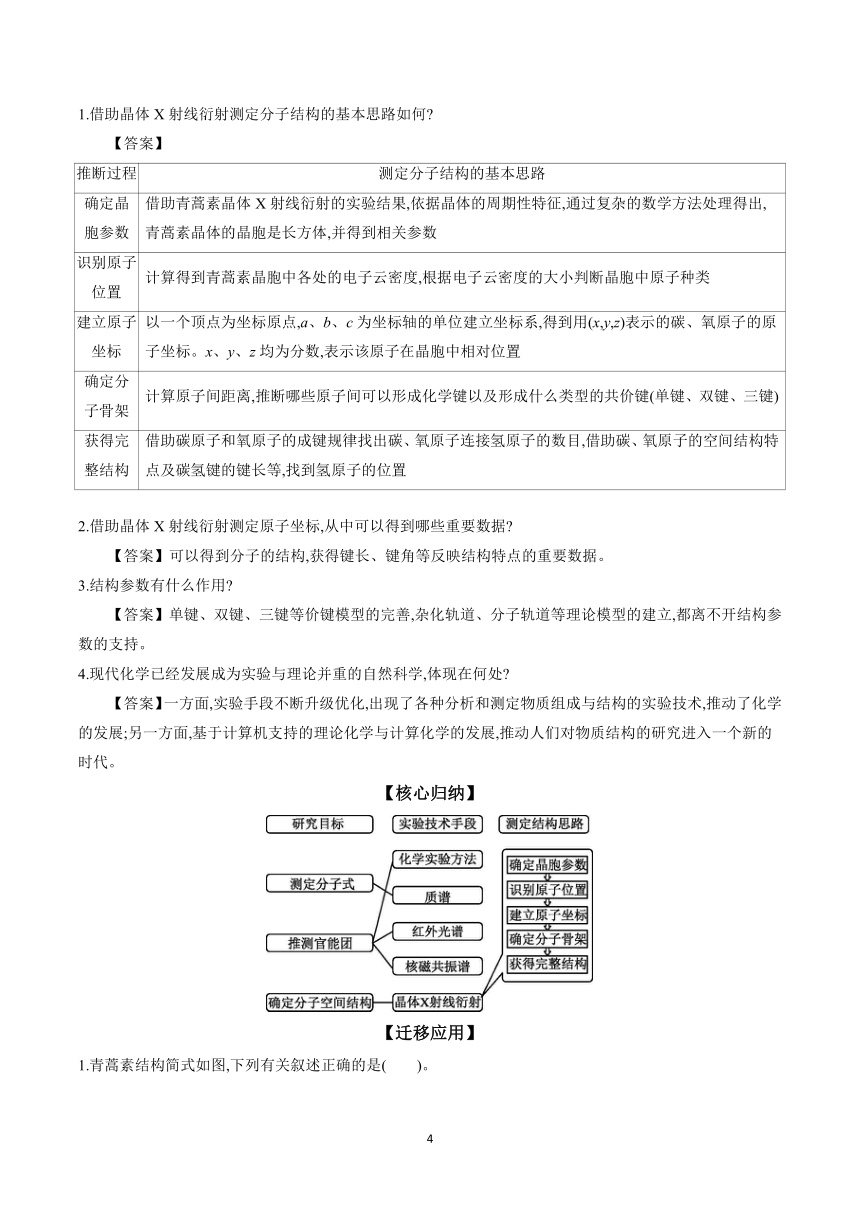
项目活动2 借助原子位置确定分子空间结构
情境导入 通过X射线衍射可以确定每个原子的位置,分析原子间的化学键类型和连接方式,勾勒出一个完整的分子结构。
问题生成
1.借助晶体X射线衍射测定分子结构的基本思路如何
【答案】
推断过程 测定分子结构的基本思路
确定晶 胞参数 借助青蒿素晶体X射线衍射的实验结果,依据晶体的周期性特征,通过复杂的数学方法处理得出,青蒿素晶体的晶胞是长方体,并得到相关参数
识别原子 位置 计算得到青蒿素晶胞中各处的电子云密度,根据电子云密度的大小判断晶胞中原子种类
建立原子 坐标 以一个顶点为坐标原点,a、b、c为坐标轴的单位建立坐标系,得到用(x,y,z)表示的碳、氧原子的原子坐标。x、y、z均为分数,表示该原子在晶胞中相对位置
确定分 子骨架 计算原子间距离,推断哪些原子间可以形成化学键以及形成什么类型的共价键(单键、双键、三键)
获得完 整结构 借助碳原子和氧原子的成键规律找出碳、氧原子连接氢原子的数目,借助碳、氧原子的空间结构特点及碳氢键的键长等,找到氢原子的位置
2.借助晶体X射线衍射测定原子坐标,从中可以得到哪些重要数据
【答案】可以得到分子的结构,获得键长、键角等反映结构特点的重要数据。
3.结构参数有什么作用
【答案】单键、双键、三键等价键模型的完善,杂化轨道、分子轨道等理论模型的建立,都离不开结构参数的支持。
4.现代化学已经发展成为实验与理论并重的自然科学,体现在何处
【答案】一方面,实验手段不断升级优化,出现了各种分析和测定物质组成与结构的实验技术,推动了化学的发展;另一方面,基于计算机支持的理论化学与计算化学的发展,推动人们对物质结构的研究进入一个新的时代。
【核心归纳】
【迁移应用】
1.青蒿素结构简式如图,下列有关叙述正确的是( )。
A.青蒿素极易溶于水
B.1 mol青蒿素与足量NaOH溶液反应最多消耗4 mol NaOH
C.青蒿素含有过氧键,有较强氧化性
D.青蒿素分子式为C15H21O5
【答案】C
【解析】根据青蒿素的结构简式可知,该有机物含有酯基、醚键,所以青蒿素难溶于水,易溶于有机溶剂,A项错误;该分子中含有一个酯基,所以1 mol青蒿素与足量NaOH溶液反应最多消耗1 mol NaOH,B项错误;青蒿素含有过氧键,有较强氧化性,C项正确;根据青蒿素的结构简式可知,青蒿素分子式为C15H22O5,D项错误。
2.某研究团队成功合成了能在室温稳定存在的五氮阴离子盐(N5)6(H3O)3(NH4)4Cl,经X射线衍射测得晶体结构,其局部结构如图所示(其中的立体结构是平面五元环)。下列说法正确的是( )。
A.所有N原子的价电子层均有孤电子对
B.氮氮键的键能:>H2N—NH2
C.两种阳离子是等电子体
D.阴、阳离子之间只存在离子键
【答案】B
【解析】N中N原子形成4个σ键,没有孤电子对,故A项错误;中氮原子间除形成σ键外,还形成一个大π键,氮氮键的键能:>H2N—NH2,故B项正确;H3O+和N原子总数不同,不是等电子体,故C项错误;由图可知,除阴、阳离子间形成离子键外,氯离子与铵根离子中H原子、H3O+中H原子与中N原子、N中H原子与中N原子形成氢键,故D项错误。
3.用晶体X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如图),已知该晶体的密度为9.00 g·cm-3,晶胞中该原子的配位数为 ;Cu的原子半径为 cm(阿伏加德罗常数为NA,列出计算表达式,不用化简)。
【答案】12 ×
【解析】根据该晶胞示意图,该晶胞为面心立方,配位数为12;设晶胞的棱长为a cm,则a3·ρ·NA=4×64,a=,面对角线为a cm,面对角线的为Cu原子半径r,r=×。
4.历史上对过氧化氢的分子结构有过不同观点,下图两种对结构的猜测中有一种正确,下列实验可以证明的是( )。
A.测定过氧化氢的沸点
B.测定过氧化氢分解时吸收的能量
C.测定过氧化氢分子中的氢氧键与氧氧键的键长
D.观察过氧化氢细液流在电场中是否发生偏转
【答案】D
【解析】题图所示两种结构,猜想1为对称结构非极性分子,猜想2为非对称结构极性分子,极性分子细液流在电场中发生偏转,观察过氧化氢细液流在电场中是否发生偏转,可确定猜测中有一种正确。
5.我国科学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。下列关于青蒿素和双氢青蒿素(结构如图)的说法错误的是( )。
A.青蒿素的分子式为C15H22O5
B.由青蒿素制备双氢青蒿素的反应属于还原反应
C.青蒿素分子中含有过氧键和酯基、醚键
D.双氢青蒿素分子中有2个六元环和2个七元环
【答案】D
【解析】由结构简式可知青蒿素的分子式为C15H22O5,故A项正确;青蒿素与氢气发生加成反应生成双氢青蒿素,属于还原反应,故B项正确;由结构简式可知青蒿素分子中含有过氧键和酯基、醚键,故C项正确;由结构可知,青蒿素和双氢青蒿素均含有3个六元环,故D项错误。
6.我国科学家屠呦呦因发现青蒿素(一种用于治疗疟疾的药物)而获得诺贝尔生理学或医学奖。青蒿素(C15H22O5)的结构如图所示。请回答下列问题:
(1)组成青蒿素的三种元素电负性由大到小的顺序是 ,基态O原子核外存在 对自旋方向相反的电子。
(2)下列关于青蒿素的说法正确的是 (填字母)。
a.青蒿素中既存在极性键又存在非极性键
b.在青蒿素分子中,所有碳原子均处于同一平面
c.图中数字标识的五个碳原子均只以σ键与其他原子相连
(3)在确定青蒿素结构的过程中,可采用NaBH4作为还原剂,其制备方法为4NaH+B(OCH3)3NaBH4+3CH3ONa。
①NaH为 晶体,NaH的晶胞结构如图,则NaH晶体的配位数是 ,若晶胞棱长为a,则Na原子间最小核间距为 。
②B(OCH3)3中B采用的杂化类型是 。写出两个与B(OCH3)3具有相同空间结构的分子或离子: 。
③NaBH4结构如图所示,结构中存在的作用力有 。
【答案】(1)O>C>H 3 (2)a (3)①离子 6 a ②sp2 SO3、C ③离子键、配位键、共价键
【解析】(1)组成青蒿素的三种元素为H、C、O,根据元素的非金属性越强,电负性越强可知,非金属性:O>C>H,则H、C、O三种元素的电负性由大到小的顺序是O>C>H;在基态O原子中,核外有8个电子,其中有3个轨道有成对电子,则核外存在3对自旋方向相反的电子。(2)青蒿素中O—O键、C—C键为非极性键,C—O键、C—H键为极性键,a项正确;含有饱和碳原子,具有烷烃的结构,则所有碳原子不处于同一平面,b项错误;CO键含有π键,c项错误。(3)①NaH为离子晶体,NaH晶体中每个Na周围有6个H,若晶胞棱长为a,则Na原子间最小核间距为a。②B(OCH3)3中B与3个O原子成键,为sp2杂化,B(OCH3)3的空间结构为平面三角形,与B(OCH3)3具有相同空间结构的分子或离子有SO3、C。③B原子核最外层有3个电子,NaBH4中存在离子键、配位键和共价键。
2
【学习目标】
1.了解测定分子结构的一般思路与方法,认识晶体对于分子结构测定的独特意义。
2.知道利用晶体X射线衍射能够测定原子坐标进而确定分子的空间结构,是测定分子结构的重要手段。
3.体会分子结构测定对于建立与优化物质结构理论模型,认识、解释和预测物质性质具有重要价值。
【自主预习】
1.测定分子结构及组成的方法
(1)质谱法:用电场和磁场将运动的离子(带电荷的原子、分子或分子碎片,有分子离子、同位素离子、碎片离子、重排离子、多电荷离子、亚稳离子、负离子和离子-分子相互作用产生的离子)按它们的质荷比分离后进行检测的方法。可以进行相对分子质量的测定、化学式的确定及结构鉴定等。
(2)红外光谱法:将分子吸收红外光的情况用仪器记录就得到该试样的红外吸收光谱图,利用光谱图中吸收峰的波长、强度和形状来判断分子中的基团,对分子进行结构分析。
(3)核磁共振谱法:NMR是研究原子核对射频辐射的吸收,它是对各种有机物和无机物的成分、结构进行定性分析的最强有力的工具之一,有时亦可进行定量分析。
(4)X射线衍射法:使用X射线探测某些分子或晶体结构的科研方法。
2.分子空间结构的测定程序
分析图像→测定晶胞参数→推算原子坐标→计算原子距离→判断化学键及其类型→确定分子结构
3.借助晶体X射线衍射测定分子结构的基本思路
【合作探究】
项目活动1 了解利用晶体测定分子结构的意义
情境导入 我国研究人员从1973年初开始测定青蒿素的组成与结构。首先,研究人员利用高分辨质谱仪测定出青蒿素的相对分子质量为282.33。结合元素分析,确定其分子式为C15H22O5。然后,研究人员经过一系列复杂的氧化还原反应实验,推测青蒿素具有含过氧基团的倍半萜内酯结构。红外光谱实验结果表明,青蒿素分子中确实含有酯基和过氧基团。结合核磁共振氢谱图提供的关于碳、氢原子的种类和数量的信息,研究人员推定了青蒿素中甲基、过氧基团、带有酯基的六元环等部分结构片段。然而,单纯依靠这些研究方法还不能精确判断青蒿素分子中所有碳原子和氧原子以何种方式连接形成骨架。1975年,研究人员采用晶体X射线衍射的方法,确定了青蒿素的分子结构。
问题生成
1.假设一个实验样品尺寸的数量级为10-4 m,原子直径的数量级为10-10 m,请估算这个实验样品中的原子数目。
【答案】晶胞一般是立方体,原子为球体,忽略原子间隙,则该样品中的原子数目约为=×1018≈2×1018。
2.上述材料中用到了哪些方法测定青蒿素分子的组成和结构 这些方法主要有什么用途
【答案】探究青蒿素分子组成和结构的过程中,科研人员使用的测定方法:
测定方法 获得的分子组成和结构的信息
质谱仪 测定出青蒿素的相对分子质量为282.33
元素分析 确定其分子式为C15H22O5
复杂的氧化还 原反应实验 推测青蒿素具有过氧基团的倍半萜结构
红外光谱 确实含有酯基和过氧基团
核磁共振谱图 推断出青蒿素中甲基、过氧基团、带有酯基的六元环等部分结构片段
晶体X射线衍射 推断所有碳原子和氧原子的连接方式,确定了青蒿素的分子结构
3.测定青蒿素分子中各原子空间排列方式时,科研人员遇到了什么困难 为什么用一般的方法无法精确地测定青蒿素的分子结构
【答案】不论是常规的化学实验方法,还是质谱、红外光谱等仪器测定的手段,都只能帮助我们了解分子的官能团等结构特点,并借此推测分子的结构,但对于所含原子数较多的分子来说,难以对其空间结构进行精确推测。
4.晶体的X射线衍射法对测定分子空间结构有什么重要意义
【答案】利用数学和物理知识对衍射所得图像进行复杂处理,可以测定晶体的晶胞参数,推算得到晶胞中所有原子的坐标,从而计算出原子间的距离,判断哪些原子间存在化学键以及化学键的类型,确定分子的空间结构。
【迁移应用】
1.下列可用于判断某物质为晶体的方法是( )。
A.质谱法 B.红外光谱法 C.核磁共振谱法 D.X射线衍射法
【答案】D
【解析】质谱法用于测定有机物的相对分子质量,不能判断某物质是否为晶体;红外光谱仪能测定出有机物的官能团和化学键,不能判断某物质是否为晶体;核磁共振氢谱法用于测定有机物分子中碳氢原子的种类和数目比,不能判断某物质是否为晶体;晶体与非晶体最本质的区别是组成物质的微粒在微观空间是否有序排列,X射线衍射可以测定微观结构,可以鉴别晶体与非晶体。
2.我国药学家屠呦呦因发现植物黄花蒿叶中含抗疟疾的物质青蒿素而荣获2015年诺贝尔生理学或医学奖。科学家对青蒿素的结构进行进一步改良,合成药效更佳的双氢青蒿素、蒿甲醚。下列说法错误的是( )。
A.利用黄花蒿叶研究青蒿素结构的基本步骤为分离、提纯→元素分析确定实验式→测定相对分子质量确定分子式→波谱分析确定结构式
B.①②的反应类型分别为还原反应、取代反应
C.双氢青蒿素在水中的溶解度大于青蒿素
D.可用质谱法确定分子中含有哪些官能团
【答案】D
【解析】研究有机物的一般思路:先分离、提纯,然后根据元素定量分析确定实验式,测定相对分子质量确定分子式,最后通过波谱分析确定结构式,A项正确;反应①中CO变成C—O,为还原反应,反应②中醇羟基变为醚键,为取代反应,B项正确;双氢青蒿素分子中含有羟基,可与水分子形成氢键,在水中的溶解度较大,C项正确;质谱法可以确定有机物的相对分子质量,确定分子中含有哪些官能团应该采用红外光谱法,D项错误。
项目活动2 借助原子位置确定分子空间结构
情境导入 通过X射线衍射可以确定每个原子的位置,分析原子间的化学键类型和连接方式,勾勒出一个完整的分子结构。
问题生成
1.借助晶体X射线衍射测定分子结构的基本思路如何
【答案】
推断过程 测定分子结构的基本思路
确定晶 胞参数 借助青蒿素晶体X射线衍射的实验结果,依据晶体的周期性特征,通过复杂的数学方法处理得出,青蒿素晶体的晶胞是长方体,并得到相关参数
识别原子 位置 计算得到青蒿素晶胞中各处的电子云密度,根据电子云密度的大小判断晶胞中原子种类
建立原子 坐标 以一个顶点为坐标原点,a、b、c为坐标轴的单位建立坐标系,得到用(x,y,z)表示的碳、氧原子的原子坐标。x、y、z均为分数,表示该原子在晶胞中相对位置
确定分 子骨架 计算原子间距离,推断哪些原子间可以形成化学键以及形成什么类型的共价键(单键、双键、三键)
获得完 整结构 借助碳原子和氧原子的成键规律找出碳、氧原子连接氢原子的数目,借助碳、氧原子的空间结构特点及碳氢键的键长等,找到氢原子的位置
2.借助晶体X射线衍射测定原子坐标,从中可以得到哪些重要数据
【答案】可以得到分子的结构,获得键长、键角等反映结构特点的重要数据。
3.结构参数有什么作用
【答案】单键、双键、三键等价键模型的完善,杂化轨道、分子轨道等理论模型的建立,都离不开结构参数的支持。
4.现代化学已经发展成为实验与理论并重的自然科学,体现在何处
【答案】一方面,实验手段不断升级优化,出现了各种分析和测定物质组成与结构的实验技术,推动了化学的发展;另一方面,基于计算机支持的理论化学与计算化学的发展,推动人们对物质结构的研究进入一个新的时代。
【核心归纳】
【迁移应用】
1.青蒿素结构简式如图,下列有关叙述正确的是( )。
A.青蒿素极易溶于水
B.1 mol青蒿素与足量NaOH溶液反应最多消耗4 mol NaOH
C.青蒿素含有过氧键,有较强氧化性
D.青蒿素分子式为C15H21O5
【答案】C
【解析】根据青蒿素的结构简式可知,该有机物含有酯基、醚键,所以青蒿素难溶于水,易溶于有机溶剂,A项错误;该分子中含有一个酯基,所以1 mol青蒿素与足量NaOH溶液反应最多消耗1 mol NaOH,B项错误;青蒿素含有过氧键,有较强氧化性,C项正确;根据青蒿素的结构简式可知,青蒿素分子式为C15H22O5,D项错误。
2.某研究团队成功合成了能在室温稳定存在的五氮阴离子盐(N5)6(H3O)3(NH4)4Cl,经X射线衍射测得晶体结构,其局部结构如图所示(其中的立体结构是平面五元环)。下列说法正确的是( )。
A.所有N原子的价电子层均有孤电子对
B.氮氮键的键能:>H2N—NH2
C.两种阳离子是等电子体
D.阴、阳离子之间只存在离子键
【答案】B
【解析】N中N原子形成4个σ键,没有孤电子对,故A项错误;中氮原子间除形成σ键外,还形成一个大π键,氮氮键的键能:>H2N—NH2,故B项正确;H3O+和N原子总数不同,不是等电子体,故C项错误;由图可知,除阴、阳离子间形成离子键外,氯离子与铵根离子中H原子、H3O+中H原子与中N原子、N中H原子与中N原子形成氢键,故D项错误。
3.用晶体X射线衍射法对Cu的测定得到以下结果:Cu的晶胞为面心立方最密堆积(如图),已知该晶体的密度为9.00 g·cm-3,晶胞中该原子的配位数为 ;Cu的原子半径为 cm(阿伏加德罗常数为NA,列出计算表达式,不用化简)。
【答案】12 ×
【解析】根据该晶胞示意图,该晶胞为面心立方,配位数为12;设晶胞的棱长为a cm,则a3·ρ·NA=4×64,a=,面对角线为a cm,面对角线的为Cu原子半径r,r=×。
4.历史上对过氧化氢的分子结构有过不同观点,下图两种对结构的猜测中有一种正确,下列实验可以证明的是( )。
A.测定过氧化氢的沸点
B.测定过氧化氢分解时吸收的能量
C.测定过氧化氢分子中的氢氧键与氧氧键的键长
D.观察过氧化氢细液流在电场中是否发生偏转
【答案】D
【解析】题图所示两种结构,猜想1为对称结构非极性分子,猜想2为非对称结构极性分子,极性分子细液流在电场中发生偏转,观察过氧化氢细液流在电场中是否发生偏转,可确定猜测中有一种正确。
5.我国科学家屠呦呦因创制新型抗疟药青蒿素和双氢青蒿素而获得2015年诺贝尔生理学或医学奖。下列关于青蒿素和双氢青蒿素(结构如图)的说法错误的是( )。
A.青蒿素的分子式为C15H22O5
B.由青蒿素制备双氢青蒿素的反应属于还原反应
C.青蒿素分子中含有过氧键和酯基、醚键
D.双氢青蒿素分子中有2个六元环和2个七元环
【答案】D
【解析】由结构简式可知青蒿素的分子式为C15H22O5,故A项正确;青蒿素与氢气发生加成反应生成双氢青蒿素,属于还原反应,故B项正确;由结构简式可知青蒿素分子中含有过氧键和酯基、醚键,故C项正确;由结构可知,青蒿素和双氢青蒿素均含有3个六元环,故D项错误。
6.我国科学家屠呦呦因发现青蒿素(一种用于治疗疟疾的药物)而获得诺贝尔生理学或医学奖。青蒿素(C15H22O5)的结构如图所示。请回答下列问题:
(1)组成青蒿素的三种元素电负性由大到小的顺序是 ,基态O原子核外存在 对自旋方向相反的电子。
(2)下列关于青蒿素的说法正确的是 (填字母)。
a.青蒿素中既存在极性键又存在非极性键
b.在青蒿素分子中,所有碳原子均处于同一平面
c.图中数字标识的五个碳原子均只以σ键与其他原子相连
(3)在确定青蒿素结构的过程中,可采用NaBH4作为还原剂,其制备方法为4NaH+B(OCH3)3NaBH4+3CH3ONa。
①NaH为 晶体,NaH的晶胞结构如图,则NaH晶体的配位数是 ,若晶胞棱长为a,则Na原子间最小核间距为 。
②B(OCH3)3中B采用的杂化类型是 。写出两个与B(OCH3)3具有相同空间结构的分子或离子: 。
③NaBH4结构如图所示,结构中存在的作用力有 。
【答案】(1)O>C>H 3 (2)a (3)①离子 6 a ②sp2 SO3、C ③离子键、配位键、共价键
【解析】(1)组成青蒿素的三种元素为H、C、O,根据元素的非金属性越强,电负性越强可知,非金属性:O>C>H,则H、C、O三种元素的电负性由大到小的顺序是O>C>H;在基态O原子中,核外有8个电子,其中有3个轨道有成对电子,则核外存在3对自旋方向相反的电子。(2)青蒿素中O—O键、C—C键为非极性键,C—O键、C—H键为极性键,a项正确;含有饱和碳原子,具有烷烃的结构,则所有碳原子不处于同一平面,b项错误;CO键含有π键,c项错误。(3)①NaH为离子晶体,NaH晶体中每个Na周围有6个H,若晶胞棱长为a,则Na原子间最小核间距为a。②B(OCH3)3中B与3个O原子成键,为sp2杂化,B(OCH3)3的空间结构为平面三角形,与B(OCH3)3具有相同空间结构的分子或离子有SO3、C。③B原子核最外层有3个电子,NaBH4中存在离子键、配位键和共价键。
2
