3.2 课时1 化石燃料 乙烯 学案(含答案) 2023-2024学年高一化学鲁科版(2019)必修第二册
文档属性
| 名称 | 3.2 课时1 化石燃料 乙烯 学案(含答案) 2023-2024学年高一化学鲁科版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 328.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-06 00:00:00 | ||
图片预览



文档简介
3.2 课时1 化石燃料 乙烯
【学习目标】
1.了解天然气和煤的组成。
2.了解石油的组成,学习如何从石油中获取燃料,了解石油的炼制方法。
3.能从有机化合物及其性质的角度对有关能源、材料、饮食、健康、环境等实际问题进行分析、讨论和评价。
4.从乙烯的结构与性质的关系及实验探究,构建“结构与性质”的关系模型,培养“证据推理与模型认知”的学科素养。
【自主预习】
一、从天然气、石油和煤中获取燃料
1.化石燃料
(1)含义:又叫作 、 ,包括 ,属于 能源。
(2)现存问题:
①化石燃料存在着逐渐枯竭的危机;
②引起的环境问题:如温室效应、有毒气体和粉尘污染等。
2.天然气和煤直接用作燃料
(1)天然气
①主要成分: 。
②甲烷的物理性质
颜色 状态 气味 密度 水溶性
无色 无味 比空气
③用途:a.优良的气体燃料,CH4燃烧的化学方程式: 。
b.化工原料,如CH4可与Cl2发生取代反应制取多种卤代烃。
【微点拨】
沼气、坑道气(瓦斯)、天然气水合物(可燃冰)的主要成分是甲烷。
(2)煤
①成分: 和 组成的复杂混合物。含有 、 、氧、氮、硫等元素。
②用途:a.燃料,但直接烧煤会产生一些大气污染物,如 、氮的氧化物、烟尘等。
b.提取化工原料。
3.从石油中获取燃料和化工原料
(1)石油的成分:石油是由分子含有不同数目碳原子的 、 等组成的复杂混合物。通常, 、 在石油中的质量分数之和高达98%。
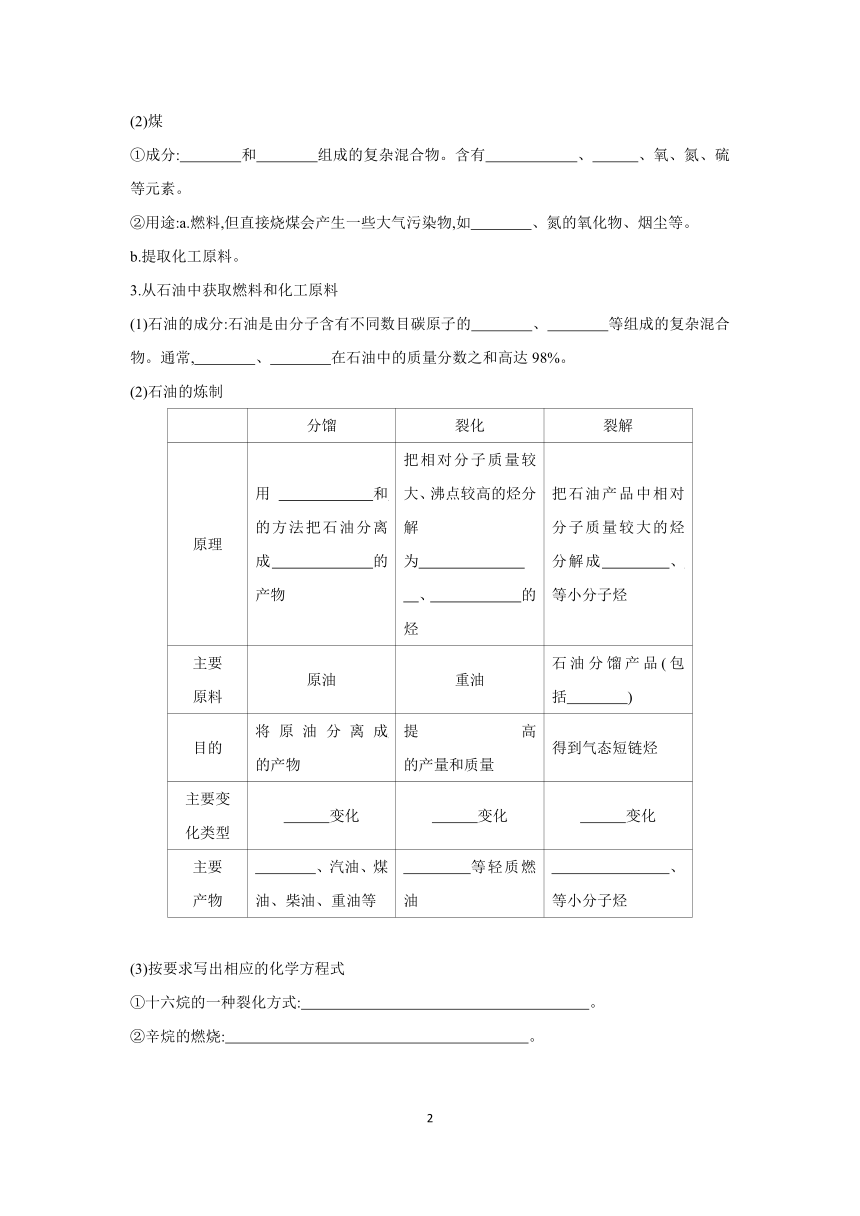
(2)石油的炼制
分馏 裂化 裂解
原理 用 和 的方法把石油分离成 的产物 把相对分子质量较大、沸点较高的烃分解为 、 的烃 把石油产品中相对分子质量较大的烃分解成 、 等小分子烃
主要 原料 原油 重油 石油分馏产品(包括 )
目的 将原油分离成 的产物 提高 的产量和质量 得到气态短链烃
主要变 化类型 变化 变化 变化
主要 产物 、汽油、煤油、柴油、重油等 等轻质燃油 、 等小分子烃
(3)按要求写出相应的化学方程式
①十六烷的一种裂化方式: 。
②辛烷的燃烧: 。
二、乙烯
1.物理性质
颜色 气味 状态 密度 水溶性
无色 稍有气味 气体 比空气 难溶于水
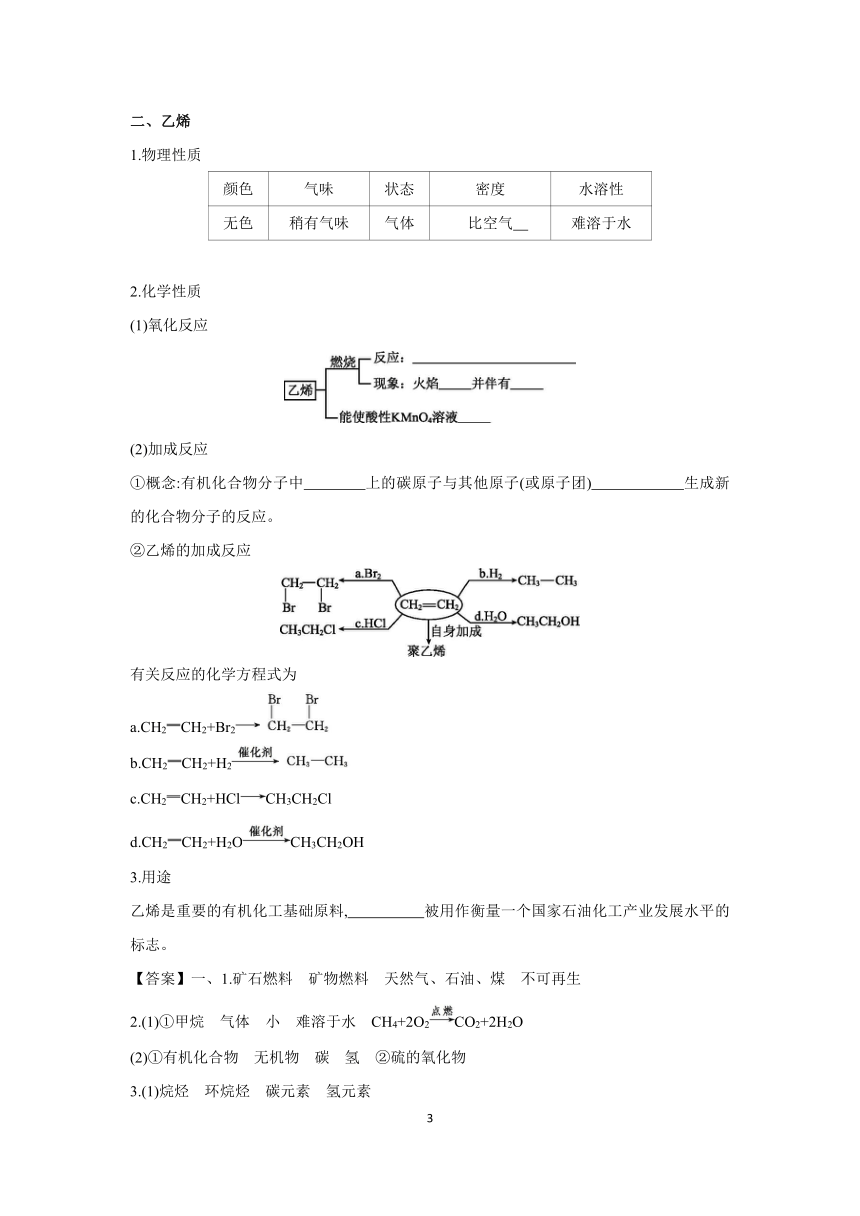
2.化学性质
(1)氧化反应
(2)加成反应
①概念:有机化合物分子中 上的碳原子与其他原子(或原子团) 生成新的化合物分子的反应。
②乙烯的加成反应
有关反应的化学方程式为
a.CH2CH2+Br2
b.CH2CH2+H2
c.CH2CH2+HClCH3CH2Cl
d.CH2CH2+H2OCH3CH2OH
3.用途
乙烯是重要的有机化工基础原料, 被用作衡量一个国家石油化工产业发展水平的标志。
【答案】一、1.矿石燃料 矿物燃料 天然气、石油、煤 不可再生
2.(1)①甲烷 气体 小 难溶于水 CH4+2O2CO2+2H2O
(2)①有机化合物 无机物 碳 氢 ②硫的氧化物
3.(1)烷烃 环烷烃 碳元素 氢元素
(2)加热 冷凝 沸点范围不同 相对分子质量较小 沸点较低 乙烯 丙烯 石油气 不同沸点范围 轻质液体燃料 物理 化学 化学 石油气 汽油 乙烯 丙烯
(3)C16H34C8H18+C8H16
十六烷 辛烷 辛烯
2C8H18+25O216CO2+18H2O
二、1.小
2.(1)C2H4+3O22CO2+2H2O 明亮 黑烟 褪色 (2)①双键 直接结合
3.乙烯的产量
【效果检测】
1.判断正误(正确的打“√”,错误的打“×”)
(1)石油、煤、天然气、可燃冰、植物油都属于化石燃料。 ( )
(2)石油的分馏是化学变化。 ( )
(3)石油裂化的目的是得到气态短链烃。 ( )
(4)乙烯完全燃烧生成水和二氧化碳的物质的量相等。 ( )
(5)乙烯可与HCl发生加成反应。 ( )
(6)裂化可以提高汽油等轻质油的产量和质量。 ( )
(7)裂化汽油不能用于萃取溴水中的溴单质。 ( )
(8)工业上可通过石油分馏直接得到甲烷、乙烯和苯。 ( )
(9)用溴的四氯化碳溶液可鉴别分馏获得的汽油和裂化获得的汽油。 ( )
(10)汽油为石油分馏产品,属于纯净物。 ( )
(11)十六烷的一种裂化方式为C16H34C8H18+C8H16。 ( )
(12)石油经直接分馏后获得的直馏汽油不可使溴水褪色,石油的分馏属于物理变化。 ( )
【答案】(1)× (2)× (3)× (4)√ (5)√ (6)√
(7)√ (8)× (9)√ (10)× (11)√ (12)√
2.乙烯和乙烷分子的空间结构差异在哪里
【答案】乙烯分子为平面结构,乙烷分子为立体结构。
3.已知:破坏1 mol化学键形成气态原子所吸收的最低能量叫键能。乙烯分子中碳碳双键的键能为610 kJ·mol-1,乙烷分子中碳碳单键的键能为345.6 kJ·mol-1,试分析碳碳双键中的两个键是否完全相同,推测乙烯和乙烷的化学性质是否相似。
【答案】碳碳双键中的一个键比碳碳单键的键能小,即碳碳双键中的一个键容易断裂,乙烯的化学性质更活泼。
【合作探究】
任务1 从天然气、石油和煤中获取燃料
情境导入 迄今为止,煤、石油和天然气仍是人类使用的主要能源,同时它们也是重要的化工原料。如何实现化石燃料的综合利用,提高利用率,减少化石燃料燃烧所造成的环境污染,是人类面临的重大挑战。
问题生成
1.石油是纯净物还是混合物
【答案】混合物。
2.石油的成分是不是全部为有机化合物
【答案】不是。
3.石油通过分馏、裂化、裂解所得到的产品是纯净物吗
【答案】不是。石油通过分馏、裂化、裂解得到的产物均是混合物。
4.石油的裂化和裂解有什么关系 其目的分别是什么
【答案】裂解是深度裂化。裂化的目的是获取更多的轻质液体燃料,裂解的目的是得到乙烯、丙烯等小分子烃。
5.直馏汽油和裂化汽油的主要化学成分有什么区别 怎样鉴别它们
【答案】直馏汽油中是C5~C11的烷烃及少量芳香烃,性质稳定,而裂化汽油含有C5~C11的烷烃和烯烃,性质活泼。其中能使溴的四氯化碳溶液褪色的是裂化汽油。
【核心归纳】
1.石油炼制的工艺流程简图
2.直馏汽油和裂化汽油的区别
获得方法 主要化学成分 鉴别方法
直馏 汽油 原油直接分馏,物理变化 一般是C5~C11的烷烃及少量的芳香烃(以后会学到)等,性质稳定 能使溴的四氯化碳溶液褪色的是裂化汽油
裂化 汽油 重油裂化,化学变化 含有C5~C11的烷烃和烯烃,性质活泼
【特别提醒】
有关石油炼制的三点说明
(1)外界压强越小,物质的沸点就越低,减压蒸馏可降低馏分的沸点,有机物在较低温度下就可以沸腾,从而得到高沸点馏分。一方面可降低生产成本,另一方面可降低常压分馏中发生炭化的可能性。
(2)石油的裂化和裂解均属于烷烃的分解反应,且裂解就是深度裂化,采用的温度比裂化的温度更高。
(3)烷烃的分解反应中生成烯烃,因此裂化汽油的成分中含有烯烃,能使溴水或溴的四氯化碳溶液褪色。
【典型例题】
【例1】 石油分馏塔的示意图如下。下列说法正确的是( )。
A.a的沸点最高
B.b的熔点最低
C.c的平均相对分子质量最大
D.每一种馏分都是纯净物
【答案】C
【解析】分馏塔内的温度从下往上逐渐降低。石油蒸气从分馏塔的底部进入,沸点低的馏分先汽化,冷凝后流出,沸点高的馏分后汽化,冷凝后流出,因此a、b、c的沸点依次升高。沸点高的物质熔点高、相对分子质量大。石油中有些成分的沸点很接近,因此石油分馏的馏分仍为混合物。
【例2】 实验室用下列仪器组装一套石油分馏的装置,并进行相关实验,可以得到汽油和煤油。
(1)写出下列仪器的名称:
① ;② ;③ 。
(2)将以上仪器按从左到右的顺序进行连接:e→ → → → → → → → → 。(用字母表示)
(3)仪器②中A是 (填“进水口”或“出水口”,下同),B是 。
(4)蒸馏时,温度计水银球应在 。
(5)在①中注入原油后,加几片碎瓷片的目的是 。
【答案】(1)蒸馏烧瓶 冷凝管 锥形瓶
(2)c d a k l b f g w
(3)进水口 出水口
(4)蒸馏烧瓶支管口处
(5)防止暴沸
【解析】(1)蒸馏需要的仪器有酒精灯、蒸馏烧瓶、铁架台、温度计、导管、冷凝管、橡胶管、牛角管、锥形瓶,根据常见仪器的名称可知,①为蒸馏烧瓶,②为冷凝管,③为锥形瓶。(2)按组装仪器顺序从左到右,从下到上,该装置为蒸馏石油的装置,冷凝管在中间,并用铁架台固定冷凝管,右边为锥形瓶,故连接顺序为e→c→d→a→k→l→b→f→g→w。(3)冷凝水应是下进上出,延长热量交换时间,即A口用于进水,B口用于出水。(4)蒸馏装置的温度计插在蒸馏烧瓶中且水银球在支管口处。(5)为防止烧瓶内液体受热不均匀而局部突然沸腾(暴沸)冲出烧瓶,需要在烧瓶内加入几块沸石(或碎瓷片)。
任务2 乙烯的结构与性质
情境导入
我们几乎每天都可以看到水果,一般水果在成熟的季节,会由青色逐渐变为红色或黄色。如果把青橘子和熟苹果放在同一个塑料袋里,系紧袋口,一段时间后青橘子就可以变黄、变熟。这是谁的功劳 乙烯被称为“石化工业之母”,是石油化学工业重要的基本原料之一,通过一系列化学反应,乙烯通过加工可得到有机高分子材料、药物等成千上万种有用的物质。乙烯的产量可以用来衡量一个国家石油化学工业的发展水平。那么,乙烯主要有哪些性质呢
问题生成
1.乙烯分子的球棍模型为,请推测出乙烯的空间结构。
【答案】根据乙烯分子的球棍模型,可推测出乙烯分子的空间结构为平面结构,即乙烯分子中的2个碳原子和4个氢原子处于同一个平面上。
2.乙烯既能使酸性高锰酸钾溶液褪色,又可使溴水褪色,二者原理是否相同
【答案】不相同。乙烯使酸性高锰酸钾溶液褪色,发生的是氧化还原反应;而乙烯使溴水褪色,发生的是加成反应。
3.如何区分乙烷和乙烯 乙烷中有乙烯如何除去
【答案】乙烯能使酸性KMnO4溶液或溴水褪色,由此可区别甲烷(烷烃)和乙烯(烯烃)。另外根据乙烯分子中含碳量大,燃烧火焰明亮,并伴有黑烟,而乙烷燃烧产生淡蓝色火焰也可以区别。乙烯被酸性KMnO4溶液氧化的产物是CO2,因此C2H6中混有乙烯时,不能用酸性高锰酸钾溶液除去(引入新的杂质),应用溴水洗气除去。
4.能否用溴的四氯化碳溶液除去乙烷中的乙烯
【答案】不能。除去乙烷中的乙烯时,一般使用溴水,不能用溴的四氯化碳溶液,因为乙烷不溶于水,但易溶于四氯化碳等有机溶剂。
5.乙烷与Cl2的取代反应和乙烯与HCl的加成反应都能制得氯乙烷,哪种方法更好
【答案】乙烯与HCl的加成反应制取氯乙烷更好,因为乙烷与Cl2发生的是连续取代反应,反应产物是多种氯代物的混合物,得不到纯净的氯乙烷;乙烯与HCl发生的加成反应没有副反应,可制得较纯净的氯乙烷。
【核心归纳】
1.乙烷和乙烯的结构与性质的比较
物质 乙烷 乙烯
结构式
碳碳键的类别 碳碳单键 碳碳双键
分子内各原子的相对位置 C、H不全在一个平面内 6个原子全在一个平面内
相同点(都能燃烧) 2C2H6+7O24CO2+6H2O C2H4+3O22CO2+2H2O
特征性质 C2H6+Cl2C2H5Cl+HCl CH2CH2+Br2CH2BrCH2Br
酸性KMnO4 不褪色 褪色
溴水 不褪色 褪色
2.加成反应与取代反应的比较
类型 取代反应 加成反应
反应物 结构特征 含有易被取代的原子或原子团 不饱和有机化合物(含等)
生成物 两种(一般是一种有机化合物和一种无机物) 一种(有机化合物)
碳碳键 变化情况 无变化 打开变为
常用试剂 卤素单质气体 H2、X2、HX、H2O
结构变化 形式举例 等价替换式 CH3CH3+Cl2CH3CH2Cl+HCl 开键加合式 CH2CH2+H2O CH3CH2OH CH2CH2+HX CH3CH2X
【典型例题】
【例3】 既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中混有的少量乙烯的最佳方法是( )。
A.混合气体通过盛水的洗气瓶
B.混合气体通过装有过量溴水的洗气瓶
C.混合气体和过量H2混合
D.混合气体通过酸性KMnO4溶液
【答案】B
【解析】水既不能鉴别也不能除去乙烷中的乙烯;利用H2不能鉴别乙烯和乙烷,乙烯与氢气在一定条件下反应生成乙烷,但H2的量不好控制;酸性KMnO4溶液可用于鉴别乙烷和乙烯,但不能用于除去乙烷中的乙烯,因为酸性KMnO4会将乙烯氧化生成CO2,引入新的杂质;溴水与乙烷不反应,与乙烯可发生加成反应而褪色,既可以鉴别乙烯和乙烷,又可以除去乙烷中的乙烯。
【例4】 某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷发生反应:C16H34C8H18+甲,甲4乙,乙的结构简式为 。
(2)B装置中乙发生反应的化学方程式为 。
(3)C装置中可观察到的现象是 ,
反应类型是 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。本实验中能证明这一点的实验现象是 。
(5)乙与氢气的加成产物与一定量的氯气混合后在光照条件下反应,反应产物最多有 种。
【答案】(1)CH2CH2
(2)CH2CH2+Br2BrCH2CH2Br
(3)溶液紫红色褪去 氧化反应
(4)D装置中的澄清石灰水变浑浊
(5)10
【解析】(1)C16H34C8H18+甲,根据原子守恒,甲的分子式为C8H16,依据反应方程式C8H164乙,结合原子守恒可知,乙的分子式为C2H4,为乙烯,结构简式为CH2CH2。
(2)乙烯含有碳碳双键,能够与溴水发生加成反应而使溴水褪色,反应的化学方程式为CH2CH2+Br2CH2BrCH2Br。
(3)乙烯具有还原性,能够被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色。
(4)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙反应生成碳酸钙沉淀,因此装置D中的澄清石灰水变浑浊,可以证明乙烯与酸性高锰酸钾溶液反应产生了二氧化碳。
(5)乙烯与氢气的加成产物为乙烷,乙烷中含有6个氢原子,与Cl2发生取代反应生成的有机物有一氯乙烷(1种)、二氯乙烷(2种)、三氯乙烷(2种)、四氯乙烷(2种)、五氯乙烷(1种)、六氯乙烷(1种),还有氯化氢,最多有10种生成物。
【随堂检测】
1.《汉书》记载“高奴(县)有洧水,可燃”;《梦溪笔谈》描述“洧水”:“予疑其烟可用,试扫其煤以为墨,黑光如漆,松墨不及也……此物后必大行于世。”上述“洧水”和“煤”的主要成分分别是( )。
A.石油和炭黑 B.石油和焦炭 C.油脂和木炭 D.油脂和石墨
【答案】A
【解析】根据“洧水”“可燃”“大行于世”,可知“洧水”是生产生活中重要的燃料,应是石油;“煤”指石油不完全燃烧产生的烟灰,根据“黑光如漆”“松墨不及”,可知“煤”应为炭黑,“洧水”和“煤”的主要成分分别是石油和炭黑。
2.石油在国民经济中的地位和作用十分重要,被誉为“黑色的金子”“工业的血液”等。下列关于石油及其应用的说法正确的是( )。
A.液化石油气的主要成分是甲烷
B.石油主要含有碳、氢两种元素
C.石油的裂化是物理变化
D.石油分馏的各馏分均是纯净物
【答案】B
【解析】液化石油气的主要成分是丙烷和丁烷,不是甲烷,A项错误;石油主要含有碳、氢两种元素,同时还含有少量的硫、氧、氮等元素,B项正确;石油裂化生成了新物质,属于化学变化,C项错误;石油分馏的各馏分均主要是沸点相近的几种烃的混合物,不是纯净物,D项错误。
3.石油裂解的主要目的是( )。
A.提高轻质液体燃料的产量
B.便于分馏
C.获得短链不饱和气态烃
D.提高汽油的质量
【答案】C
4.下列反应属于裂解反应的是( )。
A.+
B.2C8H18+25O216CO2+18H2O
C.C4H10C2H4+C2H6
D.+Cl—Cl+H—Cl
【答案】C
【解析】A项属于裂化反应,B项属于氧化反应,D项属于取代反应。
5.柠檬烯具有良好的镇咳、祛痰、抑菌作用,其键线式如图所示。下列关于柠檬烯的说法正确的是( )。
A.1 mol柠檬烯只能与1 mol H2反应
B.能发生取代反应和加成反应
C.属于乙烯的同系物
D.不能使酸性高锰酸钾溶液褪色
【答案】B
【解析】A项,1 mol柠檬烯能与2 mol H2发生加成反应,错误;B项,柠檬烯能与气态卤素单质在光照条件下发生取代反应,分子中含有碳碳双键,能发生加成反应,正确;C项,一个柠檬烯分子中有两个碳碳双键,且分子中含有环状结构,与乙烯的结构不相同,故其不属于乙烯的同系物,错误;D项,柠檬烯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色,错误。
6.利用如图所示的实验装置进行实验。
(1)装置中碎瓷片的作用是 ,矿渣棉的作用是 。
(2)请设计实验证明所得气体生成物中含有不饱和气态烃: 。
【答案】(1)作催化剂 作为石蜡油的载体
(2)将所得气体通入酸性高锰酸钾溶液或溴水中,若观察到溶液褪色,则说明所得气体中含有气态不饱和烃
【解析】(1)根据上述分析可知,装置中碎瓷片起到了催化剂的作用,矿渣棉用作石蜡油的载体。(2)因为石蜡油主要含碳、氢元素,经过裂化反应能生成气态不饱和烃,如乙烯或丙烯等。这些气态不饱和烃能使酸性高锰酸钾溶液褪色,也可以和溴水发生加成反应,所以可以将所得气体通入酸性高锰酸钾溶液或溴水中,若观察到溶液褪色,则说明所得气体中含有气态不饱和烃。
2
【学习目标】
1.了解天然气和煤的组成。
2.了解石油的组成,学习如何从石油中获取燃料,了解石油的炼制方法。
3.能从有机化合物及其性质的角度对有关能源、材料、饮食、健康、环境等实际问题进行分析、讨论和评价。
4.从乙烯的结构与性质的关系及实验探究,构建“结构与性质”的关系模型,培养“证据推理与模型认知”的学科素养。
【自主预习】
一、从天然气、石油和煤中获取燃料
1.化石燃料
(1)含义:又叫作 、 ,包括 ,属于 能源。
(2)现存问题:
①化石燃料存在着逐渐枯竭的危机;
②引起的环境问题:如温室效应、有毒气体和粉尘污染等。
2.天然气和煤直接用作燃料
(1)天然气
①主要成分: 。
②甲烷的物理性质
颜色 状态 气味 密度 水溶性
无色 无味 比空气
③用途:a.优良的气体燃料,CH4燃烧的化学方程式: 。
b.化工原料,如CH4可与Cl2发生取代反应制取多种卤代烃。
【微点拨】
沼气、坑道气(瓦斯)、天然气水合物(可燃冰)的主要成分是甲烷。
(2)煤
①成分: 和 组成的复杂混合物。含有 、 、氧、氮、硫等元素。
②用途:a.燃料,但直接烧煤会产生一些大气污染物,如 、氮的氧化物、烟尘等。
b.提取化工原料。
3.从石油中获取燃料和化工原料
(1)石油的成分:石油是由分子含有不同数目碳原子的 、 等组成的复杂混合物。通常, 、 在石油中的质量分数之和高达98%。
(2)石油的炼制
分馏 裂化 裂解
原理 用 和 的方法把石油分离成 的产物 把相对分子质量较大、沸点较高的烃分解为 、 的烃 把石油产品中相对分子质量较大的烃分解成 、 等小分子烃
主要 原料 原油 重油 石油分馏产品(包括 )
目的 将原油分离成 的产物 提高 的产量和质量 得到气态短链烃
主要变 化类型 变化 变化 变化
主要 产物 、汽油、煤油、柴油、重油等 等轻质燃油 、 等小分子烃
(3)按要求写出相应的化学方程式
①十六烷的一种裂化方式: 。
②辛烷的燃烧: 。
二、乙烯
1.物理性质
颜色 气味 状态 密度 水溶性
无色 稍有气味 气体 比空气 难溶于水
2.化学性质
(1)氧化反应
(2)加成反应
①概念:有机化合物分子中 上的碳原子与其他原子(或原子团) 生成新的化合物分子的反应。
②乙烯的加成反应
有关反应的化学方程式为
a.CH2CH2+Br2
b.CH2CH2+H2
c.CH2CH2+HClCH3CH2Cl
d.CH2CH2+H2OCH3CH2OH
3.用途
乙烯是重要的有机化工基础原料, 被用作衡量一个国家石油化工产业发展水平的标志。
【答案】一、1.矿石燃料 矿物燃料 天然气、石油、煤 不可再生
2.(1)①甲烷 气体 小 难溶于水 CH4+2O2CO2+2H2O
(2)①有机化合物 无机物 碳 氢 ②硫的氧化物
3.(1)烷烃 环烷烃 碳元素 氢元素
(2)加热 冷凝 沸点范围不同 相对分子质量较小 沸点较低 乙烯 丙烯 石油气 不同沸点范围 轻质液体燃料 物理 化学 化学 石油气 汽油 乙烯 丙烯
(3)C16H34C8H18+C8H16
十六烷 辛烷 辛烯
2C8H18+25O216CO2+18H2O
二、1.小
2.(1)C2H4+3O22CO2+2H2O 明亮 黑烟 褪色 (2)①双键 直接结合
3.乙烯的产量
【效果检测】
1.判断正误(正确的打“√”,错误的打“×”)
(1)石油、煤、天然气、可燃冰、植物油都属于化石燃料。 ( )
(2)石油的分馏是化学变化。 ( )
(3)石油裂化的目的是得到气态短链烃。 ( )
(4)乙烯完全燃烧生成水和二氧化碳的物质的量相等。 ( )
(5)乙烯可与HCl发生加成反应。 ( )
(6)裂化可以提高汽油等轻质油的产量和质量。 ( )
(7)裂化汽油不能用于萃取溴水中的溴单质。 ( )
(8)工业上可通过石油分馏直接得到甲烷、乙烯和苯。 ( )
(9)用溴的四氯化碳溶液可鉴别分馏获得的汽油和裂化获得的汽油。 ( )
(10)汽油为石油分馏产品,属于纯净物。 ( )
(11)十六烷的一种裂化方式为C16H34C8H18+C8H16。 ( )
(12)石油经直接分馏后获得的直馏汽油不可使溴水褪色,石油的分馏属于物理变化。 ( )
【答案】(1)× (2)× (3)× (4)√ (5)√ (6)√
(7)√ (8)× (9)√ (10)× (11)√ (12)√
2.乙烯和乙烷分子的空间结构差异在哪里
【答案】乙烯分子为平面结构,乙烷分子为立体结构。
3.已知:破坏1 mol化学键形成气态原子所吸收的最低能量叫键能。乙烯分子中碳碳双键的键能为610 kJ·mol-1,乙烷分子中碳碳单键的键能为345.6 kJ·mol-1,试分析碳碳双键中的两个键是否完全相同,推测乙烯和乙烷的化学性质是否相似。
【答案】碳碳双键中的一个键比碳碳单键的键能小,即碳碳双键中的一个键容易断裂,乙烯的化学性质更活泼。
【合作探究】
任务1 从天然气、石油和煤中获取燃料
情境导入 迄今为止,煤、石油和天然气仍是人类使用的主要能源,同时它们也是重要的化工原料。如何实现化石燃料的综合利用,提高利用率,减少化石燃料燃烧所造成的环境污染,是人类面临的重大挑战。
问题生成
1.石油是纯净物还是混合物
【答案】混合物。
2.石油的成分是不是全部为有机化合物
【答案】不是。
3.石油通过分馏、裂化、裂解所得到的产品是纯净物吗
【答案】不是。石油通过分馏、裂化、裂解得到的产物均是混合物。
4.石油的裂化和裂解有什么关系 其目的分别是什么
【答案】裂解是深度裂化。裂化的目的是获取更多的轻质液体燃料,裂解的目的是得到乙烯、丙烯等小分子烃。
5.直馏汽油和裂化汽油的主要化学成分有什么区别 怎样鉴别它们
【答案】直馏汽油中是C5~C11的烷烃及少量芳香烃,性质稳定,而裂化汽油含有C5~C11的烷烃和烯烃,性质活泼。其中能使溴的四氯化碳溶液褪色的是裂化汽油。
【核心归纳】
1.石油炼制的工艺流程简图
2.直馏汽油和裂化汽油的区别
获得方法 主要化学成分 鉴别方法
直馏 汽油 原油直接分馏,物理变化 一般是C5~C11的烷烃及少量的芳香烃(以后会学到)等,性质稳定 能使溴的四氯化碳溶液褪色的是裂化汽油
裂化 汽油 重油裂化,化学变化 含有C5~C11的烷烃和烯烃,性质活泼
【特别提醒】
有关石油炼制的三点说明
(1)外界压强越小,物质的沸点就越低,减压蒸馏可降低馏分的沸点,有机物在较低温度下就可以沸腾,从而得到高沸点馏分。一方面可降低生产成本,另一方面可降低常压分馏中发生炭化的可能性。
(2)石油的裂化和裂解均属于烷烃的分解反应,且裂解就是深度裂化,采用的温度比裂化的温度更高。
(3)烷烃的分解反应中生成烯烃,因此裂化汽油的成分中含有烯烃,能使溴水或溴的四氯化碳溶液褪色。
【典型例题】
【例1】 石油分馏塔的示意图如下。下列说法正确的是( )。
A.a的沸点最高
B.b的熔点最低
C.c的平均相对分子质量最大
D.每一种馏分都是纯净物
【答案】C
【解析】分馏塔内的温度从下往上逐渐降低。石油蒸气从分馏塔的底部进入,沸点低的馏分先汽化,冷凝后流出,沸点高的馏分后汽化,冷凝后流出,因此a、b、c的沸点依次升高。沸点高的物质熔点高、相对分子质量大。石油中有些成分的沸点很接近,因此石油分馏的馏分仍为混合物。
【例2】 实验室用下列仪器组装一套石油分馏的装置,并进行相关实验,可以得到汽油和煤油。
(1)写出下列仪器的名称:
① ;② ;③ 。
(2)将以上仪器按从左到右的顺序进行连接:e→ → → → → → → → → 。(用字母表示)
(3)仪器②中A是 (填“进水口”或“出水口”,下同),B是 。
(4)蒸馏时,温度计水银球应在 。
(5)在①中注入原油后,加几片碎瓷片的目的是 。
【答案】(1)蒸馏烧瓶 冷凝管 锥形瓶
(2)c d a k l b f g w
(3)进水口 出水口
(4)蒸馏烧瓶支管口处
(5)防止暴沸
【解析】(1)蒸馏需要的仪器有酒精灯、蒸馏烧瓶、铁架台、温度计、导管、冷凝管、橡胶管、牛角管、锥形瓶,根据常见仪器的名称可知,①为蒸馏烧瓶,②为冷凝管,③为锥形瓶。(2)按组装仪器顺序从左到右,从下到上,该装置为蒸馏石油的装置,冷凝管在中间,并用铁架台固定冷凝管,右边为锥形瓶,故连接顺序为e→c→d→a→k→l→b→f→g→w。(3)冷凝水应是下进上出,延长热量交换时间,即A口用于进水,B口用于出水。(4)蒸馏装置的温度计插在蒸馏烧瓶中且水银球在支管口处。(5)为防止烧瓶内液体受热不均匀而局部突然沸腾(暴沸)冲出烧瓶,需要在烧瓶内加入几块沸石(或碎瓷片)。
任务2 乙烯的结构与性质
情境导入
我们几乎每天都可以看到水果,一般水果在成熟的季节,会由青色逐渐变为红色或黄色。如果把青橘子和熟苹果放在同一个塑料袋里,系紧袋口,一段时间后青橘子就可以变黄、变熟。这是谁的功劳 乙烯被称为“石化工业之母”,是石油化学工业重要的基本原料之一,通过一系列化学反应,乙烯通过加工可得到有机高分子材料、药物等成千上万种有用的物质。乙烯的产量可以用来衡量一个国家石油化学工业的发展水平。那么,乙烯主要有哪些性质呢
问题生成
1.乙烯分子的球棍模型为,请推测出乙烯的空间结构。
【答案】根据乙烯分子的球棍模型,可推测出乙烯分子的空间结构为平面结构,即乙烯分子中的2个碳原子和4个氢原子处于同一个平面上。
2.乙烯既能使酸性高锰酸钾溶液褪色,又可使溴水褪色,二者原理是否相同
【答案】不相同。乙烯使酸性高锰酸钾溶液褪色,发生的是氧化还原反应;而乙烯使溴水褪色,发生的是加成反应。
3.如何区分乙烷和乙烯 乙烷中有乙烯如何除去
【答案】乙烯能使酸性KMnO4溶液或溴水褪色,由此可区别甲烷(烷烃)和乙烯(烯烃)。另外根据乙烯分子中含碳量大,燃烧火焰明亮,并伴有黑烟,而乙烷燃烧产生淡蓝色火焰也可以区别。乙烯被酸性KMnO4溶液氧化的产物是CO2,因此C2H6中混有乙烯时,不能用酸性高锰酸钾溶液除去(引入新的杂质),应用溴水洗气除去。
4.能否用溴的四氯化碳溶液除去乙烷中的乙烯
【答案】不能。除去乙烷中的乙烯时,一般使用溴水,不能用溴的四氯化碳溶液,因为乙烷不溶于水,但易溶于四氯化碳等有机溶剂。
5.乙烷与Cl2的取代反应和乙烯与HCl的加成反应都能制得氯乙烷,哪种方法更好
【答案】乙烯与HCl的加成反应制取氯乙烷更好,因为乙烷与Cl2发生的是连续取代反应,反应产物是多种氯代物的混合物,得不到纯净的氯乙烷;乙烯与HCl发生的加成反应没有副反应,可制得较纯净的氯乙烷。
【核心归纳】
1.乙烷和乙烯的结构与性质的比较
物质 乙烷 乙烯
结构式
碳碳键的类别 碳碳单键 碳碳双键
分子内各原子的相对位置 C、H不全在一个平面内 6个原子全在一个平面内
相同点(都能燃烧) 2C2H6+7O24CO2+6H2O C2H4+3O22CO2+2H2O
特征性质 C2H6+Cl2C2H5Cl+HCl CH2CH2+Br2CH2BrCH2Br
酸性KMnO4 不褪色 褪色
溴水 不褪色 褪色
2.加成反应与取代反应的比较
类型 取代反应 加成反应
反应物 结构特征 含有易被取代的原子或原子团 不饱和有机化合物(含等)
生成物 两种(一般是一种有机化合物和一种无机物) 一种(有机化合物)
碳碳键 变化情况 无变化 打开变为
常用试剂 卤素单质气体 H2、X2、HX、H2O
结构变化 形式举例 等价替换式 CH3CH3+Cl2CH3CH2Cl+HCl 开键加合式 CH2CH2+H2O CH3CH2OH CH2CH2+HX CH3CH2X
【典型例题】
【例3】 既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中混有的少量乙烯的最佳方法是( )。
A.混合气体通过盛水的洗气瓶
B.混合气体通过装有过量溴水的洗气瓶
C.混合气体和过量H2混合
D.混合气体通过酸性KMnO4溶液
【答案】B
【解析】水既不能鉴别也不能除去乙烷中的乙烯;利用H2不能鉴别乙烯和乙烷,乙烯与氢气在一定条件下反应生成乙烷,但H2的量不好控制;酸性KMnO4溶液可用于鉴别乙烷和乙烯,但不能用于除去乙烷中的乙烯,因为酸性KMnO4会将乙烯氧化生成CO2,引入新的杂质;溴水与乙烷不反应,与乙烯可发生加成反应而褪色,既可以鉴别乙烯和乙烷,又可以除去乙烷中的乙烯。
【例4】 某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:
(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷发生反应:C16H34C8H18+甲,甲4乙,乙的结构简式为 。
(2)B装置中乙发生反应的化学方程式为 。
(3)C装置中可观察到的现象是 ,
反应类型是 。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。本实验中能证明这一点的实验现象是 。
(5)乙与氢气的加成产物与一定量的氯气混合后在光照条件下反应,反应产物最多有 种。
【答案】(1)CH2CH2
(2)CH2CH2+Br2BrCH2CH2Br
(3)溶液紫红色褪去 氧化反应
(4)D装置中的澄清石灰水变浑浊
(5)10
【解析】(1)C16H34C8H18+甲,根据原子守恒,甲的分子式为C8H16,依据反应方程式C8H164乙,结合原子守恒可知,乙的分子式为C2H4,为乙烯,结构简式为CH2CH2。
(2)乙烯含有碳碳双键,能够与溴水发生加成反应而使溴水褪色,反应的化学方程式为CH2CH2+Br2CH2BrCH2Br。
(3)乙烯具有还原性,能够被酸性高锰酸钾溶液氧化而使高锰酸钾溶液褪色。
(4)乙烯与酸性高锰酸钾溶液反应产生二氧化碳,二氧化碳能够与氢氧化钙反应生成碳酸钙沉淀,因此装置D中的澄清石灰水变浑浊,可以证明乙烯与酸性高锰酸钾溶液反应产生了二氧化碳。
(5)乙烯与氢气的加成产物为乙烷,乙烷中含有6个氢原子,与Cl2发生取代反应生成的有机物有一氯乙烷(1种)、二氯乙烷(2种)、三氯乙烷(2种)、四氯乙烷(2种)、五氯乙烷(1种)、六氯乙烷(1种),还有氯化氢,最多有10种生成物。
【随堂检测】
1.《汉书》记载“高奴(县)有洧水,可燃”;《梦溪笔谈》描述“洧水”:“予疑其烟可用,试扫其煤以为墨,黑光如漆,松墨不及也……此物后必大行于世。”上述“洧水”和“煤”的主要成分分别是( )。
A.石油和炭黑 B.石油和焦炭 C.油脂和木炭 D.油脂和石墨
【答案】A
【解析】根据“洧水”“可燃”“大行于世”,可知“洧水”是生产生活中重要的燃料,应是石油;“煤”指石油不完全燃烧产生的烟灰,根据“黑光如漆”“松墨不及”,可知“煤”应为炭黑,“洧水”和“煤”的主要成分分别是石油和炭黑。
2.石油在国民经济中的地位和作用十分重要,被誉为“黑色的金子”“工业的血液”等。下列关于石油及其应用的说法正确的是( )。
A.液化石油气的主要成分是甲烷
B.石油主要含有碳、氢两种元素
C.石油的裂化是物理变化
D.石油分馏的各馏分均是纯净物
【答案】B
【解析】液化石油气的主要成分是丙烷和丁烷,不是甲烷,A项错误;石油主要含有碳、氢两种元素,同时还含有少量的硫、氧、氮等元素,B项正确;石油裂化生成了新物质,属于化学变化,C项错误;石油分馏的各馏分均主要是沸点相近的几种烃的混合物,不是纯净物,D项错误。
3.石油裂解的主要目的是( )。
A.提高轻质液体燃料的产量
B.便于分馏
C.获得短链不饱和气态烃
D.提高汽油的质量
【答案】C
4.下列反应属于裂解反应的是( )。
A.+
B.2C8H18+25O216CO2+18H2O
C.C4H10C2H4+C2H6
D.+Cl—Cl+H—Cl
【答案】C
【解析】A项属于裂化反应,B项属于氧化反应,D项属于取代反应。
5.柠檬烯具有良好的镇咳、祛痰、抑菌作用,其键线式如图所示。下列关于柠檬烯的说法正确的是( )。
A.1 mol柠檬烯只能与1 mol H2反应
B.能发生取代反应和加成反应
C.属于乙烯的同系物
D.不能使酸性高锰酸钾溶液褪色
【答案】B
【解析】A项,1 mol柠檬烯能与2 mol H2发生加成反应,错误;B项,柠檬烯能与气态卤素单质在光照条件下发生取代反应,分子中含有碳碳双键,能发生加成反应,正确;C项,一个柠檬烯分子中有两个碳碳双键,且分子中含有环状结构,与乙烯的结构不相同,故其不属于乙烯的同系物,错误;D项,柠檬烯分子中含有碳碳双键,能使酸性高锰酸钾溶液褪色,错误。
6.利用如图所示的实验装置进行实验。
(1)装置中碎瓷片的作用是 ,矿渣棉的作用是 。
(2)请设计实验证明所得气体生成物中含有不饱和气态烃: 。
【答案】(1)作催化剂 作为石蜡油的载体
(2)将所得气体通入酸性高锰酸钾溶液或溴水中,若观察到溶液褪色,则说明所得气体中含有气态不饱和烃
【解析】(1)根据上述分析可知,装置中碎瓷片起到了催化剂的作用,矿渣棉用作石蜡油的载体。(2)因为石蜡油主要含碳、氢元素,经过裂化反应能生成气态不饱和烃,如乙烯或丙烯等。这些气态不饱和烃能使酸性高锰酸钾溶液褪色,也可以和溴水发生加成反应,所以可以将所得气体通入酸性高锰酸钾溶液或溴水中,若观察到溶液褪色,则说明所得气体中含有气态不饱和烃。
2
