化学人教版(2019)必修第一册1.1.1物质的分类(共40张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.1物质的分类(共40张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-07 00:00:00 | ||
图片预览









文档简介
(共40张PPT)
第1节 物质的分类及其转化
第一章 物质及其变化
(1)物质的分类
超市里有成千上万种商品,
怎样能够迅速挑出你所需要的东西
??
在日常生活中我们还会在什么地方用到分类的方法呢?
图书馆
超市
查字典
药房
分类是提高效率的一种重要手段
创原家独
新知导入
美国《化学文摘》编辑部统计,已知的有机化合物的数目:
1880年约为1.2万种,
1910年约1.5万种,
1940年约为50万种,
1961年约为175万种,
1990年已超过1 000万种,
2004年,达到3 500万种以上。
要想对各物质物有条不紊地进行研究,就必须对物质分类。
1.分类的方法
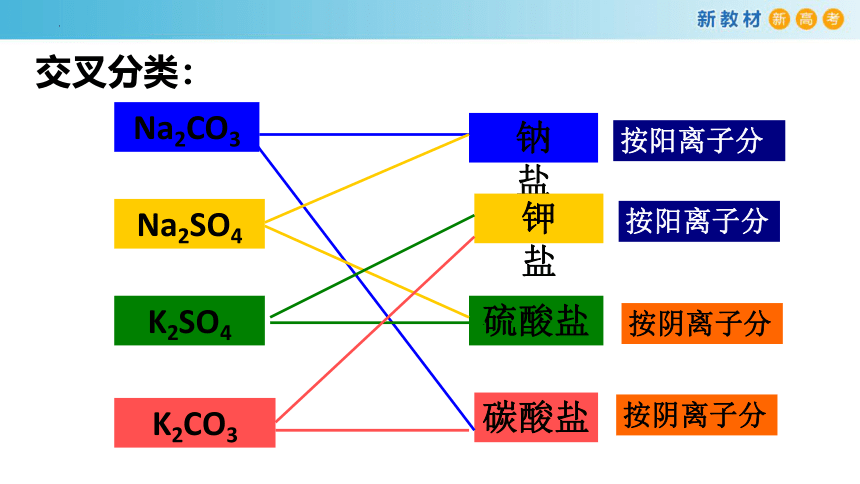
(1)交叉分类法
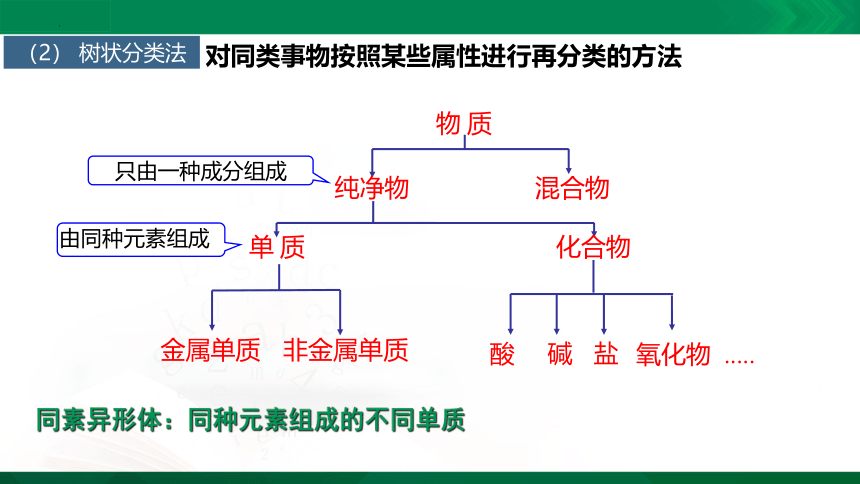
(2)树状分类法
分类
交叉分类:
Na2CO3
Na2SO4
K2SO4
K2CO3
钠 盐
钾 盐
硫酸盐
碳酸盐
按阳离子分
按阳离子分
按阴离子分
按阴离子分
学
物 质
只由一种成分组成
纯净物
混合物
由同种元素组成
单 质
化合物
金属单质
非金属单质
酸
碱
盐
氧化物 .....
对同类事物按照某些属性进行再分类的方法
(2) 树状分类法
同素异形体:同种元素组成的不同单质
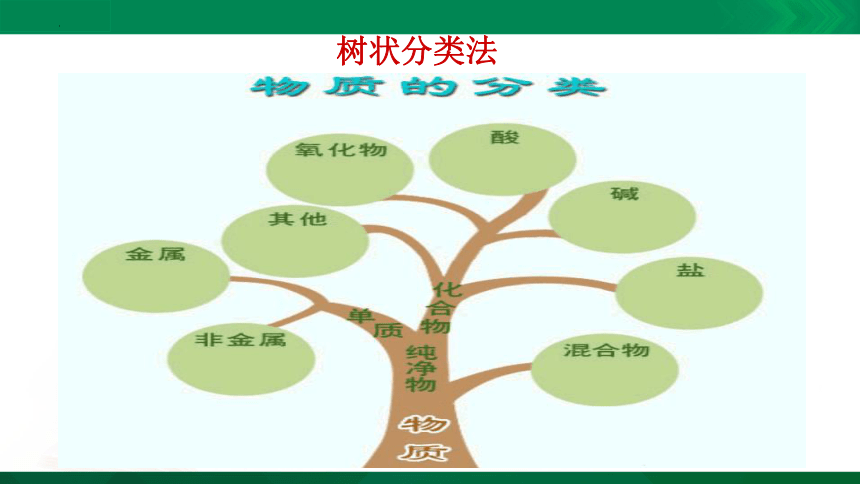
树状分类法
物质
纯净物
金属单质
非金属单质
化合物
酸
碱
盐
氧化物
单质
混合物
实践活动:选择下列合适的物质写在物质分类的下边:O2、Cu、He、H2SO4、Ba(OH)2、KNO3、CO2、 MgO 、空气、盐酸
稀有气体单质
Cu
O2
He
H2SO4
Ba(OH)2
KNO3
CO2、 MgO
空气、盐酸
2.酸的分类
按是否含氧
酸
按提供氢离子数目
一元酸:
二元酸:
多元酸:
含氧酸、 无氧酸
HNO3
HCl
HNO3、HCl
H2SO4
能提供一个H+的酸
能提供多个H+的酸
H3PO4
阳离子全部是氢离子(H+)的化合物
按酸性强弱
强酸
HCl、H2SO4、HNO3
CH3COOH、H2CO3
能提供两个H+的酸
中强酸
H3PO4、H2SO3
弱酸
1.按其在水溶液中是否溶解:
(1)可溶性碱:
(2)难溶性碱:
KOH NaOH Ba(OH)2 Ca(OH)2
Cu(OH)2 Fe(OH)3 Mg(OH)2 Zn(OH)2
3.碱的分类
2.按碱性强弱
强碱:NaOH KOH Ba(OH)2 Ca(OH)2
弱碱:NH3· H2O 、难溶性碱
阴离子全部是氢氧根离子( OH- )的化合物
K+ Na+ NH4+ NO3-
(2)按是否可溶于水:
可溶性盐:
难溶性盐:
AgCl BaSO4 CaCO3
(1) 按阴、阳离子来分:
常见阳离子:
常见阴离子:
K+ Na+ NH4+ Ag+ Cu2+ Ca2+
NO3- SO42- Cl- CO32- HCO3- PO43-
由金属阳离子(或NH4+)和酸根离子构成的化合物
4.盐的分类
(3)组成中是否有可电离的H+、OH-
正盐
酸式盐
碱式盐
Na2CO3
NaHCO3
Cu2(OH)2CO3
复盐:由两种或两种以上金属阳离子(或NH4+)和一种酸根离子构成的盐。
能电离出H+的盐
能电离出OH-的盐
不能电离出H+和OH-的盐
如KAl(SO4)2、(NH4)2Fe(SO4)2
同素异形体:同种元素形成的性质不同的单质
初中化学的学习中,同学们学习了很多的单质,其中有一些单质是由同种元素形成的,例如:金刚石和石墨都是由碳元素形成的。在化学上,我们将这样的单质命名为同素异形体。
科
【练一练】下列每组中的两种物质之间的关系为同素异形体的一组是( )
A.CaO和CaS B. 和
C.C60和C70 D.HCNO和HOCN
C
氧化物分类:
按组成分为金属氧化物和非金属氧化物
按性质分为酸性氧化物和碱性氧化物
与碱反应只生成盐和水
与酸反应只生成盐和水
(1)金属氧化物都是碱性氧化物
(2)非金属氧化物都是酸性氧化物
(3)碱性氧化物都是(3)碱性氧化物都是金属氧化物
(4)酸性氧化物都是非金属氧化物
Mn2O7是酸性氧化物
CO不是酸性氧化物也不是碱性氧化物
正确
Mn2O7是酸性氧化物
由氧元素与另外一种元素组成的二元化合物
氧化物
按组成分
按性质分
金属氧化物
非金属氧化物
酸性氧化物
碱性氧化物
( SO2、CO2 、Mn2O7)
( Na2O、CaO、BaO)
( SO2、CO2 、CO、NO2)
( Na2O、CaO)
能与碱反应,只生成对应的盐和水
能与酸反应,只生成对应的盐和水
5.氧化物的分类
不成盐氧化物
( CO、NO、NO2)
不与酸、碱、水反应
不能得到对应的盐
金属氧化物
碱性氧化物
非金属氧化物
酸性氧化物
只有碱性氧化物都是金属氧化物
1. 下列各组物质中均为纯净物的是( )
A. 生石灰,熟石灰,烧碱溶液
B. 明矾,硫磺,矿泉水
C. 乙醇,干冰,冰水混合物
D. 玻璃,盐酸,沼气
2. 下列各组概念中,后者属于前者范围的是( )
A. 化合物,单质 B. 金属,单质
C. 混合物,纯净物 D. 纯净物,化合物
C
D
课堂练习
物质/分类 碱 酸 盐 碱性氧化物 酸性氧化物
A Na2CO3 H2SO4 NaOH SO2 CO2
B NaOH HCl NaCl Na2O CO
C NaOH CH3COOH CaCl2 CO SO2
D KOH HNO3 CaCO3 CaO SO3
3、下列物质分类正确的组合是( )
D
4.分类是化学学习与研究的常用方法,下列分类正确的是( )
A.Na2O、MgO、CO均属于碱性氧化物
B.烧碱、生石灰、纯碱均属于碱
C.酸、碱、盐之间发生的反应均属于复分解反应
D.SO2、CO2 、BaO、SO3均属于酸性氧化物
C
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
混合物还可以再分类吗?
二、分散系及其分类
二、分散系及其分类
1、定义:
2、分类标准:按照分散质粒子直径的大小
溶液:小于1nm
浊液:大于100nm
胶体:1-100nm之间
分散系:把一种(或多种)物质分散在另一种(或多种)物质
中所得到的体系。
分散质:被分散的物质。
分散剂:起容纳分散质的作用。
一种液体以小液滴的形式分散在另外一种液体之中形成的分散系叫乳浊液。
固体小颗粒悬浮于液体里形成的分散系。
悬浊液:
乳浊液:
浊液
一般规律:
1.分散系中有水,水是分散剂;
2.分散系中是两种液体(没有水),量多的是分散剂。
分散质
分散剂
按照分散质或分散剂的聚集状态气、液、固来分,有9种类型。
A.交叉分类法
气
液
液
固
气
固
9种类型举例:
分散质 分散剂 实 例
气 气 空气
液 气 云、雾
固 气 烟灰尘
气 液 泡沫
液 液 牛奶、酒精的水溶液
固 液 糖水、油漆
气 固 泡沫塑料
液 固 珍珠(包藏着水的碳酸钙)
固 固 有色玻璃、合金
雾
气溶胶:分散剂为气态
烟
白云
固溶胶:分散剂为固态
烟水晶
有色玻璃
B.树状分类法(按照分散质微粒直径大小分类)
生活中常见胶体
3.常见分散系及其组成
分散系 分散质 分散剂
烟 _____________ _________
雾 _____________ _________
碘酒 _______ ________
食盐水 _________ _______
有色玻璃 _______________ ________
微小尘埃(固)
空气(气)
微小水滴(液)
空气(气)
碘(固)
酒精(液)
食盐(固)
水(液)
金属氧化物(固)
玻璃(固)
往小烧杯中加入25ml蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5-6滴FeCl3饱和溶液。继续煮沸至溶液呈红褐色,停止加热。
4.制备Fe(OH)3胶体
注意:不能过度加热,以免出现Fe(OH)3胶体凝聚。
FeCl3 + 3H2O △ Fe(OH)3(胶体)+3HCl
红褐色
1.沸水(蒸馏水)
2.逐滴加入,不能搅拌
3.饱和FeCl3溶液
4.继续煮沸至红褐色
条件
a、丁达尔效应
区分溶液与胶体
有一条“光亮”的通路
图1. 阳光穿过茂密的树林
图2. 夜晚美景
【练一练】下列说法正确的是( )
A.丁达尔效应不是胶体特有的现象,溶液与浊液也有
B.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有
C.胶体粒子的直径小于10-9m
D.丁达尔效应可用于区别胶体和溶液
×
×
分散质粒子直径
1nm=10-9m
×
D
(b)胶体的性质
①丁达尔效应
②聚沉
概念:当可见光束通过胶体时,在入射光侧面可观察到________
_______
原因:胶体中分散质微粒对可见光产生_____
应用:可用于鉴别______和_____
概念:在一定条件下胶体形成沉淀析出的现象
条件
加入酸、碱和盐等
加热或搅拌
加含有相反电荷胶粒的胶体
应用:胶体净水原理、黄河三角洲的形成等
光亮的
“通路”
散射
溶液
胶体
分散系 溶液 胶体 悬,乳浊液
分散质 粒子的大小
外观特征
能否通过滤纸
是否有丁达尔现象
事例
<1nm
1~100nm
>100nm
均匀,透明,稳定
均匀,有的透明,较稳定
不均匀,不透明,不稳定
NaCl溶液,
蔗糖溶液
Fe(OH)3胶体,
豆浆
泥水
能
能
不能
没有
没有
有
5.溶液、胶体和浊液的区别
胶体的结构
Fe(OH)3
Fe3+
Fe3+
Fe3+
Fe3+
Fe3+
Fe3+
Cl-
OH-
Cl-
OH-
Cl-
Cl-
OH-
Cl-
Cl-
OH-
OH-
Cl-
OH-
Cl-
Cl-
Cl-
Cl-
Cl-
整个体系不带电性
1.根据分散剂和分散质的状态不同可以组成( )种分散系
3 B. 11 C. 9 D. 6
2.下关于列关于溶液的叙述正确的是( )
A.所有溶液都是无色的
B.由分散质和分散剂组成的分散系一定是溶液
C.均一稳定的液体是溶液
D.溶液是由溶质和溶剂组成的
C
D
课堂练习
3.下列物质中属于溶液的是( ),属于浊液的是( ),
A.将少量二氧化碳通入石灰水后得到的混合物
B.液氮 C.碘酒 D.煮沸的FeCl3溶液
4.下列关于胶体的性质叙述正确的是( )
A.只带正电荷 B.能产生丁达尔效应
C.相当稳定 D.都是透明的
5.下列分散系属于胶体的是( )
A.淀粉 B.食盐水 C.牛奶 D.碘酒
C
D
B
AC
6. “纳米材料”是粒子直径为1~ 100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A.①④⑥ B. ②③④
C.②③⑤ D. ①③④⑥
B
第1节 物质的分类及其转化
第一章 物质及其变化
(1)物质的分类
超市里有成千上万种商品,
怎样能够迅速挑出你所需要的东西
??
在日常生活中我们还会在什么地方用到分类的方法呢?
图书馆
超市
查字典
药房
分类是提高效率的一种重要手段
创原家独
新知导入
美国《化学文摘》编辑部统计,已知的有机化合物的数目:
1880年约为1.2万种,
1910年约1.5万种,
1940年约为50万种,
1961年约为175万种,
1990年已超过1 000万种,
2004年,达到3 500万种以上。
要想对各物质物有条不紊地进行研究,就必须对物质分类。
1.分类的方法
(1)交叉分类法
(2)树状分类法
分类
交叉分类:
Na2CO3
Na2SO4
K2SO4
K2CO3
钠 盐
钾 盐
硫酸盐
碳酸盐
按阳离子分
按阳离子分
按阴离子分
按阴离子分
学
物 质
只由一种成分组成
纯净物
混合物
由同种元素组成
单 质
化合物
金属单质
非金属单质
酸
碱
盐
氧化物 .....
对同类事物按照某些属性进行再分类的方法
(2) 树状分类法
同素异形体:同种元素组成的不同单质
树状分类法
物质
纯净物
金属单质
非金属单质
化合物
酸
碱
盐
氧化物
单质
混合物
实践活动:选择下列合适的物质写在物质分类的下边:O2、Cu、He、H2SO4、Ba(OH)2、KNO3、CO2、 MgO 、空气、盐酸
稀有气体单质
Cu
O2
He
H2SO4
Ba(OH)2
KNO3
CO2、 MgO
空气、盐酸
2.酸的分类
按是否含氧
酸
按提供氢离子数目
一元酸:
二元酸:
多元酸:
含氧酸、 无氧酸
HNO3
HCl
HNO3、HCl
H2SO4
能提供一个H+的酸
能提供多个H+的酸
H3PO4
阳离子全部是氢离子(H+)的化合物
按酸性强弱
强酸
HCl、H2SO4、HNO3
CH3COOH、H2CO3
能提供两个H+的酸
中强酸
H3PO4、H2SO3
弱酸
1.按其在水溶液中是否溶解:
(1)可溶性碱:
(2)难溶性碱:
KOH NaOH Ba(OH)2 Ca(OH)2
Cu(OH)2 Fe(OH)3 Mg(OH)2 Zn(OH)2
3.碱的分类
2.按碱性强弱
强碱:NaOH KOH Ba(OH)2 Ca(OH)2
弱碱:NH3· H2O 、难溶性碱
阴离子全部是氢氧根离子( OH- )的化合物
K+ Na+ NH4+ NO3-
(2)按是否可溶于水:
可溶性盐:
难溶性盐:
AgCl BaSO4 CaCO3
(1) 按阴、阳离子来分:
常见阳离子:
常见阴离子:
K+ Na+ NH4+ Ag+ Cu2+ Ca2+
NO3- SO42- Cl- CO32- HCO3- PO43-
由金属阳离子(或NH4+)和酸根离子构成的化合物
4.盐的分类
(3)组成中是否有可电离的H+、OH-
正盐
酸式盐
碱式盐
Na2CO3
NaHCO3
Cu2(OH)2CO3
复盐:由两种或两种以上金属阳离子(或NH4+)和一种酸根离子构成的盐。
能电离出H+的盐
能电离出OH-的盐
不能电离出H+和OH-的盐
如KAl(SO4)2、(NH4)2Fe(SO4)2
同素异形体:同种元素形成的性质不同的单质
初中化学的学习中,同学们学习了很多的单质,其中有一些单质是由同种元素形成的,例如:金刚石和石墨都是由碳元素形成的。在化学上,我们将这样的单质命名为同素异形体。
科
【练一练】下列每组中的两种物质之间的关系为同素异形体的一组是( )
A.CaO和CaS B. 和
C.C60和C70 D.HCNO和HOCN
C
氧化物分类:
按组成分为金属氧化物和非金属氧化物
按性质分为酸性氧化物和碱性氧化物
与碱反应只生成盐和水
与酸反应只生成盐和水
(1)金属氧化物都是碱性氧化物
(2)非金属氧化物都是酸性氧化物
(3)碱性氧化物都是(3)碱性氧化物都是金属氧化物
(4)酸性氧化物都是非金属氧化物
Mn2O7是酸性氧化物
CO不是酸性氧化物也不是碱性氧化物
正确
Mn2O7是酸性氧化物
由氧元素与另外一种元素组成的二元化合物
氧化物
按组成分
按性质分
金属氧化物
非金属氧化物
酸性氧化物
碱性氧化物
( SO2、CO2 、Mn2O7)
( Na2O、CaO、BaO)
( SO2、CO2 、CO、NO2)
( Na2O、CaO)
能与碱反应,只生成对应的盐和水
能与酸反应,只生成对应的盐和水
5.氧化物的分类
不成盐氧化物
( CO、NO、NO2)
不与酸、碱、水反应
不能得到对应的盐
金属氧化物
碱性氧化物
非金属氧化物
酸性氧化物
只有碱性氧化物都是金属氧化物
1. 下列各组物质中均为纯净物的是( )
A. 生石灰,熟石灰,烧碱溶液
B. 明矾,硫磺,矿泉水
C. 乙醇,干冰,冰水混合物
D. 玻璃,盐酸,沼气
2. 下列各组概念中,后者属于前者范围的是( )
A. 化合物,单质 B. 金属,单质
C. 混合物,纯净物 D. 纯净物,化合物
C
D
课堂练习
物质/分类 碱 酸 盐 碱性氧化物 酸性氧化物
A Na2CO3 H2SO4 NaOH SO2 CO2
B NaOH HCl NaCl Na2O CO
C NaOH CH3COOH CaCl2 CO SO2
D KOH HNO3 CaCO3 CaO SO3
3、下列物质分类正确的组合是( )
D
4.分类是化学学习与研究的常用方法,下列分类正确的是( )
A.Na2O、MgO、CO均属于碱性氧化物
B.烧碱、生石灰、纯碱均属于碱
C.酸、碱、盐之间发生的反应均属于复分解反应
D.SO2、CO2 、BaO、SO3均属于酸性氧化物
C
物质
纯净物
混合物
单质
化合物
氧化物
酸
碱
盐
混合物还可以再分类吗?
二、分散系及其分类
二、分散系及其分类
1、定义:
2、分类标准:按照分散质粒子直径的大小
溶液:小于1nm
浊液:大于100nm
胶体:1-100nm之间
分散系:把一种(或多种)物质分散在另一种(或多种)物质
中所得到的体系。
分散质:被分散的物质。
分散剂:起容纳分散质的作用。
一种液体以小液滴的形式分散在另外一种液体之中形成的分散系叫乳浊液。
固体小颗粒悬浮于液体里形成的分散系。
悬浊液:
乳浊液:
浊液
一般规律:
1.分散系中有水,水是分散剂;
2.分散系中是两种液体(没有水),量多的是分散剂。
分散质
分散剂
按照分散质或分散剂的聚集状态气、液、固来分,有9种类型。
A.交叉分类法
气
液
液
固
气
固
9种类型举例:
分散质 分散剂 实 例
气 气 空气
液 气 云、雾
固 气 烟灰尘
气 液 泡沫
液 液 牛奶、酒精的水溶液
固 液 糖水、油漆
气 固 泡沫塑料
液 固 珍珠(包藏着水的碳酸钙)
固 固 有色玻璃、合金
雾
气溶胶:分散剂为气态
烟
白云
固溶胶:分散剂为固态
烟水晶
有色玻璃
B.树状分类法(按照分散质微粒直径大小分类)
生活中常见胶体
3.常见分散系及其组成
分散系 分散质 分散剂
烟 _____________ _________
雾 _____________ _________
碘酒 _______ ________
食盐水 _________ _______
有色玻璃 _______________ ________
微小尘埃(固)
空气(气)
微小水滴(液)
空气(气)
碘(固)
酒精(液)
食盐(固)
水(液)
金属氧化物(固)
玻璃(固)
往小烧杯中加入25ml蒸馏水,将烧杯中的蒸馏水加热至沸腾,向沸水中逐滴加入5-6滴FeCl3饱和溶液。继续煮沸至溶液呈红褐色,停止加热。
4.制备Fe(OH)3胶体
注意:不能过度加热,以免出现Fe(OH)3胶体凝聚。
FeCl3 + 3H2O △ Fe(OH)3(胶体)+3HCl
红褐色
1.沸水(蒸馏水)
2.逐滴加入,不能搅拌
3.饱和FeCl3溶液
4.继续煮沸至红褐色
条件
a、丁达尔效应
区分溶液与胶体
有一条“光亮”的通路
图1. 阳光穿过茂密的树林
图2. 夜晚美景
【练一练】下列说法正确的是( )
A.丁达尔效应不是胶体特有的现象,溶液与浊液也有
B.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有
C.胶体粒子的直径小于10-9m
D.丁达尔效应可用于区别胶体和溶液
×
×
分散质粒子直径
1nm=10-9m
×
D
(b)胶体的性质
①丁达尔效应
②聚沉
概念:当可见光束通过胶体时,在入射光侧面可观察到________
_______
原因:胶体中分散质微粒对可见光产生_____
应用:可用于鉴别______和_____
概念:在一定条件下胶体形成沉淀析出的现象
条件
加入酸、碱和盐等
加热或搅拌
加含有相反电荷胶粒的胶体
应用:胶体净水原理、黄河三角洲的形成等
光亮的
“通路”
散射
溶液
胶体
分散系 溶液 胶体 悬,乳浊液
分散质 粒子的大小
外观特征
能否通过滤纸
是否有丁达尔现象
事例
<1nm
1~100nm
>100nm
均匀,透明,稳定
均匀,有的透明,较稳定
不均匀,不透明,不稳定
NaCl溶液,
蔗糖溶液
Fe(OH)3胶体,
豆浆
泥水
能
能
不能
没有
没有
有
5.溶液、胶体和浊液的区别
胶体的结构
Fe(OH)3
Fe3+
Fe3+
Fe3+
Fe3+
Fe3+
Fe3+
Cl-
OH-
Cl-
OH-
Cl-
Cl-
OH-
Cl-
Cl-
OH-
OH-
Cl-
OH-
Cl-
Cl-
Cl-
Cl-
Cl-
整个体系不带电性
1.根据分散剂和分散质的状态不同可以组成( )种分散系
3 B. 11 C. 9 D. 6
2.下关于列关于溶液的叙述正确的是( )
A.所有溶液都是无色的
B.由分散质和分散剂组成的分散系一定是溶液
C.均一稳定的液体是溶液
D.溶液是由溶质和溶剂组成的
C
D
课堂练习
3.下列物质中属于溶液的是( ),属于浊液的是( ),
A.将少量二氧化碳通入石灰水后得到的混合物
B.液氮 C.碘酒 D.煮沸的FeCl3溶液
4.下列关于胶体的性质叙述正确的是( )
A.只带正电荷 B.能产生丁达尔效应
C.相当稳定 D.都是透明的
5.下列分散系属于胶体的是( )
A.淀粉 B.食盐水 C.牛奶 D.碘酒
C
D
B
AC
6. “纳米材料”是粒子直径为1~ 100nm的材料,纳米碳就是其中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后,会析出黑色沉淀
A.①④⑥ B. ②③④
C.②③⑤ D. ①③④⑥
B
