化学人教版(2019)选择性必修3 3.3.1乙醛(共51张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.3.1乙醛(共51张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 12.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-07 00:12:03 | ||
图片预览






文档简介
(共51张PPT)
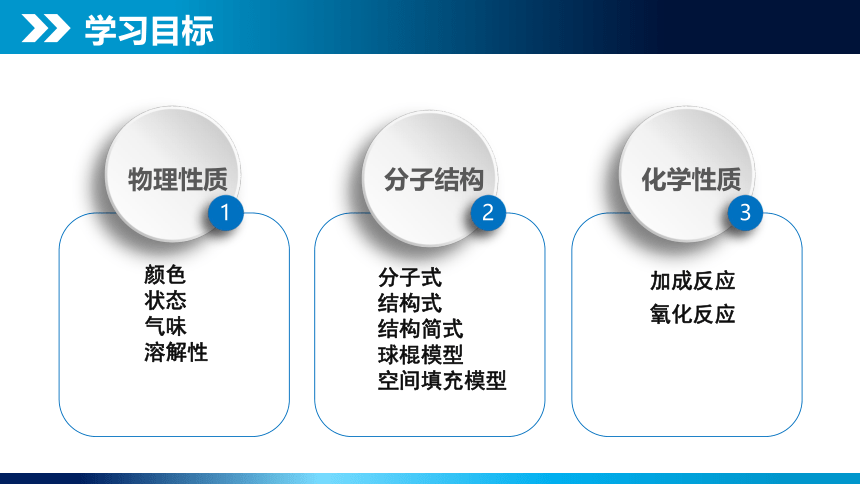
为什么有的人喝酒脸会红?
身边的化学
体内乙醛脱氢酶不丰富
饮酒后就会引起体内乙醛积累,导致血管扩张而脸发红
请写出乙醇发生催化氧化反应的化学方程式。
回顾练习
乙醛的性质和应用
学习目标
1
物理性质
2
3
分子结构
化学性质
颜色
状态
气味
溶解性
分子式
结构式
结构简式
球棍模型
空间填充模型
加成反应
氧化反应
学习任务一
乙醛长什么样子?
实验探究
乙醛
水
物理性质
1
颜色
状态
气味
挥发性
溶解性
无色
液体
刺激性
易挥发
易溶于水、乙醇
学习任务二
乙醛分子中原子是如何排布的?
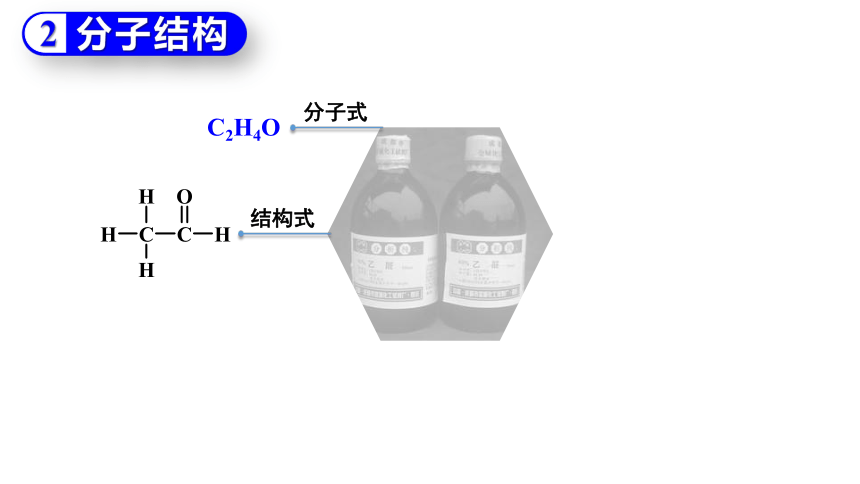
分子结构
2
分子式
C2H4O
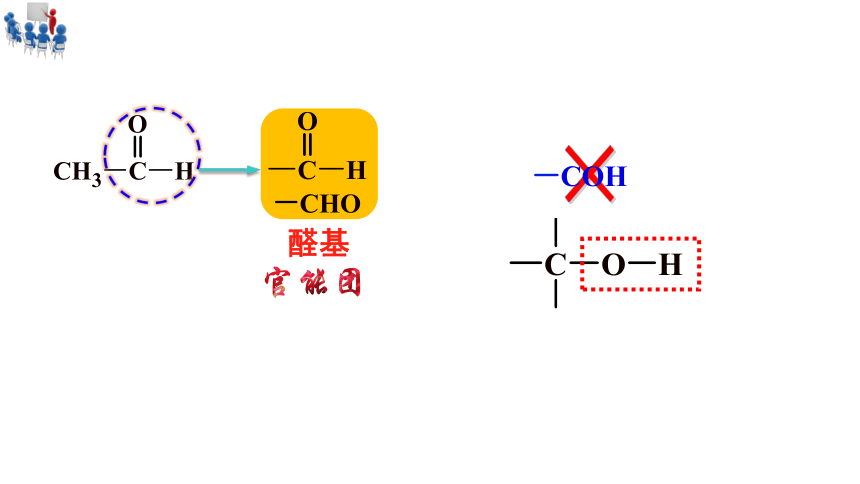
结构式
×
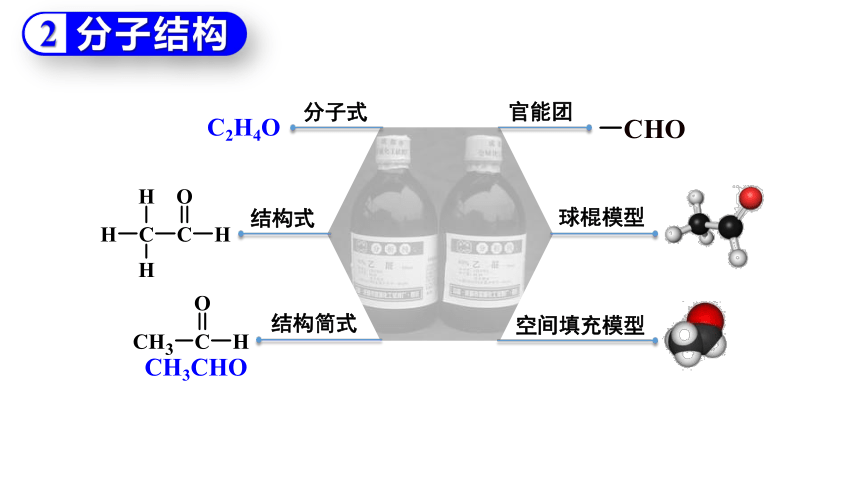
分子结构
2
分子式
C2H4O
结构式
官能团
结构简式
CH3CHO
球棍模型
空间填充模型
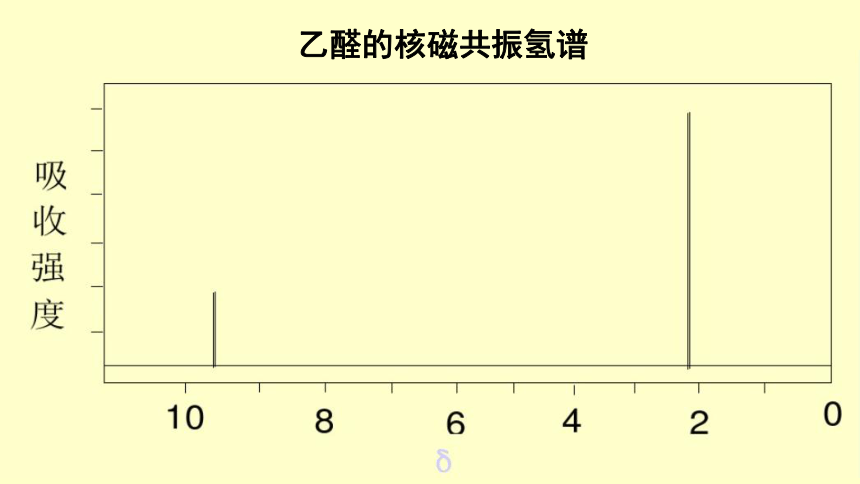
乙醛的核磁共振氢谱
学习任务三
乙醛可与哪些物质发生反应?
感受 理解
试根据乙醛的结构,预测乙醛的反应性质。
3.1 加成反应
化学性质
3
与H2反应
1
+H2
【注意】
①乙醛不能与X2、HX、H2O进行加成反应
②酯基(-COO-)和羧基 (-COOH) 中的C=O不能与H2发生加成反应
醛的催化加氢反应
也是它的还原反应
感受 理解
试根据乙醛的结构,预测乙醛可能断键部位。
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,
碳原子带部分正电荷,
A—B
A
B
从而使醛基具有较强的极性
+H—CN
2-羟基丙腈
有机合成中可以用来增长碳链
醛或酮与氢氰酸加成,反应产物的分子比原来的醛分子或酮分子多了一个碳原子。
应用
3.1 加成反应
化学性质
3
与H2反应
1
2
与HCN反应
+H2
+HCN
3
信息反应
醛+RMgBr
里昂大学
从花花公子到诺贝尔奖得主
格林尼亚
化学趣史
朗索瓦 奥古斯特 维克多 格林尼亚(1871年5月6日-1935年12月13日),法国化学家,因发明了格氏试剂与他的同事保罗 萨巴捷一同获得诺贝尔化学奖。一生之中著有科学论文6000多篇,对人类科学事业作出了巨大的贡献。
从花花公子到诺贝尔奖得主
法国化学家维克多格林尼亚出生在一个百万富翁家庭,从小养成了游手好闲、挥金如土、盛气凌人的恶习。然而,在他二十一岁的时候,却遭受了一次严重的打击。
那是一次宴会上,他对一位年轻美貌的巴黎女郎一见钟情。他仗着自己长相英俊,有钱有势,便走上前去调情。没料到这位女郎却冷冰冰地骂道:“请站远一点,我最讨厌被花花公子挡住视线。”这让格林尼亚羞愧难当。
他满含屈辱地离开了家庭,只身一人来到里昂,在那里他隐姓埋名,发奋求学,整天待在图书馆和实验室里。在菲利普巴尔教授的精心指导和自己的长期努力下,他发明了“格式试剂”,发表学术论文二百多篇。1912年,瑞典皇家科学院授予他诺贝尔化学奖。
“二流子”与诺贝尔获奖者
格氏试剂
H2O/H+
H
镜子的发明
你知道吗?
古代人把水当成镜子。池塘和水洼中的水能倒映出自己的样子。
后来,人们将金属打磨后作为镜子使用。镜子起源于青铜器时代(约公元前3000~公元前1200年)
1508年,意大利的玻璃工匠达尔卡罗兄弟研制实用的玻璃镜子。他们先把锡箔贴在玻璃面上,然后倒上水银,水银能够很好地溶解锡,随后,玻璃上形成了一层薄薄的锡与水银的合金(称为“锡汞齐”),这种锡汞齐的本领高强,能够紧紧地粘附在玻璃上而成为真正的镜子。
1843年,德国科学家发明了镀银的玻璃镜子。这种银玻镜子背面发亮的东西,是一层薄薄的银层。层银不是涂上去的,也不是靠电镀上去的。
而是利用一种特殊而有趣的化学反应电镀上去的!
银镜反应
实验探究
实验探究
加氧
还原剂
还原剂
被氧化
发生氧化反应
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
乙醛分子中醛基中的C—H为何易断裂?
交流 研讨
受碳碳双键影响,
C-H键极性增强
C-H易断裂被氧化成羧酸
银镜反应的用途
检验醛基的存在和醛基的数目
01
工业上用来制瓶胆和镜子
02
银镜反应
试管内壁必须洁净
1
实验
注意点
温馨提醒
(热NaOH溶液,蒸馏水)
2
须用新配制的银氨溶液
(久置的银氨溶液会生成易爆炸的叠氮化银AgN3)
3
必须水浴
不能用酒精灯直接加热
4
加热时不可振荡和摇动试管
实验后除银镜:
稀HNO3浸泡,再水洗
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
实验探究
还原剂
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
铜镜反应的用途
检验醛基的存在和醛基的数目
01
医学上检验病人是否患糖尿病
02
铜镜反应
氢氧化铜必须是新配制
1
实验
注意点
温馨提醒
(久置得到氢氧化铜沉淀,不易反应)
2
碱一定要过量
(保证Cu2+完全沉淀并使溶液呈碱性)
过量的NaOH溶液中滴加少量CuSO4溶液
3
加热时要将混合液加热至沸腾
既然弱氧化剂可氧化乙醛,那么强氧化剂如何?
联想与质疑
乙醛与溴水(溴的四氯化碳溶液)反应
科学探究
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
铜镜反应
2
强氧化剂
酸性高锰酸钾溶液
溴水
CH3CHO+Br2+H2O→CH3COOH +2HBr
能使溴水和KMnO4酸性溶液褪色
能跟烯烃起加成反应的试剂(如溴),一般不跟醛发生加成反应。
请设计实验证明,乙醛与溴水的反应是氧化反应,而不是加成反应。
CH3CHO+Br2+H2O→CH3COOH +2HBr
CH3CHO+Br2→CH3CHBrOBr
测反应后溶液的pH
测反应前后溶液的导电性
联想与质疑
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
铜镜反应
2
强氧化剂
酸性高锰酸钾溶液
溴水
CH3CHO+Br2+H2O→CH3COOH +2HBr
能使溴水和KMnO4酸性溶液褪色
3
O2
催化氧化
这节课我学到了什么?
(用一句话表示)
还有什么疑问?
课堂小结
课堂小结
醛基的性质
醛基中碳氧双键发生加成反应,被H2还原为醇
醛基中碳氢键较活泼,能被氧化成相应羧酸或盐
碳氧键
氧化性
碳氢键
还原性
乙醛
CH3CHO
归纳与整理
请写出乙醛发生银镜反应和铜镜反应的离子方程式。
银镜反应口诀:
银镜反应很简单,生成羧酸铵,还有一水二银三个氨
CH3CHO+2Cu(OH)2+OH-
考考你自己
茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:关于茉莉醛的下列叙述错误的是
A.在加热和催化剂作用下,能被氢气还原
B.能被高锰酸钾酸性溶液氧化
C.在一定条件下能与溴发生取代反应
D.不能与HBr发生加成反应
看谁做得既准又快
请设计实验,检验以下有机物中含有碳碳双键。
挑战自我
因为-CHO也能使溴水和高锰酸钾酸性溶液褪色,所以为防止-CHO的干扰应该先用弱氧化剂将-CHO氧化再检验碳碳双键。
先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化,然后再用酸性KMnO4溶液(或溴水)检验碳碳双键。
非常感谢您的观看
为什么有的人喝酒脸会红?
身边的化学
体内乙醛脱氢酶不丰富
饮酒后就会引起体内乙醛积累,导致血管扩张而脸发红
请写出乙醇发生催化氧化反应的化学方程式。
回顾练习
乙醛的性质和应用
学习目标
1
物理性质
2
3
分子结构
化学性质
颜色
状态
气味
溶解性
分子式
结构式
结构简式
球棍模型
空间填充模型
加成反应
氧化反应
学习任务一
乙醛长什么样子?
实验探究
乙醛
水
物理性质
1
颜色
状态
气味
挥发性
溶解性
无色
液体
刺激性
易挥发
易溶于水、乙醇
学习任务二
乙醛分子中原子是如何排布的?
分子结构
2
分子式
C2H4O
结构式
×
分子结构
2
分子式
C2H4O
结构式
官能团
结构简式
CH3CHO
球棍模型
空间填充模型
乙醛的核磁共振氢谱
学习任务三
乙醛可与哪些物质发生反应?
感受 理解
试根据乙醛的结构,预测乙醛的反应性质。
3.1 加成反应
化学性质
3
与H2反应
1
+H2
【注意】
①乙醛不能与X2、HX、H2O进行加成反应
②酯基(-COO-)和羧基 (-COOH) 中的C=O不能与H2发生加成反应
醛的催化加氢反应
也是它的还原反应
感受 理解
试根据乙醛的结构,预测乙醛可能断键部位。
在醛基的碳氧双键中,由于氧原子的电负性较大,碳氧双键中的电子偏向氧原子,使氧原子带部分负电荷,
碳原子带部分正电荷,
A—B
A
B
从而使醛基具有较强的极性
+H—CN
2-羟基丙腈
有机合成中可以用来增长碳链
醛或酮与氢氰酸加成,反应产物的分子比原来的醛分子或酮分子多了一个碳原子。
应用
3.1 加成反应
化学性质
3
与H2反应
1
2
与HCN反应
+H2
+HCN
3
信息反应
醛+RMgBr
里昂大学
从花花公子到诺贝尔奖得主
格林尼亚
化学趣史
朗索瓦 奥古斯特 维克多 格林尼亚(1871年5月6日-1935年12月13日),法国化学家,因发明了格氏试剂与他的同事保罗 萨巴捷一同获得诺贝尔化学奖。一生之中著有科学论文6000多篇,对人类科学事业作出了巨大的贡献。
从花花公子到诺贝尔奖得主
法国化学家维克多格林尼亚出生在一个百万富翁家庭,从小养成了游手好闲、挥金如土、盛气凌人的恶习。然而,在他二十一岁的时候,却遭受了一次严重的打击。
那是一次宴会上,他对一位年轻美貌的巴黎女郎一见钟情。他仗着自己长相英俊,有钱有势,便走上前去调情。没料到这位女郎却冷冰冰地骂道:“请站远一点,我最讨厌被花花公子挡住视线。”这让格林尼亚羞愧难当。
他满含屈辱地离开了家庭,只身一人来到里昂,在那里他隐姓埋名,发奋求学,整天待在图书馆和实验室里。在菲利普巴尔教授的精心指导和自己的长期努力下,他发明了“格式试剂”,发表学术论文二百多篇。1912年,瑞典皇家科学院授予他诺贝尔化学奖。
“二流子”与诺贝尔获奖者
格氏试剂
H2O/H+
H
镜子的发明
你知道吗?
古代人把水当成镜子。池塘和水洼中的水能倒映出自己的样子。
后来,人们将金属打磨后作为镜子使用。镜子起源于青铜器时代(约公元前3000~公元前1200年)
1508年,意大利的玻璃工匠达尔卡罗兄弟研制实用的玻璃镜子。他们先把锡箔贴在玻璃面上,然后倒上水银,水银能够很好地溶解锡,随后,玻璃上形成了一层薄薄的锡与水银的合金(称为“锡汞齐”),这种锡汞齐的本领高强,能够紧紧地粘附在玻璃上而成为真正的镜子。
1843年,德国科学家发明了镀银的玻璃镜子。这种银玻镜子背面发亮的东西,是一层薄薄的银层。层银不是涂上去的,也不是靠电镀上去的。
而是利用一种特殊而有趣的化学反应电镀上去的!
银镜反应
实验探究
实验探究
加氧
还原剂
还原剂
被氧化
发生氧化反应
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
乙醛分子中醛基中的C—H为何易断裂?
交流 研讨
受碳碳双键影响,
C-H键极性增强
C-H易断裂被氧化成羧酸
银镜反应的用途
检验醛基的存在和醛基的数目
01
工业上用来制瓶胆和镜子
02
银镜反应
试管内壁必须洁净
1
实验
注意点
温馨提醒
(热NaOH溶液,蒸馏水)
2
须用新配制的银氨溶液
(久置的银氨溶液会生成易爆炸的叠氮化银AgN3)
3
必须水浴
不能用酒精灯直接加热
4
加热时不可振荡和摇动试管
实验后除银镜:
稀HNO3浸泡,再水洗
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
实验探究
还原剂
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
铜镜反应的用途
检验醛基的存在和醛基的数目
01
医学上检验病人是否患糖尿病
02
铜镜反应
氢氧化铜必须是新配制
1
实验
注意点
温馨提醒
(久置得到氢氧化铜沉淀,不易反应)
2
碱一定要过量
(保证Cu2+完全沉淀并使溶液呈碱性)
过量的NaOH溶液中滴加少量CuSO4溶液
3
加热时要将混合液加热至沸腾
既然弱氧化剂可氧化乙醛,那么强氧化剂如何?
联想与质疑
乙醛与溴水(溴的四氯化碳溶液)反应
科学探究
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
铜镜反应
2
强氧化剂
酸性高锰酸钾溶液
溴水
CH3CHO+Br2+H2O→CH3COOH +2HBr
能使溴水和KMnO4酸性溶液褪色
能跟烯烃起加成反应的试剂(如溴),一般不跟醛发生加成反应。
请设计实验证明,乙醛与溴水的反应是氧化反应,而不是加成反应。
CH3CHO+Br2+H2O→CH3COOH +2HBr
CH3CHO+Br2→CH3CHBrOBr
测反应后溶液的pH
测反应前后溶液的导电性
联想与质疑
3.2 氧化反应
化学性质
3
弱氧化剂
1
银氨溶液
氢氧化铜
CH3CHO+2Ag(NH3)2OH
银镜反应
铜镜反应
2
强氧化剂
酸性高锰酸钾溶液
溴水
CH3CHO+Br2+H2O→CH3COOH +2HBr
能使溴水和KMnO4酸性溶液褪色
3
O2
催化氧化
这节课我学到了什么?
(用一句话表示)
还有什么疑问?
课堂小结
课堂小结
醛基的性质
醛基中碳氧双键发生加成反应,被H2还原为醇
醛基中碳氢键较活泼,能被氧化成相应羧酸或盐
碳氧键
氧化性
碳氢键
还原性
乙醛
CH3CHO
归纳与整理
请写出乙醛发生银镜反应和铜镜反应的离子方程式。
银镜反应口诀:
银镜反应很简单,生成羧酸铵,还有一水二银三个氨
CH3CHO+2Cu(OH)2+OH-
考考你自己
茉莉醛具有浓郁的茉莉花香,其结构简式如下所示:关于茉莉醛的下列叙述错误的是
A.在加热和催化剂作用下,能被氢气还原
B.能被高锰酸钾酸性溶液氧化
C.在一定条件下能与溴发生取代反应
D.不能与HBr发生加成反应
看谁做得既准又快
请设计实验,检验以下有机物中含有碳碳双键。
挑战自我
因为-CHO也能使溴水和高锰酸钾酸性溶液褪色,所以为防止-CHO的干扰应该先用弱氧化剂将-CHO氧化再检验碳碳双键。
先加足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化,然后再用酸性KMnO4溶液(或溴水)检验碳碳双键。
非常感谢您的观看
