【安徽专版】2024年中考化学模拟试卷一(含答案)
文档属性
| 名称 | 【安徽专版】2024年中考化学模拟试卷一(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 459.6KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-08 23:56:21 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2024年安徽省中考化学模拟试卷一(含答案)
温馨提示:
1、化学试卷共二大题17小题,满分40分物理和化学的考试时间共120分钟。
2、试卷包括“试题卷"和“答题卷"两部分请务必在“答题卷”上答题,在“试题卷"上答题是无效的。
3、附相对原子质量:H-1;C-12;N-14;O-16;Na-23。
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、化学知识有助于我们树立正确的认识、选择科学的生活。下列说法不正确的是( )
A.炒菜时油锅不慎着火,可以立即倒入青菜或者盖上锅盖灭火
B.食用海带、紫菜可补充人体所需要的微量元素碘,可预防骨质疏松
C.生铁和钢都属于金属材料,将生铁加工成不锈钢,抗腐蚀性增强
D.辨认毛衫的材质是纯棉的还是羊毛的,可通过抽丝点燃闻气味法
2、加快形成绿色生产生活方式,是建设山清水秀、天蓝地净美丽山西的第一步。下列做法与这一思想不相符的是( )
A.开发新能源,合理使用化石燃料 B.合成新型洗涤剂,减少水体污染
C.大量施用农药,减少作物病虫害 D.研发易降解塑料,减少白色污染
3、如图是某元素在元素周期表中的相关信息,下列关于该元素说法错误的是( )
A.元素符号为 B.原子核外电子数为107
C.属于金属元素 D.该原子的质量为270
4、实验操作是科学探究成功的基础。下列实验基本操作正确的是( )
A.倾倒液体 B.制取气体装置 C.读取液体体积 D.点燃酒精灯
5、中药当归、白芷中富含的紫花前胡醇(化学式C14H14O4),能增强人体免疫力。下列关于紫花前胡醇的说法正确的是( )
A.属于氧化物 B.碳、氢、氧元素的质量比为12:1:16
C.由14个碳原子、14个氢原子、4个氧原子构成D.246g紫花前胡醇中氢元素的质量为14g
6、物质的性质和用途密切相关。下列物质的用途主要体现其化学性质的是( )
A.石墨用作铅笔芯 B.氧气用于医疗急救、气焊气割
C.浓硫酸可作干燥剂 D.伍德合金用作电路保险丝
7、下列对宏观事实的微观解释错误的是( )
A.气体可以压缩在钢瓶中——分子之间存在间隙
B.变瘪的乒乓球放入热水中能鼓起来——温度升高,分子体积变大
C.CO有可燃性,没有可燃性——不同种分子化学性质不同
D.水电解生成氧气和氢气——化学反应前后分子种类发生改变
8、推理是一种重要的思维方式。下列推理中,正确的是( )
A.分子可以构成物质,则物质一定都是由分子构成的
B.置换反应有单质生成;则有单质生成的反应一定是置换反应
C.单质由同种元素组成;则由同种元素组成的纯净物一定是单质
D.碱溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定是碱溶液
9、分类和归纳是行之有效,简单易行的科学方法。下列说法错误的是( )
A.纯碱、火碱、熟石灰的溶液都显碱性 B.硫酸铜溶液和氯化钠溶液都属于透明溶液
C.生石灰和氢氧化钠固体溶于水放热,都属于物理变化D.镁、汞属于金属单质
10、清华大学的研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化为甲醇,该反应的微观示意图如图所示。下列说法错误的是( )
A.该反应前后元素的化合价没有发生改变 B.反应中涉及到三种化合物
C.该反应前后原子的种类和数目均不变 D.参加反应的甲和乙的分子个数比为1:3
11、实验是研究化学的基本方法。下列实验方案中能达到实验目的是( )
选项 实验目的 实验方案
A 探究铁锈蚀的条件 将一枚光亮的铁钉放入盛有适量水的试管中,观察现象
B 除去氧化钙中少量的碳酸钙 加水溶解,过滤
C 除去FeCl2溶液中少量的CuCl2 加入过量的铁粉,过滤
D 检验蜡烛中是否含有氧元素 在蜡烛的火焰上方罩一个干燥的烧杯,观察现象
A.A B.B C.C D.D
12、如图为NH4Cl、NaCl的溶解度曲线,下列有关说法正确的是( )
A.NaCl的溶解度一定小于NH4Cl的溶解度
B.T1℃时,NaCl、NH4Cl两饱和溶液中溶质的质量质量分数相等
C.除去NH4Cl中的NaCl,可用蒸发结晶
D.将50℃时NH4Cl饱和溶液100g冷却至0℃,析出晶体小于21g
二、本大题包括5小题,共28分
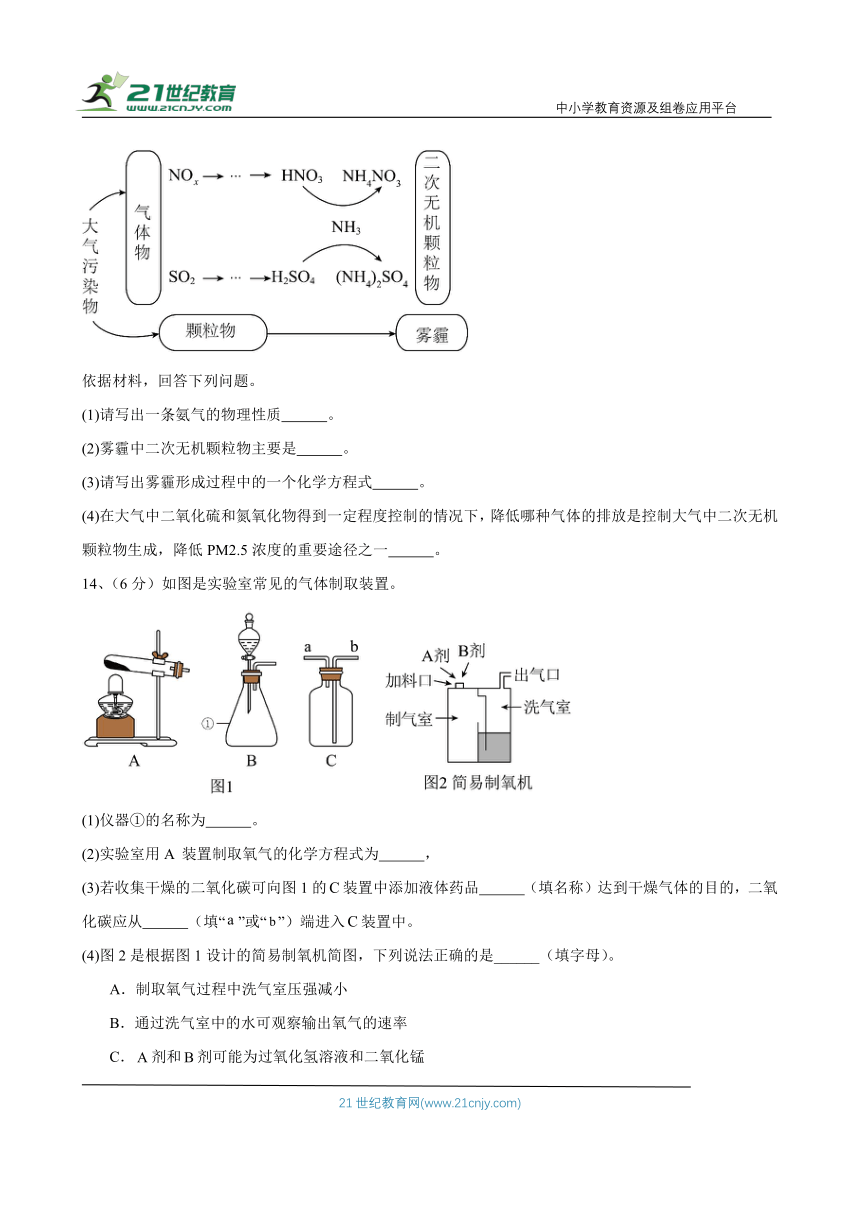
13、(5分)雾霾形成的推手——氨气
氨气是地球大气中唯一呈碱性的气体,它无色,有强烈的刺激气味,密度小于空气,极易溶于水,在常温下加压即可使其液化。
研究表明,在氨气大量存在的条件下,大气中的二氧化硫和氮氧化物转化成硫酸盐和硝酸盐的速度会急剧增加,从而促进二次无机颗粒物的生成(如图所示)。因此,加大对氨气排放的控制,对缓解雾霾具有重要意义。
全球氨排放大多与肉乳品业相关。除了畜禽养殖和废弃物处理过程产生大量氨气外,喂养畜禽所需饲料的种植过程中,氮肥的施用也会产生大量氨气。
依据材料,回答下列问题。
(1)请写出一条氨气的物理性质 。
(2)雾霾中二次无机颗粒物主要是 。
(3)请写出雾霾形成过程中的一个化学方程式 。
(4)在大气中二氧化硫和氮氧化物得到一定程度控制的情况下,降低哪种气体的排放是控制大气中二次无机颗粒物生成,降低PM2.5浓度的重要途径之一 。
14、(6分)如图是实验室常见的气体制取装置。
(1)仪器①的名称为 。
(2)实验室用A 装置制取氧气的化学方程式为 ,
(3)若收集干燥的二氧化碳可向图1的装置中添加液体药品 (填名称)达到干燥气体的目的,二氧化碳应从 (填“”或“”)端进入装置中。
(4)图2是根据图1设计的简易制氧机简图,下列说法正确的是______(填字母)。
A.制取氧气过程中洗气室压强减小
B.通过洗气室中的水可观察输出氧气的速率
C.剂和剂可能为过氧化氢溶液和二氧化锰
15、(6分)钛和钛合金是21世纪的重要金属材料。工业上利用钛铁矿——钛酸亚铁
()制备金属钛()的工艺流程如下。
【查阅资料】①为固体,化学性质稳定,不与稀硫酸、稀盐酸反应。
②沸点、沸点。
(1)将钛铁矿粉碎的目的是 。
(2)钛酸亚铁()中钛元素的化合价是 价。
(3)“反应釜”中发生的反应是,X的化学式是 。
(4)“沸腾炉”中将和的混合物分离,该操作的名称是 。
(5)“合成器”中得到的产品中含有杂质镁,可加入足量稀硫酸除去,写出除杂原理反应 (写化学方程式)。
16、(6+3分)酸和碱是两类重要的物质。了解它们的性质是化学重要的学习内容。
【探究一】探究酸碱中和反应
图1表示稀盐酸和氢氧化钠溶液的反应过程中溶液的pH变化曲线。请从曲线图中获取信息,回答下列问题:
(1)根据图1曲线所示,实验操作是按照图2中的 (填“①”或“②”)图所示进行。
(2)图1中点A处所含溶质是 ;(填化学式)。
(3)图3表示该反应到B点时溶液中存在的离子的情况,请将该图补充完整。
(4)下列试剂不能验证反应到达B点的是 (填字母序号)。
A.锌粒
B.大理石
C.无色酚酞试液
D.澄清石灰水
(5)小明通过查阅资料得知中和反应的过程伴随着热量释放,若用稀盐酸和氢氧化钠固体进行实验验证,却无法得出正确结论,原因是 。
【探究二】探究久置的氢氧化钠溶液变质程度。
氢氧化钠溶液敞口久置于空气中会发生变质,该反应的化学方程式为 。
【查阅资料】
Ⅰ.氯化钙溶液呈中性。
Ⅱ.氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl,为探究久置氢氧化钠溶液的变质程度,进行了如下实验:
【若正确回答下列问题加3分,总分不超过40分】
【实验报告】
实验结论 实验现象 实验结论
①取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,充分反应 (6)有 生成 说明原溶液中一定有Na2CO3
②取步骤①试管中的少量上层清液,滴加无色酚酞试液 溶液变红色 (7)说明原溶液中一定有 。
【实验结论】(8)氢氧化钠溶液 (填“部分”或“全部”)变质。
17、(5分)利用电解食盐水制取烧碱的原理为2X+2NaCl2NaOH+H2↑+Cl2↑。将20℃时117g的食盐水完全电解(忽略水的蒸发和气体的溶解),共收集到0.4g氢气。
(1) X的化学式为 。
(2)计算所得烧碱的质量。(写出计算过程)
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、B 2、C 3、D 4、C 5、D 6、B 7、B 8、C 9、C 10、A
11、C 12、B
二、本大题包括5小题,共28分
13、(5分)(1)无色或有强烈的刺激气味或密度小于空气或极易溶于水等;(2)硫酸铵和硝酸铵;
(3)NH3+HNO3=NH4NO3或2NH3+H2SO4=(NH4)2SO4;(4)氨气。
14、(6分)(1)锥形瓶;
(3)浓硫酸;b;(4)BC。
15、(6分)(1)增大反应物的接触面积,加快反应速率;(2)+4;(3)CO;(4)蒸馏;
(5) Mg+H2SO4=MgSO4+H2↑。
16、(6+3分)(1)②;(2)NaCl、NaOH;
(3);
(4)CD;(5)氢氧化钠固体溶于水也放出热量;
【探究二】2NaOH+CO2=Na2CO3+H2O;
(6)白色沉淀;(7)氢氧化钠(或NaOH);(8)部分。
17、(5分)(1)H2O;
解:(2)设所得烧碱的质量为x,则
解得x=16g
答:所得烧碱的质量为16g。
21世纪教育网(www.21cnjy.com)
2024年安徽省中考化学模拟试卷一(含答案)
温馨提示:
1、化学试卷共二大题17小题,满分40分物理和化学的考试时间共120分钟。
2、试卷包括“试题卷"和“答题卷"两部分请务必在“答题卷”上答题,在“试题卷"上答题是无效的。
3、附相对原子质量:H-1;C-12;N-14;O-16;Na-23。
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、化学知识有助于我们树立正确的认识、选择科学的生活。下列说法不正确的是( )
A.炒菜时油锅不慎着火,可以立即倒入青菜或者盖上锅盖灭火
B.食用海带、紫菜可补充人体所需要的微量元素碘,可预防骨质疏松
C.生铁和钢都属于金属材料,将生铁加工成不锈钢,抗腐蚀性增强
D.辨认毛衫的材质是纯棉的还是羊毛的,可通过抽丝点燃闻气味法
2、加快形成绿色生产生活方式,是建设山清水秀、天蓝地净美丽山西的第一步。下列做法与这一思想不相符的是( )
A.开发新能源,合理使用化石燃料 B.合成新型洗涤剂,减少水体污染
C.大量施用农药,减少作物病虫害 D.研发易降解塑料,减少白色污染
3、如图是某元素在元素周期表中的相关信息,下列关于该元素说法错误的是( )
A.元素符号为 B.原子核外电子数为107
C.属于金属元素 D.该原子的质量为270
4、实验操作是科学探究成功的基础。下列实验基本操作正确的是( )
A.倾倒液体 B.制取气体装置 C.读取液体体积 D.点燃酒精灯
5、中药当归、白芷中富含的紫花前胡醇(化学式C14H14O4),能增强人体免疫力。下列关于紫花前胡醇的说法正确的是( )
A.属于氧化物 B.碳、氢、氧元素的质量比为12:1:16
C.由14个碳原子、14个氢原子、4个氧原子构成D.246g紫花前胡醇中氢元素的质量为14g
6、物质的性质和用途密切相关。下列物质的用途主要体现其化学性质的是( )
A.石墨用作铅笔芯 B.氧气用于医疗急救、气焊气割
C.浓硫酸可作干燥剂 D.伍德合金用作电路保险丝
7、下列对宏观事实的微观解释错误的是( )
A.气体可以压缩在钢瓶中——分子之间存在间隙
B.变瘪的乒乓球放入热水中能鼓起来——温度升高,分子体积变大
C.CO有可燃性,没有可燃性——不同种分子化学性质不同
D.水电解生成氧气和氢气——化学反应前后分子种类发生改变
8、推理是一种重要的思维方式。下列推理中,正确的是( )
A.分子可以构成物质,则物质一定都是由分子构成的
B.置换反应有单质生成;则有单质生成的反应一定是置换反应
C.单质由同种元素组成;则由同种元素组成的纯净物一定是单质
D.碱溶液能使酚酞试液变红,所以能使酚酞试液变红的溶液一定是碱溶液
9、分类和归纳是行之有效,简单易行的科学方法。下列说法错误的是( )
A.纯碱、火碱、熟石灰的溶液都显碱性 B.硫酸铜溶液和氯化钠溶液都属于透明溶液
C.生石灰和氢氧化钠固体溶于水放热,都属于物理变化D.镁、汞属于金属单质
10、清华大学的研究人员成功研制出一种纳米纤维催化剂,可将二氧化碳转化为甲醇,该反应的微观示意图如图所示。下列说法错误的是( )
A.该反应前后元素的化合价没有发生改变 B.反应中涉及到三种化合物
C.该反应前后原子的种类和数目均不变 D.参加反应的甲和乙的分子个数比为1:3
11、实验是研究化学的基本方法。下列实验方案中能达到实验目的是( )
选项 实验目的 实验方案
A 探究铁锈蚀的条件 将一枚光亮的铁钉放入盛有适量水的试管中,观察现象
B 除去氧化钙中少量的碳酸钙 加水溶解,过滤
C 除去FeCl2溶液中少量的CuCl2 加入过量的铁粉,过滤
D 检验蜡烛中是否含有氧元素 在蜡烛的火焰上方罩一个干燥的烧杯,观察现象
A.A B.B C.C D.D
12、如图为NH4Cl、NaCl的溶解度曲线,下列有关说法正确的是( )
A.NaCl的溶解度一定小于NH4Cl的溶解度
B.T1℃时,NaCl、NH4Cl两饱和溶液中溶质的质量质量分数相等
C.除去NH4Cl中的NaCl,可用蒸发结晶
D.将50℃时NH4Cl饱和溶液100g冷却至0℃,析出晶体小于21g
二、本大题包括5小题,共28分
13、(5分)雾霾形成的推手——氨气
氨气是地球大气中唯一呈碱性的气体,它无色,有强烈的刺激气味,密度小于空气,极易溶于水,在常温下加压即可使其液化。
研究表明,在氨气大量存在的条件下,大气中的二氧化硫和氮氧化物转化成硫酸盐和硝酸盐的速度会急剧增加,从而促进二次无机颗粒物的生成(如图所示)。因此,加大对氨气排放的控制,对缓解雾霾具有重要意义。
全球氨排放大多与肉乳品业相关。除了畜禽养殖和废弃物处理过程产生大量氨气外,喂养畜禽所需饲料的种植过程中,氮肥的施用也会产生大量氨气。
依据材料,回答下列问题。
(1)请写出一条氨气的物理性质 。
(2)雾霾中二次无机颗粒物主要是 。
(3)请写出雾霾形成过程中的一个化学方程式 。
(4)在大气中二氧化硫和氮氧化物得到一定程度控制的情况下,降低哪种气体的排放是控制大气中二次无机颗粒物生成,降低PM2.5浓度的重要途径之一 。
14、(6分)如图是实验室常见的气体制取装置。
(1)仪器①的名称为 。
(2)实验室用A 装置制取氧气的化学方程式为 ,
(3)若收集干燥的二氧化碳可向图1的装置中添加液体药品 (填名称)达到干燥气体的目的,二氧化碳应从 (填“”或“”)端进入装置中。
(4)图2是根据图1设计的简易制氧机简图,下列说法正确的是______(填字母)。
A.制取氧气过程中洗气室压强减小
B.通过洗气室中的水可观察输出氧气的速率
C.剂和剂可能为过氧化氢溶液和二氧化锰
15、(6分)钛和钛合金是21世纪的重要金属材料。工业上利用钛铁矿——钛酸亚铁
()制备金属钛()的工艺流程如下。
【查阅资料】①为固体,化学性质稳定,不与稀硫酸、稀盐酸反应。
②沸点、沸点。
(1)将钛铁矿粉碎的目的是 。
(2)钛酸亚铁()中钛元素的化合价是 价。
(3)“反应釜”中发生的反应是,X的化学式是 。
(4)“沸腾炉”中将和的混合物分离,该操作的名称是 。
(5)“合成器”中得到的产品中含有杂质镁,可加入足量稀硫酸除去,写出除杂原理反应 (写化学方程式)。
16、(6+3分)酸和碱是两类重要的物质。了解它们的性质是化学重要的学习内容。
【探究一】探究酸碱中和反应
图1表示稀盐酸和氢氧化钠溶液的反应过程中溶液的pH变化曲线。请从曲线图中获取信息,回答下列问题:
(1)根据图1曲线所示,实验操作是按照图2中的 (填“①”或“②”)图所示进行。
(2)图1中点A处所含溶质是 ;(填化学式)。
(3)图3表示该反应到B点时溶液中存在的离子的情况,请将该图补充完整。
(4)下列试剂不能验证反应到达B点的是 (填字母序号)。
A.锌粒
B.大理石
C.无色酚酞试液
D.澄清石灰水
(5)小明通过查阅资料得知中和反应的过程伴随着热量释放,若用稀盐酸和氢氧化钠固体进行实验验证,却无法得出正确结论,原因是 。
【探究二】探究久置的氢氧化钠溶液变质程度。
氢氧化钠溶液敞口久置于空气中会发生变质,该反应的化学方程式为 。
【查阅资料】
Ⅰ.氯化钙溶液呈中性。
Ⅱ.氯化钙溶液能与碳酸钠溶液反应:CaCl2+Na2CO3═CaCO3↓+2NaCl,为探究久置氢氧化钠溶液的变质程度,进行了如下实验:
【若正确回答下列问题加3分,总分不超过40分】
【实验报告】
实验结论 实验现象 实验结论
①取少量该溶液于试管中,向溶液中滴加过量的氯化钙溶液,充分反应 (6)有 生成 说明原溶液中一定有Na2CO3
②取步骤①试管中的少量上层清液,滴加无色酚酞试液 溶液变红色 (7)说明原溶液中一定有 。
【实验结论】(8)氢氧化钠溶液 (填“部分”或“全部”)变质。
17、(5分)利用电解食盐水制取烧碱的原理为2X+2NaCl2NaOH+H2↑+Cl2↑。将20℃时117g的食盐水完全电解(忽略水的蒸发和气体的溶解),共收集到0.4g氢气。
(1) X的化学式为 。
(2)计算所得烧碱的质量。(写出计算过程)
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、B 2、C 3、D 4、C 5、D 6、B 7、B 8、C 9、C 10、A
11、C 12、B
二、本大题包括5小题,共28分
13、(5分)(1)无色或有强烈的刺激气味或密度小于空气或极易溶于水等;(2)硫酸铵和硝酸铵;
(3)NH3+HNO3=NH4NO3或2NH3+H2SO4=(NH4)2SO4;(4)氨气。
14、(6分)(1)锥形瓶;
(3)浓硫酸;b;(4)BC。
15、(6分)(1)增大反应物的接触面积,加快反应速率;(2)+4;(3)CO;(4)蒸馏;
(5) Mg+H2SO4=MgSO4+H2↑。
16、(6+3分)(1)②;(2)NaCl、NaOH;
(3);
(4)CD;(5)氢氧化钠固体溶于水也放出热量;
【探究二】2NaOH+CO2=Na2CO3+H2O;
(6)白色沉淀;(7)氢氧化钠(或NaOH);(8)部分。
17、(5分)(1)H2O;
解:(2)设所得烧碱的质量为x,则
解得x=16g
答:所得烧碱的质量为16g。
21世纪教育网(www.21cnjy.com)
同课章节目录
