人教版九年级化学上册第四单元 自然界的水章节测试试题(含解析)
文档属性
| 名称 | 人教版九年级化学上册第四单元 自然界的水章节测试试题(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 165.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-08 00:00:00 | ||
图片预览



文档简介
九年级化学上册第四单元 自然界的水章节测试
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、二氧化硅(SiO2)是制备电子芯片硅的原料。SiO2中硅元素的化合价是
A.+1 B.+2 C.+4 D.-2
2、下列物质的化学式书写正确的是
A.铁FE B.氯化钠NaCl2 C.硫酸铜CuSO4 D.氧化铝AlO
3、2021年世界水日主题是“珍惜水、爱护水“。下列说法正确的是
A.地球上的淡水资源十分丰富,可以任意随便用水
B.部分结冰的蒸馏水属于混合物
C.水是由氢分子和氧原子构成的
D.硬水中含有较多可溶性钙、镁化合物
4、下列化学用语书写正确的是
A.氯离子:Cl-1 B.2 个二氧化硫分子:2SO2
C.60 个碳原子:C60 D.氢氧化铝:AlOH3
5、下列物质属于氧化物的是
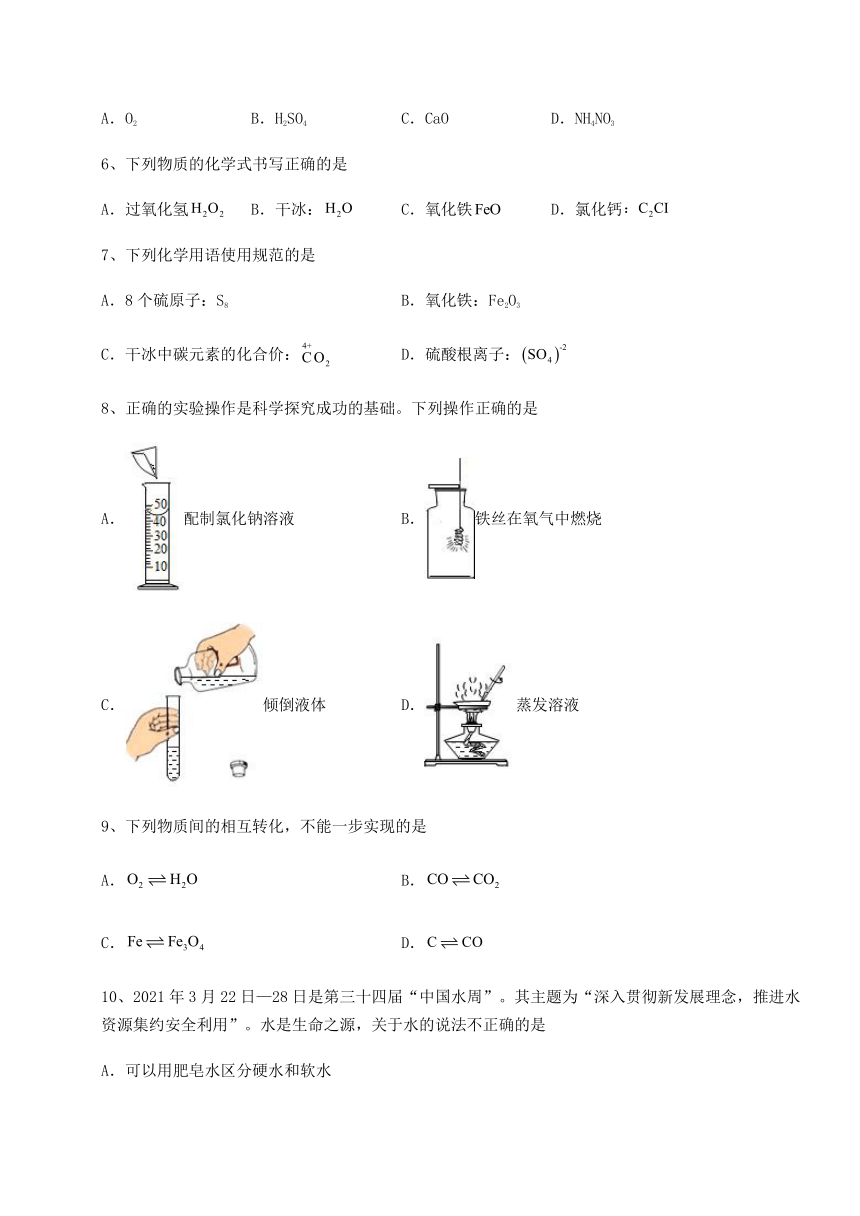
A.O2 B.H2SO4 C.CaO D.NH4NO3
6、下列物质的化学式书写正确的是
A.过氧化氢 B.干冰: C.氧化铁 D.氯化钙
7、下列化学用语使用规范的是
A.8个硫原子:S8 B.氧化铁:Fe2O3
C.干冰中碳元素的化合价: D.硫酸根离子:
8、正确的实验操作是科学探究成功的基础。下列操作正确的是
A.配制氯化钠溶液 B.铁丝在氧气中燃烧
C.倾倒液体 D.蒸发溶液
9、下列物质间的相互转化,不能一步实现的是
A. B.
C. D.
10、2021年3月22日—28日是第三十四届“中国水周”。其主题为“深入贯彻新发展理念,推进水资源集约安全利用”。水是生命之源,关于水的说法不正确的是
A.可以用肥皂水区分硬水和软水
B.水由液态变为气态时,分子间间隔变大
C.电解水实验中正负极得到的气体质量之比为1:2
D.明矾可以净水是因为其溶于水生成的胶状物能吸附悬浮的杂质
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题4分,共计20分)
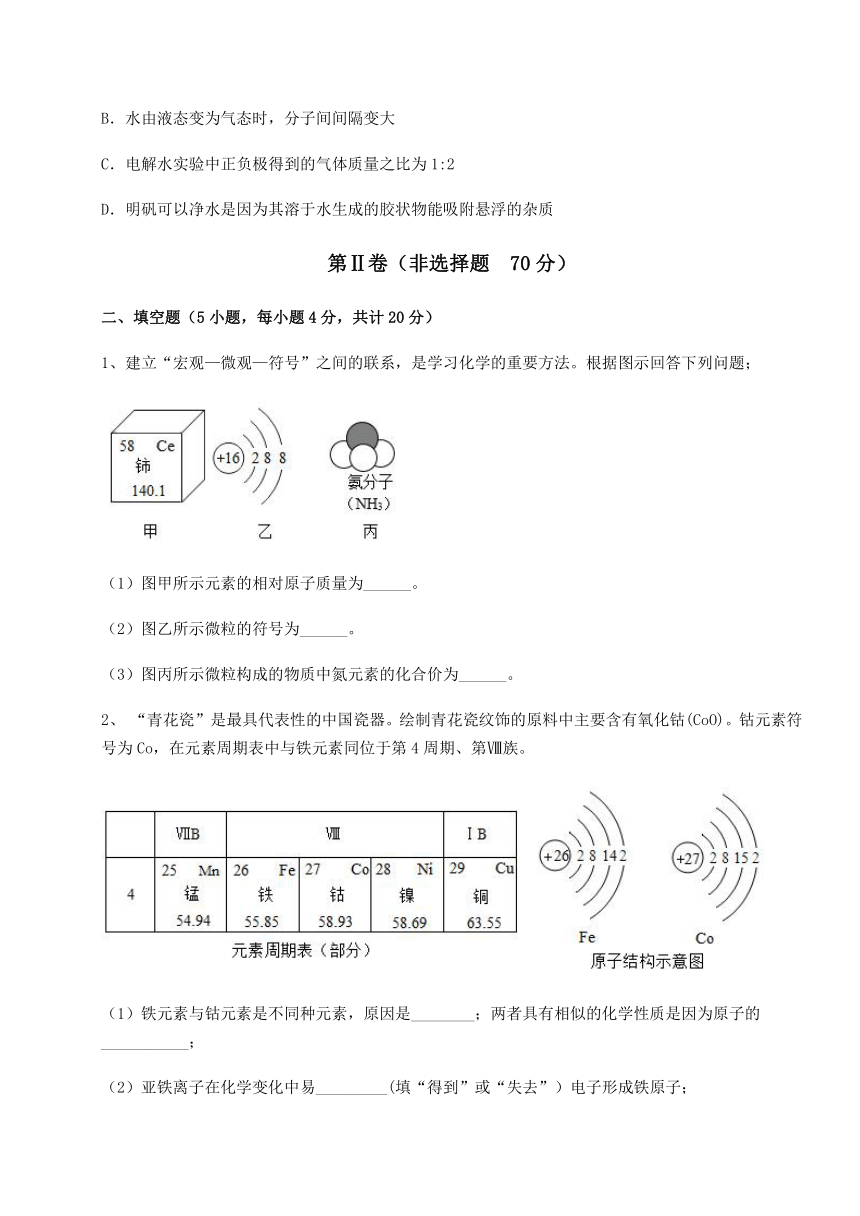
1、建立“宏观—微观—符号”之间的联系,是学习化学的重要方法。根据图示回答下列问题;
(1)图甲所示元素的相对原子质量为______。
(2)图乙所示微粒的符号为______。
(3)图丙所示微粒构成的物质中氮元素的化合价为______。
2、 “青花瓷”是最具代表性的中国瓷器。绘制青花瓷纹饰的原料中主要含有氧化钴(CoO)。钴元素符号为Co,在元素周期表中与铁元素同位于第4周期、第Ⅷ族。
(1)铁元素与钴元素是不同种元素,原因是________;两者具有相似的化学性质是因为原子的___________;
(2)亚铁离子在化学变化中易_________(填“得到”或“失去”)电子形成铁原子;
(3)钴的化合物钴酸锂(化学式为 LiCoO2,锂元素化合价为+1)常用作手机电池的正极材料,钴酸锂中钴元素的化合价为________。
3、冬季容易在路面产生积雪和冰,为减少积雪和冰对交通的影响,“融雪剂”发挥了一定的作用。其中一种融雪效果好、无污染的“融雪剂”的主要成份是醋酸钾(CH3COOK)。请回答:
(1)在醋酸钾分子中,钾元素的化合价是_______,其相对分子质量为_____。
(2)醋酸钾中C、H、O元素的质量比为______,钾元素的质量分数为_____(保留两位有效数字)。
4、一种新物质,其分子结构像一只小狗(如图),于是取名叫小狗烯,小狗烯的化学式为(C26H26)请计算:
小狗烯属于________(填“氧化物”或“化合物”)。“小狗烯”的相对分子质量是________。其中碳元素和氢元素的质量比________(填最简整数比)。2.6g“小狗烯”中含碳元素_______g。
5、用化学用语填空:
(1)氦气______;
(2)硫酸铝______;
(3)亚铁离子______;
(4)17号元素离子的结构示意图______。
三、计算题(5小题,每小题8分,共计40分)
1、疫情期间,使用的过氧乙酸(CH3 COOOH)是国家卫健委公布的消毒剂之一。将计算结果填在横线上。
(1)过氧乙酸分子中,碳、氢、氧三种原子的个数比是______。
(2)过氧乙酸的相对分子质量是______。
(3)过氧乙酸中,碳、氢、氧三种元素的质量比是______。
2、国家卫健委高级专家李兰娟院士透露,新型冠状病毒怕酒精,不耐高温等。按照以往对冠状病毒的经验,乙醚、乙醇(俗名酒精)化学式为(C2H6O),等含氯消毒剂均可灭活病毒。
(1)乙醇分子中碳原子和氢原子的个数比为______。
(2)已知一个碳12原子质量是mg,一个氧原子质量为ng,其中氧原子有X个质子,则该氧原子的相对原子质量为______,该氧原子中的中子数为______。
(3)92kg的乙醇中,含有氧元素的质量为多少kg?(列式并计算)
3、少数不法商贩对海产品的保鲜以及室内装修材料中都涉及到甲醛,其化学式为CH2O,是一种易挥发、有强烈刺激性气味的有机物.回答下列有关问题:
(1)甲醛的相对分子质量是_________。
(2)甲醛中H、O两种元素的质量比为________________。
(3)甲醛中碳元素的质量分数为_______________。
4、如图是某品牌补铁剂的标签。请回答:
(1)富马酸亚铁中含有_________种元素,其中碳、氢、氧原子的个数比为_______。
(2)富马酸亚铁的相对分子质量为_______,其中碳、氢元素的质量比为_________。
(3)已知富马酸亚铁颗粒中只有富马酸亚铁含铁元素,求1包富马酸亚铁颗粒中含铁元素的质量为______g。(写出计算过程,结果保留小数点后两位)
5、咖啡因是一种中枢神经兴奋剂,能够暂时的驱走睡意并恢复精力,有咖啡因成分的咖啡、茶、饮料及能量饮料十分畅销。因此,咖啡因也是世界上最普遍被使用的精神药物,其化学式为C8H10N4O2,完成填空
(1)咖啡因由___________种元素组成,咖啡因的相对分子质量为___________;
(2)咖啡因中碳元素与氢元素的质量比为___________(最简比);
(3)97g咖啡因中碳元素的质量为___________g。
四、实验探究(1小题,每小题10分,共计10分)
1、某课外小组利用H2 还原CuO 粉末的实验测定水的组成,图甲是测定装置的示意图。
(设计实验步骤)
①连接好装置,并检查气密性
②装入药品,打开弹簧夹,通入一段时间氢气后关闭弹簧夹
③分别称量装置C、D 的质量
④再次打开弹簧夹,通入氢气后,加热装置C
⑤待C 中固体全部变为红色后,停止加热
⑥继续通入氢气,待装置C 恢复至室温后,关闭弹簧夹
⑦再次分别称量装置C、D 的质量
(完善实验设计)经过讨论同学们认为,为了提高实验的安全性,步骤④加热装置 C 前, 应在 E 导管口收集一试管气体后,进行如图乙所示操作,若操作过程中听到尖锐爆鸣声, 则反应的化学方程式是_____。
(进行实验)该小组的同学按上述步骤进行实验,并进行了实验数据(C 中玻璃管质量为60.0g)
装置C 的质量/g 装置D 的质量/g
反应前 68.0 158.2
反应后 67.2 159.1
(1)小组同学利用锌粒和稀硫酸反应制氢气,请写出反应的化学方程式_____。在锌与稀硫酸反应的过程中,若夹紧弹簧夹,则A 中反应停止,其原理是_____。
(2)步骤⑥的目的是_____。
(数据处理)
(1)根据上表中数据,水中氢、氧元素的质量比等于_____(使用原始数据列式,不用计算出结果)。
(拓展探究)该小组同学参考上述实验原理,模仿实验步骤,设计了如图装置(假设氢氧化钠溶液能完全吸收二氧化碳),打算测定二氧化碳中碳、氧元素的质量比。但测出的碳、氧元素的质量比总是小于 3:8,请分析可能的原因_____。
-参考答案-
一、单选题
1、C
【详解】
二氧化硅中氧元素化合价为-2价,设硅元素化合价为x,根据化合物中正负化合价代数为0,则有x+(-2)×2=0,得x=+4价;
故选C。
2、C
【分析】
元素符号的书写:一个字母大写,两个字母第一个字母大写,第二个字母小写。化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约简,得化学式右下角的数字,数字为1时不写。
【详解】
铁:Fe; 氯化钠:NaCl;硫酸铜:CuSO4 ;氧化铝:Al2O3。
故选C。
3、D
【详解】
A.地球上的水资源十分丰富,但淡水资源有限,可直接利用更少,所以不可以任意随便用水,选项说法错误。
B.部分结冰的蒸馏水中也只有水,所以属于纯净物,选项说法错误。
C.水是由水分子构成的,水分子由氢原子和氧原子构成,选项说法错误。
D.硬水中含有较多可溶性钙、镁化合物,选项说法正确。
故选:D
4、B
【详解】
A、离子的表示方法,在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个单位电荷时,1要省略。氯离子可表示为Cl-,故选项化学用语书写错误;
B、由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则2个二氧化硫分子可表示为2SO2,故选项化学用语书写正确;
C、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故60个碳原子可表示为60C,故选项化学用语书写错误;
D、氢氧化铝中铝元素显+3价,氢氧根显-1价,其化学式为Al(OH)3,故选项化学用语书写错误。
故选:B。
5、C
【详解】
氧化物是指由两种元素组成,并且其中一种是氧元素的化合物。
A、O2只由一种元素组成,属于单质,不符合题意;
B、H2SO4由三种元素组成,不属于氧化物,不符合题意;
C、CaO由两种元素组成,并且其中一种是氧元素,属于氧化物,符合题意;
D、NH4NO3由三种元素组成,不属于氧化物,不符合题意。
故选C。
6、A
【详解】
A、过氧化氢化学式书写正确,正确;
B、干冰为固体二氧化碳CO2,错误;
C、氧化铁化学式为Fe2O3,错误;
D、氯化钙化学式为CaCl2,错误。
故选A。
7、B
【详解】
A、表示原子的个数应该在原子前面加上数字,8S,故不符合题意;
B、氧化铁中铁的化合价为+3价,氧的化合价为-2价,所以化学式为Fe2O3,故符合题意;
C、化合价在写的时候写到元素正上方,符号应写在数字之前,故不符合题意;
D、硫酸根粒子电荷数标在离子团的右上角,数字在前,符号在后,表示为,故不符合题意。
故选:B。
【点睛】
8、D
【详解】
A、量筒只能量取液体体积,不能配制溶液,故图示操作不正确;
B、为防止铁丝在氧气中燃烧时,高温熔化物溅落,使集气瓶炸裂,瓶底需要放少量水或细沙,故图示操作不正确;
C、向试管中倒入液体,试管倾斜,瓶塞要倒放,标签朝向手心,瓶口紧挨试管口,图中试管未倾斜,瓶塞未倒放,标签未朝向手心,瓶口未紧挨试管口,故图示操作不正确;
D、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,故图示操作正确。
故选D。
9、D
【详解】
A、氢气燃烧和氧气反应生成水,水电解生成氧气,能一步实现,故A不符合题意;
B、一氧化碳燃烧生成二氧化碳,二氧化碳和碳高温生成一氧化碳,可一步实现,故B不符合题意;
C、铁在氧气中燃烧生成了四氧化三铁,一氧化碳还原四氧化三铁生成铁,可一步实现,故C不符合题意;
D、碳在氧气(不足)中燃烧生成一氧化碳,一氧化碳不能一步生成碳单质,不可一步实现,故D符合题意。
故选D。
10、C
【详解】
A、硬水加肥皂水泡沫少,浮渣多,软水加肥皂水泡沫多,浮渣少,可以用肥皂水区分硬水和软水,正确。
B、水由液态变为气态时,分子间间隔变大,正确。
C、电解水实验中正负极得到的气体体积之比为1:2,不是质量比,错误。
D、明矾可以净水是因为其溶于水生成的胶状物能吸附悬浮的杂质,正确。
故选:C。
二、填空题
1、
(1)140.1
(2)S2-
(3)-3
【分析】
(1)
元素周期表小方格最下方数字,表示相对原子质量,故填:140.1。
(2)
图乙质子数16,属于硫元素,核外电子数大于核电荷数,属于硫离子,故填:S2-。
(3)
氢元素+1价,设氮元素化和价为x,根据化合价代数和为零,x+(+1)3=0,x=-3,故填:-3。
2、
(1) 质子数不同 最外层电子数相同
(2)得到
(3)+3
【解析】
(1)
同一元素质子数不同,铁元素与钴元素是不同种元素,原因是质子数;元素化学性质与原子最外层电子数有密切关系,两者具有相似的化学性质是因为原子的最外层电子数相同。
(2)
亚铁离子是铁原子失去电子后形成的,故在化学变化中得到电子形成铁原子;
(3)
LiCoO2中锂元素化合价为正一价、氧元素化合价为负二价,化合物中正负化合价代数和为零;则钴元素的化合价为+3。
3、
(1) +1 98
(2) 24∶3∶32 40%
【分析】
(1)
钾元素在化合物中一般显+1价,在醋酸钾分子中,钾元素的化合价是+1,其相对分子质量为。
(2)
醋酸钾中C、H、O元素的质量比为;钾元素的质量分数为。
4、化合物 338 12:1 2.4
【详解】
由化学式可知,小狗烯中不含氧元素,不符合氧化物的特点,不属于氧化物,小狗烯是碳元素与氢元素组成的纯净物,属于化合物,故填化合物;
小狗烯的相对分子质量=12×26+1×26=338,故填338;
小狗烯中碳元素和氢元素的质量比=(12×26):(1×26)=12:1,故填12:1;
2.6g“小狗烯”中含碳元素的质量=2.6g××100%=2.4g,故填2.4。
5、
(1)
(2)
(3)
(4)
【分析】
(1)
稀有气体的化学式用元素符号表示,氦气用表示。
(2)
硫酸铝由铝离子和硫酸根离子构成。铝显+3价,硫酸根显-2价。所以硫酸铝用表示。
(3)
亚铁离子带两个正电荷,所以用表示。
(4)
17号元素离子的结构示意图中17个质子,18个电子,最外层8个电子。如图所示
【点睛】
稀有气体的化学式用元素符号表示,氦气用表示。
三、计算题
1、
(1)2:4:3
(2)76
(3)6:1:12
【解析】
(1)
根据过氧乙酸的化学式CH3COOOH可知,一个过氧乙酸分子中含有2个碳原子,4个氢原子和3个氧原子,故碳、氢、氧的原子个数比为2:4:3;
(2)
根据过氧乙酸化学式可知,其相对分子质量为,故填76;
(3)
根据化学式可知,碳、氢、氧的三种元素质量比比为,故填6:1:12。
2、
(1)1:3
(2) -X
(3)32kg
含有氧元素的质量92Kg×=32kg
答:氧元素质量32kg。
【解析】
(1)
乙醇分子中碳原子和氢原子的个数比为2:6=1:3,故填:1:3。
(2)
氧原子的相对原子质量为 ,中子数=相对原子质量-质子数,-X,故填:;-X。
(3)
见答案
3、
(1)30
(2)1:8
(3)40%
【分析】
相对分子质量是组成分子的各原子的相对原子质量的总和;C的相对原子质量为12,H的相对原子质量为1,O的相对原子质量为16。
(1)
由甲醛的化学式可知,甲醛由碳、氢、氧元素组成,其相对分子质量:12+12+16=30,故填:30;
(2)
甲醛中氢、氧元素的质量比为: ,故填:1:8;
(3)
甲醛中碳元素的质量分数= ,故填:40%。
4、
(1) 4四 2:1:2
(2) 170 24:1
(3)0.07g
1包富马酸亚铁颗粒中含铁元素的质量为0.2g××100%≈0.07g;
答:1包富马酸亚铁颗粒中含铁元素的质量为0.07g。
【解析】
(1)
物质由元素组成,富马酸亚铁由碳、氢、铁、氧四种元素组成,1个富马酸亚铁分子中含有4个碳原子、2个氢原子、1个铁原子和4个氧原子,所以碳、氢、氧原子的个数比为4:2:4=2:1:2,故填: 4或四;2:1:2;
(2)
富马酸亚铁的相对分子质量为12×4+1×2+56+16×4=170;碳、氢元素的质量比为(12×4):(1×2) =24:1,故填:170;24:1;
(3)
见答案。
5、
(1) 四 194
(2)48:5
(3)48g
【解析】
(1)
咖啡因由C、H、O、N四种元素组成,C8H10N4O2的相对分子质量为:;
(2)
由咖啡因分子式,咖啡因中碳元素与氢元素的质量比为(12×8):(1×10)=48:5;
(3)
97g咖啡因中碳元素的质量为。
四、实验探究
1、2H2+O22H2O Zn+H2SO4=ZnSO4+H2↑ 关闭弹簧夹后,试管内生成气体,气压增大,将液体压回长颈漏斗,固液分离,反应停止 让生成的水蒸气全部进入D装置,使其被充分吸收减少误差;或防止空气进入C中,使铜又被氧化造成误差;或答防止空气中的水蒸气被吸入D中造成误差 [(159.1-158.2)-(68.0-67.2)]:(68.0-67.2) 气体经过氢氧化钠溶液带出水蒸气,使测得的二氧化碳质量偏小
【详解】
[完善实验设计]
氢气在空气中燃烧生成水,反应的化学方程式是:2H2+O22H2O。故填:2H2+O22H2O;
[进行实验]
(1)锌和稀硫酸反应生成氢气和硫酸锌;在锌与稀硫酸反应的过程中,若夹紧弹簧夹,则A 中反应停止,其原理是关闭弹簧夹后,试管内生成气体,气压增大,将液体压回长颈漏斗,固液分离,反应停止。故填:Zn+H2SO4=ZnSO4+H2↑;关闭弹簧夹后,试管内生成气体,气压增大,将液体压回长颈漏斗,固液分离,反应停止;
(2)步骤⑥的目的是让生成的水蒸气全部进入D装置,使其被充分吸收减少误差。故填:让生成的水蒸气全部进入D装置,使其被充分吸收减少误差。
[数据处理]
(1)根据上表中数据,水中氢、氧元素的质量比等于[(159.1-158.2)-(68.0-67.2)]:(68.0-67.2),故填:[(159.1-158.2)-(68.0-67.2)]:(68.0-67.2);
[拓展探究]该小组同学参考上述实验原理,模仿实验步骤,设计了如图装置(假设氢氧化钠溶液能完全吸收二氧化碳),打算测定二氧化碳中碳、氧元素的质量比。但测出的碳、氧元素的质量比总是小于 3:8,请分析可能的原因是:气体经过氢氧化钠溶液带出水蒸气,使测得的二氧化碳质量偏小。
故填:气体经过氢氧化钠溶液带出水蒸气,使测得的二氧化碳质量偏小。
考试时间:90分钟;命题人:化学教研组
考生注意:
1、本卷分第I卷(选择题)和第Ⅱ卷(非选择题)两部分,满分100分,考试时间90分钟
2、答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、班级填写在试卷规定位置上
3、答案必须写在试卷各个题目指定区域内相应的位置,如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带,不按以上要求作答的答案无效。
第I卷(选择题 30分)
一、单选题(10小题,每小题3分,共计30分)
1、二氧化硅(SiO2)是制备电子芯片硅的原料。SiO2中硅元素的化合价是
A.+1 B.+2 C.+4 D.-2
2、下列物质的化学式书写正确的是
A.铁FE B.氯化钠NaCl2 C.硫酸铜CuSO4 D.氧化铝AlO
3、2021年世界水日主题是“珍惜水、爱护水“。下列说法正确的是
A.地球上的淡水资源十分丰富,可以任意随便用水
B.部分结冰的蒸馏水属于混合物
C.水是由氢分子和氧原子构成的
D.硬水中含有较多可溶性钙、镁化合物
4、下列化学用语书写正确的是
A.氯离子:Cl-1 B.2 个二氧化硫分子:2SO2
C.60 个碳原子:C60 D.氢氧化铝:AlOH3
5、下列物质属于氧化物的是
A.O2 B.H2SO4 C.CaO D.NH4NO3
6、下列物质的化学式书写正确的是
A.过氧化氢 B.干冰: C.氧化铁 D.氯化钙
7、下列化学用语使用规范的是
A.8个硫原子:S8 B.氧化铁:Fe2O3
C.干冰中碳元素的化合价: D.硫酸根离子:
8、正确的实验操作是科学探究成功的基础。下列操作正确的是
A.配制氯化钠溶液 B.铁丝在氧气中燃烧
C.倾倒液体 D.蒸发溶液
9、下列物质间的相互转化,不能一步实现的是
A. B.
C. D.
10、2021年3月22日—28日是第三十四届“中国水周”。其主题为“深入贯彻新发展理念,推进水资源集约安全利用”。水是生命之源,关于水的说法不正确的是
A.可以用肥皂水区分硬水和软水
B.水由液态变为气态时,分子间间隔变大
C.电解水实验中正负极得到的气体质量之比为1:2
D.明矾可以净水是因为其溶于水生成的胶状物能吸附悬浮的杂质
第Ⅱ卷(非选择题 70分)
二、填空题(5小题,每小题4分,共计20分)
1、建立“宏观—微观—符号”之间的联系,是学习化学的重要方法。根据图示回答下列问题;
(1)图甲所示元素的相对原子质量为______。
(2)图乙所示微粒的符号为______。
(3)图丙所示微粒构成的物质中氮元素的化合价为______。
2、 “青花瓷”是最具代表性的中国瓷器。绘制青花瓷纹饰的原料中主要含有氧化钴(CoO)。钴元素符号为Co,在元素周期表中与铁元素同位于第4周期、第Ⅷ族。
(1)铁元素与钴元素是不同种元素,原因是________;两者具有相似的化学性质是因为原子的___________;
(2)亚铁离子在化学变化中易_________(填“得到”或“失去”)电子形成铁原子;
(3)钴的化合物钴酸锂(化学式为 LiCoO2,锂元素化合价为+1)常用作手机电池的正极材料,钴酸锂中钴元素的化合价为________。
3、冬季容易在路面产生积雪和冰,为减少积雪和冰对交通的影响,“融雪剂”发挥了一定的作用。其中一种融雪效果好、无污染的“融雪剂”的主要成份是醋酸钾(CH3COOK)。请回答:
(1)在醋酸钾分子中,钾元素的化合价是_______,其相对分子质量为_____。
(2)醋酸钾中C、H、O元素的质量比为______,钾元素的质量分数为_____(保留两位有效数字)。
4、一种新物质,其分子结构像一只小狗(如图),于是取名叫小狗烯,小狗烯的化学式为(C26H26)请计算:
小狗烯属于________(填“氧化物”或“化合物”)。“小狗烯”的相对分子质量是________。其中碳元素和氢元素的质量比________(填最简整数比)。2.6g“小狗烯”中含碳元素_______g。
5、用化学用语填空:
(1)氦气______;
(2)硫酸铝______;
(3)亚铁离子______;
(4)17号元素离子的结构示意图______。
三、计算题(5小题,每小题8分,共计40分)
1、疫情期间,使用的过氧乙酸(CH3 COOOH)是国家卫健委公布的消毒剂之一。将计算结果填在横线上。
(1)过氧乙酸分子中,碳、氢、氧三种原子的个数比是______。
(2)过氧乙酸的相对分子质量是______。
(3)过氧乙酸中,碳、氢、氧三种元素的质量比是______。
2、国家卫健委高级专家李兰娟院士透露,新型冠状病毒怕酒精,不耐高温等。按照以往对冠状病毒的经验,乙醚、乙醇(俗名酒精)化学式为(C2H6O),等含氯消毒剂均可灭活病毒。
(1)乙醇分子中碳原子和氢原子的个数比为______。
(2)已知一个碳12原子质量是mg,一个氧原子质量为ng,其中氧原子有X个质子,则该氧原子的相对原子质量为______,该氧原子中的中子数为______。
(3)92kg的乙醇中,含有氧元素的质量为多少kg?(列式并计算)
3、少数不法商贩对海产品的保鲜以及室内装修材料中都涉及到甲醛,其化学式为CH2O,是一种易挥发、有强烈刺激性气味的有机物.回答下列有关问题:
(1)甲醛的相对分子质量是_________。
(2)甲醛中H、O两种元素的质量比为________________。
(3)甲醛中碳元素的质量分数为_______________。
4、如图是某品牌补铁剂的标签。请回答:
(1)富马酸亚铁中含有_________种元素,其中碳、氢、氧原子的个数比为_______。
(2)富马酸亚铁的相对分子质量为_______,其中碳、氢元素的质量比为_________。
(3)已知富马酸亚铁颗粒中只有富马酸亚铁含铁元素,求1包富马酸亚铁颗粒中含铁元素的质量为______g。(写出计算过程,结果保留小数点后两位)
5、咖啡因是一种中枢神经兴奋剂,能够暂时的驱走睡意并恢复精力,有咖啡因成分的咖啡、茶、饮料及能量饮料十分畅销。因此,咖啡因也是世界上最普遍被使用的精神药物,其化学式为C8H10N4O2,完成填空
(1)咖啡因由___________种元素组成,咖啡因的相对分子质量为___________;
(2)咖啡因中碳元素与氢元素的质量比为___________(最简比);
(3)97g咖啡因中碳元素的质量为___________g。
四、实验探究(1小题,每小题10分,共计10分)
1、某课外小组利用H2 还原CuO 粉末的实验测定水的组成,图甲是测定装置的示意图。
(设计实验步骤)
①连接好装置,并检查气密性
②装入药品,打开弹簧夹,通入一段时间氢气后关闭弹簧夹
③分别称量装置C、D 的质量
④再次打开弹簧夹,通入氢气后,加热装置C
⑤待C 中固体全部变为红色后,停止加热
⑥继续通入氢气,待装置C 恢复至室温后,关闭弹簧夹
⑦再次分别称量装置C、D 的质量
(完善实验设计)经过讨论同学们认为,为了提高实验的安全性,步骤④加热装置 C 前, 应在 E 导管口收集一试管气体后,进行如图乙所示操作,若操作过程中听到尖锐爆鸣声, 则反应的化学方程式是_____。
(进行实验)该小组的同学按上述步骤进行实验,并进行了实验数据(C 中玻璃管质量为60.0g)
装置C 的质量/g 装置D 的质量/g
反应前 68.0 158.2
反应后 67.2 159.1
(1)小组同学利用锌粒和稀硫酸反应制氢气,请写出反应的化学方程式_____。在锌与稀硫酸反应的过程中,若夹紧弹簧夹,则A 中反应停止,其原理是_____。
(2)步骤⑥的目的是_____。
(数据处理)
(1)根据上表中数据,水中氢、氧元素的质量比等于_____(使用原始数据列式,不用计算出结果)。
(拓展探究)该小组同学参考上述实验原理,模仿实验步骤,设计了如图装置(假设氢氧化钠溶液能完全吸收二氧化碳),打算测定二氧化碳中碳、氧元素的质量比。但测出的碳、氧元素的质量比总是小于 3:8,请分析可能的原因_____。
-参考答案-
一、单选题
1、C
【详解】
二氧化硅中氧元素化合价为-2价,设硅元素化合价为x,根据化合物中正负化合价代数为0,则有x+(-2)×2=0,得x=+4价;
故选C。
2、C
【分析】
元素符号的书写:一个字母大写,两个字母第一个字母大写,第二个字母小写。化合物的化学式书写:显正价的元素其符号写在左边,显负价的写在右边,化合价的绝对值交叉约简,得化学式右下角的数字,数字为1时不写。
【详解】
铁:Fe; 氯化钠:NaCl;硫酸铜:CuSO4 ;氧化铝:Al2O3。
故选C。
3、D
【详解】
A.地球上的水资源十分丰富,但淡水资源有限,可直接利用更少,所以不可以任意随便用水,选项说法错误。
B.部分结冰的蒸馏水中也只有水,所以属于纯净物,选项说法错误。
C.水是由水分子构成的,水分子由氢原子和氧原子构成,选项说法错误。
D.硬水中含有较多可溶性钙、镁化合物,选项说法正确。
故选:D
4、B
【详解】
A、离子的表示方法,在表示该离子的元素符号或原子团的右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个单位电荷时,1要省略。氯离子可表示为Cl-,故选项化学用语书写错误;
B、由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则2个二氧化硫分子可表示为2SO2,故选项化学用语书写正确;
C、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故60个碳原子可表示为60C,故选项化学用语书写错误;
D、氢氧化铝中铝元素显+3价,氢氧根显-1价,其化学式为Al(OH)3,故选项化学用语书写错误。
故选:B。
5、C
【详解】
氧化物是指由两种元素组成,并且其中一种是氧元素的化合物。
A、O2只由一种元素组成,属于单质,不符合题意;
B、H2SO4由三种元素组成,不属于氧化物,不符合题意;
C、CaO由两种元素组成,并且其中一种是氧元素,属于氧化物,符合题意;
D、NH4NO3由三种元素组成,不属于氧化物,不符合题意。
故选C。
6、A
【详解】
A、过氧化氢化学式书写正确,正确;
B、干冰为固体二氧化碳CO2,错误;
C、氧化铁化学式为Fe2O3,错误;
D、氯化钙化学式为CaCl2,错误。
故选A。
7、B
【详解】
A、表示原子的个数应该在原子前面加上数字,8S,故不符合题意;
B、氧化铁中铁的化合价为+3价,氧的化合价为-2价,所以化学式为Fe2O3,故符合题意;
C、化合价在写的时候写到元素正上方,符号应写在数字之前,故不符合题意;
D、硫酸根粒子电荷数标在离子团的右上角,数字在前,符号在后,表示为,故不符合题意。
故选:B。
【点睛】
8、D
【详解】
A、量筒只能量取液体体积,不能配制溶液,故图示操作不正确;
B、为防止铁丝在氧气中燃烧时,高温熔化物溅落,使集气瓶炸裂,瓶底需要放少量水或细沙,故图示操作不正确;
C、向试管中倒入液体,试管倾斜,瓶塞要倒放,标签朝向手心,瓶口紧挨试管口,图中试管未倾斜,瓶塞未倒放,标签未朝向手心,瓶口未紧挨试管口,故图示操作不正确;
D、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,故图示操作正确。
故选D。
9、D
【详解】
A、氢气燃烧和氧气反应生成水,水电解生成氧气,能一步实现,故A不符合题意;
B、一氧化碳燃烧生成二氧化碳,二氧化碳和碳高温生成一氧化碳,可一步实现,故B不符合题意;
C、铁在氧气中燃烧生成了四氧化三铁,一氧化碳还原四氧化三铁生成铁,可一步实现,故C不符合题意;
D、碳在氧气(不足)中燃烧生成一氧化碳,一氧化碳不能一步生成碳单质,不可一步实现,故D符合题意。
故选D。
10、C
【详解】
A、硬水加肥皂水泡沫少,浮渣多,软水加肥皂水泡沫多,浮渣少,可以用肥皂水区分硬水和软水,正确。
B、水由液态变为气态时,分子间间隔变大,正确。
C、电解水实验中正负极得到的气体体积之比为1:2,不是质量比,错误。
D、明矾可以净水是因为其溶于水生成的胶状物能吸附悬浮的杂质,正确。
故选:C。
二、填空题
1、
(1)140.1
(2)S2-
(3)-3
【分析】
(1)
元素周期表小方格最下方数字,表示相对原子质量,故填:140.1。
(2)
图乙质子数16,属于硫元素,核外电子数大于核电荷数,属于硫离子,故填:S2-。
(3)
氢元素+1价,设氮元素化和价为x,根据化合价代数和为零,x+(+1)3=0,x=-3,故填:-3。
2、
(1) 质子数不同 最外层电子数相同
(2)得到
(3)+3
【解析】
(1)
同一元素质子数不同,铁元素与钴元素是不同种元素,原因是质子数;元素化学性质与原子最外层电子数有密切关系,两者具有相似的化学性质是因为原子的最外层电子数相同。
(2)
亚铁离子是铁原子失去电子后形成的,故在化学变化中得到电子形成铁原子;
(3)
LiCoO2中锂元素化合价为正一价、氧元素化合价为负二价,化合物中正负化合价代数和为零;则钴元素的化合价为+3。
3、
(1) +1 98
(2) 24∶3∶32 40%
【分析】
(1)
钾元素在化合物中一般显+1价,在醋酸钾分子中,钾元素的化合价是+1,其相对分子质量为。
(2)
醋酸钾中C、H、O元素的质量比为;钾元素的质量分数为。
4、化合物 338 12:1 2.4
【详解】
由化学式可知,小狗烯中不含氧元素,不符合氧化物的特点,不属于氧化物,小狗烯是碳元素与氢元素组成的纯净物,属于化合物,故填化合物;
小狗烯的相对分子质量=12×26+1×26=338,故填338;
小狗烯中碳元素和氢元素的质量比=(12×26):(1×26)=12:1,故填12:1;
2.6g“小狗烯”中含碳元素的质量=2.6g××100%=2.4g,故填2.4。
5、
(1)
(2)
(3)
(4)
【分析】
(1)
稀有气体的化学式用元素符号表示,氦气用表示。
(2)
硫酸铝由铝离子和硫酸根离子构成。铝显+3价,硫酸根显-2价。所以硫酸铝用表示。
(3)
亚铁离子带两个正电荷,所以用表示。
(4)
17号元素离子的结构示意图中17个质子,18个电子,最外层8个电子。如图所示
【点睛】
稀有气体的化学式用元素符号表示,氦气用表示。
三、计算题
1、
(1)2:4:3
(2)76
(3)6:1:12
【解析】
(1)
根据过氧乙酸的化学式CH3COOOH可知,一个过氧乙酸分子中含有2个碳原子,4个氢原子和3个氧原子,故碳、氢、氧的原子个数比为2:4:3;
(2)
根据过氧乙酸化学式可知,其相对分子质量为,故填76;
(3)
根据化学式可知,碳、氢、氧的三种元素质量比比为,故填6:1:12。
2、
(1)1:3
(2) -X
(3)32kg
含有氧元素的质量92Kg×=32kg
答:氧元素质量32kg。
【解析】
(1)
乙醇分子中碳原子和氢原子的个数比为2:6=1:3,故填:1:3。
(2)
氧原子的相对原子质量为 ,中子数=相对原子质量-质子数,-X,故填:;-X。
(3)
见答案
3、
(1)30
(2)1:8
(3)40%
【分析】
相对分子质量是组成分子的各原子的相对原子质量的总和;C的相对原子质量为12,H的相对原子质量为1,O的相对原子质量为16。
(1)
由甲醛的化学式可知,甲醛由碳、氢、氧元素组成,其相对分子质量:12+12+16=30,故填:30;
(2)
甲醛中氢、氧元素的质量比为: ,故填:1:8;
(3)
甲醛中碳元素的质量分数= ,故填:40%。
4、
(1) 4四 2:1:2
(2) 170 24:1
(3)0.07g
1包富马酸亚铁颗粒中含铁元素的质量为0.2g××100%≈0.07g;
答:1包富马酸亚铁颗粒中含铁元素的质量为0.07g。
【解析】
(1)
物质由元素组成,富马酸亚铁由碳、氢、铁、氧四种元素组成,1个富马酸亚铁分子中含有4个碳原子、2个氢原子、1个铁原子和4个氧原子,所以碳、氢、氧原子的个数比为4:2:4=2:1:2,故填: 4或四;2:1:2;
(2)
富马酸亚铁的相对分子质量为12×4+1×2+56+16×4=170;碳、氢元素的质量比为(12×4):(1×2) =24:1,故填:170;24:1;
(3)
见答案。
5、
(1) 四 194
(2)48:5
(3)48g
【解析】
(1)
咖啡因由C、H、O、N四种元素组成,C8H10N4O2的相对分子质量为:;
(2)
由咖啡因分子式,咖啡因中碳元素与氢元素的质量比为(12×8):(1×10)=48:5;
(3)
97g咖啡因中碳元素的质量为。
四、实验探究
1、2H2+O22H2O Zn+H2SO4=ZnSO4+H2↑ 关闭弹簧夹后,试管内生成气体,气压增大,将液体压回长颈漏斗,固液分离,反应停止 让生成的水蒸气全部进入D装置,使其被充分吸收减少误差;或防止空气进入C中,使铜又被氧化造成误差;或答防止空气中的水蒸气被吸入D中造成误差 [(159.1-158.2)-(68.0-67.2)]:(68.0-67.2) 气体经过氢氧化钠溶液带出水蒸气,使测得的二氧化碳质量偏小
【详解】
[完善实验设计]
氢气在空气中燃烧生成水,反应的化学方程式是:2H2+O22H2O。故填:2H2+O22H2O;
[进行实验]
(1)锌和稀硫酸反应生成氢气和硫酸锌;在锌与稀硫酸反应的过程中,若夹紧弹簧夹,则A 中反应停止,其原理是关闭弹簧夹后,试管内生成气体,气压增大,将液体压回长颈漏斗,固液分离,反应停止。故填:Zn+H2SO4=ZnSO4+H2↑;关闭弹簧夹后,试管内生成气体,气压增大,将液体压回长颈漏斗,固液分离,反应停止;
(2)步骤⑥的目的是让生成的水蒸气全部进入D装置,使其被充分吸收减少误差。故填:让生成的水蒸气全部进入D装置,使其被充分吸收减少误差。
[数据处理]
(1)根据上表中数据,水中氢、氧元素的质量比等于[(159.1-158.2)-(68.0-67.2)]:(68.0-67.2),故填:[(159.1-158.2)-(68.0-67.2)]:(68.0-67.2);
[拓展探究]该小组同学参考上述实验原理,模仿实验步骤,设计了如图装置(假设氢氧化钠溶液能完全吸收二氧化碳),打算测定二氧化碳中碳、氧元素的质量比。但测出的碳、氧元素的质量比总是小于 3:8,请分析可能的原因是:气体经过氢氧化钠溶液带出水蒸气,使测得的二氧化碳质量偏小。
故填:气体经过氢氧化钠溶液带出水蒸气,使测得的二氧化碳质量偏小。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
