3.4 第2课时 羧酸衍生物 学案(含答案) 2023-2024学年高二化学人教版(2019)选择性必修第三册
文档属性
| 名称 | 3.4 第2课时 羧酸衍生物 学案(含答案) 2023-2024学年高二化学人教版(2019)选择性必修第三册 |

|
|
| 格式 | docx | ||
| 文件大小 | 398.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-10 00:00:00 | ||
图片预览




文档简介
3.4第2课时 羧酸衍生物
【学习目标】
1.了解酯的组成和结构特点。
2.了解酯的物理性质及存在。
3.掌握乙酸乙酯的结构特点和主要性质,理解乙酸乙酯水解反应的基本规律。
4.了解油脂的概念、组成和结构特点。
5.掌握油脂的主要化学性质及油脂的氢化和皂化反应等。
6.初步了解肥皂去污原理和合成洗涤剂的应用。
7.了解胺、酰胺的组成、结构特点和化学性质。
【自主预习】
1.酯
(1)酯:羧酸分子中羧基中的 被 取代后的产物,可简写为 ,官能团为。
(2)酯的物理性质
(3)酯的化学性质
+H2O+R'OH
+NaOH+R'OH
(4)酯在生产、生活中的应用
①日常生活中的饮料、糖果和糕点等常使用酯类香料。
②酯还是重要的化工原料。
2.油脂
(1)组成
油脂是 和 的统称,都是 和 形成的酯,属于 类化合物,含 三种元素。
(2)结构特点
结构通式:
(3)分类
(4)化学性质
①油脂的氢化(硬化)
如油酸甘油酯与H2反应的化学方程式为 。
②水解反应
a.酸性条件下
如硬脂酸甘油酯的水解反应方程式为 。
b.碱性条件下——皂化反应
如硬脂酸甘油酯的水解反应方程式为 。
碱性条件下油脂的水解程度比酸性条件下水解程度 。
3.肥皂的制备
肥皂的生产流程如下所示:
4.胺和酰胺
(1)胺是烃基取代 中的氢原子而形成的化合物。
(2)酰胺是 分子中 中的 被 取代而形成的化合物。
【答案】
1.(1)—OH —OR' RCOOR' (2)难 易
2.(1)油 脂肪 高级脂肪酸 甘油 酯 C、H、O
(4)①+3H2
②a.+3H2O3C17H35COOH+
b.+3NaOH3C17H35COONa+ 大
4.(1)氨分子 (2)羧酸 羧基 羟基 氨基
【效果检测】
1.判断正误(正确的打“√”,错误的打“×”)。
(1)酯、胺和酰胺都是羧酸衍生物。 ( )
(2)酯和酰胺在酸性条件下水解均生成羧酸。 ( )
(3)油脂是由高级脂肪酸与任意醇通过酯化反应生成的。 ( )
(4)油脂的水解反应为皂化反应。 ( )
(5)胺和酰胺的官能团都是氨基—NH2。 ( )
(6)天然油脂都是混合物,没有固定的熔、沸点。 ( )
(7)天然油脂都是高分子化合物。 ( )
(8)植物油、动物脂肪和矿物油都是油脂。 ( )
(9)所有的油脂在酸性条件下或碱性条件下都能发生水解反应。 ( )
(10)能发生氢化反应的油脂都能使酸性高锰酸钾溶液褪色。 ( )
【答案】(1)× (2)√ (3)× (4)× (5)× (6)√ (7)× (8)× (9)√ (10)√
2.乙酸乙酯分子结构中的官能团是什么 试写出该官能团的结构式。
【答案】(酯基)。
3.油脂和酯有什么关系
【答案】油脂属于酯类,但酯不一定是油脂。
4.如何鉴别植物油和矿物油
【答案】利用植物油能在碱性条件下水解,向样品中加入含酚酞的NaOH溶液,加热,溶液颜色变浅的为植物油,无明显现象的是矿物油。
【合作探究】
任务1 酯类
情境导入 我们在日常生活中经常吃一些不同的水果,这些水果除了有酸味、甜味外,还有不同的清香味,这些香味来源于酯类。低级酯存在于各种水果和花草中。如苹果里含有戊酸戊酯,菠萝里含有丁酸乙酯,香蕉里含有乙酸异戊酯等。
问题生成
1.酯类的结构特点是什么 其官能团的名称是什么
【答案】酯类的通式可写成RCOOR',酯的官能团是。
2.低级酯具有怎样的物理性质
【答案】低级酯是具有芳香气味的液体,密度一般比水的小,易溶于有机溶剂。
3.酯类水解反应具有什么特点
【答案】酯的水解在酸性条件下是可逆的,在碱性条件下是不可逆的。
4.酯的水解反应和酯化反应是否属于同一反应类型
【答案】酯的水解反应和酯化反应均属于取代反应。
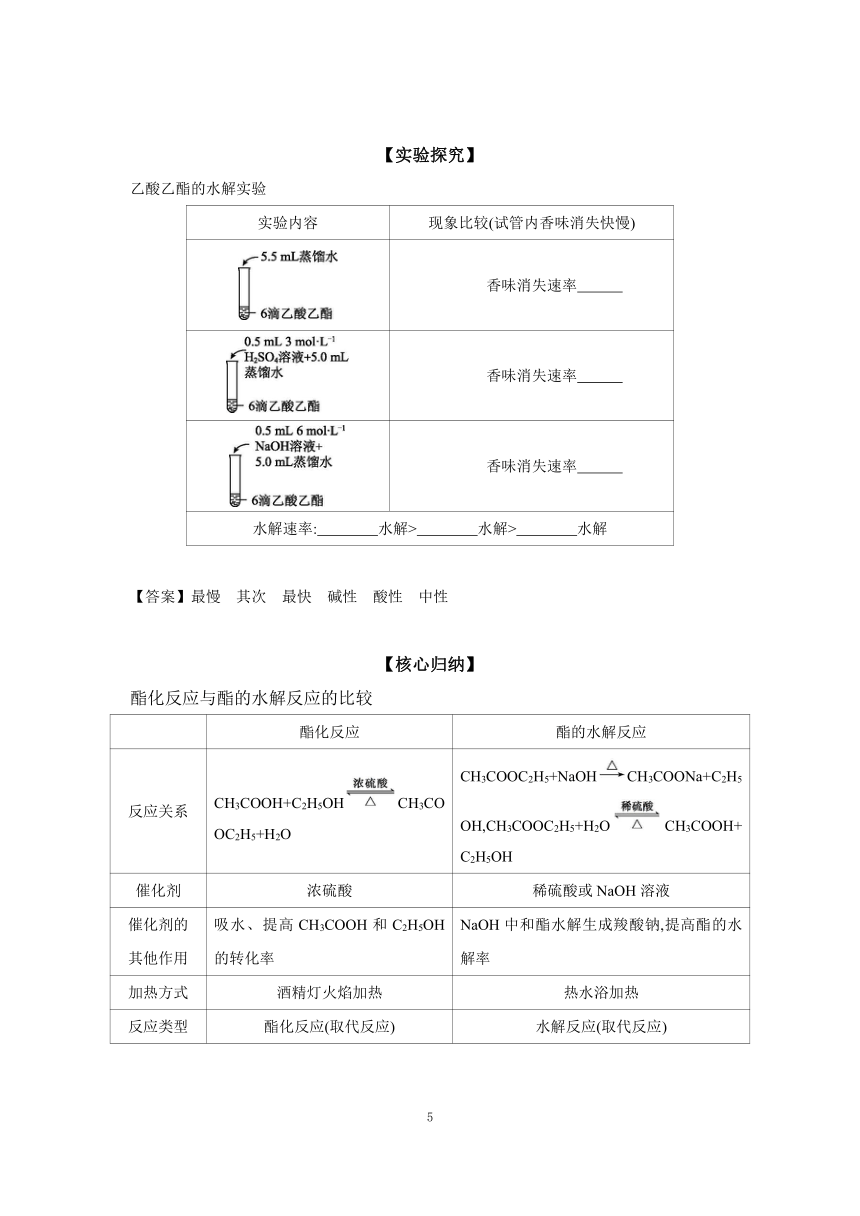
【实验探究】
乙酸乙酯的水解实验
实验内容 现象比较(试管内香味消失快慢)
香味消失速率
香味消失速率
香味消失速率
水解速率: 水解> 水解> 水解
【答案】最慢 其次 最快 碱性 酸性 中性
【核心归纳】
酯化反应与酯的水解反应的比较
酯化反应 酯的水解反应
反应关系 CH3COOH+C2H5OHCH3COOC2H5+H2O CH3COOC2H5+NaOHCH3COONa+C2H5OH,CH3COOC2H5+H2OCH3COOH+C2H5OH
催化剂 浓硫酸 稀硫酸或NaOH溶液
催化剂的 其他作用 吸水、提高CH3COOH和C2H5OH的转化率 NaOH中和酯水解生成羧酸钠,提高酯的水解率
加热方式 酒精灯火焰加热 热水浴加热
反应类型 酯化反应(取代反应) 水解反应(取代反应)
【典型例题】
【例1】某有机物具有下列性质:①难溶于水,能发生银镜反应;②滴入紫色石蕊溶液不变色;③加入少量碱液并滴入酚酞溶液,加热后红色消失。则原有机物可能是下列物质中的( )。
A.甲酸乙酯 B.乙酸甲酯
C.乙醛 D.甲酸
【答案】A
【解析】乙醛、甲酸都易溶于水,酯难溶于水;能发生银镜反应的有机物,其分子结构中一定含有醛基;滴入紫色石蕊溶液不变色,说明该有机物不含有羧基;加入少量碱液并滴入酚酞溶液,加热后红色消失,说明该有机物能与碱溶液发生反应,A项符合题意。
【例2】乙酸乙酯在NaOH的重水(D2O)溶液中加热水解,其产物是( )。
A.CH3COOD、C2H5OD
B.CH3COONa、C2H5OD、HOD
C.CH3COONa、C2H5OH、HOD
D.CH3COONa、C2H5OD、H2O
【答案】B
【解析】乙酸乙酯的碱性水解可分为两步,乙酸乙酯先与D2O反应,生成CH3COOD和C2H5OD,然后CH3COOD再与NaOH反应,生成物为CH3COONa和HOD。
【例3】下列关于分子式为C4H8O2的有机物的同分异构体的说法中不正确的是( )。
A.属于酯类的有4种
B.属于羧酸类的有2种
C.存在分子中含有六元环的同分异构体
D.既含有羟基又含有醛基的有3种
【答案】D
【解析】分子式为C4H8O2的有机物属于酯类的共有4种,分别是HCOOCH2CH2CH3、、CH3COOC2H5、CH3CH2COOCH3,A项正确;分子式为C4H8O2的有机物属于羧酸类的共有2种,分别是CH3CH2CH2COOH、,B项正确;分子式为C4H8O2的有机物中含有六元环的是等,C项正确;分子式为C4H8O2的有机物属于羟基醛的有、、HOCH2CH2CH2CHO、、,共5种,D项不正确。
【例4】下列方法中,能将有机化合物转变为的有( )。
①跟足量NaOH溶液共热后,通入CO2直至过量
②与稀硫酸共热后,加入足量Na2CO3溶液
③与稀硫酸共热后,加入足量NaOH溶液
④与稀硫酸共热后,加入足量NaHCO3溶液
A.①② B.②③ C.③④ D.①④
【答案】D
【解析】①跟足量NaOH溶液共热后生成,再通入二氧化碳直至过量,二氧化碳和水与酚钠反应生成,符合题意;②与稀硫酸共热后生成邻羟基苯甲酸,加入足量Na2CO3溶液,羧基和酚羟基都与碳酸钠反应,生成,不符合题意;③与稀硫酸共热后生成邻羟基苯甲酸,加入足量NaOH溶液,羧基和酚羟基都与NaOH反应,生成,不符合题意;④与稀硫酸共热后生成邻羟基苯甲酸,加入足量NaHCO3溶液,羧基会与碳酸氢钠反应而酚羟基不与碳酸氢钠反应,生成,符合题意。
任务2 油脂
情境导入 唐代诗人李商隐《无题》一诗:“春蚕到死丝方尽,蜡炬成灰泪始干”中“蜡炬”描述的是古代蜡烛(动植物油脂)燃烧的过程。现代生活中,许多美味的食物都富含油脂,油脂被称为人体的备用“油箱”,油脂是人类的主要食物之一,是人体中重要的能源物质。可也有不少人谈脂色变,肥胖、高血脂、脂肪肝这些也和油脂有关。
问题生成
1.油和脂有哪些区别和联系
【答案】植物油通常呈液态,叫作油;动物油通常呈固态,叫作脂肪,油和脂肪统称为油脂。油脂属于酯。
2.联系生活实际,思考油脂有哪些物理性质
【答案】油脂的密度比水小,不溶于水,易溶于有机溶剂。工业上根据这一性质,常用有机溶剂来提取植物种子里的油。油脂本身也是一种较好的溶剂。
3.油脂是否是有机高分子
【答案】油脂是不同种高级脂肪酸甘油酯的混合物。油脂的相对分子质量一般小于10000,不属于高分子化合物。
4.组成油脂的常见高级脂肪酸有哪些
【答案】饱和高级脂肪酸:硬脂酸(十八酸)C17H35COOH;软脂酸(十六酸)C15H31COOH;不饱和高级脂肪酸:油酸(9-十八碳烯酸)C17H33COOH;亚油酸(9,12-十八碳二烯酸)C17H31COOH。
【核心归纳】
脂肪、油、矿物油三者的比较
物质 油脂 矿物油
脂肪 油
组成 多种高级脂肪酸的甘油酯 多种烃(石油及其分馏产品)
含饱和烃基多 含不饱和烃基多
性质 固态或半固态 液态 液态
具有酯的性质,能水解,有的油脂兼有烯烃的性质 具有烃的性质,不能水解
鉴别 加含酚酞的NaOH溶液,加热,红色变浅,不再分层 加含酚酞的NaOH溶液,加热,无明显变化
用途 营养素可食用,化工原料如制肥皂、甘油 燃料、化工原料
【特别提醒】①植物油与裂化汽油均含碳碳双键,能使溴水和酸性KMnO4溶液褪色。②区别油脂(酯)与矿物油(烃)的一般方法是加含酚酞的NaOH溶液,加热,红色变浅,最后不分层的为油脂(酯),否则为矿物油(烃)。
【典型例题】
【例5】植物油和石蜡油虽然都称为“油”,但从化学组成和分子结构看,它们是完全不同的。下列说法中正确的是( )。
A.植物油属于纯净物,石蜡油属于混合物
B.植物油属于酯类,石蜡油属于烃类
C.植物油属于有机化合物,石蜡油属于无机物
D.植物油属于高分子化合物,石蜡油属于小分子化合物
【答案】B
【解析】植物油、石蜡油都属于混合物、有机化合物,都不属于高分子化合物。
【例6】能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是( )。
A.点燃,能燃烧的是矿物油
B.测定沸点,有固定沸点的是矿物油
C.加入水中,浮在水面上的是地沟油
D.加入足量氢氧化钠溶液共热,不分层的是地沟油
【答案】D
【解析】地沟油的主要成分是高级脂肪酸甘油酯,主要是从饭店剩菜残渣中提取的,与矿物油一样,也能燃烧,A项错误;矿物油和地沟油都是混合物,都没有固定的沸点,B项错误;矿物油和地沟油的密度都小于水且都不溶于水,加入水中都会浮在水面上,C项错误;地沟油能与氢氧化钠溶液反应生成溶于水的甘油和高级脂肪酸钠,溶液不分层,而矿物油不能与氢氧化钠溶液反应,溶液分层,D项正确。
任务3 酰胺
情境导入
甲胺(CH3NH2)与乙酰胺(CH3CONH2)都是重要的化工原料。近几年烟酰胺火遍了全网,作为美白爱好者护肤宝库里必备的一款护肤品,它的美白功效一直以来都广受好评。烟酰胺的结构简式如图所示。
问题生成
1.甲胺(CH3NH2)与乙酰胺(CH3CONH2)分子中均有—NH2,二者互为同系物吗 为什么
【答案】不是。因为二者不是同类物质,结构不相似,且不相差若干个CH2原子团。
2.烟酰胺属于胺类物质吗 其分子中含有的含氧官能团有哪些
【答案】烟酰胺不属于胺,属于酰胺。分子中含有酰胺基。
3.酰胺与酯类的化学性质有什么相似性
【答案】二者均可以在酸性、碱性条件下发生水解反应。
4.烟酰胺能水解吗 其酸性水解、碱性水解的产物是什么
【答案】烟酰胺能水解。酸性水解的产物为和铵盐;碱性水解的产物为和氨气。
【核心归纳】
1.酰胺的化学性质
(1)在酸性(HCl溶液)条件下水解的化学方程式:RCONH2+H2O+HClRCOOH+NH4Cl。
(2)在碱性(NaOH溶液)条件下水解的化学方程式:RCONH2+NaOHRCOONa+NH3↑。
2.氨、胺、酰胺和铵盐的比较
物质 氨 胺(甲胺)
组成元素 N、H C、N、H
结构式
化学性质 与酸反应生成铵盐 与酸反应生成盐
用途 化工原料 化工原料
物质 酰胺(乙酰胺) 铵盐(NH4Cl)
组成元素 C、N、O、H N、H、Cl
结构式
化学性质 水解反应:酸性时生成羧酸与铵盐,碱性时生成羧酸盐和NH3 与碱反应生成盐和NH3
用途 化工原料和溶剂 化工原料、化肥
[注意]酰胺基的结构简式为,R、R'可以是H或烃基。
【典型例题】
【例7】毒奶粉事件曾一度震惊全国,有毒添加剂主要是奶粉中含有的三聚氰胺(其结构如下所示)。下列关于三聚氰胺分子的说法中正确的是( )。
A.三聚氰胺分子中所有碳原子均采取sp3杂化
B.一个三聚氰胺分子中共含有15个σ键
C.三聚氰胺的分子式为C3N3H6
D.三聚氰胺分子中同时含有极性键和非极性键
【答案】B
【解析】三聚氰胺分子中的碳原子均为sp2杂化,A项错误;一个三聚氰胺分子中共含有6个N—H、6个N—C、3个
NC,共含有15个σ键,B项正确;三聚氰胺的分子式为C3N6H6,C项错误;三聚氰胺分子中不存在由同种元素的原子形成的共价键,故不存在非极性键,D项错误。
【例8】乙酰苯胺是磺胺类药物的原料,其结构如图所示,下列关于乙酰苯胺的说法中正确的是( )。
A.分子式为C8H9NO
B.乙酰苯胺是一种芳香烃
C.1 mol乙酰苯胺最多能和2 mol NaOH完全反应
D.分子中所有原子一定在同一平面上
【答案】A
【解析】A项,根据该有机物的结构简式可知,其分子式为C8H9NO,正确;B项,该有机物含有碳、氢、氧、氮元素,不属于芳香烃,错误;C项,断裂1 mol —CO—NH—,消耗1 mol NaOH,错误;D项,甲烷为正四面体结构,因该分子含有甲基,所以分子中所有原子一定不在同一平面上,错误。
【例9】食品中含有过量的(丙烯酰胺)可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述:①能使酸性高锰酸钾溶液褪色;②能发生加聚反应;③能与氢气发生加成反应;④能发生水解反应生成酸。其中正确的是( )。
A.①②④ B.②③④
C.①②③④ D.①③④
【答案】C
【解析】丙烯酰胺含有的官能团有碳碳双键、酮羰基、氨基,所以具有烯烃的性质,能发生加聚反应、加成反应,能使酸性高锰酸钾溶液褪色,丙烯酰胺分子中含有酰胺基,能发生水解反应生成酸,故选C项。
【灵犀一点】 酰胺水解的断键
水解时,中的C—N断裂,连接—OH形成羧基,连接—H形成氨基。
【随堂检测】
1.下列叙述中错误的是( )。
A.CH3COOCH3的名称是乙酸甲酯
B.酯的官能团是酯基
C.乙酸乙酯分子中含有甲基、乙基和酯基
D.酯的分子中一定有—COOH
【答案】D
【解析】酯的分子中一定有。
2.下列物质不属于酰胺的是( )。
A. B.
C. D.CH3CONH2
【答案】C
【解析】C项分子中只有氨基和羧基,不属于酰胺。
3.下列关于的叙述中不正确的是( )。
A.该物质能发生缩聚反应
B.该物质有7种不同化学环境的氢原子
C.该物质遇FeCl3溶液显紫色,1 mol该物质最多能与含1 mol Br2的溴水发生取代反应
D.1 mol该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为2∶2∶1
【答案】B
【解析】该物质含有氨基、羟基、羧基等多种官能团,因此可以发生缩聚反应,A项正确;该物质有8种不同化学环境的氢原子,B项错误;该物质含有酚羟基,所以遇FeCl3溶液显紫色,由于在苯环上羟基邻、对位只有一个H原子,所以1 mol该物质最多能与含1 mol Br2的溴水发生取代反应,C项正确;羧基、羟基可以与Na发生反应,羧基和酚羟基都可以与NaOH发生反应,只有羧基可以与NaHCO3发生反应,在该化合物的一个分子中含有一个酚羟基、一个羧基,所以1 mol该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为2∶2∶1,D项正确。
4.(2022·海南卷,双选)化合物“E7974”具有抗肿瘤活性,结构简式如下,下列有关该化合物说法正确的是( )。
A. 能使Br2的CCl4溶液褪色
B. 分子中含有4种官能团
C. 分子中含有4个手性碳原子
D. 1 mol该化合物最多与2 mol NaOH反应
【答案】AB
【解析】该物质分子中含有碳碳双键,能使Br2的CCl4溶液褪色,A项正确;由结构简式可知,分子中含有酰胺基、羧基、碳碳双键、次氨基,共4种官能团,其中有两个酰胺基,B项正确; “E7974”分子含有的手性碳原子如图所示,共3个,C项错误;分子中的酰胺基(2个)和羧基(1个)均能与NaOH溶液反应,故1 mol该化合物最多与3 mol NaOH反应,D项错误。
5.(2021·辽宁卷)我国科技工作者发现某“小分子胶水”(结构如图)能助力自噬细胞“吞没”致病蛋白。下列说法正确的是( )。
A.该分子中所有碳原子一定共平面
B.该分子能与蛋白质分子形成氢键
C.1 mol该物质最多能与3 mol NaOH反应
D.该物质能发生取代、加成和消去反应
【答案】B
【解析】该分子中2个苯环、碳碳双键所在的三个平面,平面间单键连接可以旋转,故所有碳原子可能共平面,A项错误;由题干信息可知,该分子中有羟基,能与蛋白质分子中的氨基之间形成氢键,B项正确;由题干信息可知,1 mol该物质含有2 mol酚羟基,可以消耗2 mol NaOH,含1 mol酚酯基,可以消耗2 mol NaOH,故最多能与4 mol NaOH反应,C项错误;该物质中含有酚羟基且邻对位上有H,能发生取代反应,含有苯环和碳碳双键,能发生加成反应,但没有卤素原子和醇羟基,不能发生消去反应,D项错误。
2
【学习目标】
1.了解酯的组成和结构特点。
2.了解酯的物理性质及存在。
3.掌握乙酸乙酯的结构特点和主要性质,理解乙酸乙酯水解反应的基本规律。
4.了解油脂的概念、组成和结构特点。
5.掌握油脂的主要化学性质及油脂的氢化和皂化反应等。
6.初步了解肥皂去污原理和合成洗涤剂的应用。
7.了解胺、酰胺的组成、结构特点和化学性质。
【自主预习】
1.酯
(1)酯:羧酸分子中羧基中的 被 取代后的产物,可简写为 ,官能团为。
(2)酯的物理性质
(3)酯的化学性质
+H2O+R'OH
+NaOH+R'OH
(4)酯在生产、生活中的应用
①日常生活中的饮料、糖果和糕点等常使用酯类香料。
②酯还是重要的化工原料。
2.油脂
(1)组成
油脂是 和 的统称,都是 和 形成的酯,属于 类化合物,含 三种元素。
(2)结构特点
结构通式:
(3)分类
(4)化学性质
①油脂的氢化(硬化)
如油酸甘油酯与H2反应的化学方程式为 。
②水解反应
a.酸性条件下
如硬脂酸甘油酯的水解反应方程式为 。
b.碱性条件下——皂化反应
如硬脂酸甘油酯的水解反应方程式为 。
碱性条件下油脂的水解程度比酸性条件下水解程度 。
3.肥皂的制备
肥皂的生产流程如下所示:
4.胺和酰胺
(1)胺是烃基取代 中的氢原子而形成的化合物。
(2)酰胺是 分子中 中的 被 取代而形成的化合物。
【答案】
1.(1)—OH —OR' RCOOR' (2)难 易
2.(1)油 脂肪 高级脂肪酸 甘油 酯 C、H、O
(4)①+3H2
②a.+3H2O3C17H35COOH+
b.+3NaOH3C17H35COONa+ 大
4.(1)氨分子 (2)羧酸 羧基 羟基 氨基
【效果检测】
1.判断正误(正确的打“√”,错误的打“×”)。
(1)酯、胺和酰胺都是羧酸衍生物。 ( )
(2)酯和酰胺在酸性条件下水解均生成羧酸。 ( )
(3)油脂是由高级脂肪酸与任意醇通过酯化反应生成的。 ( )
(4)油脂的水解反应为皂化反应。 ( )
(5)胺和酰胺的官能团都是氨基—NH2。 ( )
(6)天然油脂都是混合物,没有固定的熔、沸点。 ( )
(7)天然油脂都是高分子化合物。 ( )
(8)植物油、动物脂肪和矿物油都是油脂。 ( )
(9)所有的油脂在酸性条件下或碱性条件下都能发生水解反应。 ( )
(10)能发生氢化反应的油脂都能使酸性高锰酸钾溶液褪色。 ( )
【答案】(1)× (2)√ (3)× (4)× (5)× (6)√ (7)× (8)× (9)√ (10)√
2.乙酸乙酯分子结构中的官能团是什么 试写出该官能团的结构式。
【答案】(酯基)。
3.油脂和酯有什么关系
【答案】油脂属于酯类,但酯不一定是油脂。
4.如何鉴别植物油和矿物油
【答案】利用植物油能在碱性条件下水解,向样品中加入含酚酞的NaOH溶液,加热,溶液颜色变浅的为植物油,无明显现象的是矿物油。
【合作探究】
任务1 酯类
情境导入 我们在日常生活中经常吃一些不同的水果,这些水果除了有酸味、甜味外,还有不同的清香味,这些香味来源于酯类。低级酯存在于各种水果和花草中。如苹果里含有戊酸戊酯,菠萝里含有丁酸乙酯,香蕉里含有乙酸异戊酯等。
问题生成
1.酯类的结构特点是什么 其官能团的名称是什么
【答案】酯类的通式可写成RCOOR',酯的官能团是。
2.低级酯具有怎样的物理性质
【答案】低级酯是具有芳香气味的液体,密度一般比水的小,易溶于有机溶剂。
3.酯类水解反应具有什么特点
【答案】酯的水解在酸性条件下是可逆的,在碱性条件下是不可逆的。
4.酯的水解反应和酯化反应是否属于同一反应类型
【答案】酯的水解反应和酯化反应均属于取代反应。
【实验探究】
乙酸乙酯的水解实验
实验内容 现象比较(试管内香味消失快慢)
香味消失速率
香味消失速率
香味消失速率
水解速率: 水解> 水解> 水解
【答案】最慢 其次 最快 碱性 酸性 中性
【核心归纳】
酯化反应与酯的水解反应的比较
酯化反应 酯的水解反应
反应关系 CH3COOH+C2H5OHCH3COOC2H5+H2O CH3COOC2H5+NaOHCH3COONa+C2H5OH,CH3COOC2H5+H2OCH3COOH+C2H5OH
催化剂 浓硫酸 稀硫酸或NaOH溶液
催化剂的 其他作用 吸水、提高CH3COOH和C2H5OH的转化率 NaOH中和酯水解生成羧酸钠,提高酯的水解率
加热方式 酒精灯火焰加热 热水浴加热
反应类型 酯化反应(取代反应) 水解反应(取代反应)
【典型例题】
【例1】某有机物具有下列性质:①难溶于水,能发生银镜反应;②滴入紫色石蕊溶液不变色;③加入少量碱液并滴入酚酞溶液,加热后红色消失。则原有机物可能是下列物质中的( )。
A.甲酸乙酯 B.乙酸甲酯
C.乙醛 D.甲酸
【答案】A
【解析】乙醛、甲酸都易溶于水,酯难溶于水;能发生银镜反应的有机物,其分子结构中一定含有醛基;滴入紫色石蕊溶液不变色,说明该有机物不含有羧基;加入少量碱液并滴入酚酞溶液,加热后红色消失,说明该有机物能与碱溶液发生反应,A项符合题意。
【例2】乙酸乙酯在NaOH的重水(D2O)溶液中加热水解,其产物是( )。
A.CH3COOD、C2H5OD
B.CH3COONa、C2H5OD、HOD
C.CH3COONa、C2H5OH、HOD
D.CH3COONa、C2H5OD、H2O
【答案】B
【解析】乙酸乙酯的碱性水解可分为两步,乙酸乙酯先与D2O反应,生成CH3COOD和C2H5OD,然后CH3COOD再与NaOH反应,生成物为CH3COONa和HOD。
【例3】下列关于分子式为C4H8O2的有机物的同分异构体的说法中不正确的是( )。
A.属于酯类的有4种
B.属于羧酸类的有2种
C.存在分子中含有六元环的同分异构体
D.既含有羟基又含有醛基的有3种
【答案】D
【解析】分子式为C4H8O2的有机物属于酯类的共有4种,分别是HCOOCH2CH2CH3、、CH3COOC2H5、CH3CH2COOCH3,A项正确;分子式为C4H8O2的有机物属于羧酸类的共有2种,分别是CH3CH2CH2COOH、,B项正确;分子式为C4H8O2的有机物中含有六元环的是等,C项正确;分子式为C4H8O2的有机物属于羟基醛的有、、HOCH2CH2CH2CHO、、,共5种,D项不正确。
【例4】下列方法中,能将有机化合物转变为的有( )。
①跟足量NaOH溶液共热后,通入CO2直至过量
②与稀硫酸共热后,加入足量Na2CO3溶液
③与稀硫酸共热后,加入足量NaOH溶液
④与稀硫酸共热后,加入足量NaHCO3溶液
A.①② B.②③ C.③④ D.①④
【答案】D
【解析】①跟足量NaOH溶液共热后生成,再通入二氧化碳直至过量,二氧化碳和水与酚钠反应生成,符合题意;②与稀硫酸共热后生成邻羟基苯甲酸,加入足量Na2CO3溶液,羧基和酚羟基都与碳酸钠反应,生成,不符合题意;③与稀硫酸共热后生成邻羟基苯甲酸,加入足量NaOH溶液,羧基和酚羟基都与NaOH反应,生成,不符合题意;④与稀硫酸共热后生成邻羟基苯甲酸,加入足量NaHCO3溶液,羧基会与碳酸氢钠反应而酚羟基不与碳酸氢钠反应,生成,符合题意。
任务2 油脂
情境导入 唐代诗人李商隐《无题》一诗:“春蚕到死丝方尽,蜡炬成灰泪始干”中“蜡炬”描述的是古代蜡烛(动植物油脂)燃烧的过程。现代生活中,许多美味的食物都富含油脂,油脂被称为人体的备用“油箱”,油脂是人类的主要食物之一,是人体中重要的能源物质。可也有不少人谈脂色变,肥胖、高血脂、脂肪肝这些也和油脂有关。
问题生成
1.油和脂有哪些区别和联系
【答案】植物油通常呈液态,叫作油;动物油通常呈固态,叫作脂肪,油和脂肪统称为油脂。油脂属于酯。
2.联系生活实际,思考油脂有哪些物理性质
【答案】油脂的密度比水小,不溶于水,易溶于有机溶剂。工业上根据这一性质,常用有机溶剂来提取植物种子里的油。油脂本身也是一种较好的溶剂。
3.油脂是否是有机高分子
【答案】油脂是不同种高级脂肪酸甘油酯的混合物。油脂的相对分子质量一般小于10000,不属于高分子化合物。
4.组成油脂的常见高级脂肪酸有哪些
【答案】饱和高级脂肪酸:硬脂酸(十八酸)C17H35COOH;软脂酸(十六酸)C15H31COOH;不饱和高级脂肪酸:油酸(9-十八碳烯酸)C17H33COOH;亚油酸(9,12-十八碳二烯酸)C17H31COOH。
【核心归纳】
脂肪、油、矿物油三者的比较
物质 油脂 矿物油
脂肪 油
组成 多种高级脂肪酸的甘油酯 多种烃(石油及其分馏产品)
含饱和烃基多 含不饱和烃基多
性质 固态或半固态 液态 液态
具有酯的性质,能水解,有的油脂兼有烯烃的性质 具有烃的性质,不能水解
鉴别 加含酚酞的NaOH溶液,加热,红色变浅,不再分层 加含酚酞的NaOH溶液,加热,无明显变化
用途 营养素可食用,化工原料如制肥皂、甘油 燃料、化工原料
【特别提醒】①植物油与裂化汽油均含碳碳双键,能使溴水和酸性KMnO4溶液褪色。②区别油脂(酯)与矿物油(烃)的一般方法是加含酚酞的NaOH溶液,加热,红色变浅,最后不分层的为油脂(酯),否则为矿物油(烃)。
【典型例题】
【例5】植物油和石蜡油虽然都称为“油”,但从化学组成和分子结构看,它们是完全不同的。下列说法中正确的是( )。
A.植物油属于纯净物,石蜡油属于混合物
B.植物油属于酯类,石蜡油属于烃类
C.植物油属于有机化合物,石蜡油属于无机物
D.植物油属于高分子化合物,石蜡油属于小分子化合物
【答案】B
【解析】植物油、石蜡油都属于混合物、有机化合物,都不属于高分子化合物。
【例6】能区别地沟油(加工过的餐饮废弃油)与矿物油(汽油、煤油、柴油等)的方法是( )。
A.点燃,能燃烧的是矿物油
B.测定沸点,有固定沸点的是矿物油
C.加入水中,浮在水面上的是地沟油
D.加入足量氢氧化钠溶液共热,不分层的是地沟油
【答案】D
【解析】地沟油的主要成分是高级脂肪酸甘油酯,主要是从饭店剩菜残渣中提取的,与矿物油一样,也能燃烧,A项错误;矿物油和地沟油都是混合物,都没有固定的沸点,B项错误;矿物油和地沟油的密度都小于水且都不溶于水,加入水中都会浮在水面上,C项错误;地沟油能与氢氧化钠溶液反应生成溶于水的甘油和高级脂肪酸钠,溶液不分层,而矿物油不能与氢氧化钠溶液反应,溶液分层,D项正确。
任务3 酰胺
情境导入
甲胺(CH3NH2)与乙酰胺(CH3CONH2)都是重要的化工原料。近几年烟酰胺火遍了全网,作为美白爱好者护肤宝库里必备的一款护肤品,它的美白功效一直以来都广受好评。烟酰胺的结构简式如图所示。
问题生成
1.甲胺(CH3NH2)与乙酰胺(CH3CONH2)分子中均有—NH2,二者互为同系物吗 为什么
【答案】不是。因为二者不是同类物质,结构不相似,且不相差若干个CH2原子团。
2.烟酰胺属于胺类物质吗 其分子中含有的含氧官能团有哪些
【答案】烟酰胺不属于胺,属于酰胺。分子中含有酰胺基。
3.酰胺与酯类的化学性质有什么相似性
【答案】二者均可以在酸性、碱性条件下发生水解反应。
4.烟酰胺能水解吗 其酸性水解、碱性水解的产物是什么
【答案】烟酰胺能水解。酸性水解的产物为和铵盐;碱性水解的产物为和氨气。
【核心归纳】
1.酰胺的化学性质
(1)在酸性(HCl溶液)条件下水解的化学方程式:RCONH2+H2O+HClRCOOH+NH4Cl。
(2)在碱性(NaOH溶液)条件下水解的化学方程式:RCONH2+NaOHRCOONa+NH3↑。
2.氨、胺、酰胺和铵盐的比较
物质 氨 胺(甲胺)
组成元素 N、H C、N、H
结构式
化学性质 与酸反应生成铵盐 与酸反应生成盐
用途 化工原料 化工原料
物质 酰胺(乙酰胺) 铵盐(NH4Cl)
组成元素 C、N、O、H N、H、Cl
结构式
化学性质 水解反应:酸性时生成羧酸与铵盐,碱性时生成羧酸盐和NH3 与碱反应生成盐和NH3
用途 化工原料和溶剂 化工原料、化肥
[注意]酰胺基的结构简式为,R、R'可以是H或烃基。
【典型例题】
【例7】毒奶粉事件曾一度震惊全国,有毒添加剂主要是奶粉中含有的三聚氰胺(其结构如下所示)。下列关于三聚氰胺分子的说法中正确的是( )。
A.三聚氰胺分子中所有碳原子均采取sp3杂化
B.一个三聚氰胺分子中共含有15个σ键
C.三聚氰胺的分子式为C3N3H6
D.三聚氰胺分子中同时含有极性键和非极性键
【答案】B
【解析】三聚氰胺分子中的碳原子均为sp2杂化,A项错误;一个三聚氰胺分子中共含有6个N—H、6个N—C、3个
NC,共含有15个σ键,B项正确;三聚氰胺的分子式为C3N6H6,C项错误;三聚氰胺分子中不存在由同种元素的原子形成的共价键,故不存在非极性键,D项错误。
【例8】乙酰苯胺是磺胺类药物的原料,其结构如图所示,下列关于乙酰苯胺的说法中正确的是( )。
A.分子式为C8H9NO
B.乙酰苯胺是一种芳香烃
C.1 mol乙酰苯胺最多能和2 mol NaOH完全反应
D.分子中所有原子一定在同一平面上
【答案】A
【解析】A项,根据该有机物的结构简式可知,其分子式为C8H9NO,正确;B项,该有机物含有碳、氢、氧、氮元素,不属于芳香烃,错误;C项,断裂1 mol —CO—NH—,消耗1 mol NaOH,错误;D项,甲烷为正四面体结构,因该分子含有甲基,所以分子中所有原子一定不在同一平面上,错误。
【例9】食品中含有过量的(丙烯酰胺)可能引起令人不安的食品安全问题。关于丙烯酰胺有下列叙述:①能使酸性高锰酸钾溶液褪色;②能发生加聚反应;③能与氢气发生加成反应;④能发生水解反应生成酸。其中正确的是( )。
A.①②④ B.②③④
C.①②③④ D.①③④
【答案】C
【解析】丙烯酰胺含有的官能团有碳碳双键、酮羰基、氨基,所以具有烯烃的性质,能发生加聚反应、加成反应,能使酸性高锰酸钾溶液褪色,丙烯酰胺分子中含有酰胺基,能发生水解反应生成酸,故选C项。
【灵犀一点】 酰胺水解的断键
水解时,中的C—N断裂,连接—OH形成羧基,连接—H形成氨基。
【随堂检测】
1.下列叙述中错误的是( )。
A.CH3COOCH3的名称是乙酸甲酯
B.酯的官能团是酯基
C.乙酸乙酯分子中含有甲基、乙基和酯基
D.酯的分子中一定有—COOH
【答案】D
【解析】酯的分子中一定有。
2.下列物质不属于酰胺的是( )。
A. B.
C. D.CH3CONH2
【答案】C
【解析】C项分子中只有氨基和羧基,不属于酰胺。
3.下列关于的叙述中不正确的是( )。
A.该物质能发生缩聚反应
B.该物质有7种不同化学环境的氢原子
C.该物质遇FeCl3溶液显紫色,1 mol该物质最多能与含1 mol Br2的溴水发生取代反应
D.1 mol该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为2∶2∶1
【答案】B
【解析】该物质含有氨基、羟基、羧基等多种官能团,因此可以发生缩聚反应,A项正确;该物质有8种不同化学环境的氢原子,B项错误;该物质含有酚羟基,所以遇FeCl3溶液显紫色,由于在苯环上羟基邻、对位只有一个H原子,所以1 mol该物质最多能与含1 mol Br2的溴水发生取代反应,C项正确;羧基、羟基可以与Na发生反应,羧基和酚羟基都可以与NaOH发生反应,只有羧基可以与NaHCO3发生反应,在该化合物的一个分子中含有一个酚羟基、一个羧基,所以1 mol该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为2∶2∶1,D项正确。
4.(2022·海南卷,双选)化合物“E7974”具有抗肿瘤活性,结构简式如下,下列有关该化合物说法正确的是( )。
A. 能使Br2的CCl4溶液褪色
B. 分子中含有4种官能团
C. 分子中含有4个手性碳原子
D. 1 mol该化合物最多与2 mol NaOH反应
【答案】AB
【解析】该物质分子中含有碳碳双键,能使Br2的CCl4溶液褪色,A项正确;由结构简式可知,分子中含有酰胺基、羧基、碳碳双键、次氨基,共4种官能团,其中有两个酰胺基,B项正确; “E7974”分子含有的手性碳原子如图所示,共3个,C项错误;分子中的酰胺基(2个)和羧基(1个)均能与NaOH溶液反应,故1 mol该化合物最多与3 mol NaOH反应,D项错误。
5.(2021·辽宁卷)我国科技工作者发现某“小分子胶水”(结构如图)能助力自噬细胞“吞没”致病蛋白。下列说法正确的是( )。
A.该分子中所有碳原子一定共平面
B.该分子能与蛋白质分子形成氢键
C.1 mol该物质最多能与3 mol NaOH反应
D.该物质能发生取代、加成和消去反应
【答案】B
【解析】该分子中2个苯环、碳碳双键所在的三个平面,平面间单键连接可以旋转,故所有碳原子可能共平面,A项错误;由题干信息可知,该分子中有羟基,能与蛋白质分子中的氨基之间形成氢键,B项正确;由题干信息可知,1 mol该物质含有2 mol酚羟基,可以消耗2 mol NaOH,含1 mol酚酯基,可以消耗2 mol NaOH,故最多能与4 mol NaOH反应,C项错误;该物质中含有酚羟基且邻对位上有H,能发生取代反应,含有苯环和碳碳双键,能发生加成反应,但没有卤素原子和醇羟基,不能发生消去反应,D项错误。
2
