化学人教版(2019)选择性必修1 2.3化学反应进行的方向(共20张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修1 2.3化学反应进行的方向(共20张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-10 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
2NO(g)+2CO(g)= N2(g)+2CO2(g)
H = -746.8 kJ mol-1
该方案是否可行?
设计方案
思考
化学反应进行的方向
思考
从能量的角度思考,以上客观事实具有什么特点?
1、自发过程
在一定条件下,不借助外部力量就能自动进行的过程
2、自发反应
在一定条件下,不借助外部力量,经引发就能自动进行的化学反应
放热反应
Na(s)+H2O(l)= NaOH(aq)+1/2H2(g)
H = -184 kJ mol-1
证实
NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(l)
H = -57.3 kJ mol-1
H2(g)+1/2O2(g)= H2O(l)
H = -286 kJ mol-1
条件:25℃,1.01*105 Pa
证实
时间线
汤姆逊
19世纪中叶
范霍夫
焓判据:
自发反应更倾向于焓减的方向
证伪
2N2O5(g)= 4NO2(g)+O2(g)
H = +56.7 kJ mol-1
(NH4)2CO3(s)= NH4HCO3(s)+NH3(g)
H = +74.9 kJ mol-1
自发进行的吸热反应
条件:25℃,1.01*105 Pa
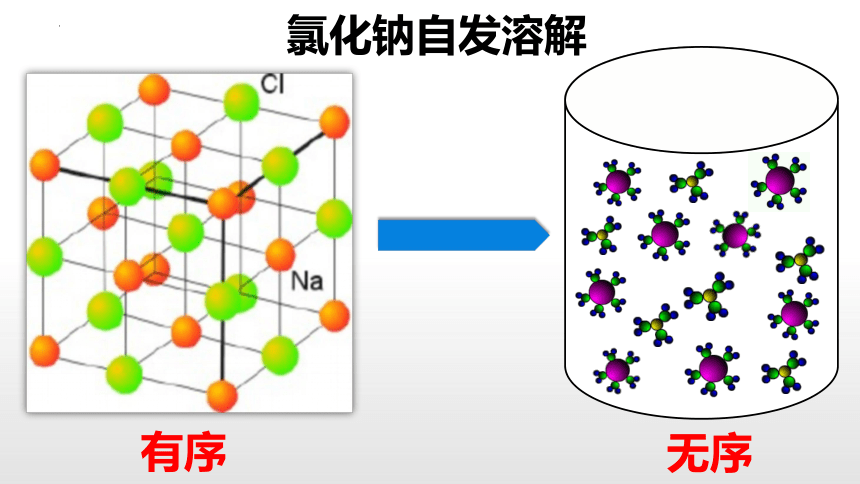
氯化钠自发溶解
有序
无序
在水中滴加红墨水
有序
无序
烟雾自发扩散
有序
无序
混乱度增加
证实
时间线
汤姆逊
19世纪中叶
1865
克劳修斯
范霍夫
最早提出熵的概念
熵:微观状态混乱度的度量,用符号 S 表示
证实
时间线
汤姆逊
19世纪中叶
1865
克劳修斯
范霍夫
玻尔兹曼
1877
解释了熵的物理意义,提出了熵判据
建立了熵与概率的关系 S = k logW
NH4Cl(s)=NH3(g)+HCl(g)
S = +284.76 J mol-1 K-1
证实
CaCO3(s)= CaO(s)+CO2(g)
S = +160.5 J mol-1 K-1
C(s)+H2O(g)= CO(g)+H2(g)
S= +133.8 J mol-1 K-1
熵判据:
自发反应更倾向于熵增的方向
证伪
2Al(s)+Fe2O3(s) = Al2O3(s)+2Fe(s)
S = -38.58 J mol-1 K-1
4Fe(OH)2(s)+2H2O(l)+O2(g)= 4Fe(OH)3(s)
S = -280 J mol-1 K-1
自发进行的熵减反应
证实
时间线
汤姆逊
19世纪中叶
1865
克劳修斯
范霍夫
玻尔兹曼
1877
1878
吉布斯
提出吉布斯自由能与吉布斯相律
奠定了热力学基础
复合判据
自发反应更倾向于吉布斯自由能减小的方向
G = H - T S
2NO(g)+2CO(g)= N2(g)+2CO2(g)
H = -746.8 kJ mol-1
活学活用
S = -197.5 J mol-1 K-1
根据公式
G = H - T S
G < 0
该反应为自发反应
课后查阅资料,研究该反应的反应速率
科学探究
提出问题
做出解释
证实
修正解释
证伪
得出结论
证伪、证实
科学探究
提出问题
做出解释
证实
修正解释
证伪
得出结论
证伪、证实
谢谢大家!
化学反应进行的方向
一、两个概念
1、自发过程
在一定条件下,不借助外部力量就能自动进行的过程
2、自发反应
在一定条件下,不借助外部力量,经引发就能自动进行的化学反应
二、焓判据
焓减
三、熵判据
熵增
四、吉布斯自由能判据
G = H - T S
2NO(g)+2CO(g)= N2(g)+2CO2(g)
H = -746.8 kJ mol-1
该方案是否可行?
设计方案
思考
化学反应进行的方向
思考
从能量的角度思考,以上客观事实具有什么特点?
1、自发过程
在一定条件下,不借助外部力量就能自动进行的过程
2、自发反应
在一定条件下,不借助外部力量,经引发就能自动进行的化学反应
放热反应
Na(s)+H2O(l)= NaOH(aq)+1/2H2(g)
H = -184 kJ mol-1
证实
NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(l)
H = -57.3 kJ mol-1
H2(g)+1/2O2(g)= H2O(l)
H = -286 kJ mol-1
条件:25℃,1.01*105 Pa
证实
时间线
汤姆逊
19世纪中叶
范霍夫
焓判据:
自发反应更倾向于焓减的方向
证伪
2N2O5(g)= 4NO2(g)+O2(g)
H = +56.7 kJ mol-1
(NH4)2CO3(s)= NH4HCO3(s)+NH3(g)
H = +74.9 kJ mol-1
自发进行的吸热反应
条件:25℃,1.01*105 Pa
氯化钠自发溶解
有序
无序
在水中滴加红墨水
有序
无序
烟雾自发扩散
有序
无序
混乱度增加
证实
时间线
汤姆逊
19世纪中叶
1865
克劳修斯
范霍夫
最早提出熵的概念
熵:微观状态混乱度的度量,用符号 S 表示
证实
时间线
汤姆逊
19世纪中叶
1865
克劳修斯
范霍夫
玻尔兹曼
1877
解释了熵的物理意义,提出了熵判据
建立了熵与概率的关系 S = k logW
NH4Cl(s)=NH3(g)+HCl(g)
S = +284.76 J mol-1 K-1
证实
CaCO3(s)= CaO(s)+CO2(g)
S = +160.5 J mol-1 K-1
C(s)+H2O(g)= CO(g)+H2(g)
S= +133.8 J mol-1 K-1
熵判据:
自发反应更倾向于熵增的方向
证伪
2Al(s)+Fe2O3(s) = Al2O3(s)+2Fe(s)
S = -38.58 J mol-1 K-1
4Fe(OH)2(s)+2H2O(l)+O2(g)= 4Fe(OH)3(s)
S = -280 J mol-1 K-1
自发进行的熵减反应
证实
时间线
汤姆逊
19世纪中叶
1865
克劳修斯
范霍夫
玻尔兹曼
1877
1878
吉布斯
提出吉布斯自由能与吉布斯相律
奠定了热力学基础
复合判据
自发反应更倾向于吉布斯自由能减小的方向
G = H - T S
2NO(g)+2CO(g)= N2(g)+2CO2(g)
H = -746.8 kJ mol-1
活学活用
S = -197.5 J mol-1 K-1
根据公式
G = H - T S
G < 0
该反应为自发反应
课后查阅资料,研究该反应的反应速率
科学探究
提出问题
做出解释
证实
修正解释
证伪
得出结论
证伪、证实
科学探究
提出问题
做出解释
证实
修正解释
证伪
得出结论
证伪、证实
谢谢大家!
化学反应进行的方向
一、两个概念
1、自发过程
在一定条件下,不借助外部力量就能自动进行的过程
2、自发反应
在一定条件下,不借助外部力量,经引发就能自动进行的化学反应
二、焓判据
焓减
三、熵判据
熵增
四、吉布斯自由能判据
G = H - T S
