化学人教版(2019)必修第一册1.1.1物质的分类(共32张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.1物质的分类(共32张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 32.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-11 08:37:52 | ||
图片预览








文档简介
(共32张PPT)
第一章 物质及其变化
第一节 物质的分类及转化
第1课时 物质的分类
机器人对快递件的高速分拣
设问:在日常生活中我们还会在什么地方用到分类的方法呢?
图书馆
超市
查字典
药房
实验室
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
《开心辞典》
考一考:
看看你能说出多少内容???
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
分类法是把某些特征相似的物体归类到一起的方法。
成语概括:
物以类聚
He was an oldman who fished alone
He was an old man who fished alone in a skiff
机器是怎样将快递件进行分类的?
分类是根据研究对象的共同点和差异点,将其区分为不同种类和层次的科学方法。科学的分类能够反映事物的本质特征,有利于人们分门别类进行研究。分类有一定的标准,根据不同的标准,人们可以对研究对象进行不同的分类。分类一定要科学,这样才能进行有效的研究,那么怎样才能保证分类的科学性?
按目的地分类
大小?
发件地?
科学分类的关键在于建立科学、准确的分类标准
如果以其他方式分类是科学的吗?
1. 如何对化学物质进行分类?任选分类标准,选取初中学过的化学物质进行分类。
小组讨论
2. 我们可以根据研究目的选择分类标准,只要分类标准科学合理,分类正确无误,任何一种分类方式都是可行的。初中我们已经学过“任何物质都是由元素组成的”同种元素能够形成单质,不同种元素能够形成化合物。
由Na、K、H、C、O、S六中元素中的一种或任意几种形成的物质有哪些?(写出尽可能多的物质)
可选分类标准:如颜色,状态,水溶性,物质的组成、性质… …
同素异形体:由同一种元素形成性质不同的几种单质,叫作这种元素的“同素异形体”。
如:O2、O3 白磷和红磷 金刚石、石墨、C60等
思考:同一种元素是不是只能形成一种单质?
一、物质的分类
1. 根据物质的组成和性质分类
思考:同一种元素形成物质一定是纯净物吗?
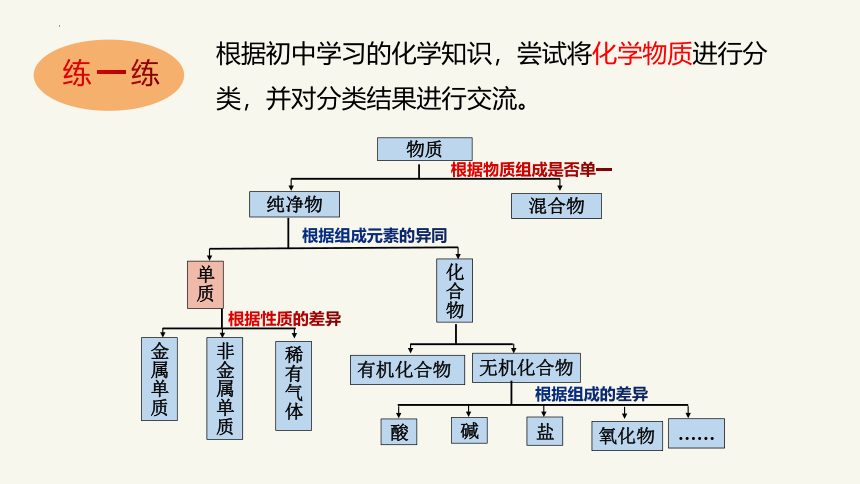
根据初中学习的化学知识,尝试将化学物质进行分类,并对分类结果进行交流。
物质
纯净物
混合物
单质
化合物
金属单质
稀有气体
盐
碱
酸
无机化合物
有机化合物
根据物质组成是否单一
根据组成元素的异同
根据性质的差异
根据组成的差异
……
氧化物
非金属单质
练一练
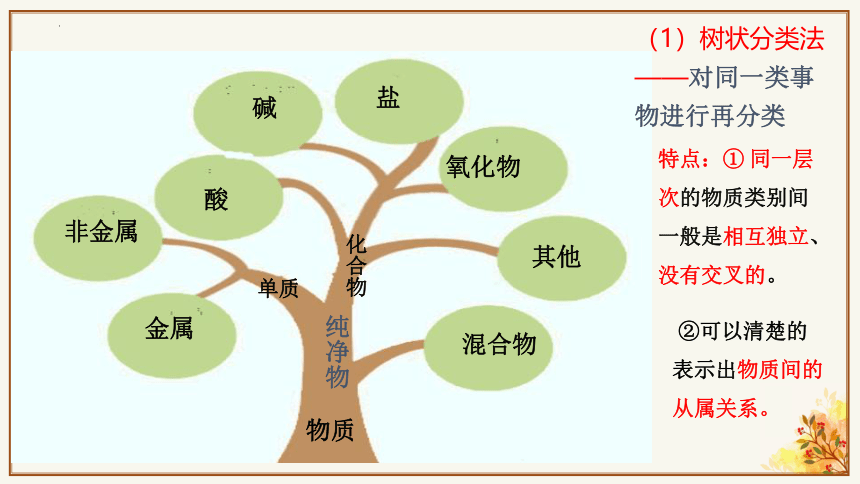
特点:① 同一层次的物质类别间一般是相互独立、没有交叉的。
纯净物
混合物
物质
单质
金属
非金属
酸
氧化物
盐
碱
其他
化合物
(1)树状分类法
——对同一类事物进行再分类
②可以清楚的表示出物质间的从属关系。
氧化物
按组成分
按性质分
金属氧化物
非金属氧化物
酸性氧化物
碱性氧化物
两性氧化物
( SO2、CO2 )
( Na2O、K2O)
( Al2O3 )
( SO2、SO3、CO2 、CO)
( Na2O、K2O)
不成盐氧化物
(CO、NO)
思考:
(1)金属氧化物都是碱性氧化物
(2)非金属氧化物都是酸性氧化物
(3)碱性氧化物都是金属氧化物
(4)酸性氧化物都是非金属氧化物
Mn2O7是酸性氧化物
CO不是酸性氧化物也不是碱性氧化物
正确
Mn2O7是酸性氧化物
酸性氧化物:与碱反应生成盐和水的氧化物,如CO2、SO3等
碱性氧化物:与酸反应生成盐和水的氧化物,如Na2O、K2O等
酸
按组成元素分
按性质分
含氧酸
强酸
中强酸
弱酸
( HCl 、HNO3)
( H3PO4)
( HCl )
( H2CO3、H2SO3、H2SO4)
按电离出H+的个数分
无氧酸
一元酸
二元酸
三元酸
( H2CO3、H2SO4)
( HCl 、 H2SO4 、HNO3)
( H3PO4)
( H2CO3)
碱
按溶解性分
按性质分
可溶性碱
强碱
弱碱
( Mg(OH)2、Cu(OH)2)
( NaOH、KOH、Ba(OH)2)
按电离出OH-的个数分
难溶性碱
一元碱
二元碱
多元碱
( NaOH)
( NaOH、Ba(OH)2、KOH)
(NH3·H2O、Al(OH)3)
( Mg(OH)2、Cu(OH)2)
( Al(OH)3)
盐
按是否溶于水分
按组成离子分
无氧酸盐
钠盐
钾盐
氨盐
硫酸盐
碳酸盐
硝酸盐
按酸根是否含氧分
含氧酸盐
可溶盐
难溶盐
NaCl、KCl、AgNO3、CuSO4
CaCO3、BaSO4、ZnS
KNO3、KMnO4、FeSO4
NaCl、ZnS、CaCl2
……
酸式盐
碱式盐
正盐
KHSO4、 Ca(H2PO4)2
Cu2(OH)2CO3
按组成分
分类并没有唯一性,它会根据分类的标准不同而不同。
单一分类标准有一定的局限,所能提供的信息少,对同一事物,我们可以从不同的角度,按不同的标准来分类。
如交叉分类法:
(2)交叉分类法 —— 对同一事物采用多种标准进行分类的方法。
Na2CO3
Na2SO4
K2SO4
K2CO3
钠 盐
钾 盐
硫酸盐
碳酸盐
按阳离子分
按阳离子分
按阴离子分
按阴离子分
钠 盐
碳酸盐
Na2CO3
Na2CO3
物质类别之间有部分交叉
特点:
使我们对事物的认识更全面
2. 分散系及其分类
(1)分散系:
分散质:
分散剂:
把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。
被分散的物质
能分散分散质的物质
分
散
系
根据物质的组成和性质,对纯净物进行分类;根据物质研究的具体需要,还可以对纯净物进行其他类型的分类。但是,自然界中的物质往往都是混合物,对混合物我们又该如何分类?
想一想
分散系
胶 体
浊 液
溶 液
悬浊液
乳浊液
当分散剂是水或其他液体时,按照分散质粒子直径的大小来分:
树状分类法
(2)分散系的分类
【思考与交流】阅读课本,然后画出分散剂是水或其他液体时的分散系的树状分类图?
三者本质特征比较:
胶 体
浊 液
溶 液
100 nm
1nm
分散质粒子直径
可以通过滤纸
胶体:分散质粒子的直径大小在1―100 nm 之间的分散系(即胶体区别于其他分散系的本质特征)
几种分散系的比较:
分散系 实例 分散质 分散剂 特征
悬浊液
乳浊液
溶液
水
水
水
土壤粒子
油
酒精分子
浑浊,静置沉淀
浑浊,静置分层
澄清 透明 均一 稳定
泥水
油水
酒精溶液
液溶胶
烟水晶
有色玻璃
固溶胶
雾
白云
气溶胶
常见的胶体:
分散剂为气体(如:烟、云、雾)
分散剂为固体(如:有色玻璃、宝石)
分散剂为液体(如:牛奶、豆浆)
(按分散剂的不同分)
实 验 探 究
实验1-1:
实验1 取100mL烧杯,加入40mL蒸馏水,加热至沸腾。向沸水中滴加5~6滴FeCl3的饱和溶液。继续煮沸至液体呈红褐色,停止加热。
实验2 取100mL烧杯,加入40mL硫酸铜溶液
分别用激光笔照射Fe(OH)3胶体和CuSO4溶液,在与光束垂直的方向进行观察,并记录实验现象。
CuSO4 溶液
Fe(OH)3 胶体
光束照射时的现象
Fe(OH)3胶体 形成一条光亮的通路
CuSO4溶液 没有光亮的通路现象产生
丁达尔效应是区分胶体和溶液的一种常用的物理方法。
当一束光线照射胶体时,从侧面观察,可看见一条光亮的通路的现象。
(3) 胶体的性质
①丁达尔效应:
胶体产生丁达尔效应的原因:
光波偏离原来方向而分散传播
生活中的丁达尔效应
②介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,属于介稳体系,其原因是:胶体粒子 相同,相互排斥;
所带电荷
③聚沉:胶体粒子聚集成较大颗粒,从而形成沉淀从分散剂里析出的过程叫做聚沉。
使胶体聚沉的方法有:
① ;
② ; ③ 。
加入电解质
加入带相反电荷的胶体
加热
④电泳:在 作用下,胶体粒子在分散剂中 。
如带正电荷的Fe(OH)3胶体粒子向 移动。
电场
阴极
作定向移动
※ 胶体性质的应用
①丁达尔效应:鉴别溶液和胶体。
②聚沉:三角洲的形成,明矾、铁盐溶液净水,盐卤点豆腐,不同品牌墨水不能混用。
盐析:肥皂的制备与分离。
③电泳:工厂静电除尘。
※ 胶体的提纯:渗析法
由于胶体粒子较大,不能透过半透膜,而离子、小分子较小,可以透过半透膜,用此法提纯胶体。
小结:
1. 分类是一种科学的学习方法,科学分类的前提是有准确的分类标准
3. 树状分类法:按物质组成对物质进行分类;按物质组成和性质对氧化物、酸、碱、盐进行分类;交叉分类法
2. 同素异形体的概念
4. 分散系的概念与分类;
5. 胶体的概念与分类;
6. 氢氧化铁胶体的制备;
7. 丁达尔效应。
感谢聆听
第一章 物质及其变化
第一节 物质的分类及转化
第1课时 物质的分类
机器人对快递件的高速分拣
设问:在日常生活中我们还会在什么地方用到分类的方法呢?
图书馆
超市
查字典
药房
实验室
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
《开心辞典》
考一考:
看看你能说出多少内容???
语文
液体
固体
四
数学
六
化学
春天
三
夏天
物理
冬天
英语
气体
秋天
五
七
生物
分类法是把某些特征相似的物体归类到一起的方法。
成语概括:
物以类聚
He was an oldman who fished alone
He was an old man who fished alone in a skiff
机器是怎样将快递件进行分类的?
分类是根据研究对象的共同点和差异点,将其区分为不同种类和层次的科学方法。科学的分类能够反映事物的本质特征,有利于人们分门别类进行研究。分类有一定的标准,根据不同的标准,人们可以对研究对象进行不同的分类。分类一定要科学,这样才能进行有效的研究,那么怎样才能保证分类的科学性?
按目的地分类
大小?
发件地?
科学分类的关键在于建立科学、准确的分类标准
如果以其他方式分类是科学的吗?
1. 如何对化学物质进行分类?任选分类标准,选取初中学过的化学物质进行分类。
小组讨论
2. 我们可以根据研究目的选择分类标准,只要分类标准科学合理,分类正确无误,任何一种分类方式都是可行的。初中我们已经学过“任何物质都是由元素组成的”同种元素能够形成单质,不同种元素能够形成化合物。
由Na、K、H、C、O、S六中元素中的一种或任意几种形成的物质有哪些?(写出尽可能多的物质)
可选分类标准:如颜色,状态,水溶性,物质的组成、性质… …
同素异形体:由同一种元素形成性质不同的几种单质,叫作这种元素的“同素异形体”。
如:O2、O3 白磷和红磷 金刚石、石墨、C60等
思考:同一种元素是不是只能形成一种单质?
一、物质的分类
1. 根据物质的组成和性质分类
思考:同一种元素形成物质一定是纯净物吗?
根据初中学习的化学知识,尝试将化学物质进行分类,并对分类结果进行交流。
物质
纯净物
混合物
单质
化合物
金属单质
稀有气体
盐
碱
酸
无机化合物
有机化合物
根据物质组成是否单一
根据组成元素的异同
根据性质的差异
根据组成的差异
……
氧化物
非金属单质
练一练
特点:① 同一层次的物质类别间一般是相互独立、没有交叉的。
纯净物
混合物
物质
单质
金属
非金属
酸
氧化物
盐
碱
其他
化合物
(1)树状分类法
——对同一类事物进行再分类
②可以清楚的表示出物质间的从属关系。
氧化物
按组成分
按性质分
金属氧化物
非金属氧化物
酸性氧化物
碱性氧化物
两性氧化物
( SO2、CO2 )
( Na2O、K2O)
( Al2O3 )
( SO2、SO3、CO2 、CO)
( Na2O、K2O)
不成盐氧化物
(CO、NO)
思考:
(1)金属氧化物都是碱性氧化物
(2)非金属氧化物都是酸性氧化物
(3)碱性氧化物都是金属氧化物
(4)酸性氧化物都是非金属氧化物
Mn2O7是酸性氧化物
CO不是酸性氧化物也不是碱性氧化物
正确
Mn2O7是酸性氧化物
酸性氧化物:与碱反应生成盐和水的氧化物,如CO2、SO3等
碱性氧化物:与酸反应生成盐和水的氧化物,如Na2O、K2O等
酸
按组成元素分
按性质分
含氧酸
强酸
中强酸
弱酸
( HCl 、HNO3)
( H3PO4)
( HCl )
( H2CO3、H2SO3、H2SO4)
按电离出H+的个数分
无氧酸
一元酸
二元酸
三元酸
( H2CO3、H2SO4)
( HCl 、 H2SO4 、HNO3)
( H3PO4)
( H2CO3)
碱
按溶解性分
按性质分
可溶性碱
强碱
弱碱
( Mg(OH)2、Cu(OH)2)
( NaOH、KOH、Ba(OH)2)
按电离出OH-的个数分
难溶性碱
一元碱
二元碱
多元碱
( NaOH)
( NaOH、Ba(OH)2、KOH)
(NH3·H2O、Al(OH)3)
( Mg(OH)2、Cu(OH)2)
( Al(OH)3)
盐
按是否溶于水分
按组成离子分
无氧酸盐
钠盐
钾盐
氨盐
硫酸盐
碳酸盐
硝酸盐
按酸根是否含氧分
含氧酸盐
可溶盐
难溶盐
NaCl、KCl、AgNO3、CuSO4
CaCO3、BaSO4、ZnS
KNO3、KMnO4、FeSO4
NaCl、ZnS、CaCl2
……
酸式盐
碱式盐
正盐
KHSO4、 Ca(H2PO4)2
Cu2(OH)2CO3
按组成分
分类并没有唯一性,它会根据分类的标准不同而不同。
单一分类标准有一定的局限,所能提供的信息少,对同一事物,我们可以从不同的角度,按不同的标准来分类。
如交叉分类法:
(2)交叉分类法 —— 对同一事物采用多种标准进行分类的方法。
Na2CO3
Na2SO4
K2SO4
K2CO3
钠 盐
钾 盐
硫酸盐
碳酸盐
按阳离子分
按阳离子分
按阴离子分
按阴离子分
钠 盐
碳酸盐
Na2CO3
Na2CO3
物质类别之间有部分交叉
特点:
使我们对事物的认识更全面
2. 分散系及其分类
(1)分散系:
分散质:
分散剂:
把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。
被分散的物质
能分散分散质的物质
分
散
系
根据物质的组成和性质,对纯净物进行分类;根据物质研究的具体需要,还可以对纯净物进行其他类型的分类。但是,自然界中的物质往往都是混合物,对混合物我们又该如何分类?
想一想
分散系
胶 体
浊 液
溶 液
悬浊液
乳浊液
当分散剂是水或其他液体时,按照分散质粒子直径的大小来分:
树状分类法
(2)分散系的分类
【思考与交流】阅读课本,然后画出分散剂是水或其他液体时的分散系的树状分类图?
三者本质特征比较:
胶 体
浊 液
溶 液
100 nm
1nm
分散质粒子直径
可以通过滤纸
胶体:分散质粒子的直径大小在1―100 nm 之间的分散系(即胶体区别于其他分散系的本质特征)
几种分散系的比较:
分散系 实例 分散质 分散剂 特征
悬浊液
乳浊液
溶液
水
水
水
土壤粒子
油
酒精分子
浑浊,静置沉淀
浑浊,静置分层
澄清 透明 均一 稳定
泥水
油水
酒精溶液
液溶胶
烟水晶
有色玻璃
固溶胶
雾
白云
气溶胶
常见的胶体:
分散剂为气体(如:烟、云、雾)
分散剂为固体(如:有色玻璃、宝石)
分散剂为液体(如:牛奶、豆浆)
(按分散剂的不同分)
实 验 探 究
实验1-1:
实验1 取100mL烧杯,加入40mL蒸馏水,加热至沸腾。向沸水中滴加5~6滴FeCl3的饱和溶液。继续煮沸至液体呈红褐色,停止加热。
实验2 取100mL烧杯,加入40mL硫酸铜溶液
分别用激光笔照射Fe(OH)3胶体和CuSO4溶液,在与光束垂直的方向进行观察,并记录实验现象。
CuSO4 溶液
Fe(OH)3 胶体
光束照射时的现象
Fe(OH)3胶体 形成一条光亮的通路
CuSO4溶液 没有光亮的通路现象产生
丁达尔效应是区分胶体和溶液的一种常用的物理方法。
当一束光线照射胶体时,从侧面观察,可看见一条光亮的通路的现象。
(3) 胶体的性质
①丁达尔效应:
胶体产生丁达尔效应的原因:
光波偏离原来方向而分散传播
生活中的丁达尔效应
②介稳性:胶体的稳定性介于溶液和浊液之间,在一定条件下能稳定存在,属于介稳体系,其原因是:胶体粒子 相同,相互排斥;
所带电荷
③聚沉:胶体粒子聚集成较大颗粒,从而形成沉淀从分散剂里析出的过程叫做聚沉。
使胶体聚沉的方法有:
① ;
② ; ③ 。
加入电解质
加入带相反电荷的胶体
加热
④电泳:在 作用下,胶体粒子在分散剂中 。
如带正电荷的Fe(OH)3胶体粒子向 移动。
电场
阴极
作定向移动
※ 胶体性质的应用
①丁达尔效应:鉴别溶液和胶体。
②聚沉:三角洲的形成,明矾、铁盐溶液净水,盐卤点豆腐,不同品牌墨水不能混用。
盐析:肥皂的制备与分离。
③电泳:工厂静电除尘。
※ 胶体的提纯:渗析法
由于胶体粒子较大,不能透过半透膜,而离子、小分子较小,可以透过半透膜,用此法提纯胶体。
小结:
1. 分类是一种科学的学习方法,科学分类的前提是有准确的分类标准
3. 树状分类法:按物质组成对物质进行分类;按物质组成和性质对氧化物、酸、碱、盐进行分类;交叉分类法
2. 同素异形体的概念
4. 分散系的概念与分类;
5. 胶体的概念与分类;
6. 氢氧化铁胶体的制备;
7. 丁达尔效应。
感谢聆听
