选择题突破四 无机物的性质、转化与应用 专项特训(含解析)2024年高考化学二轮复习
文档属性
| 名称 | 选择题突破四 无机物的性质、转化与应用 专项特训(含解析)2024年高考化学二轮复习 |  | |
| 格式 | DOCX | ||
| 文件大小 | 857.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-11 21:50:32 | ||
图片预览



文档简介
选择题突破四 无机物的性质、转化与应用
A卷
1.(2023·广州执信中学期中)下列说法不正确的是( )
A.二氧化硫可用于杀菌消毒,还是一种食品添加剂
B.常温下,铁、铝和浓硝酸不反应,因此可用铁或铝制容器来盛装浓硝酸
C.太阳能、风能、地热能、海洋能和氢能都是新能源
D.浸泡酸性高锰酸钾溶液的硅藻土可用于水果长途运输的保鲜
2.(2023·汕头潮阳区三模)物质的性质决定其用途。下列生产活动与化学原理均正确且有关联的是( )
选项 生产活动 化学原理
A 石英坩埚可用于加热KOH固体 SiO2熔点高
B P2O5可作食品干燥剂 P2O5具有强吸水性
C NaHCO3可用于抗酸药物 NaHCO3受热易分解
D 钠的化合物可用于制作烟花 钠元素焰色试验显黄色
3.劳动成就梦想。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 厨房帮厨:饭后用热的纯碱溶液洗涤餐具 油脂在碱性条件下发生水解
B 工厂生产:制作玻璃装饰品 HF是一种有刺激性气味的气体
C 社区服务:用泡沫灭火器演练如何灭火 铝离子与碳酸氢根离子在溶液中相互促进水解
D 自主探究:以锌、铜和柠檬为原料制作水果电池 锌能与柠檬中酸性物质发生反应
4.(2023·揭阳联考)化学创造美好生活,下列活动中涉及的物质或反应与相关解释不相符的是( )
选项 物质或反应 相关解释
A “84”消毒液不能与洁厕灵(主要成分是盐酸)混合使用 两种物质混合会放出Cl2
B 做面包时用NaHCO3作蓬松剂 NaHCO3受热易分解
C NaNO2中毒时可用维生素C解毒 利用了维生素C的强还原性
D 用FeCl3溶液刻蚀铜的线路板 FeCl3溶液和Cu发生置换反应
5.(2023·揭阳联考)如图所示是氮元素的几种价态与物质类别的对应关系,下列说法错误的是( )
A.物质B可与物质A反应
B.物质B可经催化氧化直接生成物质A
C.N2―→物质A、物质A―→NO2均为自然固氮
D.HNO3和物质C常用于检验Cl-,则C为AgNO3
6.部分含铜物质的价类关系如图所示。下列说法正确的是( )
A.a能与FeCl3溶液反应:Cu+Fe3+===Cu2++Fe2+
B.b在酸性环境中可以转化为a和e
C.c经一步反应可转化为d
D.若e为Cu(NO3)2,则其水溶液中可能大量存在H+、SO、Fe2+
7.(2023·茂名一模)陈述 Ⅰ 和 Ⅱ 均正确且具有因果关系的是( )
选项 陈述 Ⅰ 陈述 Ⅱ
A 用铁槽盛放浓HNO3 铁不与浓HNO3反应
B 用氢氟酸刻蚀玻璃 HF能与玻璃中的SiO2反应
C 用钾盐作紫色烟花原料 电子跃迁到激发态释放能量,产生紫色光
D Na高温还原KCl制备金属K 金属性:Na8.(2023·汕头二模)化学创造美好生活。下列选项中生产活动和化学原理没有关联的是( )
选项 生产活动 化学原理
A 葡萄酒中添加少量SO2 SO2可杀菌且防止营养物质被氧化
B 用聚乙烯塑料制作食品保鲜膜 聚乙烯燃烧生成CO2和H2O
C 利用氧化银冶炼金属Ag 氧化银在一定条件下发生分解反应
D 用地沟油为原料制作肥皂 地沟油发生皂化反应
9.(2023·梅州大埔县三模)下列叙述Ⅰ和Ⅱ均正确且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A SO2具有氧化性 在葡萄酒酿制过程中添加适量SO2
B 断裂NH3分子中的N—H键需要吸收热量 工业上用液氨作制冷剂
C 氢氟酸可与SiO2反应得到SiF4 二氧化硅是一种两性氧化物
D 蔗糖遇浓硫酸变黑,同时产生有刺激性气味的气体 浓硫酸具有脱水性和强氧化性
10.如图是M元素高中常见物质的价类二维图。其中A到D、D到E的转化都可加同一种物质实现,且E的相对分子质量比D的相对分子质量大16,则下列说法不正确的是( )
A.物质B可用作火箭燃料,其电子式为
B.依据题给价类二维图综合分析可知M元素为氮元素
C.氢化物A或B均可在一定条件下与氧气反应得到单质C
D.物质F的浓溶液具有强氧化性,可以用铁制或铝制容器盛放
B卷
11.(2023·揭阳联考)陈述Ⅰ和Ⅱ均正确且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A Al(OH)3不与碱反应 氨水和AlCl3制备Al(OH)3
B 用氢氟酸雕刻玻璃 氢氟酸与玻璃中的SiO2反应生成SiF4和H2O
C Fe(SCN)3溶液中加入NH4F变为无色 Fe3+和NH形成配位键
D 生产中用铁槽盛放浓硫酸 铁不与浓硫酸反应
12.劳动创造幸福。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 分析员用X射线衍射仪区分普通玻璃和水晶 普通玻璃属于非晶体,水晶属于晶体
B 面点师制作糕点时添加小苏打作膨松剂 NaHCO3可与碱反应
C 实验员用加热法分离I2和NaCl I2易升华
D 维修工用NaOH和铝粉疏通厨卫管道 Al与NaOH溶液反应产生H2
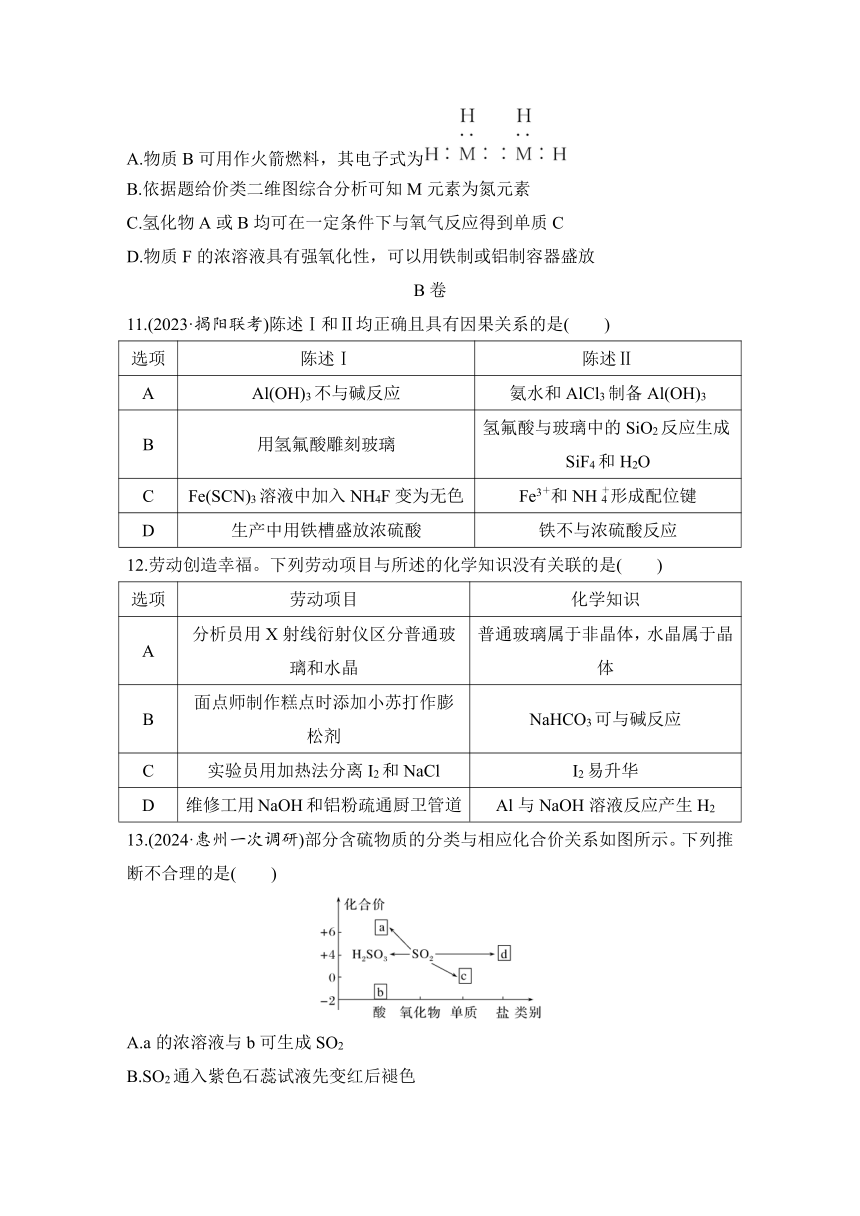
13.(2024·惠州一次调研)部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与b可生成SO2
B.SO2通入紫色石蕊试液先变红后褪色
C.c在空气中燃烧生成SO2
D.d既可被氧化,也可被还原
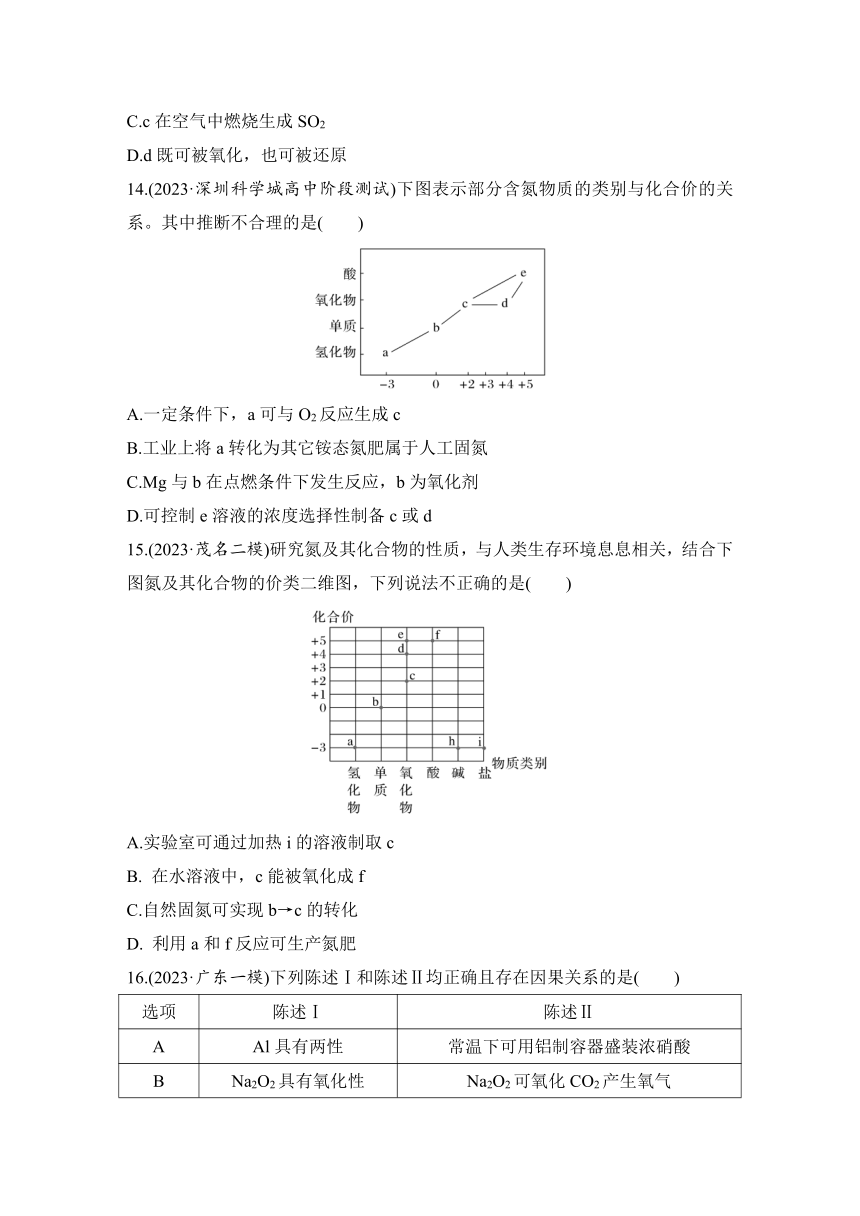
14.(2023·深圳科学城高中阶段测试)下图表示部分含氮物质的类别与化合价的关系。其中推断不合理的是( )
A.一定条件下,a可与O2反应生成c
B.工业上将a转化为其它铵态氮肥属于人工固氮
C.Mg与b在点燃条件下发生反应,b为氧化剂
D.可控制e溶液的浓度选择性制备c或d
15.(2023·茂名二模)研究氮及其化合物的性质,与人类生存环境息息相关,结合下图氮及其化合物的价类二维图,下列说法不正确的是( )
A.实验室可通过加热i的溶液制取c
B. 在水溶液中,c能被氧化成f
C.自然固氮可实现b→c的转化
D. 利用a和f反应可生产氮肥
16.(2023·广东一模)下列陈述Ⅰ和陈述Ⅱ均正确且存在因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A Al具有两性 常温下可用铝制容器盛装浓硝酸
B Na2O2具有氧化性 Na2O2可氧化CO2产生氧气
C 纯碱溶液呈碱性 纯碱溶液可用于清洗厨房油污
D SO2具有漂白性 SO2通入紫色石蕊溶液后溶液褪色
17.(2023·深圳统考)下列实践活动与所述的化学知识没有关联的是( )
选项 实践活动 化学知识
A 用NH4NO3对农作物施肥 NH4NO3属于氮肥
B 用白醋清除水垢(主要成分是CaCO3) 乙酸可与CaCO3发生反应
C 用75%的乙醇溶液消毒 蛋白质在乙醇作用下会发生变性
D 蒸馒头时加入小苏打 NaHCO3是白色晶体
18.(2023·江门调研)下图所示为氯的单质及其化合物的价类二维图,其中X、Y、Z、W为含氯化合物。下列说法正确的是( )
A.Y的酸性比碳酸强
B.可以通过焰色试验区别Z、W两种化合物
C.液氯可使湿润的红布条褪色,所以液氯具有漂白性
D.Z是“84”消毒液的主要成分
19.(2023·清远清新模拟预测)六氟磷酸锂(LiPF6)是锂离子电池的关键材料。一种LiPF6的制备工艺流程如图所示。
已知:①6HF+H3PO4===HPF6+4H2O,HPF6易发生分解反应;
②PF5熔点为-93.8 ℃,沸点为-84.6 ℃。
下列说法错误的是( )
A.N2环境中,反应先生成六氟磷酸(HPF6),HPF6再分解生成五氟化磷(PF5)
B.发烟硫酸(H2S2O7)的作用是吸收铅皿中的水分:H2S2O7+H2O===2H2SO4
C.工艺流程中,无水HF只是反应物
D.五氟化磷冷却到-40 ℃,保证了PF5与LiF、无水HF在液相中反应生成LiPF6
20.(2023·深圳外国语学校模拟)亚铁氰化钾K4[Fe(CN)6]是一种黄色颜料。以含铁废水[主要成分为Fe2(SO4)3,含少量NiSO4、CuSO4等]为原料合成亚铁氰化钾的工艺流程如下:
下列说法错误的是( )
A.“调pH”时,选用的试剂X可以是Fe2O3
B.“还原”后,可用溶液KSCN检验Fe3+是否完全被还原
C.“反应”时,发生的反应有:Ca2++SO===CaSO4↓和Fe2++6CN-===[Fe(CN)6]4-
D.“滤渣Ⅱ”的主要成分是CaCO3,K4[Fe(CN)6]的溶解度比Na4[Fe(CN)6]的大
板块Ⅱ 物质结构与转化
选择题突破四 无机物的性质、转化与应用
1.B [A.二氧化硫具有毒性,可用于杀菌、消毒,且还具有还原性,适量添加可用作食品添加剂,如用作葡萄酒抗氧化剂,故A正确;B.浓硝酸具有强的氧化性,常温下使铁和铝发生钝化生成致密氧化膜可以阻止反应继续进行,所以用铁或铝制容器来盛装浓硝酸,钝化属于化学反应,故B错误;C.太阳能、风能、地热能、海洋能和氢能都是新能源,故C正确;D.乙烯具有催熟作用,高锰酸钾溶液能吸收乙烯,故可以用于水果保鲜,故D正确。]
2.D [A.石英坩埚加热KOH固体时能与SiO2反应生成硅酸盐,故A错误;B.P2O5与水反应生成有毒的偏磷酸(HPO3),故不能用作食品干燥剂,故B错误;C.碳酸氢钠与盐酸反应,消耗盐酸,所以可以用于治疗胃酸过多,与其受热分解的性质无关,故C错误;D.钠元素焰色试验显黄色,钠的化合物可用于制作烟花,故D正确。]
3.B [氢氟酸能与SiO2反应,与HF气体的气味无关,B项符合题意。]
4.D [NaClO与HCl反应生成Cl2:ClO-+Cl-+2H+===Cl2↑+H2O,A项不符合题意;NaHCO3受热分解为CO2、Na2CO3和水,可用于做蓬松剂,B项不符合题意;NaNO2具有较强的氧化性,利用维生素C的强还原性可消除体内的NaNO2,C项不符合题意;FeCl3溶液和Cu反应生成FeCl2和CuCl2,不属于置换反应,D项符合题意。]
5.C [物质B是NH3,物质A是NO,由化合价变化规律可知,二者有可能发生反应生成N2,A项正确;氨催化氧化的产物是NO,B项正确;NO→NO2不属于氮的固定,C项错误;常用HNO3和AgNO3检验Cl-,D项正确。]
6.B [如图,a为铜单质;b为+1价铜的氧化物,为Cu2O;c为+2价铜的氧化物,为CuO;d为含铜的碱,为Cu(OH)2;e为+2价铜的盐,如CuCl2;A.氯化铁溶液可作为印刷电路板的刻蚀液,其反应为Cu+2Fe3+===Cu2++2Fe2+,故A错误;B.b为Cu2O,在酸性溶液中发生歧化反应,其反应为Cu2O+2H+===Cu+Cu2++H2O,故B正确;C.c为CuO,d为Cu(OH)2,CuO不能直接转化为Cu(OH)2,故C错误; D.若e为Cu(NO3)2,在酸性条件下NO具有氧化性,Fe2+具有还原性,发生反应3Fe2++4H++NO===3Fe3++NO↑+2H2O,所以Cu(NO3)2溶液中不能大量存在H+、Fe2+,故D错误。]
7.B [A.铁与浓HNO3常温下发生钝化,因此常用铁槽盛放浓HNO3,故A不符合题意;B.HF能与玻璃中的SiO2反应,所以用氢氟酸刻蚀玻璃,故B符合题意;C.用钾盐作紫色烟花原料是因为电子从激发态跃迁到基态释放能量,产生紫色光,故C不符合题意;D.Na高温还原KCl制备金属K ,主要是K的沸点低,故D不符合题意。]
8.B [A.二氧化硫有杀菌作用,并具有较强还原性,可作葡萄酒中的抗氧化剂,防止营养物质被氧化,故A不符合题意;B.用聚乙烯塑料制作食品保鲜膜原因:聚乙烯无毒、无味、无臭,性质稳定,不易分解,易加工,故B符合题意;C.Ag不活泼,冶炼银可用热分解法,2Ag2O4Ag+O2↑,故C不符合题意;D.肥皂主要成分为高级脂肪酸盐,地沟油主要成分是油脂,在碱性条件下发生皂化反应生成高级脂肪酸盐,故D不符合题意。]
9.D [A.二氧化硫具有毒性和还原性,在葡萄酒酿制过程中添加适量二氧化硫的目的是起到杀菌消毒和防止葡萄酒氧化变质的作用,故A不符合题意;B.液氨作制冷剂是因为液氨气化时会吸收热量,使周围环境的温度降低,与破坏氮氢键无关,故B不符合题意;C.二氧化硅是酸性氧化物,不是两性氧化物,故C不符合题意;D.蔗糖遇浓硫酸变黑说明浓硫酸具有脱水性,同时产生有刺激性气味的气体说明碳和浓硫酸反应生成二氧化硫,体现浓硫酸的强氧化性,故D符合题意。]
10.A [从图中可以看出,C为单质,所含元素化合价为0价,A和B均为氢化物,M元素的化合价分别为-3和-2,所以M为氮元素,则A为NH3,B为N2H4,D为NO,E为NO2,F为HNO3,G为硝酸盐。A.物质B为N2H4,其N元素之间只有1个共用电子对,故A错误;B项,依据题给价类二维图有两种氢化物且M的化合价为-3、-2价,综合分析可知M元素为氮元素,故B正确;C项,氢化物NH3或N2H4均可在一定条件下与O2发生反应得到N2和H2O,故C正确;D项,物质F为HNO3,其浓溶液具有强氧化性,可以使铁或铝在常温下发生钝化,因此可以用铁制或铝制容器盛放,故D正确。]
11.B [Al(OH)3能与NaOH等强碱反应,A项错误;氢氟酸与SiO2反应生成SiF4和H2O,可用氢氟酸雕刻玻璃,B项正确;Fe3+和F-形成配位键,NH无孤对电子,无法形成配位键,C项错误;常温下,铁与浓硫酸形成致密氧化膜,阻碍继续反应,D项错误。]
12.B [A.X射线衍射可以区分晶体和非晶体,普通玻璃属于非晶体,水晶属于晶体,故可以区别普通玻璃和水晶,与所述的化学知识有关联,故A不符合题意;B.碳酸氢钠受热分解生成二氧化碳使得糕点疏松,不是NaHCO3可与碱反应,与所述的化学知识没有关联,故B符合题意;C.碘单质易升华而氯化钠不升华,可以加热法分离I2和NaCl,与所述的化学知识有关联,故C不符合题意;D.Al与NaOH溶液反应产生H2,生成气体膨胀可以疏通厨卫管道,与所述的化学知识有关联,故D不符合题意。]
13.B [由图像可知,a为硫酸,b为硫化氢,c为硫单质,d为亚硫酸根,据此分析解题。A.浓硫酸有强氧化性,可与H2S反应生成中间价态的S或SO2,A正确;B.SO2通入紫色石蕊试液中,能变红,但不能褪色,B错误;C.S在空气中燃烧只能生成SO2,C正确;D.SO中S为+4价,既可被氧化,也可被还原,D正确。]
14.B [由图可知,a为氮元素-3价的氢化物,即NH3,b为N2,c为+2价的氧化物,即NO,d为+4价的氧化物,即NO2,e为+5价的酸,即HNO3,据此分析作答。A.根据分析可知,a为NH3,c为NO,一定条件下,a可与O2反应生成c和水,故A正确;B.根据分析可知,a为NH3,工业上将a转化为其他铵态氮肥不属于人工固氮,属于含氮化合物转化为另外一种含氮化合物,故B错误;C.根据分析可知,b为N2,Mg与b在点燃条件下发生反应生成Mg3N2,N元素化合价降低,N2为氧化剂,故C正确;D.根据分析可知,c为NO,d为NO2,e为HNO3,可控制硝酸溶液的浓度选择性制备c或d,故D正确。]
15.A [A.由物质价态及物质类别可知,i为铵盐,c为一氧化氮,无法通过加热铵盐溶液制备一氧化氮,A错误;B.c为一氧化氮,f为硝酸,由元素价态可知一氧化氮在溶液中可被氧化为硝酸,B正确;C.b为氮气,c为一氧化氮,氮的固定是指游离态的氮转化为化合态的氮,自然界中的氮气可在闪电作用下转化为一氧化氮,实现氮的固定,C正确;D.a为氨气,f为硝酸,二者反应生成硝酸铵,可作氮肥,D正确。]
16.C [铝具有两性,所以铝既能与强酸反应又能与强碱反应,常温下,铝遇浓硝酸发生钝化,所以能用铝制容器盛装浓硝酸,二者不存在因果关系,A项错误;Na2O2具有氧化性,但Na2O2与CO2反应产生氧气,二氧化碳既不是氧化剂也不是还原剂,B项错误;纯碱属于强碱弱酸盐,纯碱溶液显碱性,可促进油脂水解,故可用于清洗厨房油污,C项正确;SO2为酸性氧化物,所以SO2通入紫色石蕊溶液后,溶液变红色,D项错误。]
17.D [A.NH4NO3属于氮肥,因此常用NH4NO3对农作物施肥,两者有关联,故A不符合题意;B.乙酸可与CaCO3发生反应,因此用白醋清除水垢,两者有关联,故B不符合题意;C.蛋白质在乙醇作用下会发生变性,因此常用75%的乙醇溶液消毒,两者有关联,故C不符合题意;D.NaHCO3受热分解生成碳酸钠、二氧化碳和水,因此蒸馒头时加入小苏打,与碳酸氢钠是白色固体无关联,故D符合题意。]
18.D [结合价态及物质类别可知X为HCl,Y为HClO,Z为NaClO,W为NaCl;A.Y为HClO,其酸性比碳酸弱,故A错误;B.Z、W均为钠盐,两者焰色试验均观察到黄色焰色,因此不能通过焰色反应区别,故B错误;C.液氯可使湿润的红布条褪色,是因氯气与水反应生成具有漂白性的次氯酸,而液氯自身不具有漂白性,故C错误;D.NaClO具有强氧化性是“84”消毒液的主要成分,故D正确。]
19.C [在铅皿中HF和磷酸发生6HF+H3PO4===HPF6+4H2O,HPF6不稳定,易发生分解反应生成PF5和HF,加入发烟硫酸,发烟硫酸和水结合,在常温下除杂,再将五氟化磷冷却到-40 ℃,加到LiF和无水HF的混合物中反应生成LiPF6。A.N2环境中,根据题中信息6HF+H3PO4===HPF6+4H2O,HPF6易发生分解反应;则反应先生成六氟磷酸(HPF6),HPF6再分解生成五氟化磷(PF5),故A正确;B.发烟硫酸(H2S2O7)的作用是吸收铅皿中的水分:H2S2O7+H2O===2H2SO4,将HF变为无水HF,故B正确;C.工艺流程中,无水HF不仅只是反应物,在HPF6发生分解反应中是产物,故C错误;D.无水HF在-40 ℃状态下是液态,五氟化磷冷却到-40 ℃,保证了PF5与LiF、无水HF在液相中反应生成LiPF6,故D正确。]
20.D [含铁废水中含有Fe2(SO4)3及少量NiSO4,CuSO4等,向其中加入FeO或NiO,反应消耗溶液中的H+,调整溶液pH,弃去滤液,再向固体中同时加入H2SO4、Fe,H2SO4溶解Fe(OH)3生成Fe3+,Fe与溶液中Fe2(SO4)3反应产生FeSO4,然后加入NaCN、CaCl2,FeSO4、CaCl2加入反应器后过滤得到滤渣CaSO4,反应器中生成Na4Fe(CN)6,根据元素守恒知还生成NaCl,向滤液中加入Na2CO3,得到更难溶的CaCO3,在转化罐中加入KCl溶液,过滤、洗涤、干燥得到K4Fe(CN)6,说明在转化罐中发生反应,溶解度大的Na4Fe(CN)6转化为溶解度较小的K4Fe(CN)6。A.由于以含铁废水[主要成分为Fe2(SO4)3,含少量NiSO4,CuSO4等] ,“调pH”时不能引入杂质元素,结合废水成分可知选用的试剂X可以是Fe2O3,A正确;B.Fe3+与KSCN作用使溶液变为红色,“还原”后加入KSCN溶液,若溶液不变红色,说明Fe3+被完全还原,据此检验Fe3+的存在,B正确;C.“反应”之前的溶液中含有硫酸根离子和二价铁离子,由分析可知,“反应”后生成[Fe(CN)6]4-,故该过程发生的反应有:Ca2++SO===CaSO4↓和Fe2++6CN-===[Fe(CN)6]4-,C正确;D.根据上述分析可知“滤渣Ⅱ”的主要成分是CaCO3,由分析可知K4[Fe(CN)6]的溶解度比Na4[Fe(CN)6]的小,D错误。]
A卷
1.(2023·广州执信中学期中)下列说法不正确的是( )
A.二氧化硫可用于杀菌消毒,还是一种食品添加剂
B.常温下,铁、铝和浓硝酸不反应,因此可用铁或铝制容器来盛装浓硝酸
C.太阳能、风能、地热能、海洋能和氢能都是新能源
D.浸泡酸性高锰酸钾溶液的硅藻土可用于水果长途运输的保鲜
2.(2023·汕头潮阳区三模)物质的性质决定其用途。下列生产活动与化学原理均正确且有关联的是( )
选项 生产活动 化学原理
A 石英坩埚可用于加热KOH固体 SiO2熔点高
B P2O5可作食品干燥剂 P2O5具有强吸水性
C NaHCO3可用于抗酸药物 NaHCO3受热易分解
D 钠的化合物可用于制作烟花 钠元素焰色试验显黄色
3.劳动成就梦想。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 厨房帮厨:饭后用热的纯碱溶液洗涤餐具 油脂在碱性条件下发生水解
B 工厂生产:制作玻璃装饰品 HF是一种有刺激性气味的气体
C 社区服务:用泡沫灭火器演练如何灭火 铝离子与碳酸氢根离子在溶液中相互促进水解
D 自主探究:以锌、铜和柠檬为原料制作水果电池 锌能与柠檬中酸性物质发生反应
4.(2023·揭阳联考)化学创造美好生活,下列活动中涉及的物质或反应与相关解释不相符的是( )
选项 物质或反应 相关解释
A “84”消毒液不能与洁厕灵(主要成分是盐酸)混合使用 两种物质混合会放出Cl2
B 做面包时用NaHCO3作蓬松剂 NaHCO3受热易分解
C NaNO2中毒时可用维生素C解毒 利用了维生素C的强还原性
D 用FeCl3溶液刻蚀铜的线路板 FeCl3溶液和Cu发生置换反应
5.(2023·揭阳联考)如图所示是氮元素的几种价态与物质类别的对应关系,下列说法错误的是( )
A.物质B可与物质A反应
B.物质B可经催化氧化直接生成物质A
C.N2―→物质A、物质A―→NO2均为自然固氮
D.HNO3和物质C常用于检验Cl-,则C为AgNO3
6.部分含铜物质的价类关系如图所示。下列说法正确的是( )
A.a能与FeCl3溶液反应:Cu+Fe3+===Cu2++Fe2+
B.b在酸性环境中可以转化为a和e
C.c经一步反应可转化为d
D.若e为Cu(NO3)2,则其水溶液中可能大量存在H+、SO、Fe2+
7.(2023·茂名一模)陈述 Ⅰ 和 Ⅱ 均正确且具有因果关系的是( )
选项 陈述 Ⅰ 陈述 Ⅱ
A 用铁槽盛放浓HNO3 铁不与浓HNO3反应
B 用氢氟酸刻蚀玻璃 HF能与玻璃中的SiO2反应
C 用钾盐作紫色烟花原料 电子跃迁到激发态释放能量,产生紫色光
D Na高温还原KCl制备金属K 金属性:Na
选项 生产活动 化学原理
A 葡萄酒中添加少量SO2 SO2可杀菌且防止营养物质被氧化
B 用聚乙烯塑料制作食品保鲜膜 聚乙烯燃烧生成CO2和H2O
C 利用氧化银冶炼金属Ag 氧化银在一定条件下发生分解反应
D 用地沟油为原料制作肥皂 地沟油发生皂化反应
9.(2023·梅州大埔县三模)下列叙述Ⅰ和Ⅱ均正确且有因果关系的是( )
选项 叙述Ⅰ 叙述Ⅱ
A SO2具有氧化性 在葡萄酒酿制过程中添加适量SO2
B 断裂NH3分子中的N—H键需要吸收热量 工业上用液氨作制冷剂
C 氢氟酸可与SiO2反应得到SiF4 二氧化硅是一种两性氧化物
D 蔗糖遇浓硫酸变黑,同时产生有刺激性气味的气体 浓硫酸具有脱水性和强氧化性
10.如图是M元素高中常见物质的价类二维图。其中A到D、D到E的转化都可加同一种物质实现,且E的相对分子质量比D的相对分子质量大16,则下列说法不正确的是( )
A.物质B可用作火箭燃料,其电子式为
B.依据题给价类二维图综合分析可知M元素为氮元素
C.氢化物A或B均可在一定条件下与氧气反应得到单质C
D.物质F的浓溶液具有强氧化性,可以用铁制或铝制容器盛放
B卷
11.(2023·揭阳联考)陈述Ⅰ和Ⅱ均正确且具有因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A Al(OH)3不与碱反应 氨水和AlCl3制备Al(OH)3
B 用氢氟酸雕刻玻璃 氢氟酸与玻璃中的SiO2反应生成SiF4和H2O
C Fe(SCN)3溶液中加入NH4F变为无色 Fe3+和NH形成配位键
D 生产中用铁槽盛放浓硫酸 铁不与浓硫酸反应
12.劳动创造幸福。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 分析员用X射线衍射仪区分普通玻璃和水晶 普通玻璃属于非晶体,水晶属于晶体
B 面点师制作糕点时添加小苏打作膨松剂 NaHCO3可与碱反应
C 实验员用加热法分离I2和NaCl I2易升华
D 维修工用NaOH和铝粉疏通厨卫管道 Al与NaOH溶液反应产生H2
13.(2024·惠州一次调研)部分含硫物质的分类与相应化合价关系如图所示。下列推断不合理的是( )
A.a的浓溶液与b可生成SO2
B.SO2通入紫色石蕊试液先变红后褪色
C.c在空气中燃烧生成SO2
D.d既可被氧化,也可被还原
14.(2023·深圳科学城高中阶段测试)下图表示部分含氮物质的类别与化合价的关系。其中推断不合理的是( )
A.一定条件下,a可与O2反应生成c
B.工业上将a转化为其它铵态氮肥属于人工固氮
C.Mg与b在点燃条件下发生反应,b为氧化剂
D.可控制e溶液的浓度选择性制备c或d
15.(2023·茂名二模)研究氮及其化合物的性质,与人类生存环境息息相关,结合下图氮及其化合物的价类二维图,下列说法不正确的是( )
A.实验室可通过加热i的溶液制取c
B. 在水溶液中,c能被氧化成f
C.自然固氮可实现b→c的转化
D. 利用a和f反应可生产氮肥
16.(2023·广东一模)下列陈述Ⅰ和陈述Ⅱ均正确且存在因果关系的是( )
选项 陈述Ⅰ 陈述Ⅱ
A Al具有两性 常温下可用铝制容器盛装浓硝酸
B Na2O2具有氧化性 Na2O2可氧化CO2产生氧气
C 纯碱溶液呈碱性 纯碱溶液可用于清洗厨房油污
D SO2具有漂白性 SO2通入紫色石蕊溶液后溶液褪色
17.(2023·深圳统考)下列实践活动与所述的化学知识没有关联的是( )
选项 实践活动 化学知识
A 用NH4NO3对农作物施肥 NH4NO3属于氮肥
B 用白醋清除水垢(主要成分是CaCO3) 乙酸可与CaCO3发生反应
C 用75%的乙醇溶液消毒 蛋白质在乙醇作用下会发生变性
D 蒸馒头时加入小苏打 NaHCO3是白色晶体
18.(2023·江门调研)下图所示为氯的单质及其化合物的价类二维图,其中X、Y、Z、W为含氯化合物。下列说法正确的是( )
A.Y的酸性比碳酸强
B.可以通过焰色试验区别Z、W两种化合物
C.液氯可使湿润的红布条褪色,所以液氯具有漂白性
D.Z是“84”消毒液的主要成分
19.(2023·清远清新模拟预测)六氟磷酸锂(LiPF6)是锂离子电池的关键材料。一种LiPF6的制备工艺流程如图所示。
已知:①6HF+H3PO4===HPF6+4H2O,HPF6易发生分解反应;
②PF5熔点为-93.8 ℃,沸点为-84.6 ℃。
下列说法错误的是( )
A.N2环境中,反应先生成六氟磷酸(HPF6),HPF6再分解生成五氟化磷(PF5)
B.发烟硫酸(H2S2O7)的作用是吸收铅皿中的水分:H2S2O7+H2O===2H2SO4
C.工艺流程中,无水HF只是反应物
D.五氟化磷冷却到-40 ℃,保证了PF5与LiF、无水HF在液相中反应生成LiPF6
20.(2023·深圳外国语学校模拟)亚铁氰化钾K4[Fe(CN)6]是一种黄色颜料。以含铁废水[主要成分为Fe2(SO4)3,含少量NiSO4、CuSO4等]为原料合成亚铁氰化钾的工艺流程如下:
下列说法错误的是( )
A.“调pH”时,选用的试剂X可以是Fe2O3
B.“还原”后,可用溶液KSCN检验Fe3+是否完全被还原
C.“反应”时,发生的反应有:Ca2++SO===CaSO4↓和Fe2++6CN-===[Fe(CN)6]4-
D.“滤渣Ⅱ”的主要成分是CaCO3,K4[Fe(CN)6]的溶解度比Na4[Fe(CN)6]的大
板块Ⅱ 物质结构与转化
选择题突破四 无机物的性质、转化与应用
1.B [A.二氧化硫具有毒性,可用于杀菌、消毒,且还具有还原性,适量添加可用作食品添加剂,如用作葡萄酒抗氧化剂,故A正确;B.浓硝酸具有强的氧化性,常温下使铁和铝发生钝化生成致密氧化膜可以阻止反应继续进行,所以用铁或铝制容器来盛装浓硝酸,钝化属于化学反应,故B错误;C.太阳能、风能、地热能、海洋能和氢能都是新能源,故C正确;D.乙烯具有催熟作用,高锰酸钾溶液能吸收乙烯,故可以用于水果保鲜,故D正确。]
2.D [A.石英坩埚加热KOH固体时能与SiO2反应生成硅酸盐,故A错误;B.P2O5与水反应生成有毒的偏磷酸(HPO3),故不能用作食品干燥剂,故B错误;C.碳酸氢钠与盐酸反应,消耗盐酸,所以可以用于治疗胃酸过多,与其受热分解的性质无关,故C错误;D.钠元素焰色试验显黄色,钠的化合物可用于制作烟花,故D正确。]
3.B [氢氟酸能与SiO2反应,与HF气体的气味无关,B项符合题意。]
4.D [NaClO与HCl反应生成Cl2:ClO-+Cl-+2H+===Cl2↑+H2O,A项不符合题意;NaHCO3受热分解为CO2、Na2CO3和水,可用于做蓬松剂,B项不符合题意;NaNO2具有较强的氧化性,利用维生素C的强还原性可消除体内的NaNO2,C项不符合题意;FeCl3溶液和Cu反应生成FeCl2和CuCl2,不属于置换反应,D项符合题意。]
5.C [物质B是NH3,物质A是NO,由化合价变化规律可知,二者有可能发生反应生成N2,A项正确;氨催化氧化的产物是NO,B项正确;NO→NO2不属于氮的固定,C项错误;常用HNO3和AgNO3检验Cl-,D项正确。]
6.B [如图,a为铜单质;b为+1价铜的氧化物,为Cu2O;c为+2价铜的氧化物,为CuO;d为含铜的碱,为Cu(OH)2;e为+2价铜的盐,如CuCl2;A.氯化铁溶液可作为印刷电路板的刻蚀液,其反应为Cu+2Fe3+===Cu2++2Fe2+,故A错误;B.b为Cu2O,在酸性溶液中发生歧化反应,其反应为Cu2O+2H+===Cu+Cu2++H2O,故B正确;C.c为CuO,d为Cu(OH)2,CuO不能直接转化为Cu(OH)2,故C错误; D.若e为Cu(NO3)2,在酸性条件下NO具有氧化性,Fe2+具有还原性,发生反应3Fe2++4H++NO===3Fe3++NO↑+2H2O,所以Cu(NO3)2溶液中不能大量存在H+、Fe2+,故D错误。]
7.B [A.铁与浓HNO3常温下发生钝化,因此常用铁槽盛放浓HNO3,故A不符合题意;B.HF能与玻璃中的SiO2反应,所以用氢氟酸刻蚀玻璃,故B符合题意;C.用钾盐作紫色烟花原料是因为电子从激发态跃迁到基态释放能量,产生紫色光,故C不符合题意;D.Na高温还原KCl制备金属K ,主要是K的沸点低,故D不符合题意。]
8.B [A.二氧化硫有杀菌作用,并具有较强还原性,可作葡萄酒中的抗氧化剂,防止营养物质被氧化,故A不符合题意;B.用聚乙烯塑料制作食品保鲜膜原因:聚乙烯无毒、无味、无臭,性质稳定,不易分解,易加工,故B符合题意;C.Ag不活泼,冶炼银可用热分解法,2Ag2O4Ag+O2↑,故C不符合题意;D.肥皂主要成分为高级脂肪酸盐,地沟油主要成分是油脂,在碱性条件下发生皂化反应生成高级脂肪酸盐,故D不符合题意。]
9.D [A.二氧化硫具有毒性和还原性,在葡萄酒酿制过程中添加适量二氧化硫的目的是起到杀菌消毒和防止葡萄酒氧化变质的作用,故A不符合题意;B.液氨作制冷剂是因为液氨气化时会吸收热量,使周围环境的温度降低,与破坏氮氢键无关,故B不符合题意;C.二氧化硅是酸性氧化物,不是两性氧化物,故C不符合题意;D.蔗糖遇浓硫酸变黑说明浓硫酸具有脱水性,同时产生有刺激性气味的气体说明碳和浓硫酸反应生成二氧化硫,体现浓硫酸的强氧化性,故D符合题意。]
10.A [从图中可以看出,C为单质,所含元素化合价为0价,A和B均为氢化物,M元素的化合价分别为-3和-2,所以M为氮元素,则A为NH3,B为N2H4,D为NO,E为NO2,F为HNO3,G为硝酸盐。A.物质B为N2H4,其N元素之间只有1个共用电子对,故A错误;B项,依据题给价类二维图有两种氢化物且M的化合价为-3、-2价,综合分析可知M元素为氮元素,故B正确;C项,氢化物NH3或N2H4均可在一定条件下与O2发生反应得到N2和H2O,故C正确;D项,物质F为HNO3,其浓溶液具有强氧化性,可以使铁或铝在常温下发生钝化,因此可以用铁制或铝制容器盛放,故D正确。]
11.B [Al(OH)3能与NaOH等强碱反应,A项错误;氢氟酸与SiO2反应生成SiF4和H2O,可用氢氟酸雕刻玻璃,B项正确;Fe3+和F-形成配位键,NH无孤对电子,无法形成配位键,C项错误;常温下,铁与浓硫酸形成致密氧化膜,阻碍继续反应,D项错误。]
12.B [A.X射线衍射可以区分晶体和非晶体,普通玻璃属于非晶体,水晶属于晶体,故可以区别普通玻璃和水晶,与所述的化学知识有关联,故A不符合题意;B.碳酸氢钠受热分解生成二氧化碳使得糕点疏松,不是NaHCO3可与碱反应,与所述的化学知识没有关联,故B符合题意;C.碘单质易升华而氯化钠不升华,可以加热法分离I2和NaCl,与所述的化学知识有关联,故C不符合题意;D.Al与NaOH溶液反应产生H2,生成气体膨胀可以疏通厨卫管道,与所述的化学知识有关联,故D不符合题意。]
13.B [由图像可知,a为硫酸,b为硫化氢,c为硫单质,d为亚硫酸根,据此分析解题。A.浓硫酸有强氧化性,可与H2S反应生成中间价态的S或SO2,A正确;B.SO2通入紫色石蕊试液中,能变红,但不能褪色,B错误;C.S在空气中燃烧只能生成SO2,C正确;D.SO中S为+4价,既可被氧化,也可被还原,D正确。]
14.B [由图可知,a为氮元素-3价的氢化物,即NH3,b为N2,c为+2价的氧化物,即NO,d为+4价的氧化物,即NO2,e为+5价的酸,即HNO3,据此分析作答。A.根据分析可知,a为NH3,c为NO,一定条件下,a可与O2反应生成c和水,故A正确;B.根据分析可知,a为NH3,工业上将a转化为其他铵态氮肥不属于人工固氮,属于含氮化合物转化为另外一种含氮化合物,故B错误;C.根据分析可知,b为N2,Mg与b在点燃条件下发生反应生成Mg3N2,N元素化合价降低,N2为氧化剂,故C正确;D.根据分析可知,c为NO,d为NO2,e为HNO3,可控制硝酸溶液的浓度选择性制备c或d,故D正确。]
15.A [A.由物质价态及物质类别可知,i为铵盐,c为一氧化氮,无法通过加热铵盐溶液制备一氧化氮,A错误;B.c为一氧化氮,f为硝酸,由元素价态可知一氧化氮在溶液中可被氧化为硝酸,B正确;C.b为氮气,c为一氧化氮,氮的固定是指游离态的氮转化为化合态的氮,自然界中的氮气可在闪电作用下转化为一氧化氮,实现氮的固定,C正确;D.a为氨气,f为硝酸,二者反应生成硝酸铵,可作氮肥,D正确。]
16.C [铝具有两性,所以铝既能与强酸反应又能与强碱反应,常温下,铝遇浓硝酸发生钝化,所以能用铝制容器盛装浓硝酸,二者不存在因果关系,A项错误;Na2O2具有氧化性,但Na2O2与CO2反应产生氧气,二氧化碳既不是氧化剂也不是还原剂,B项错误;纯碱属于强碱弱酸盐,纯碱溶液显碱性,可促进油脂水解,故可用于清洗厨房油污,C项正确;SO2为酸性氧化物,所以SO2通入紫色石蕊溶液后,溶液变红色,D项错误。]
17.D [A.NH4NO3属于氮肥,因此常用NH4NO3对农作物施肥,两者有关联,故A不符合题意;B.乙酸可与CaCO3发生反应,因此用白醋清除水垢,两者有关联,故B不符合题意;C.蛋白质在乙醇作用下会发生变性,因此常用75%的乙醇溶液消毒,两者有关联,故C不符合题意;D.NaHCO3受热分解生成碳酸钠、二氧化碳和水,因此蒸馒头时加入小苏打,与碳酸氢钠是白色固体无关联,故D符合题意。]
18.D [结合价态及物质类别可知X为HCl,Y为HClO,Z为NaClO,W为NaCl;A.Y为HClO,其酸性比碳酸弱,故A错误;B.Z、W均为钠盐,两者焰色试验均观察到黄色焰色,因此不能通过焰色反应区别,故B错误;C.液氯可使湿润的红布条褪色,是因氯气与水反应生成具有漂白性的次氯酸,而液氯自身不具有漂白性,故C错误;D.NaClO具有强氧化性是“84”消毒液的主要成分,故D正确。]
19.C [在铅皿中HF和磷酸发生6HF+H3PO4===HPF6+4H2O,HPF6不稳定,易发生分解反应生成PF5和HF,加入发烟硫酸,发烟硫酸和水结合,在常温下除杂,再将五氟化磷冷却到-40 ℃,加到LiF和无水HF的混合物中反应生成LiPF6。A.N2环境中,根据题中信息6HF+H3PO4===HPF6+4H2O,HPF6易发生分解反应;则反应先生成六氟磷酸(HPF6),HPF6再分解生成五氟化磷(PF5),故A正确;B.发烟硫酸(H2S2O7)的作用是吸收铅皿中的水分:H2S2O7+H2O===2H2SO4,将HF变为无水HF,故B正确;C.工艺流程中,无水HF不仅只是反应物,在HPF6发生分解反应中是产物,故C错误;D.无水HF在-40 ℃状态下是液态,五氟化磷冷却到-40 ℃,保证了PF5与LiF、无水HF在液相中反应生成LiPF6,故D正确。]
20.D [含铁废水中含有Fe2(SO4)3及少量NiSO4,CuSO4等,向其中加入FeO或NiO,反应消耗溶液中的H+,调整溶液pH,弃去滤液,再向固体中同时加入H2SO4、Fe,H2SO4溶解Fe(OH)3生成Fe3+,Fe与溶液中Fe2(SO4)3反应产生FeSO4,然后加入NaCN、CaCl2,FeSO4、CaCl2加入反应器后过滤得到滤渣CaSO4,反应器中生成Na4Fe(CN)6,根据元素守恒知还生成NaCl,向滤液中加入Na2CO3,得到更难溶的CaCO3,在转化罐中加入KCl溶液,过滤、洗涤、干燥得到K4Fe(CN)6,说明在转化罐中发生反应,溶解度大的Na4Fe(CN)6转化为溶解度较小的K4Fe(CN)6。A.由于以含铁废水[主要成分为Fe2(SO4)3,含少量NiSO4,CuSO4等] ,“调pH”时不能引入杂质元素,结合废水成分可知选用的试剂X可以是Fe2O3,A正确;B.Fe3+与KSCN作用使溶液变为红色,“还原”后加入KSCN溶液,若溶液不变红色,说明Fe3+被完全还原,据此检验Fe3+的存在,B正确;C.“反应”之前的溶液中含有硫酸根离子和二价铁离子,由分析可知,“反应”后生成[Fe(CN)6]4-,故该过程发生的反应有:Ca2++SO===CaSO4↓和Fe2++6CN-===[Fe(CN)6]4-,C正确;D.根据上述分析可知“滤渣Ⅱ”的主要成分是CaCO3,由分析可知K4[Fe(CN)6]的溶解度比Na4[Fe(CN)6]的小,D错误。]
同课章节目录
