4.1.2元素周期和核素课件(共35张ppt)化学人教版(2019)必修第一册
文档属性
| 名称 | 4.1.2元素周期和核素课件(共35张ppt)化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 16.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-12 00:00:00 | ||
图片预览






文档简介
(共35张PPT)
4.1 原子结构与元素周期表
第二课时 元素周期和核素
化学人教版(2019)必修第一册
导入新课:门捷列夫与元素周期表
知识目标:
了解元素周期表的结构,掌握周期、族等概念,熟练掌握1-20号元素在元素周期表中位置。
能力目标:
能根据原子序数推断出元素在周期表中位置,培养分析推理能力和模型认知能力。
素养目标:
了解元素周期表发展史,体会元素周期表在学习元素及其化合物知识及科学研究中的重要作用,培养科学探究、社会责任素养。
·学习目标·
1.什么是原子序数?
2.原子序数= = =
任务一 知识梳理
质子数
核电荷数
核外电子数
按照元素在周期表中的顺序给元素编号,得到原子序数
揭示化学元素间的内在联系和规律性
为未知元素留下的空位先后被填满
1869年,俄国化学家_________制出
门捷列夫
将元素按____________由小到大排列,将____________的元素放在一起
相对原子质量
化学性质相似
排序依据改为原子的_________
核电荷数
任务二 元素周期表发展
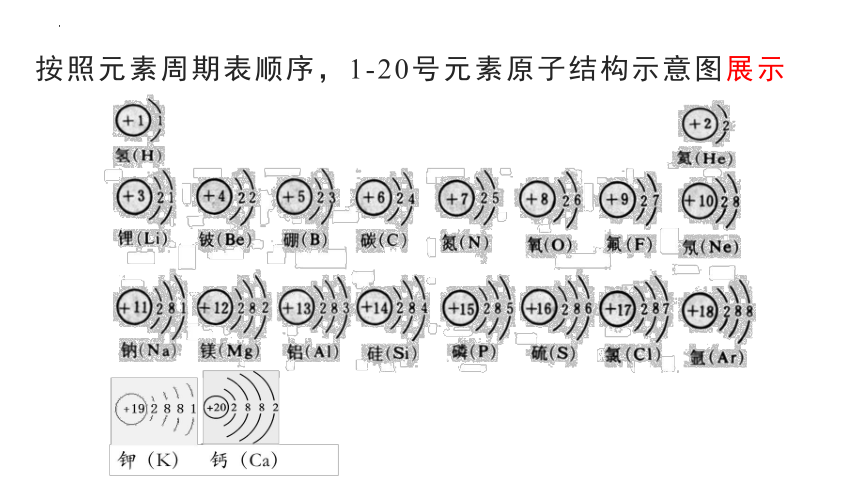
按照元素周期表顺序,1-20号元素原子结构示意图展示
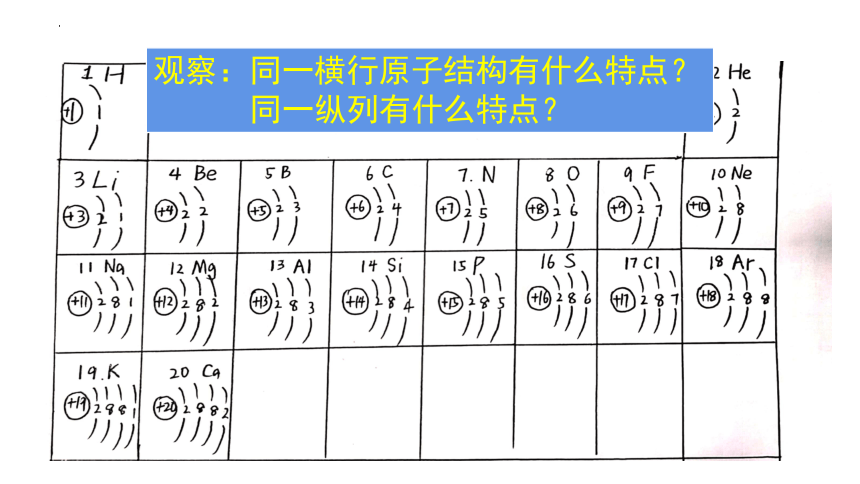
观察:同一横行原子结构有什么特点?
同一纵列有什么特点?
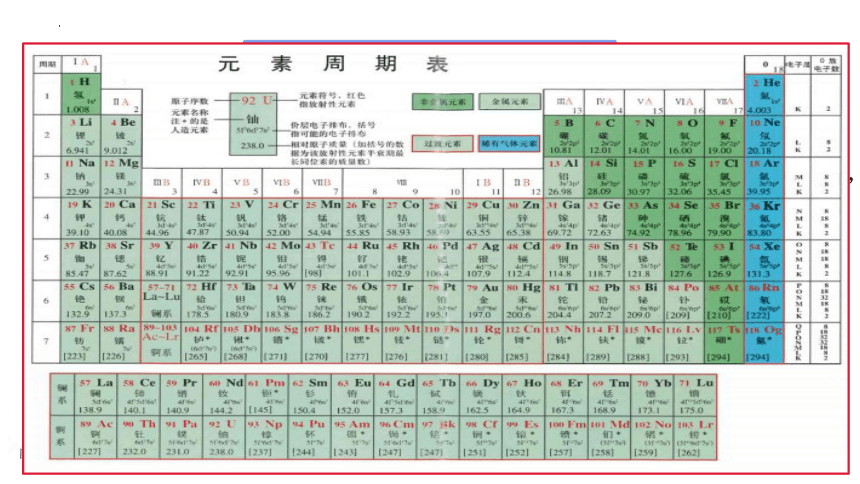
任务三 元素周期表的结构
(1)按________________递增的顺序从左到右排列
(2)将________________的元素排成一个横行 ,叫: ;
(3)把__________________的元素排成一个纵列,叫: 。
原子的核电荷数
电子层数相同
最外层电子数相同
元素周期表的编排原则
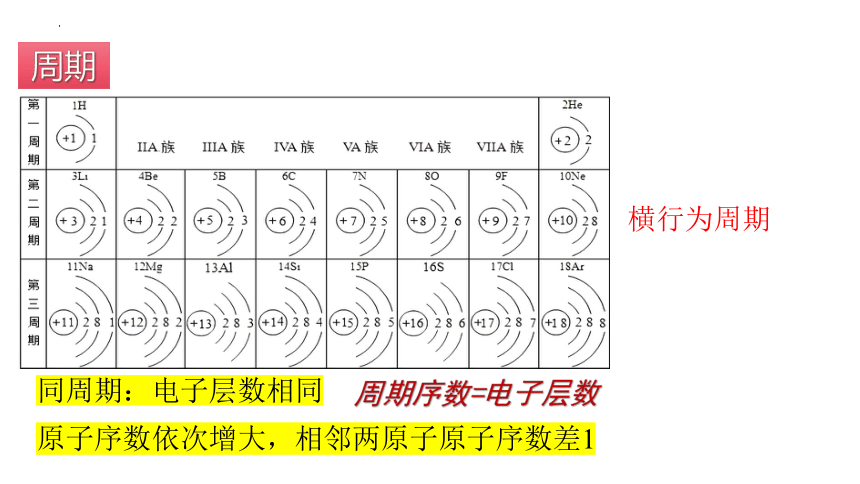
周期
族
周期
横行为周期
同周期:电子层数相同
原子序数依次增大,相邻两原子原子序数差1
周期序数=电子层数
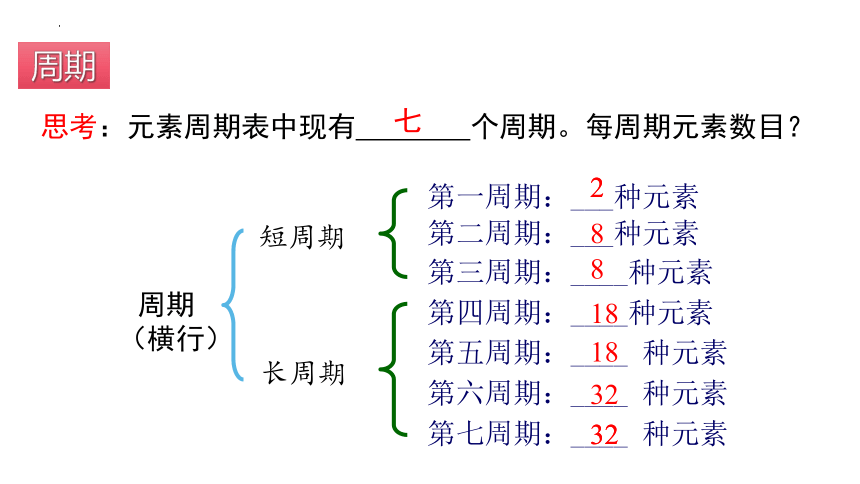
短周期
长周期
第一周期:___种元素
第二周期:___种元素
第三周期:____种元素
第四周期:____种元素
第五周期:____ 种元素
第六周期:____ 种元素
第七周期:____ 种元素
周期
(横行)
8
2
18
8
18
32
32
思考:元素周期表中现有 个周期。每周期元素数目?
七
周期
2
32
长周期
短周期
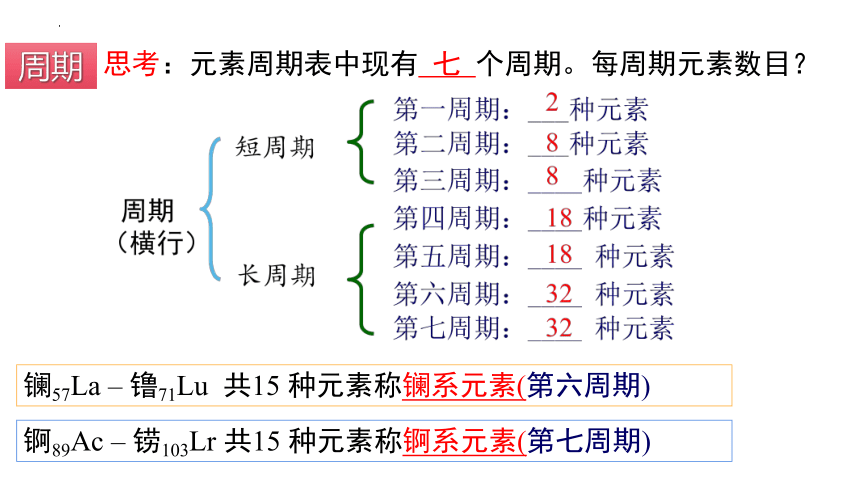
镧57La – 镥71Lu 共15 种元素称镧系元素(第六周期)
锕89Ac – 铹103Lr 共15 种元素称锕系元素(第七周期)
思考:元素周期表中现有 七 个周期。每周期元素数目?
周期
类别 周期序数 起止元素 包括元 素种数 核外电 子层数 稀有气体 原子序数 位置与结
构的关系
短周期 1 H~He 周期序数___电子层数
2 3 长周期 4 5 6 7 Fr~Og(118号) 2
1
2
8
2
10
8
3
18
18
4
36
18
5
54
32
6
86
32
7
118
=
三短四长七周期
Li~Ne
Na~Ar
K~Kr
Rb~Xe
Cs~Rn
完成P89思考与讨论
族
同族元素最外层电子数相同,电子层数依次增加
纵列为族
主族:
副族:
ⅠA , ⅡA , ⅢA , ⅣA ,ⅤA , ⅥA , ⅦA
第VIII 族
稀有气体元素(第18列)
主族序数 最外层电子数
族
(纵列)
0族:
共七个主族
ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB , ⅠB , ⅡB
共八个副族:
8、9、10三个纵列,位于Ⅶ B 与Ⅰ B中间
思考:1.元素周期表中共有 个纵列;
2.罗马数字标注的为族,一共 个族;
18
16
第VIII族有3列
由 周期组成
由 周期组成,共10列
各族元素是在周期表中分布在哪一列?是连续排列的么?
长、短
长
=
族
主族
副族(8个)10列
第VIII族
零族
主族
1.不看元素周期表,结合以上学习,你能不能写出0族元素原子序数?
2
10
18
36
54
86
118
思考与讨论
2.第Ⅰ A族,相邻元素原子序数差值为?
3.哪周期元素种类最多?族呢?
第ⅢB族
第六周期、第七周期
族的别称
第ⅠA族称为 元素
第ⅡA族称为 元素
第ⅣA族称为 元素
第ⅤA族称为 元素
碱金属
碱土金属
碳族
氮族
氧族
卤族
稀有气体
拓展延伸
第ⅥA族称为 元素
第ⅦA族称为 元素
零族称为 元素
过渡元素:元素周期表中从ⅢB到ⅡB共10个纵行,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为金属元素,统称为过渡元素。
思考:Cl的位置的描述:
第七主族
VII族
第VIIA族
第III周期
第三周期
第3周期
第三周期第VIIA族
1、氦元素原子最外层有两个电子,为什么不把它排在ⅡA族?
2、哪周期元素种类最多?族呢?
第ⅢB族
第六周期、第七周期
头脑风暴
放在一族是表示这一族的元素化学性质接近,如H被放在和Li,Na等同一族,是因为它们在反应中都容易失去1个电子变成+1价离子. 但He最外层2电子是稳定结构,它不会像Mg,Ca这样在反应中失去2电子变成+2价离子,它们化学性质完全不同,
小结:
一到八 先主后副 八是VⅢ
一到八 先副后主 八是0
逢2剪断
任务四 元素周期表的规律和典型应用
1.原子结构定元素位置——主族已知某主族元素的原子结构示意图如下,判断其位于第几周期?第几族?
C在元素周期表中的位置?
Si在元素周期表中的位置?
短周期主族元素
电子层数=周期序数
最外层电子数=主族序数
第一主族
I族
第IA族
第III周期
第三周期
第3周期
2.零族定位
(1)第17号元素位于第________周期________族。
(2) 56号元素位于第________周期________族。
0族元素 He Ne Ar Kr Xe Rn Og
周期序数 一 二 三 四 五 六 七
原子序数 2 10 18 36 54 86 118
找出与其相邻近的0族元素,
①若某元素原子序数比相应的0族元素多1或2,则该元素应处在0族元素所在周期的下一个周期的ⅠA族或ⅡA族。
②若比相应的0族元素少1~5时,则应处在同周期的ⅦA~ⅢA族。
③若差其他数,则由相应差数找出相应的族。
比大小定周期,求差值定族数
下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是( )
A
B
C
D
A
B
C
D
单选题
3.十字定位
同主族相邻元素原子序数的差值
8
8
18
18
18
32
32
练习:
X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示。已知X、Y、Z三种元素的质子数之和为40,则X、Y、Z分别是()
A.N、S、Cl B.B、Si、P
C.C、P、S D.Be、Al、Si
4.根据元素周期表排布思考,同周期,第ⅡA 族和第ⅢA族原子序数差值不可能为?
A.1 B.11 C.19 D.25
为什么课本P90页图4-4b中 H 的质量数有3个呢?
1、元素
1
1H
2
1H
3
1H
氢元素的三种原子
元素是具有相同质子数(核电荷数)的一类原子的总称。
决定元素种类的是质子数,与中子数和核外电子无关。
2、核素
把具有一定数目质子和一定数目中子的一种原子叫做核素
1
1H
2
1H
3
1H
是氢元素的三种核素
决定核素种类的是质子数与中子数,与核外电子无关。
任务五 核素
氢元素的 原子核 原子 名称
质子数(Z) 中子数(N) 1 0 氕(pie)
1 1 氘(dao)
1 2 氚(chuan)
3、同位素
①概念:质子数相同而中子数不同的同一元素的不同原子的互称同位素(即同一种元素的不同核素互称为同位素)
1
1H
2
1H
3
1H
氢元素的三种核素
不能。原子的种类远大于元素的种类
2
1H
3
1H
(符号T。又称超重氢)
(符号D。又称重氢)
思考:至今已发现了118种元素,能否说人们已发现了118种原子?
互称同位素
“同位”即指核素的质子数相同,在周期表中占有相同位置
a:同位素的化学性质几乎完全相同,物理性质略有差异。
b:在天然存在的某种元素里,不论是游离态还是化合态,各种同位素的原子个数百分比(丰度)一般为定值。
②同位素的特征:
③同种元素不同的同位素原子也可组成不同单质或化合物的分子。
1
1H
2
1H
3
1H
④同位素的种类和应用:
氢元素:
氧元素:
碳元素:
铀元素:
16
8O
17
8O
18
8O
12
6C
13
6C
14
6C
234
92U
235
92U
238
92U
制造氢弹
考古时测一些文物的年代
原子弹的原料和核反应堆的燃料
同位素示踪
相对原子质量和阿伏伽德罗常数的标准
天然存在的同位素
人工制造的同位素
放射性同位素
利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病……
a:分类
b:应用
4、元素的相对原子质量
天然存在的同位素,相互间保持着一定的比率。元素的相对原子质量,就是按照该元素各种核素所占的一定百分比计算出来的平均值。
原子的相对原子质量=
原子的近似相对原子质量
原子的质量÷碳原子质量的1/12
≈质量数
5、元素、核素、同位素与同素异形体的关系
一种元素可能有多种核素,
这几种核素互称为同位素
元素 核素 同位素 同素异形体
本质
范畴
特性
决定因素
举例
质子数相同的一类原子
质子数、中子数都一定的原子
质子数相同、中子数不同的核素
同种元素形成的不同单质
同类原子
原子
原子
单质
只有种类,没有个数
化学反应中的最小微粒
化学性质几乎完全相同
元素相同
性质不同
质子数
质子数、中子数
质子数、中子数
组成元素、结构
H、C、O
三种元素
1H
1
1H
2
1H
3
三种核素
1H
1
1H
2
1H
3
互称同位素
O2、O3互为同素异形体
项目
内容
“四素”的区别
课堂小结
1、知识梳理
2、元素周期表的发展
5、核素
3、元素周期表的结构
4、元素周期表的规律和典型应用
4.1 原子结构与元素周期表
第二课时 元素周期和核素
化学人教版(2019)必修第一册
导入新课:门捷列夫与元素周期表
知识目标:
了解元素周期表的结构,掌握周期、族等概念,熟练掌握1-20号元素在元素周期表中位置。
能力目标:
能根据原子序数推断出元素在周期表中位置,培养分析推理能力和模型认知能力。
素养目标:
了解元素周期表发展史,体会元素周期表在学习元素及其化合物知识及科学研究中的重要作用,培养科学探究、社会责任素养。
·学习目标·
1.什么是原子序数?
2.原子序数= = =
任务一 知识梳理
质子数
核电荷数
核外电子数
按照元素在周期表中的顺序给元素编号,得到原子序数
揭示化学元素间的内在联系和规律性
为未知元素留下的空位先后被填满
1869年,俄国化学家_________制出
门捷列夫
将元素按____________由小到大排列,将____________的元素放在一起
相对原子质量
化学性质相似
排序依据改为原子的_________
核电荷数
任务二 元素周期表发展
按照元素周期表顺序,1-20号元素原子结构示意图展示
观察:同一横行原子结构有什么特点?
同一纵列有什么特点?
任务三 元素周期表的结构
(1)按________________递增的顺序从左到右排列
(2)将________________的元素排成一个横行 ,叫: ;
(3)把__________________的元素排成一个纵列,叫: 。
原子的核电荷数
电子层数相同
最外层电子数相同
元素周期表的编排原则
周期
族
周期
横行为周期
同周期:电子层数相同
原子序数依次增大,相邻两原子原子序数差1
周期序数=电子层数
短周期
长周期
第一周期:___种元素
第二周期:___种元素
第三周期:____种元素
第四周期:____种元素
第五周期:____ 种元素
第六周期:____ 种元素
第七周期:____ 种元素
周期
(横行)
8
2
18
8
18
32
32
思考:元素周期表中现有 个周期。每周期元素数目?
七
周期
2
32
长周期
短周期
镧57La – 镥71Lu 共15 种元素称镧系元素(第六周期)
锕89Ac – 铹103Lr 共15 种元素称锕系元素(第七周期)
思考:元素周期表中现有 七 个周期。每周期元素数目?
周期
类别 周期序数 起止元素 包括元 素种数 核外电 子层数 稀有气体 原子序数 位置与结
构的关系
短周期 1 H~He 周期序数___电子层数
2 3 长周期 4 5 6 7 Fr~Og(118号) 2
1
2
8
2
10
8
3
18
18
4
36
18
5
54
32
6
86
32
7
118
=
三短四长七周期
Li~Ne
Na~Ar
K~Kr
Rb~Xe
Cs~Rn
完成P89思考与讨论
族
同族元素最外层电子数相同,电子层数依次增加
纵列为族
主族:
副族:
ⅠA , ⅡA , ⅢA , ⅣA ,ⅤA , ⅥA , ⅦA
第VIII 族
稀有气体元素(第18列)
主族序数 最外层电子数
族
(纵列)
0族:
共七个主族
ⅢB , ⅣB ,ⅤB , ⅥB , ⅦB , ⅠB , ⅡB
共八个副族:
8、9、10三个纵列,位于Ⅶ B 与Ⅰ B中间
思考:1.元素周期表中共有 个纵列;
2.罗马数字标注的为族,一共 个族;
18
16
第VIII族有3列
由 周期组成
由 周期组成,共10列
各族元素是在周期表中分布在哪一列?是连续排列的么?
长、短
长
=
族
主族
副族(8个)10列
第VIII族
零族
主族
1.不看元素周期表,结合以上学习,你能不能写出0族元素原子序数?
2
10
18
36
54
86
118
思考与讨论
2.第Ⅰ A族,相邻元素原子序数差值为?
3.哪周期元素种类最多?族呢?
第ⅢB族
第六周期、第七周期
族的别称
第ⅠA族称为 元素
第ⅡA族称为 元素
第ⅣA族称为 元素
第ⅤA族称为 元素
碱金属
碱土金属
碳族
氮族
氧族
卤族
稀有气体
拓展延伸
第ⅥA族称为 元素
第ⅦA族称为 元素
零族称为 元素
过渡元素:元素周期表中从ⅢB到ⅡB共10个纵行,包括了第Ⅷ族和全部副族元素,共60多种元素,全部为金属元素,统称为过渡元素。
思考:Cl的位置的描述:
第七主族
VII族
第VIIA族
第III周期
第三周期
第3周期
第三周期第VIIA族
1、氦元素原子最外层有两个电子,为什么不把它排在ⅡA族?
2、哪周期元素种类最多?族呢?
第ⅢB族
第六周期、第七周期
头脑风暴
放在一族是表示这一族的元素化学性质接近,如H被放在和Li,Na等同一族,是因为它们在反应中都容易失去1个电子变成+1价离子. 但He最外层2电子是稳定结构,它不会像Mg,Ca这样在反应中失去2电子变成+2价离子,它们化学性质完全不同,
小结:
一到八 先主后副 八是VⅢ
一到八 先副后主 八是0
逢2剪断
任务四 元素周期表的规律和典型应用
1.原子结构定元素位置——主族已知某主族元素的原子结构示意图如下,判断其位于第几周期?第几族?
C在元素周期表中的位置?
Si在元素周期表中的位置?
短周期主族元素
电子层数=周期序数
最外层电子数=主族序数
第一主族
I族
第IA族
第III周期
第三周期
第3周期
2.零族定位
(1)第17号元素位于第________周期________族。
(2) 56号元素位于第________周期________族。
0族元素 He Ne Ar Kr Xe Rn Og
周期序数 一 二 三 四 五 六 七
原子序数 2 10 18 36 54 86 118
找出与其相邻近的0族元素,
①若某元素原子序数比相应的0族元素多1或2,则该元素应处在0族元素所在周期的下一个周期的ⅠA族或ⅡA族。
②若比相应的0族元素少1~5时,则应处在同周期的ⅦA~ⅢA族。
③若差其他数,则由相应差数找出相应的族。
比大小定周期,求差值定族数
下列各图为元素周期表的一部分,表中的数字为原子序数,其中M为37的是( )
A
B
C
D
A
B
C
D
单选题
3.十字定位
同主族相邻元素原子序数的差值
8
8
18
18
18
32
32
练习:
X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示。已知X、Y、Z三种元素的质子数之和为40,则X、Y、Z分别是()
A.N、S、Cl B.B、Si、P
C.C、P、S D.Be、Al、Si
4.根据元素周期表排布思考,同周期,第ⅡA 族和第ⅢA族原子序数差值不可能为?
A.1 B.11 C.19 D.25
为什么课本P90页图4-4b中 H 的质量数有3个呢?
1、元素
1
1H
2
1H
3
1H
氢元素的三种原子
元素是具有相同质子数(核电荷数)的一类原子的总称。
决定元素种类的是质子数,与中子数和核外电子无关。
2、核素
把具有一定数目质子和一定数目中子的一种原子叫做核素
1
1H
2
1H
3
1H
是氢元素的三种核素
决定核素种类的是质子数与中子数,与核外电子无关。
任务五 核素
氢元素的 原子核 原子 名称
质子数(Z) 中子数(N) 1 0 氕(pie)
1 1 氘(dao)
1 2 氚(chuan)
3、同位素
①概念:质子数相同而中子数不同的同一元素的不同原子的互称同位素(即同一种元素的不同核素互称为同位素)
1
1H
2
1H
3
1H
氢元素的三种核素
不能。原子的种类远大于元素的种类
2
1H
3
1H
(符号T。又称超重氢)
(符号D。又称重氢)
思考:至今已发现了118种元素,能否说人们已发现了118种原子?
互称同位素
“同位”即指核素的质子数相同,在周期表中占有相同位置
a:同位素的化学性质几乎完全相同,物理性质略有差异。
b:在天然存在的某种元素里,不论是游离态还是化合态,各种同位素的原子个数百分比(丰度)一般为定值。
②同位素的特征:
③同种元素不同的同位素原子也可组成不同单质或化合物的分子。
1
1H
2
1H
3
1H
④同位素的种类和应用:
氢元素:
氧元素:
碳元素:
铀元素:
16
8O
17
8O
18
8O
12
6C
13
6C
14
6C
234
92U
235
92U
238
92U
制造氢弹
考古时测一些文物的年代
原子弹的原料和核反应堆的燃料
同位素示踪
相对原子质量和阿伏伽德罗常数的标准
天然存在的同位素
人工制造的同位素
放射性同位素
利用放射性同位素释放的射线育种、给金属探伤、诊断和治疗疾病……
a:分类
b:应用
4、元素的相对原子质量
天然存在的同位素,相互间保持着一定的比率。元素的相对原子质量,就是按照该元素各种核素所占的一定百分比计算出来的平均值。
原子的相对原子质量=
原子的近似相对原子质量
原子的质量÷碳原子质量的1/12
≈质量数
5、元素、核素、同位素与同素异形体的关系
一种元素可能有多种核素,
这几种核素互称为同位素
元素 核素 同位素 同素异形体
本质
范畴
特性
决定因素
举例
质子数相同的一类原子
质子数、中子数都一定的原子
质子数相同、中子数不同的核素
同种元素形成的不同单质
同类原子
原子
原子
单质
只有种类,没有个数
化学反应中的最小微粒
化学性质几乎完全相同
元素相同
性质不同
质子数
质子数、中子数
质子数、中子数
组成元素、结构
H、C、O
三种元素
1H
1
1H
2
1H
3
三种核素
1H
1
1H
2
1H
3
互称同位素
O2、O3互为同素异形体
项目
内容
“四素”的区别
课堂小结
1、知识梳理
2、元素周期表的发展
5、核素
3、元素周期表的结构
4、元素周期表的规律和典型应用
