2024年中考化学专题——化学式与化合价(含解析)
文档属性
| 名称 | 2024年中考化学专题——化学式与化合价(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 418.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-12 09:13:43 | ||
图片预览



文档简介
2024年中考化学专题——化学式与化合价
一、选择题
1.“遥知不是雪,为有暗香来”,梅花有香味的主要因为含有苯甲醇(化学式C7H8O)。下列有关苯甲醇的说法错误的是
A.由碳、氢、氧三种元素组成 B.其中氧元素的质量分数最小
C.一个苯甲醇分子含有16个原子 D.完全燃烧生成CO2和H2O
2.下列化学观念及描述合理的是
A.元素观:高锰酸钾是由钾元素和锰元素组成的化合物
B.守恒观:铜在空气中灼烧前后固体的质量不变
C.微粒观;二氧化碳是碳原子和氧分子构成的
D.转化观;和在一定条件下可相互转化
3.下列说法正确的是
A.蜡烛燃烧后质量减少,不符合质量守恒定律 B.在H2O中,氧元素的化合价为2价
C.一种元素在一种化合物中只能表现一种化合价 D.在化合物中,正、负化合价的代数和为零
4.意大利科学家最近合成了新型的氧分子,对其说法正确的是
A.是一种新型的化合物 B.是一种混合物
C.和都是氧元素的单质 D.一个分子含有2个分子
5.没食子酸(化学式为)是世界上最早制得的有机酸,中医常用其治疗流感。明代李梴的《医学入门》中记载了制取没食子酸的方法。下列说法错误的是
A.没食子酸属于化合物 B.没食子酸由碳、氢、氧三种元素组成
C.没食子酸中碳、氧元素的质量比为7:5 D.没食子酸中氢元素的质量分数最小
6.学生作业中出现的包含数字“2”的符号及其意义均正确的是
A.:镁离子带两个单位的正电荷 B.:两个氧原子
C.2N:两个氮分子 D.:-2价的硫元素
7.工业用盐亚硝酸钠,其化学式为NaNO2,外观与食盐相似,有咸味,但价格更低,有不法分子常在食盐中可加入NaNO2牟利。NaNO2中N的化合价为
A.0 B.+5 C.+3 D.-2
8.《木草纲目》中记载的金银花具有清热解毒、疏散风热的功效,其有效成分之一是绿原酸(化学式为C16H18O9)。下列有关绿原酸的说法错误的是
A.由碳、氢、氧元素组成 B.由43个原子构成
C.相对分子质量为354 D.其中氢元素的质量分数最小
9.在纳米纸上“铺”一层“萘胺”(C10H9N)制作而成的试纸,可用于检测食品中亚硝酸盐的含量,保证食品安全。下列有关萘胺的说法正确的是
A.萘胺属于有机物
B.一个萘胺分子的质量为143g
C.萘胺中氮元素的质量分数最小
D.萘胺在氧气中燃烧产物只有CO2
10.我国自主知识产权的抗癌新药“西达本胺”已全球上市。西达本胺的化学式为,下列有关西达本胺的说法正确的是
A.西达本胺由碳、氢、氟、氮、氧五个元素组成
B.西达本胺是由22个碳原子、19个氢原子、1个氟原子、4个氮原子和2个氧原子构成
C.西达本胺中碳、氧元素的质量比为11:1
D.西达本胺中碳元素的质量分数最大
二、实验题
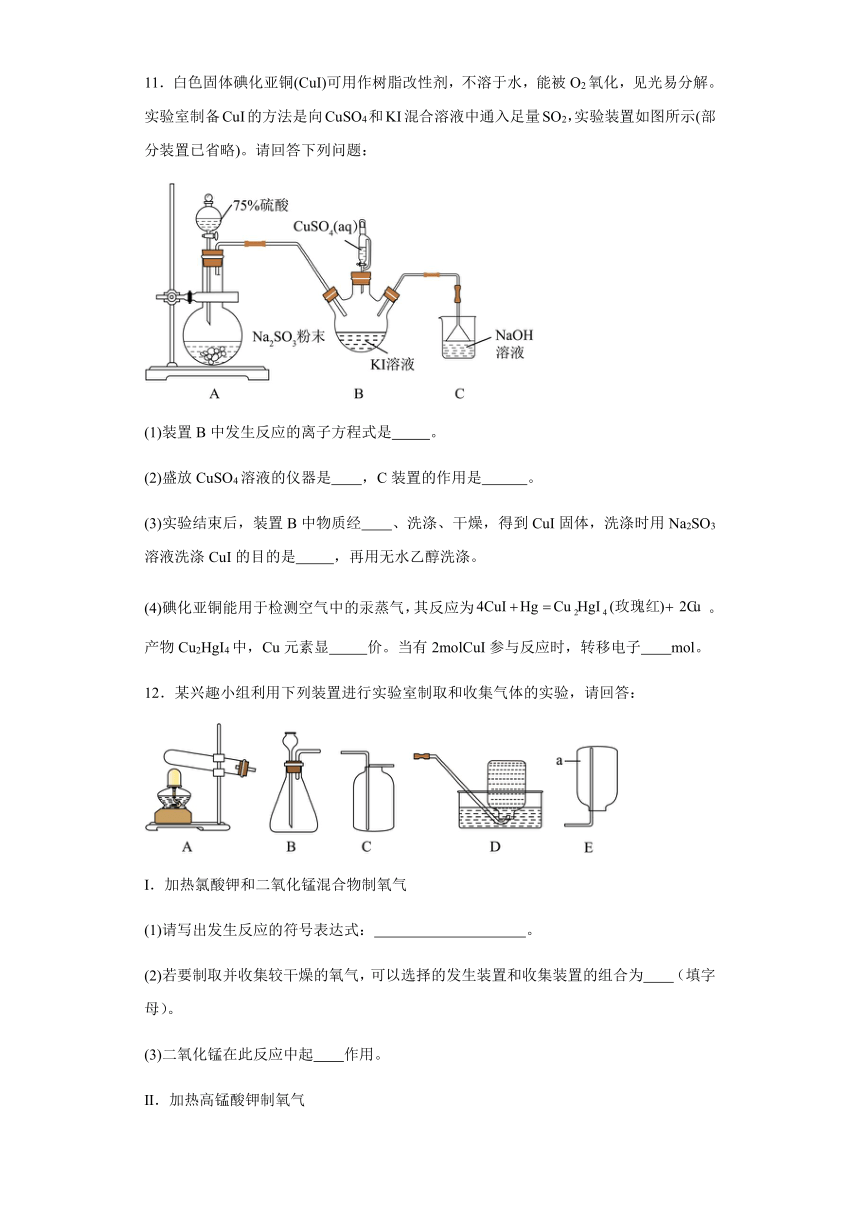
11.白色固体碘化亚铜(CuI)可用作树脂改性剂,不溶于水,能被O2氧化,见光易分解。实验室制备CuI的方法是向CuSO4和KI混合溶液中通入足量SO2,实验装置如图所示(部分装置已省略)。请回答下列问题:
(1)装置B中发生反应的离子方程式是 。
(2)盛放CuSO4溶液的仪器是 ,C装置的作用是 。
(3)实验结束后,装置B中物质经 、洗涤、干燥,得到CuI固体,洗涤时用Na2SO3溶液洗涤CuI的目的是 ,再用无水乙醇洗涤。
(4)碘化亚铜能用于检测空气中的汞蒸气,其反应为。产物Cu2HgI4中,Cu元素显 价。当有2molCuI参与反应时,转移电子 mol。
12.某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答:
Ⅰ.加热氯酸钾和二氧化锰混合物制氧气
(1)请写出发生反应的符号表达式: 。
(2)若要制取并收集较干燥的氧气,可以选择的发生装置和收集装置的组合为 (填字母)。
(3)二氧化锰在此反应中起 作用。
Ⅱ.加热高锰酸钾制氧气
(4)仪器a的名称为 。
(5)制取氧气的过程有多步操作,其中的两步操作:①将集气瓶盛满水,连同玻璃片一起倒立在盛水的水槽内;②让试管均匀受热,然后对药品所在部位加热,①在② (填“之前”或“之后”)相对合理。
(6)用仪器D收集氧气,当观察到液面下导管口有连续并比较均匀的气泡冒出时,发生装置中试管内固体物质的成分是 (填化学式)。
(7)已知,空气的平均相对分子质量为29,如果某气体的相对分子质量大于29,则这种气体的密度比空气的大;如果小于29,则密度比空气的小,所以二氧化碳的密度比空气的密度 (填“大”或“小”)。
三、计算题
13.合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳酸氢钾,反应的化学方程式为:K2CO3+CO2+H2O=2KHCO3。现向碳酸钾溶液中通入二氧化碳,恰好完全反应,得到溶质质量分数为10%的溶液100g。试计算:
(1)K2CO3中碳元素、氧元素的质量比为 ;
(2)原碳酸钾溶液的溶质质量分数(计算结果精确到0.1%);
(3)若需把上述100g质量分数为10%的碳酸氢钾溶液,稀释为溶质质量分数为4%的溶液,需要加入水的质量。
四、填空与简答
14.请用化学用语回答:
(1)保持氮气化学性质的最小粒子 。
(2)改良酸性土壤的碱 。
(3)硝酸银溶液中的金属阳离子 。
(4)3P2O5 。
(5)由60个碳原子构成的单质分子 。
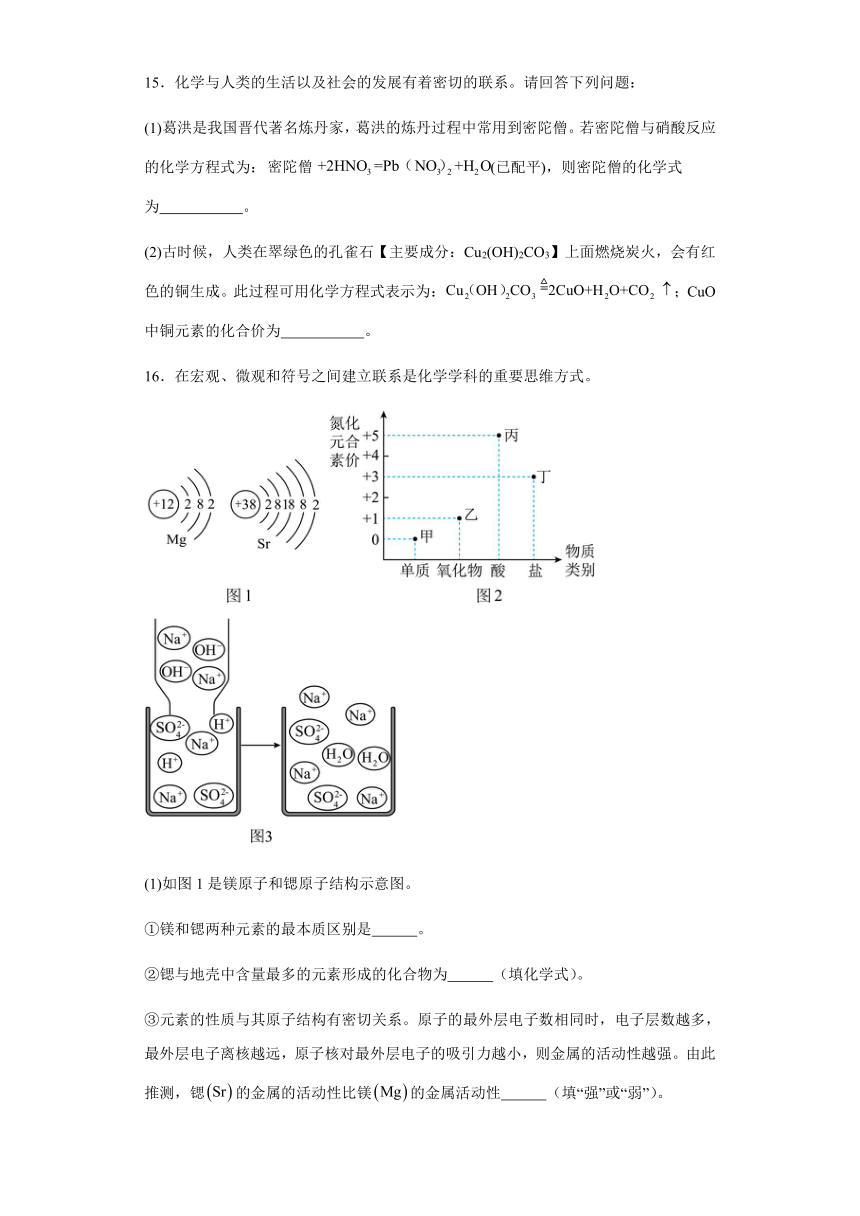
15.化学与人类的生活以及社会的发展有着密切的联系。请回答下列问题:
(1)葛洪是我国晋代著名炼丹家,葛洪的炼丹过程中常用到密陀僧。若密陀僧与硝酸反应的化学方程式为:(已配平),则密陀僧的化学式为 。
(2)古时候,人类在翠绿色的孔雀石【主要成分:Cu2(OH)2CO3】上面燃烧炭火,会有红色的铜生成。此过程可用化学方程式表示为:;CuO中铜元素的化合价为 。
16.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)如图1是镁原子和锶原子结构示意图。
①镁和锶两种元素的最本质区别是 。
②锶与地壳中含量最多的元素形成的化合物为 (填化学式)。
③元素的性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小,则金属的活动性越强。由此推测,锶的金属的活动性比镁的金属活动性 (填“强”或“弱”)。
(2)氮及其化合物的“化合价一物质类别”关系图如图2。
①甲在空气中的体积分数约为 ;丙的化学式为,该物质的名称是 。
②若丁是工业用盐,能区别溶液与食盐溶液的一种试剂是 。(友情提示:有毒,有咸味,外形与食盐相似,其水溶液呈碱性,微溶于水。)
(3)图3描述了与两溶液反应的微观示意图。
①物质类别属于 (填“酸”、“碱”或“盐”)。
②写出与该反应微观本质相同的另一化学方程式 。
试卷第1页,共3页
参考答案:
1.B
【详解】A、苯甲醇是由碳、氢、氧三种元素组成的物质,故选项说法正确;
B、苯甲醇中碳、氢、氧元素的质量比为(12×7):(1×8):(16×1)=21:2:4,则苯甲醇中氢元素的质量分数为最低,故选项说法错误;
C、苯甲醇是由苯甲醇分子构成的,1个苯甲醇分子是由7个碳原子、8个氢原子和1个氧原子共16个原子构成的,故选项说法正确;
D、苯甲醇(化学式C7H8O) 含有碳、氢元素,完全燃烧会生成CO2和H2O,故选项说法正确;
故选:B。
2.D
【详解】A、高锰酸钾由K、Mn、O三种元素组成,故错误;
B、铜与空气中的氧气在灼烧的条件下反应生成氧化铜,生成氧化铜的质量等于参加反应的氧气的质量与参加反应的铜的质量之和,故铜在空气中灼烧前后固体的质量增加,故错误;
C、二氧化碳是由二氧化碳分子构成的,故错误;
D、氢氧化钙和二氧化碳反应生成碳酸钙和水,碳酸钙能与稀盐酸反应生成氯化钙和水和二氧化碳,故正确。
故选D。
3.D
【详解】A、蜡烛燃烧后质量减少,是因为生成的二氧化碳和水逸散到空气中,符合质量守恒定律,说法错误,不符合题意;
B、在H2O中,氧元素的化合价为-2价,说法错误,不符合题意;
C、一种元素在一种化合物中不一定只表现一种化合价,如中氮元素表现出-3价、+5价两种化合价,说法错误,不符合题意;
D、在化合物中,正、负化合价的代数和为零,说法正确,符合题意。
故选:D。
4.C
【详解】A、O4是由氧元素组成的纯净物,属于单质,故A说法错误;
B、O4是由一种物质组成的,属于纯净物,故B说法错误;
C、单质是由一种元素组成的纯净物,O3、O4都是由氧元素组成的不同单质,故C说法正确;
D、分子是由原子构成的,一个O4分子中含有4个氧原子,不含有氧分子.故D说法错误;
故选C。
5.C
【详解】A、根据没食子酸化学式(C7H6O5)可知, 没食子酸由不同种元素组成的纯净物,属于化合物,说法正确;
B、根据没食子酸化学式(C7H6O5)可知,没食子酸由碳、氢、氧三种元素组成,说法正确;
C、没食子酸中碳、氧元素的质量比为:(12×7):(16×5)=21:20,说法错误;
D、 根据没食子酸中碳、氢、氧元素的质量比=(12×7):(1×6):(16×5)=42:3:40可知,氢元素的质量分数最小,说法正确。
故选C。
6.D
【详解】A、离子符号右上角的数字表示离子所带的电荷数,镁离子带两个单位的正电荷,根据离子符号的书写,将数字和正负号标在元素符号的右上角,先写数字,后标正负号,数值为1,省略不写,镁离子表示为:,符号书写错误,选项错误;
B、化学式中的角数表示分子中原子的个数,O2中的2表示一个氧分子中含有2个氧原子,选项错误;
C、标在元素符号前面的数字表示原子的个数,2N中的“2”表示2个氮原子,选项错误;
D、标在元素符号正上方的正负号和数字的组合表示该元素化合价,中的-2表示硫元素的化合价,选项正确;
故选D。
7.C
【详解】在化合物中,各元素化合价的代数和为零,NaNO2中钠元素化合价为+1价,氧元素化合价为-2价,设氮元素的化合价为x,则,解得,故NaNO2中氮元素的化合价为+3价,故选:C。
8.B
【详解】A、绿原酸是由碳、氢、氧三种元素组成,故A说法正确;
B、绿原酸是由绿原酸分子构成的,一个绿原酸分子是由16+18+9=43个原子构成,故B说法错误;
C、绿原酸的相对分子质量为16×12+1×18+16×9=354,故C说法正确;
D、绿原酸中碳、氢、氧三种元素的质量比为:(12×16):(1×18):(16×9)=32:3:24,其中氢元素的质量分数最小,故D说法正确;
故选:B。
9.A
【详解】A、萘胺(C10H9N)是含碳的化合物,属于有机物,故A正确;
B、萘胺的相对分子质量为143,且单位不是“g”而是“1”,通常省略不写,故B错误;
C、萘胺中碳、氢、氮三种元素的质量比=,可见其中氢元素的质量分数最小,故C错误;
D、由化学反应前后元素种类不变可知,萘胺由碳、氢、氮三种元素组成,在氧气中燃烧产物有CO2和H2O及氮的氧化物NO2,故D错误。
故选A。
10.D
【详解】A、西达本胺的化学式为,西达本胺由碳、氢、氟、氮、氧五种元素组成,错误;
B、西达本胺由西达本胺分子构成,1个西达本胺分子由22个碳原子、19个氢原子、1个氟原子、4个氮原子和2个氧原子构成,错误;
C、西达本胺中碳、氧元素的质量比为,错误;
D、根据西达本胺中碳、氢、氟、氮、氧元素的质量比为可知,西达本胺中碳元素的质量分数最大,正确。
故选D。
11.(1)
(2) 恒压滴液漏斗 吸收剩余的SO2,防止其污染空气
(3) 过滤 防止CuI被空气的氧气氧化
(4) +1 1
【详解】(1)装置B中发生的反应是SO2与CuSO4和KI混合溶液反应生成CuI,该反应的化学方程式为,则离子方程式为;
(2)盛放CuSO4溶液的仪器是恒压滴液漏斗;SO2属于空气污染物,因此C装置的作用是吸收剩余的SO2,防止污染空气;
(3)CuI不溶于水,将生成的混合物经过过滤、洗涤、干燥得到CuI固体;CuI能被O2氧化,因此洗涤时用Na2SO3溶液洗涤CuI的目的是防止CuI被空气中的氧气氧化,再用无水乙醇洗涤,减少其溶解损失,便于干燥;
(4)产物Cu2HgI4中,Hg元素显+2价,I元素显-1价,设铜元素化合价为x,根据在化合物中各元素化合价代数和为零可得,解得,故产物Cu2HgI4中,Cu元素显+1价;在化学方程式中,CuI中两个+1价铜降低为0价,Hg从0价变为+2价,因此该反应转移2个电子,故当有2molCuI参与反应时,转移电子1mol。
12.(1)KClO3KCl+O2
(2)AC
(3)催化
(4)集气瓶
(5)之前
(6)KMnO4、K2MnO4、MnO2
(7)大
【详解】(1)氯酸钾在二氧化锰的催化下受热分解生成氯化钾和氧气,反应的符号表达式为KClO3KCl+O2。
(2)加热氯酸钾和二氧化锰混合物制氧气是固体加热型反应,则发生装置选择装置A;排水法收集的气体较湿润,氧气的密度比空气略大,要收集较干燥的氧气,应选择向上排空气法,则收集装置选择装置C。
(3)该反应中,二氧化锰作催化剂,起催化作用。
(4)由图可知,仪器a为集气瓶。
(5)制取氧气的过程中,应先将集气瓶盛满水,连同玻璃片一起倒立在盛水的水槽内,再让试管均匀受热,然后对药品所在部位加热,为了便于收集气体,①在②之前较合理,否则可能会导致浪费药品或收集不到气体。
(6)排水法氧气,观察到液面下导管口有连续并比较均匀的气泡冒出时,装置内的空气被完全排出可以开始收集,反应刚开始未反应完,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,所以发生装置中试管内固体物质的成分为高锰酸钾(KMnO4)、锰酸钾(K2MnO4)和二氧化锰(MnO2)。
(7)二氧化碳的相对分子质量为12×1+16×2=44>29,比空气的密度大。
13.(1)1:4
(2)溶质的质量分数为10%的溶液100g中碳酸氢钾的质量为10%×100g=10g
设碳酸钾的质量为x,二氧化碳的质量为y,
x=6.9g
y=2.2g
原碳酸钾溶液中溶质的质量分数为×100%≈7.1%;
答:原碳酸钾溶液中溶质的质量分数约为7.1%;
(3)若把该100g10%该溶液,稀释为溶质的质量分数为4%的溶液,设加入的水的质量为z,则:
100g×10%=(100g+x)×4%
解得z=150g,
答:若把该50g该溶液,稀释为溶质的质量分数为4%的溶液,需要加入水的质量为150g。
【详解】(1)碳酸钾(K2CO3)中碳元素、氧元素的质量比12:(16×3)=1:4;
(2)见答案;
(3)见答案。
14.(1)N2
(2)Ca(OH)2
(3)Ag+
(4)3个五氧化二磷分子
(5)C60
【详解】(1)氮气是由氮分子构成的,保持氮气化学性质的最小粒子为氮分子,表示为N2;
(2)氢氧化钙属于碱,显碱性,能与酸性物质反应,可用于改良酸性土壤,氢氧化钙中钙元素显+2价,氢氧根显-1价,化学式为Ca(OH)2;
(3)硝酸银是由银离子和硝酸根离子构成的,所以硝酸银溶液中的金属阳离子是银离子,表示为Ag+;
(4)标在化学式前面的数字表示分子的个数,3P2O5表示3个五氧化二磷分子;
(5)元素符号右下角的数字表示一个分子中所含有的原子个数,则由60个碳原子构成的单质分子的符号为C60。
15.(1)PbO
(2)+2
【详解】(1)根据质量守恒定律,反应前后原子的种类和个数不变,如题所示,反应后铅原子、氮原子、氧原子、氢原子的个数分别是1、2、7、2,反应前铅原子、氮原子、氧原子、氢原子的个数分别是0、2、6、2,因此还差1个铅原子和1个氧原子,故密陀僧的化学式为PbO;
(2)CuO中氧元素显-2价,根据在化合物中各元素的正负化合价代数和为0,则铜元素的化合价为+2。
16.(1) 核电荷数/质子数 SrO 强
(2) 78% 硝酸 无色酚酞试液
(3) 盐 2NaOH+H2SO4=Na2SO4+2H2O(合理即可)
【详解】(1)①元素是具有相同的核电荷数(质子数)的一类原子的总称镁和锶两种元素的最本质区别是:质子数不同(或核电核数不同);
②锶原子最外层有2个电子,在化学反应中容易失电子,通常显+2价,地壳中含量最多元素是氧元素,通常显-2价,书写化学式时,一般正价的写在左边,负价的写在右边,根据化合物中各元素化合价代数和为零,它们形成的化合物的化学式为:SrO;
③锶与镁原子的最外层电子数相同时,但是锶电子层数多,最外层电子离核越远,原子核对最外层电子的吸引力越小。由此推测,锶的(Sr)金属的活动性比Mg的金属活动性强;
(2)①甲为单质,是氮气,氮气大约占空气体积的78%;丙的化学式为HNO3,该物质的名称是硝酸;
②若丁是工业用盐NaNO2,其水溶液呈碱性,能区别NaNO2溶液与食盐溶液的一种试剂是无色酚酞试液,能使无色变红色的是NaNO2,不变的是氯化钠;
(3)①NaHSO4是由钠离子、氢离子和硫酸根离子构成的,其类别属于盐;
②根据微观示意图可知,反应过程中氢离子和氢氧根离子被消耗,生成水分子,该反应微观本质是氢离子和氢氧根离子结合成水,中和反应的实质也是与氢离子和氢氧根离子结合成水,该反应微观本质相同的另一化学方程式可以为2NaOH+H2SO4=Na2SO4+2H2O(合理即可)
答案第1页,共2页
一、选择题
1.“遥知不是雪,为有暗香来”,梅花有香味的主要因为含有苯甲醇(化学式C7H8O)。下列有关苯甲醇的说法错误的是
A.由碳、氢、氧三种元素组成 B.其中氧元素的质量分数最小
C.一个苯甲醇分子含有16个原子 D.完全燃烧生成CO2和H2O
2.下列化学观念及描述合理的是
A.元素观:高锰酸钾是由钾元素和锰元素组成的化合物
B.守恒观:铜在空气中灼烧前后固体的质量不变
C.微粒观;二氧化碳是碳原子和氧分子构成的
D.转化观;和在一定条件下可相互转化
3.下列说法正确的是
A.蜡烛燃烧后质量减少,不符合质量守恒定律 B.在H2O中,氧元素的化合价为2价
C.一种元素在一种化合物中只能表现一种化合价 D.在化合物中,正、负化合价的代数和为零
4.意大利科学家最近合成了新型的氧分子,对其说法正确的是
A.是一种新型的化合物 B.是一种混合物
C.和都是氧元素的单质 D.一个分子含有2个分子
5.没食子酸(化学式为)是世界上最早制得的有机酸,中医常用其治疗流感。明代李梴的《医学入门》中记载了制取没食子酸的方法。下列说法错误的是
A.没食子酸属于化合物 B.没食子酸由碳、氢、氧三种元素组成
C.没食子酸中碳、氧元素的质量比为7:5 D.没食子酸中氢元素的质量分数最小
6.学生作业中出现的包含数字“2”的符号及其意义均正确的是
A.:镁离子带两个单位的正电荷 B.:两个氧原子
C.2N:两个氮分子 D.:-2价的硫元素
7.工业用盐亚硝酸钠,其化学式为NaNO2,外观与食盐相似,有咸味,但价格更低,有不法分子常在食盐中可加入NaNO2牟利。NaNO2中N的化合价为
A.0 B.+5 C.+3 D.-2
8.《木草纲目》中记载的金银花具有清热解毒、疏散风热的功效,其有效成分之一是绿原酸(化学式为C16H18O9)。下列有关绿原酸的说法错误的是
A.由碳、氢、氧元素组成 B.由43个原子构成
C.相对分子质量为354 D.其中氢元素的质量分数最小
9.在纳米纸上“铺”一层“萘胺”(C10H9N)制作而成的试纸,可用于检测食品中亚硝酸盐的含量,保证食品安全。下列有关萘胺的说法正确的是
A.萘胺属于有机物
B.一个萘胺分子的质量为143g
C.萘胺中氮元素的质量分数最小
D.萘胺在氧气中燃烧产物只有CO2
10.我国自主知识产权的抗癌新药“西达本胺”已全球上市。西达本胺的化学式为,下列有关西达本胺的说法正确的是
A.西达本胺由碳、氢、氟、氮、氧五个元素组成
B.西达本胺是由22个碳原子、19个氢原子、1个氟原子、4个氮原子和2个氧原子构成
C.西达本胺中碳、氧元素的质量比为11:1
D.西达本胺中碳元素的质量分数最大
二、实验题
11.白色固体碘化亚铜(CuI)可用作树脂改性剂,不溶于水,能被O2氧化,见光易分解。实验室制备CuI的方法是向CuSO4和KI混合溶液中通入足量SO2,实验装置如图所示(部分装置已省略)。请回答下列问题:
(1)装置B中发生反应的离子方程式是 。
(2)盛放CuSO4溶液的仪器是 ,C装置的作用是 。
(3)实验结束后,装置B中物质经 、洗涤、干燥,得到CuI固体,洗涤时用Na2SO3溶液洗涤CuI的目的是 ,再用无水乙醇洗涤。
(4)碘化亚铜能用于检测空气中的汞蒸气,其反应为。产物Cu2HgI4中,Cu元素显 价。当有2molCuI参与反应时,转移电子 mol。
12.某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答:
Ⅰ.加热氯酸钾和二氧化锰混合物制氧气
(1)请写出发生反应的符号表达式: 。
(2)若要制取并收集较干燥的氧气,可以选择的发生装置和收集装置的组合为 (填字母)。
(3)二氧化锰在此反应中起 作用。
Ⅱ.加热高锰酸钾制氧气
(4)仪器a的名称为 。
(5)制取氧气的过程有多步操作,其中的两步操作:①将集气瓶盛满水,连同玻璃片一起倒立在盛水的水槽内;②让试管均匀受热,然后对药品所在部位加热,①在② (填“之前”或“之后”)相对合理。
(6)用仪器D收集氧气,当观察到液面下导管口有连续并比较均匀的气泡冒出时,发生装置中试管内固体物质的成分是 (填化学式)。
(7)已知,空气的平均相对分子质量为29,如果某气体的相对分子质量大于29,则这种气体的密度比空气的大;如果小于29,则密度比空气的小,所以二氧化碳的密度比空气的密度 (填“大”或“小”)。
三、计算题
13.合成氨工业中,常用碳酸钾溶液吸收产生的二氧化碳得到碳酸氢钾,反应的化学方程式为:K2CO3+CO2+H2O=2KHCO3。现向碳酸钾溶液中通入二氧化碳,恰好完全反应,得到溶质质量分数为10%的溶液100g。试计算:
(1)K2CO3中碳元素、氧元素的质量比为 ;
(2)原碳酸钾溶液的溶质质量分数(计算结果精确到0.1%);
(3)若需把上述100g质量分数为10%的碳酸氢钾溶液,稀释为溶质质量分数为4%的溶液,需要加入水的质量。
四、填空与简答
14.请用化学用语回答:
(1)保持氮气化学性质的最小粒子 。
(2)改良酸性土壤的碱 。
(3)硝酸银溶液中的金属阳离子 。
(4)3P2O5 。
(5)由60个碳原子构成的单质分子 。
15.化学与人类的生活以及社会的发展有着密切的联系。请回答下列问题:
(1)葛洪是我国晋代著名炼丹家,葛洪的炼丹过程中常用到密陀僧。若密陀僧与硝酸反应的化学方程式为:(已配平),则密陀僧的化学式为 。
(2)古时候,人类在翠绿色的孔雀石【主要成分:Cu2(OH)2CO3】上面燃烧炭火,会有红色的铜生成。此过程可用化学方程式表示为:;CuO中铜元素的化合价为 。
16.在宏观、微观和符号之间建立联系是化学学科的重要思维方式。
(1)如图1是镁原子和锶原子结构示意图。
①镁和锶两种元素的最本质区别是 。
②锶与地壳中含量最多的元素形成的化合物为 (填化学式)。
③元素的性质与其原子结构有密切关系。原子的最外层电子数相同时,电子层数越多,最外层电子离核越远,原子核对最外层电子的吸引力越小,则金属的活动性越强。由此推测,锶的金属的活动性比镁的金属活动性 (填“强”或“弱”)。
(2)氮及其化合物的“化合价一物质类别”关系图如图2。
①甲在空气中的体积分数约为 ;丙的化学式为,该物质的名称是 。
②若丁是工业用盐,能区别溶液与食盐溶液的一种试剂是 。(友情提示:有毒,有咸味,外形与食盐相似,其水溶液呈碱性,微溶于水。)
(3)图3描述了与两溶液反应的微观示意图。
①物质类别属于 (填“酸”、“碱”或“盐”)。
②写出与该反应微观本质相同的另一化学方程式 。
试卷第1页,共3页
参考答案:
1.B
【详解】A、苯甲醇是由碳、氢、氧三种元素组成的物质,故选项说法正确;
B、苯甲醇中碳、氢、氧元素的质量比为(12×7):(1×8):(16×1)=21:2:4,则苯甲醇中氢元素的质量分数为最低,故选项说法错误;
C、苯甲醇是由苯甲醇分子构成的,1个苯甲醇分子是由7个碳原子、8个氢原子和1个氧原子共16个原子构成的,故选项说法正确;
D、苯甲醇(化学式C7H8O) 含有碳、氢元素,完全燃烧会生成CO2和H2O,故选项说法正确;
故选:B。
2.D
【详解】A、高锰酸钾由K、Mn、O三种元素组成,故错误;
B、铜与空气中的氧气在灼烧的条件下反应生成氧化铜,生成氧化铜的质量等于参加反应的氧气的质量与参加反应的铜的质量之和,故铜在空气中灼烧前后固体的质量增加,故错误;
C、二氧化碳是由二氧化碳分子构成的,故错误;
D、氢氧化钙和二氧化碳反应生成碳酸钙和水,碳酸钙能与稀盐酸反应生成氯化钙和水和二氧化碳,故正确。
故选D。
3.D
【详解】A、蜡烛燃烧后质量减少,是因为生成的二氧化碳和水逸散到空气中,符合质量守恒定律,说法错误,不符合题意;
B、在H2O中,氧元素的化合价为-2价,说法错误,不符合题意;
C、一种元素在一种化合物中不一定只表现一种化合价,如中氮元素表现出-3价、+5价两种化合价,说法错误,不符合题意;
D、在化合物中,正、负化合价的代数和为零,说法正确,符合题意。
故选:D。
4.C
【详解】A、O4是由氧元素组成的纯净物,属于单质,故A说法错误;
B、O4是由一种物质组成的,属于纯净物,故B说法错误;
C、单质是由一种元素组成的纯净物,O3、O4都是由氧元素组成的不同单质,故C说法正确;
D、分子是由原子构成的,一个O4分子中含有4个氧原子,不含有氧分子.故D说法错误;
故选C。
5.C
【详解】A、根据没食子酸化学式(C7H6O5)可知, 没食子酸由不同种元素组成的纯净物,属于化合物,说法正确;
B、根据没食子酸化学式(C7H6O5)可知,没食子酸由碳、氢、氧三种元素组成,说法正确;
C、没食子酸中碳、氧元素的质量比为:(12×7):(16×5)=21:20,说法错误;
D、 根据没食子酸中碳、氢、氧元素的质量比=(12×7):(1×6):(16×5)=42:3:40可知,氢元素的质量分数最小,说法正确。
故选C。
6.D
【详解】A、离子符号右上角的数字表示离子所带的电荷数,镁离子带两个单位的正电荷,根据离子符号的书写,将数字和正负号标在元素符号的右上角,先写数字,后标正负号,数值为1,省略不写,镁离子表示为:,符号书写错误,选项错误;
B、化学式中的角数表示分子中原子的个数,O2中的2表示一个氧分子中含有2个氧原子,选项错误;
C、标在元素符号前面的数字表示原子的个数,2N中的“2”表示2个氮原子,选项错误;
D、标在元素符号正上方的正负号和数字的组合表示该元素化合价,中的-2表示硫元素的化合价,选项正确;
故选D。
7.C
【详解】在化合物中,各元素化合价的代数和为零,NaNO2中钠元素化合价为+1价,氧元素化合价为-2价,设氮元素的化合价为x,则,解得,故NaNO2中氮元素的化合价为+3价,故选:C。
8.B
【详解】A、绿原酸是由碳、氢、氧三种元素组成,故A说法正确;
B、绿原酸是由绿原酸分子构成的,一个绿原酸分子是由16+18+9=43个原子构成,故B说法错误;
C、绿原酸的相对分子质量为16×12+1×18+16×9=354,故C说法正确;
D、绿原酸中碳、氢、氧三种元素的质量比为:(12×16):(1×18):(16×9)=32:3:24,其中氢元素的质量分数最小,故D说法正确;
故选:B。
9.A
【详解】A、萘胺(C10H9N)是含碳的化合物,属于有机物,故A正确;
B、萘胺的相对分子质量为143,且单位不是“g”而是“1”,通常省略不写,故B错误;
C、萘胺中碳、氢、氮三种元素的质量比=,可见其中氢元素的质量分数最小,故C错误;
D、由化学反应前后元素种类不变可知,萘胺由碳、氢、氮三种元素组成,在氧气中燃烧产物有CO2和H2O及氮的氧化物NO2,故D错误。
故选A。
10.D
【详解】A、西达本胺的化学式为,西达本胺由碳、氢、氟、氮、氧五种元素组成,错误;
B、西达本胺由西达本胺分子构成,1个西达本胺分子由22个碳原子、19个氢原子、1个氟原子、4个氮原子和2个氧原子构成,错误;
C、西达本胺中碳、氧元素的质量比为,错误;
D、根据西达本胺中碳、氢、氟、氮、氧元素的质量比为可知,西达本胺中碳元素的质量分数最大,正确。
故选D。
11.(1)
(2) 恒压滴液漏斗 吸收剩余的SO2,防止其污染空气
(3) 过滤 防止CuI被空气的氧气氧化
(4) +1 1
【详解】(1)装置B中发生的反应是SO2与CuSO4和KI混合溶液反应生成CuI,该反应的化学方程式为,则离子方程式为;
(2)盛放CuSO4溶液的仪器是恒压滴液漏斗;SO2属于空气污染物,因此C装置的作用是吸收剩余的SO2,防止污染空气;
(3)CuI不溶于水,将生成的混合物经过过滤、洗涤、干燥得到CuI固体;CuI能被O2氧化,因此洗涤时用Na2SO3溶液洗涤CuI的目的是防止CuI被空气中的氧气氧化,再用无水乙醇洗涤,减少其溶解损失,便于干燥;
(4)产物Cu2HgI4中,Hg元素显+2价,I元素显-1价,设铜元素化合价为x,根据在化合物中各元素化合价代数和为零可得,解得,故产物Cu2HgI4中,Cu元素显+1价;在化学方程式中,CuI中两个+1价铜降低为0价,Hg从0价变为+2价,因此该反应转移2个电子,故当有2molCuI参与反应时,转移电子1mol。
12.(1)KClO3KCl+O2
(2)AC
(3)催化
(4)集气瓶
(5)之前
(6)KMnO4、K2MnO4、MnO2
(7)大
【详解】(1)氯酸钾在二氧化锰的催化下受热分解生成氯化钾和氧气,反应的符号表达式为KClO3KCl+O2。
(2)加热氯酸钾和二氧化锰混合物制氧气是固体加热型反应,则发生装置选择装置A;排水法收集的气体较湿润,氧气的密度比空气略大,要收集较干燥的氧气,应选择向上排空气法,则收集装置选择装置C。
(3)该反应中,二氧化锰作催化剂,起催化作用。
(4)由图可知,仪器a为集气瓶。
(5)制取氧气的过程中,应先将集气瓶盛满水,连同玻璃片一起倒立在盛水的水槽内,再让试管均匀受热,然后对药品所在部位加热,为了便于收集气体,①在②之前较合理,否则可能会导致浪费药品或收集不到气体。
(6)排水法氧气,观察到液面下导管口有连续并比较均匀的气泡冒出时,装置内的空气被完全排出可以开始收集,反应刚开始未反应完,高锰酸钾受热分解为锰酸钾、二氧化锰和氧气,所以发生装置中试管内固体物质的成分为高锰酸钾(KMnO4)、锰酸钾(K2MnO4)和二氧化锰(MnO2)。
(7)二氧化碳的相对分子质量为12×1+16×2=44>29,比空气的密度大。
13.(1)1:4
(2)溶质的质量分数为10%的溶液100g中碳酸氢钾的质量为10%×100g=10g
设碳酸钾的质量为x,二氧化碳的质量为y,
x=6.9g
y=2.2g
原碳酸钾溶液中溶质的质量分数为×100%≈7.1%;
答:原碳酸钾溶液中溶质的质量分数约为7.1%;
(3)若把该100g10%该溶液,稀释为溶质的质量分数为4%的溶液,设加入的水的质量为z,则:
100g×10%=(100g+x)×4%
解得z=150g,
答:若把该50g该溶液,稀释为溶质的质量分数为4%的溶液,需要加入水的质量为150g。
【详解】(1)碳酸钾(K2CO3)中碳元素、氧元素的质量比12:(16×3)=1:4;
(2)见答案;
(3)见答案。
14.(1)N2
(2)Ca(OH)2
(3)Ag+
(4)3个五氧化二磷分子
(5)C60
【详解】(1)氮气是由氮分子构成的,保持氮气化学性质的最小粒子为氮分子,表示为N2;
(2)氢氧化钙属于碱,显碱性,能与酸性物质反应,可用于改良酸性土壤,氢氧化钙中钙元素显+2价,氢氧根显-1价,化学式为Ca(OH)2;
(3)硝酸银是由银离子和硝酸根离子构成的,所以硝酸银溶液中的金属阳离子是银离子,表示为Ag+;
(4)标在化学式前面的数字表示分子的个数,3P2O5表示3个五氧化二磷分子;
(5)元素符号右下角的数字表示一个分子中所含有的原子个数,则由60个碳原子构成的单质分子的符号为C60。
15.(1)PbO
(2)+2
【详解】(1)根据质量守恒定律,反应前后原子的种类和个数不变,如题所示,反应后铅原子、氮原子、氧原子、氢原子的个数分别是1、2、7、2,反应前铅原子、氮原子、氧原子、氢原子的个数分别是0、2、6、2,因此还差1个铅原子和1个氧原子,故密陀僧的化学式为PbO;
(2)CuO中氧元素显-2价,根据在化合物中各元素的正负化合价代数和为0,则铜元素的化合价为+2。
16.(1) 核电荷数/质子数 SrO 强
(2) 78% 硝酸 无色酚酞试液
(3) 盐 2NaOH+H2SO4=Na2SO4+2H2O(合理即可)
【详解】(1)①元素是具有相同的核电荷数(质子数)的一类原子的总称镁和锶两种元素的最本质区别是:质子数不同(或核电核数不同);
②锶原子最外层有2个电子,在化学反应中容易失电子,通常显+2价,地壳中含量最多元素是氧元素,通常显-2价,书写化学式时,一般正价的写在左边,负价的写在右边,根据化合物中各元素化合价代数和为零,它们形成的化合物的化学式为:SrO;
③锶与镁原子的最外层电子数相同时,但是锶电子层数多,最外层电子离核越远,原子核对最外层电子的吸引力越小。由此推测,锶的(Sr)金属的活动性比Mg的金属活动性强;
(2)①甲为单质,是氮气,氮气大约占空气体积的78%;丙的化学式为HNO3,该物质的名称是硝酸;
②若丁是工业用盐NaNO2,其水溶液呈碱性,能区别NaNO2溶液与食盐溶液的一种试剂是无色酚酞试液,能使无色变红色的是NaNO2,不变的是氯化钠;
(3)①NaHSO4是由钠离子、氢离子和硫酸根离子构成的,其类别属于盐;
②根据微观示意图可知,反应过程中氢离子和氢氧根离子被消耗,生成水分子,该反应微观本质是氢离子和氢氧根离子结合成水,中和反应的实质也是与氢离子和氢氧根离子结合成水,该反应微观本质相同的另一化学方程式可以为2NaOH+H2SO4=Na2SO4+2H2O(合理即可)
答案第1页,共2页
同课章节目录
