【全国版】2024年九年级中考化学模拟预测试题一
文档属性
| 名称 | 【全国版】2024年九年级中考化学模拟预测试题一 |

|
|
| 格式 | docx | ||
| 文件大小 | 610.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-14 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2024年九年级中考化学模拟预测试题一
说 明: 1. 全卷满分 70分,考试时间 50分钟。
2. 本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共四个大题,17个小题。
可能用到的相对原子质量: H-1 C-12 O-16 Na-23 Mg-24 S-32 Fe-56 Cu-64 Zn-65 Ba-137
第Ⅰ卷 选择题(共30分)
一、选择题(本题共 10个小题,每小题只有一个选项符合题意,每小题 3分,共 30分)
1.“女儿节”是广元的地方性传统节日,源于民间“正月二十三、妇女游河湾”的传统习俗。下列活动中一定涉及化学变化的是 ( )
A.彩船巡游 B.燃放礼花弹
C.穿汉服、抛绣球 D.观剑门关、翠云廊
2.化学与人们的生产、生活密切相关。下列有关做法不恰当的是 ( )
A.用新型可降解塑料制作农用塑料薄膜
B.霉变食物煮熟后可以食用
C.铁制品表面刷漆或涂油防止锈蚀
D.为节约石油资源,可在汽油中加入适量乙醇作为汽车燃料
3.物质的性质决定其用途。下列物质的性质与用途关系对应正确的是 ( )
A.氧气能支持燃烧——可作燃料
B.活性炭具有吸附性——可用于降低水的硬度
C.金刚石的硬度大——可作装饰品
D.一氧化碳具有还原性——可用于冶炼金属
4.下列实验操作、实验现象和实验结论的对应关系不正确的是 ( )
选项 实验操作 实验现象 实验结论
A 在蜡烛的火焰上方罩一内壁蘸有澄清石灰水的烧杯 澄清石灰水变浑浊 蜡烛中含有碳元素
B 取少量嘉陵江的水于烧杯中,加入一定量肥皂水,搅拌 出现大量的浮渣 该水的硬度大
C 将氢气通入装有氧化铜的试管中,加热 试管内黑色固体变成红色 该反应有 H O生成
D 将盛有燃着硫的燃烧匙伸入充满氧气的集气瓶中 有刺激性气味的气体生成 硫能与氧气发生反应
5.某化学反应的微观示意图如图所示,下列说法正确的是 ( )
A.该反应中原子和分子的种类都发生改变
B.参加反应的两种分子的个数比为 3:2
C.符合该微观示意图的化学方程式可以为
D.该反应中元素的化合价均不变
6.除去下列物质中混有的杂质,所用试剂或操作方法正确的是 ( )
选项 物质(括号内为杂质) 所用试剂或操作方法
A KCl溶液(FeCl ) 向溶液中加入适量的氢氧化钾溶液,充分反应后过滤
B NaCl(NaNO ) 加水溶解后降温结晶
C O (CH ) 点燃
D CaCO (CaO) 加入足量的稀盐酸,充分反应后过滤、洗涤、干燥
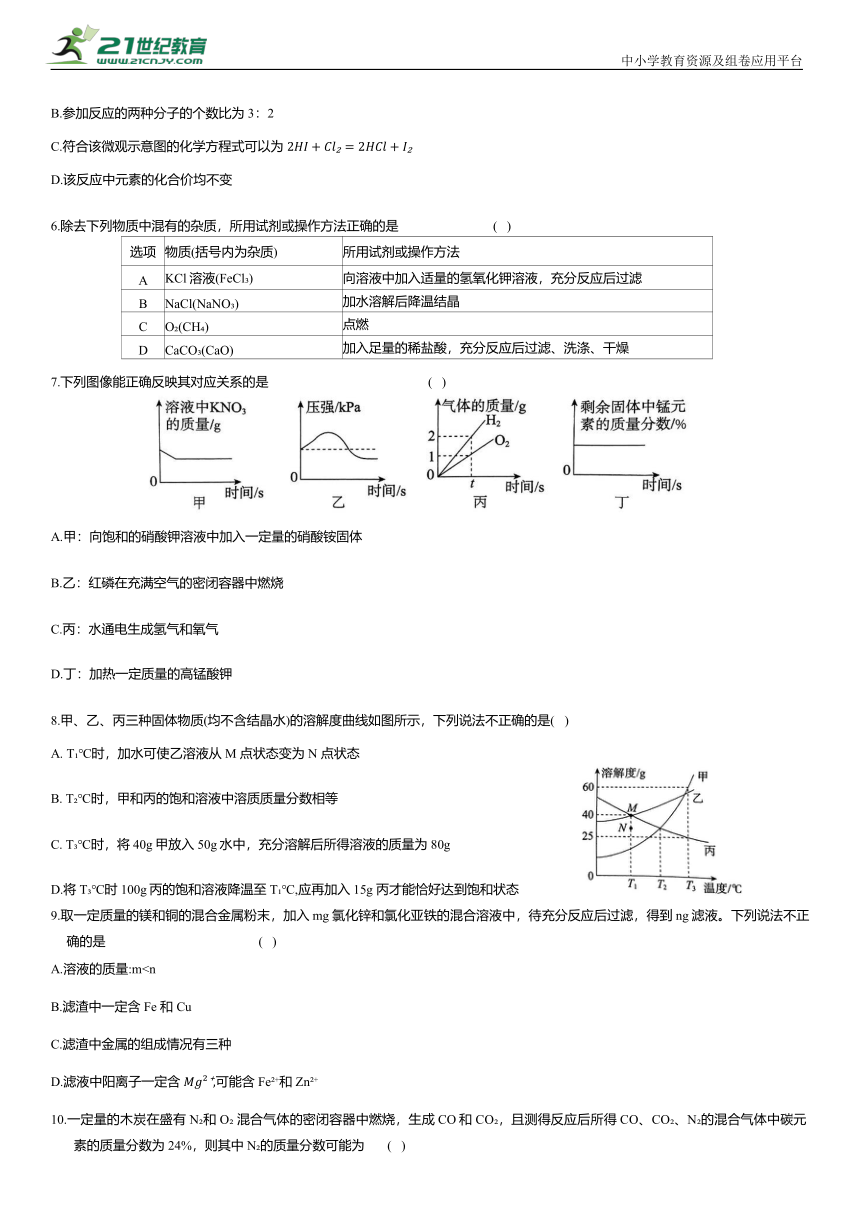
7.下列图像能正确反映其对应关系的是 ( )
A.甲:向饱和的硝酸钾溶液中加入一定量的硝酸铵固体
B.乙:红磷在充满空气的密闭容器中燃烧
C.丙:水通电生成氢气和氧气
D.丁:加热一定质量的高锰酸钾
8.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法不正确的是( )
A. T ℃时,加水可使乙溶液从 M 点状态变为 N 点状态
B. T ℃时,甲和丙的饱和溶液中溶质质量分数相等
C. T ℃时,将40g甲放入50g水中,充分溶解后所得溶液的质量为 80g
D.将 T ℃时100g丙的饱和溶液降温至 T ℃,应再加入15g 丙才能恰好达到饱和状态
9.取一定质量的镁和铜的混合金属粉末,加入mg氯化锌和氯化亚铁的混合溶液中,待充分反应后过滤,得到ng滤液。下列说法不正确的是 ( )
A.溶液的质量:mB.滤渣中一定含 Fe 和 Cu
C.滤渣中金属的组成情况有三种
D.滤液中阳离子一定含 可能含 Fe 和Zn
10.一定量的木炭在盛有 N 和 O 混合气体的密闭容器中燃烧,生成CO和 CO ,且测得反应后所得CO、CO 、N 的混合气体中碳元素的质量分数为24%,则其中 N 的质量分数可能为 ( )
A.12% B.30% C.44% D.60%
第Ⅱ卷 非选择题(共 40 分)
二、填空题(本题共4个小题,每空1分,共20分)
11.(5分)化学用语是学习和研究化学的重要工具。请用化学用语填空:
(1)氩气: 。
(2)4个铵根离子: 。
(3)2个乙醇分子: 。
(4)标出 Na SiO 中硅元素的化合价: 。
(5)写出小苏打治疗胃酸过多的化学方程式: 。
12.(6分)人类的发展离不开化学,化学在农业生产和科技发展中发挥着重要的作用。请根据所学化学知识回答下列问题:
(1)2023 年 9月,广元昭化举办了以“庆丰收·促和美”为主题的丰收节活动。
①辛弃疾的《西江月·夜行黄沙道中》写到“稻花香里说丰年,听取蛙声一片”,诗中描写“稻花香”的情景,请从微观角度解释: 。
②农作物的生长需要 N、P、K等营养元素,下列化肥中属于复合肥的是 (填字母)。
A.磷矿粉 B.尿素 C.硝酸钾
③农作物一般适宜在 pH=7或接近7的土壤中生长。近年来由于空气污染形成酸雨,导致土壤酸性增强,不利于农作物生长,于是人们常将适量的 加入土壤中,以中和其酸性。
(2)广元昭化王家贡米是依托搭乘火箭飞船遨游太空的“太空种子”而孕育的。
①火箭外壳的主要材料为铝合金,下列属于铝合金性质的是 (填字母)。
A.硬度大 B.密度大 C.抗腐蚀
②火箭整流罩的端头帽是由玻璃钢纤维材料制成的,玻璃钢属于 材料。
③发射火箭时常用肼和四氧化二氮作为推进剂,其反应的化学方程式为: 3R+4H O,,则 R 的化学式为 。
13.(5分)中国科学院院士张青莲教授为相对原子质量的测定作出了卓越贡献。他主持测定了铟、铱、锑、销、铈、铒、锗、锌、镝几种元素相对原子质量的新值,被国际原子量委员会采用为国际新标准。铟元素在元素周期表中显示的信息及其原子结构示意图如下。请回答下列问题:
(1)铟的相对原子质量为 ,铟元素位于元素周期表中第 周期。
(2)在化学反应中铟原子易失去电子,形成的离子为 (填符号),在1~18号元素中,与铟元素化学性质相似的金属元素是 (填名称)。
(3)在医学上,常用铟的不同化合物来对人体的各个器官进行扫描。在加热条件下,铟能与氯气发生化合反应,其生成物的化学式为 。
14.(4分)A~L是初中化学常见的物质,它们之间的转化关系如下图所示(图中每个反应都是一步实现,其中“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系,反应条件和部分物质已略去)。其中 A 是碳酸氢铵,D、G组成元素相同,H 为黑色固体,J 俗称纯碱,K 是常见的酸,L是蓝色沉淀。请回答下列问题:
(1)写出 H 的化学式: 。
(2)写出D的一种用途: 。
(3)反应①~⑥中复分解反应有 个。
(4)写出反应②的化学方程式: 。
三、实验探究题(本题共 2个小题,每空1分,共 14分)
15.(6分)下图是实验室制取气体的常用装置,请回答下列问题:
(1)写出仪器①的名称: 。
(2)实验室制取CO 的化学方程式为 ,从控制反应的发生和停止角度考虑,其发生装置最好选择 (填字母)。若选用装置G除去 CO 中混有的水蒸气,则装置G中应装入的试剂是 ,气体应从 (填“a”或“b”)端导管通入。
(3)实验室常用铜和稀硝酸反应制取一氧化氮气体,一氧化氮是一种无色无味的有毒气体,难溶于水;在常温下一氧化氮能与氧气反应生成红棕色的气体二氧化氮。若实验室要收集一瓶一氧化氮气体,收集装置应选择 (填字母)。
16.(8分)实验室有一瓶已过保质期的淡黄色固体药品,标签上的药品名称是过氧化钠( 某化学兴趣小组同学想知道这瓶固体究竟含有哪些成分,他们在化学老师的指导下进行了如下实验探究。
【查阅资料】i.过氧化钠是一种淡黄色的固体。
.在常温下过氧化钠能与 CO 和 H O 反应,其反应原理是
【猜想与假设】(1)该小组同学一致认为该固体药品中一定含 Na O ,理由是 。
(2)提出猜想:一、全部是 Na O ;
二、只含有 Na O 和 Na CO ;
三、只含有 Na O 和 NaOH;
四、你的猜想是含有 。
【设计实验】实验一:取2.0g 固体样品于试管中,加入适量的水,完全反应后(无固体剩余),测得收集到的气体的质量为0.16g,由此推出猜想 错误。
实验二:向实验一反应后的溶液中加入过量的) 溶液,有白色沉淀生成,由此推知固体样品中含有 ,其反应的化学方程式为 ,因此猜想 错误。
实验三:将实验二中生成的白色沉淀过滤、洗涤、干燥后,称得其质量为1.97 g。
【得出结论】通过上述实验操作得出结论,猜想 正确。
【拓展延伸】过氧化钠常用在潜艇中制造氧气,其主要优点是 (答出一条即可)。
四、计算题(本题1个小题,共6分)
17.向5.8g某生铁(只含铁和碳)样品中,逐滴加入溶质质量分数为9.8%的稀硫酸,待刚好不再产生气泡时停止滴入,反应过程中加入稀硫酸的质量与生成气体的质量关系如图所示。请计算(结果保留到小数点后一位):
(1)m的值为 。
(2)生铁样品中碳元素的质量分数为 。
(3)反应后所得溶液中溶质的质量分数(写出计算过程)。
一、选择题(每小题3分,共 30分)
1. B 2. B 3. D 4. C 5. C 6. A 7. B 8. D 9. A10. B
二、填空题(每空1分,共 20分)
11.(1) Ar (2)4NH (3)2C H OH(或2C H O)
12.(1)①分子在不断地运动 ②C
③熟石灰[或消石灰、Ca(OH) 、氢氧化钙]
(2)①AC ②复合 ③N
13.(1)114.8 五 (2)In 铝 (3)InCl
14.(1)CuO
(2)用于灭火(或制碳酸饮料、作气体肥料等,合理即可)
三、实验探究题(每空 1分,共 14分)
15.(1)铁架台
C 浓硫酸 b (3)D
16.【猜想与假设】(1)Na O 是一种淡黄色固体,该固体药品为淡黄色
(2)Na O 、Na CO 和 NaOH
【设计实验】实验一:一
实验二:Na CO (或碳酸钠)
三
【得出结论】四
【拓展延伸】吸收呼出的 CO 气体,同时生成 O ,能使潜艇中的气体成分相对稳定(合理即可)
四、计算题(共 6分)
17.(1)0.2 (1分)
(2)3.4%……………………………………………(1分)
(3)解:100g稀硫酸中 H SO 的质量为100g×9.8%=9.8g设生成 FeSO 的质量为x。
…(1分)
98 152
9.8g x
…(1分)
x=15.2g……………………………………………(1分)
反应后所得溶液中溶质的质量分数为
… (1分)
答:反应后所得溶液中溶质的质量分数为 14.4%。
2024年九年级中考化学模拟预测试题一
说 明: 1. 全卷满分 70分,考试时间 50分钟。
2. 本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共四个大题,17个小题。
可能用到的相对原子质量: H-1 C-12 O-16 Na-23 Mg-24 S-32 Fe-56 Cu-64 Zn-65 Ba-137
第Ⅰ卷 选择题(共30分)
一、选择题(本题共 10个小题,每小题只有一个选项符合题意,每小题 3分,共 30分)
1.“女儿节”是广元的地方性传统节日,源于民间“正月二十三、妇女游河湾”的传统习俗。下列活动中一定涉及化学变化的是 ( )
A.彩船巡游 B.燃放礼花弹
C.穿汉服、抛绣球 D.观剑门关、翠云廊
2.化学与人们的生产、生活密切相关。下列有关做法不恰当的是 ( )
A.用新型可降解塑料制作农用塑料薄膜
B.霉变食物煮熟后可以食用
C.铁制品表面刷漆或涂油防止锈蚀
D.为节约石油资源,可在汽油中加入适量乙醇作为汽车燃料
3.物质的性质决定其用途。下列物质的性质与用途关系对应正确的是 ( )
A.氧气能支持燃烧——可作燃料
B.活性炭具有吸附性——可用于降低水的硬度
C.金刚石的硬度大——可作装饰品
D.一氧化碳具有还原性——可用于冶炼金属
4.下列实验操作、实验现象和实验结论的对应关系不正确的是 ( )
选项 实验操作 实验现象 实验结论
A 在蜡烛的火焰上方罩一内壁蘸有澄清石灰水的烧杯 澄清石灰水变浑浊 蜡烛中含有碳元素
B 取少量嘉陵江的水于烧杯中,加入一定量肥皂水,搅拌 出现大量的浮渣 该水的硬度大
C 将氢气通入装有氧化铜的试管中,加热 试管内黑色固体变成红色 该反应有 H O生成
D 将盛有燃着硫的燃烧匙伸入充满氧气的集气瓶中 有刺激性气味的气体生成 硫能与氧气发生反应
5.某化学反应的微观示意图如图所示,下列说法正确的是 ( )
A.该反应中原子和分子的种类都发生改变
B.参加反应的两种分子的个数比为 3:2
C.符合该微观示意图的化学方程式可以为
D.该反应中元素的化合价均不变
6.除去下列物质中混有的杂质,所用试剂或操作方法正确的是 ( )
选项 物质(括号内为杂质) 所用试剂或操作方法
A KCl溶液(FeCl ) 向溶液中加入适量的氢氧化钾溶液,充分反应后过滤
B NaCl(NaNO ) 加水溶解后降温结晶
C O (CH ) 点燃
D CaCO (CaO) 加入足量的稀盐酸,充分反应后过滤、洗涤、干燥
7.下列图像能正确反映其对应关系的是 ( )
A.甲:向饱和的硝酸钾溶液中加入一定量的硝酸铵固体
B.乙:红磷在充满空气的密闭容器中燃烧
C.丙:水通电生成氢气和氧气
D.丁:加热一定质量的高锰酸钾
8.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法不正确的是( )
A. T ℃时,加水可使乙溶液从 M 点状态变为 N 点状态
B. T ℃时,甲和丙的饱和溶液中溶质质量分数相等
C. T ℃时,将40g甲放入50g水中,充分溶解后所得溶液的质量为 80g
D.将 T ℃时100g丙的饱和溶液降温至 T ℃,应再加入15g 丙才能恰好达到饱和状态
9.取一定质量的镁和铜的混合金属粉末,加入mg氯化锌和氯化亚铁的混合溶液中,待充分反应后过滤,得到ng滤液。下列说法不正确的是 ( )
A.溶液的质量:m
C.滤渣中金属的组成情况有三种
D.滤液中阳离子一定含 可能含 Fe 和Zn
10.一定量的木炭在盛有 N 和 O 混合气体的密闭容器中燃烧,生成CO和 CO ,且测得反应后所得CO、CO 、N 的混合气体中碳元素的质量分数为24%,则其中 N 的质量分数可能为 ( )
A.12% B.30% C.44% D.60%
第Ⅱ卷 非选择题(共 40 分)
二、填空题(本题共4个小题,每空1分,共20分)
11.(5分)化学用语是学习和研究化学的重要工具。请用化学用语填空:
(1)氩气: 。
(2)4个铵根离子: 。
(3)2个乙醇分子: 。
(4)标出 Na SiO 中硅元素的化合价: 。
(5)写出小苏打治疗胃酸过多的化学方程式: 。
12.(6分)人类的发展离不开化学,化学在农业生产和科技发展中发挥着重要的作用。请根据所学化学知识回答下列问题:
(1)2023 年 9月,广元昭化举办了以“庆丰收·促和美”为主题的丰收节活动。
①辛弃疾的《西江月·夜行黄沙道中》写到“稻花香里说丰年,听取蛙声一片”,诗中描写“稻花香”的情景,请从微观角度解释: 。
②农作物的生长需要 N、P、K等营养元素,下列化肥中属于复合肥的是 (填字母)。
A.磷矿粉 B.尿素 C.硝酸钾
③农作物一般适宜在 pH=7或接近7的土壤中生长。近年来由于空气污染形成酸雨,导致土壤酸性增强,不利于农作物生长,于是人们常将适量的 加入土壤中,以中和其酸性。
(2)广元昭化王家贡米是依托搭乘火箭飞船遨游太空的“太空种子”而孕育的。
①火箭外壳的主要材料为铝合金,下列属于铝合金性质的是 (填字母)。
A.硬度大 B.密度大 C.抗腐蚀
②火箭整流罩的端头帽是由玻璃钢纤维材料制成的,玻璃钢属于 材料。
③发射火箭时常用肼和四氧化二氮作为推进剂,其反应的化学方程式为: 3R+4H O,,则 R 的化学式为 。
13.(5分)中国科学院院士张青莲教授为相对原子质量的测定作出了卓越贡献。他主持测定了铟、铱、锑、销、铈、铒、锗、锌、镝几种元素相对原子质量的新值,被国际原子量委员会采用为国际新标准。铟元素在元素周期表中显示的信息及其原子结构示意图如下。请回答下列问题:
(1)铟的相对原子质量为 ,铟元素位于元素周期表中第 周期。
(2)在化学反应中铟原子易失去电子,形成的离子为 (填符号),在1~18号元素中,与铟元素化学性质相似的金属元素是 (填名称)。
(3)在医学上,常用铟的不同化合物来对人体的各个器官进行扫描。在加热条件下,铟能与氯气发生化合反应,其生成物的化学式为 。
14.(4分)A~L是初中化学常见的物质,它们之间的转化关系如下图所示(图中每个反应都是一步实现,其中“一”表示两种物质间能发生化学反应,“→”表示两种物质间的转化关系,反应条件和部分物质已略去)。其中 A 是碳酸氢铵,D、G组成元素相同,H 为黑色固体,J 俗称纯碱,K 是常见的酸,L是蓝色沉淀。请回答下列问题:
(1)写出 H 的化学式: 。
(2)写出D的一种用途: 。
(3)反应①~⑥中复分解反应有 个。
(4)写出反应②的化学方程式: 。
三、实验探究题(本题共 2个小题,每空1分,共 14分)
15.(6分)下图是实验室制取气体的常用装置,请回答下列问题:
(1)写出仪器①的名称: 。
(2)实验室制取CO 的化学方程式为 ,从控制反应的发生和停止角度考虑,其发生装置最好选择 (填字母)。若选用装置G除去 CO 中混有的水蒸气,则装置G中应装入的试剂是 ,气体应从 (填“a”或“b”)端导管通入。
(3)实验室常用铜和稀硝酸反应制取一氧化氮气体,一氧化氮是一种无色无味的有毒气体,难溶于水;在常温下一氧化氮能与氧气反应生成红棕色的气体二氧化氮。若实验室要收集一瓶一氧化氮气体,收集装置应选择 (填字母)。
16.(8分)实验室有一瓶已过保质期的淡黄色固体药品,标签上的药品名称是过氧化钠( 某化学兴趣小组同学想知道这瓶固体究竟含有哪些成分,他们在化学老师的指导下进行了如下实验探究。
【查阅资料】i.过氧化钠是一种淡黄色的固体。
.在常温下过氧化钠能与 CO 和 H O 反应,其反应原理是
【猜想与假设】(1)该小组同学一致认为该固体药品中一定含 Na O ,理由是 。
(2)提出猜想:一、全部是 Na O ;
二、只含有 Na O 和 Na CO ;
三、只含有 Na O 和 NaOH;
四、你的猜想是含有 。
【设计实验】实验一:取2.0g 固体样品于试管中,加入适量的水,完全反应后(无固体剩余),测得收集到的气体的质量为0.16g,由此推出猜想 错误。
实验二:向实验一反应后的溶液中加入过量的) 溶液,有白色沉淀生成,由此推知固体样品中含有 ,其反应的化学方程式为 ,因此猜想 错误。
实验三:将实验二中生成的白色沉淀过滤、洗涤、干燥后,称得其质量为1.97 g。
【得出结论】通过上述实验操作得出结论,猜想 正确。
【拓展延伸】过氧化钠常用在潜艇中制造氧气,其主要优点是 (答出一条即可)。
四、计算题(本题1个小题,共6分)
17.向5.8g某生铁(只含铁和碳)样品中,逐滴加入溶质质量分数为9.8%的稀硫酸,待刚好不再产生气泡时停止滴入,反应过程中加入稀硫酸的质量与生成气体的质量关系如图所示。请计算(结果保留到小数点后一位):
(1)m的值为 。
(2)生铁样品中碳元素的质量分数为 。
(3)反应后所得溶液中溶质的质量分数(写出计算过程)。
一、选择题(每小题3分,共 30分)
1. B 2. B 3. D 4. C 5. C 6. A 7. B 8. D 9. A10. B
二、填空题(每空1分,共 20分)
11.(1) Ar (2)4NH (3)2C H OH(或2C H O)
12.(1)①分子在不断地运动 ②C
③熟石灰[或消石灰、Ca(OH) 、氢氧化钙]
(2)①AC ②复合 ③N
13.(1)114.8 五 (2)In 铝 (3)InCl
14.(1)CuO
(2)用于灭火(或制碳酸饮料、作气体肥料等,合理即可)
三、实验探究题(每空 1分,共 14分)
15.(1)铁架台
C 浓硫酸 b (3)D
16.【猜想与假设】(1)Na O 是一种淡黄色固体,该固体药品为淡黄色
(2)Na O 、Na CO 和 NaOH
【设计实验】实验一:一
实验二:Na CO (或碳酸钠)
三
【得出结论】四
【拓展延伸】吸收呼出的 CO 气体,同时生成 O ,能使潜艇中的气体成分相对稳定(合理即可)
四、计算题(共 6分)
17.(1)0.2 (1分)
(2)3.4%……………………………………………(1分)
(3)解:100g稀硫酸中 H SO 的质量为100g×9.8%=9.8g设生成 FeSO 的质量为x。
…(1分)
98 152
9.8g x
…(1分)
x=15.2g……………………………………………(1分)
反应后所得溶液中溶质的质量分数为
… (1分)
答:反应后所得溶液中溶质的质量分数为 14.4%。
同课章节目录
