【全国版】2024年九年级中考化学模拟预测试题二
文档属性
| 名称 | 【全国版】2024年九年级中考化学模拟预测试题二 | 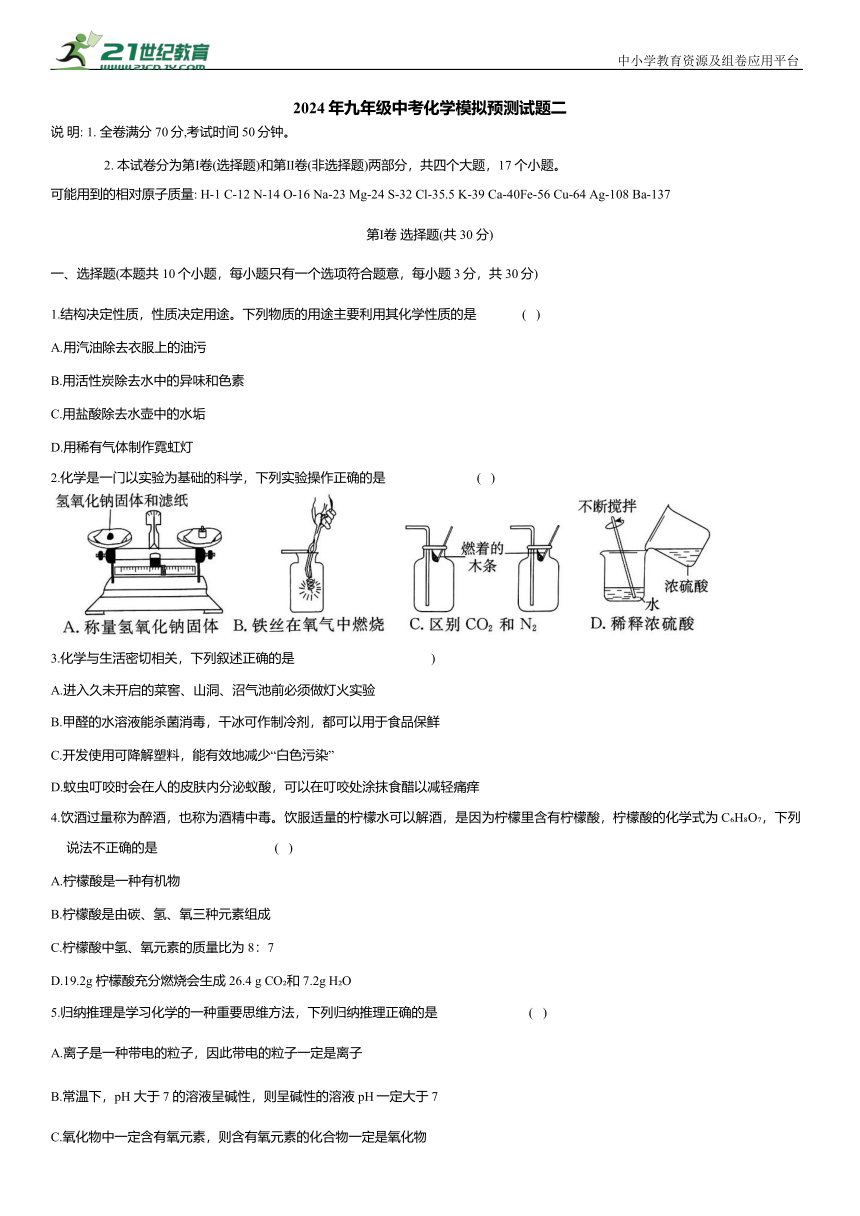 | |
| 格式 | docx | ||
| 文件大小 | 937.1KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-14 22:16:23 | ||
图片预览



文档简介
2024年九年级中考化学模拟预测试题二
说 明: 1. 全卷满分 70分,考试时间50分钟。
2. 本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共四个大题,17 个小题。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5 K-39 Ca-40Fe-56 Cu-64 Ag-108 Ba-137
第Ⅰ卷 选择题(共 30 分)
一、选择题(本题共10个小题,每小题只有一个选项符合题意,每小题3分,共30分)
1.结构决定性质,性质决定用途。下列物质的用途主要利用其化学性质的是 ( )
A.用汽油除去衣服上的油污
B.用活性炭除去水中的异味和色素
C.用盐酸除去水壶中的水垢
D.用稀有气体制作霓虹灯
2.化学是一门以实验为基础的科学,下列实验操作正确的是 ( )
3.化学与生活密切相关,下列叙述正确的是 )
A.进入久未开启的菜窖、山洞、沼气池前必须做灯火实验
B.甲醛的水溶液能杀菌消毒,干冰可作制冷剂,都可以用于食品保鲜
C.开发使用可降解塑料,能有效地减少“白色污染”
D.蚊虫叮咬时会在人的皮肤内分泌蚁酸,可以在叮咬处涂抹食醋以减轻痛痒
4.饮酒过量称为醉酒,也称为酒精中毒。饮服适量的柠檬水可以解酒,是因为柠檬里含有柠檬酸,柠檬酸的化学式为C H O ,下列说法不正确的是 ( )
A.柠檬酸是一种有机物
B.柠檬酸是由碳、氢、氧三种元素组成
C.柠檬酸中氢、氧元素的质量比为 8:7
D.19.2g 柠檬酸充分燃烧会生成26.4 g CO 和7.2g H O
5.归纳推理是学习化学的一种重要思维方法,下列归纳推理正确的是 ( )
A.离子是一种带电的粒子,因此带电的粒子一定是离子
B.常温下,pH 大于7 的溶液呈碱性,则呈碱性的溶液 pH一定大于7
C.氧化物中一定含有氧元素,则含有氧元素的化合物一定是氧化物
D.酸能使紫色石蕊溶液变红,将CO 通入紫色石蕊溶液中,紫色石蕊溶液变红,故CO 属于酸
6.根据实验目的,下列实验的方案设计、现象和结论均正确的是 ( )
选项 实验目的 方案设计 现象和结论
A 比较金属 Zn、Mg的活动性强弱 向锌粒和镁条中加入等体积、等浓度的稀盐酸 镁条表面产生的气泡比锌粒产生的多,证明金属活动性:Mg>Zn
B 区 别 NH NO 固 体 和 NaOH固体 分别取等量样品于试管中,向其中加入适量的等质量的水,振荡,触摸试管外壁 试 管 外 壁 温 度 升 高 的 为NH NO 固体,温度降低 的为NaOH 固体
C 除去 CaCO 中的 CaCl 向样品中加入适量的稀盐酸 有气泡产生,待不再产生气泡时表明杂质除尽
D 鉴别羊毛和棉花 将样品分别点燃,闻气味 有烧焦羽毛气味的为羊毛,有烧纸气味的为棉花
7.元素化合价有升降的反应叫做氧化还原反应,反应物中元素化合价升高的物质称为还原剂,元素化合价降低的物质称为氧化剂。常温下铜与稀硫酸不会反应,但是加热情况下铜会与浓硫酸发生反应,其化学方程式为: 下列说法不正确的是 ( )
A.生成物X 的化学式是 H O ,推导依据为化学反应前后原子种类、原子个数不变
B.反应物 Cu的化合价为0价,CuSO 中 Cu的化合价为+2 价,故此反应中 Cu 是还原剂
C.生成物中的 SO 不能随意排放到空气中,因为它是产生酸雨的罪魁祸首之一
D.浓硫酸具有强烈的腐蚀性,不小心弄到皮肤上,应立即用大量清水冲洗,再涂上3%~5%的碳酸氢钠溶液
8.如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是 ( )
A.甲中混有少量的乙,用蒸发结晶的方法提纯甲
B. T ℃时,将20g丙物质投入50g 水中,所得溶液的质量为70g
C.将 T ℃时等质量的甲、乙、丙饱和溶液降温到 T ℃,所得溶液中溶剂由多到少的关系是:丙>乙>甲
D.将 T ℃时甲、乙、丙的饱和溶液升温到 T ℃,所得溶液溶质质量分数由大到小的关系是:甲>乙>丙
9.下列图像对应的变化关系正确的是 ( )
A.甲:向稀硫酸和硫酸铜的混合溶液中加入足量的氢氧化钡溶液
B.乙:将足量的锌和铁投入质量相等的同浓度稀盐酸中
C.丙:将足量的铁粉加入硝酸银和硝酸铜的混合溶液中
D.丁:将足量的碳酸钠溶液逐滴加入盐酸和氯化钙的混合溶液中
10.现有 CaCO 和 CaO的混合物,测得其中钙元素的质量分数为60%,现取 10g 混合物投入一定质量的稀盐酸中恰好完全反应,最终得到100g溶液,所得溶液的溶质质量分数为 ( )
A.17.65% B.18.5% C.6% D.16.65%
第Ⅱ卷 非选择题(共 40 分)
二、填空题(本题共4个小题,每空1分,共21分)
11.(8分)(1)化学用语是学习化学的重要工具。请用化学用语填空:
①保持氖气化学性质的最小粒子: 。
②使溶液显浅绿色的离子: 。
③标出硝酸铵中氮元素的化合价: 。
(2)图1是铝元素在元素周期表中的一些信息,图2是另外几种微粒的结构示意图,根据图示回答下列问题:
①根据图1中信息,铝原子的相对原子质量为 ,铝的化学性质活泼,但是抗腐蚀性能却很强,其原因是 (用化学方程式表示)。
②图2中一共有 种元素,其中化学性质相似的是 (填序号),D元素位于元素周期表中第 周期。
12.(7分)(1)2023年 9 月 23 日,全国首创的绿色零碳甲醇点燃了杭州亚运会主火炬。甲醇可以利用二氧化碳和氢气在一定条件下获得,下面是有关反应的微观示意图,请回答下列问题:
①写出上图中氧化物的化学式: 。
②参加反应的8和 的质量比为 。
(2)一年一度的广元女儿节于2023年9月1日隆重召开,女儿节彰显了广元人民的文化风采。开幕式时虽然天空下起蒙蒙细雨,但丝毫没有阻挡广元人民参与女儿节的热情,大家纷纷穿上了塑料雨衣,去观看游船、划龙舟、品美食……
①塑料雨衣属于 (填“复合”或“合成”)材料。
②此次女儿节“大华1939”美食分会场中涉及的美食众多,有“贵州特色米粉”“内蒙古大草原烤肉串”“长沙臭豆腐”“龙卷风巨型薯塔”“烤糖人”……其中富含蛋白质的食物有 ,制作美食的燃料有木炭、天然气,请写出天然气燃烧的化学方程式: 。
③女儿节中不仅有美食,还有广元“七绝”,其中包含米仓山的富硒富锌绿茶。其中“硒”和“锌”是指 (填“单质”或“元素”),喝茶时茶壶中的金属网起 作用。
13.(2分)有一包 K SO 样品,其中可能含有 中的一种或几种,为了探究其组成,某化学兴趣小组做了如下实验:
(1)该白色粉末中除了 K SO 外,一定还含有 。
(2)样品中导致产生无色气体 C的物质的质量分数为 (保留小数点后一位)。
14.(4分)A~G是初中化学常见的物质(图中每个反应都是一步实现,其中“一”表示两种物质间能发生反应,“→”表示两种物质间的转化关系,反应条件和部分物质已略去)。其中 B是一种红棕色固体,D是人体胃液中所含的酸,F广泛用于玻璃、造纸、纺织和洗涤剂的生产,E 和 G 属于同一类别的物质。请回答下列问题:
(1)写出E的一个用途: 。
(2)写出反应②的化学方程式: ,其基本反应类型为 。
(3)写出反应 的化学方程式: 。
三、实验探究题(本题共 2个小题,每空1分,共 14分)
15.(6分)下图是实验室制取气体的常用装置,请回答下列问题:
(1)写出仪器a的名称: 。
(2)用A、C来制取一瓶氧气,写出有关的化学方程式: 。
(3)若用D来收集一瓶CO ,验满的方法为 。F 装置是某同学用废弃塑料瓶等组装的制取(CO 的发生装置,该装置与 B 比较除了废物利用的优点外,还有的优点为 。
(4)硫化氢(H S)是一种无色、有臭鸡蛋气味的有毒气体,易溶于水,其水溶液显酸性,与盐酸化学性质相似,我们通常选择 E 装置来处理含 H S的尾气,其反应的化学方程式为 ,装置中使用倒置漏斗而没有直接用玻璃管的优点为 。
16.(8分)某化学兴趣小组在整理化学实验室时发现有失去标签的 A、B、C、D 四种溶液,经过了解它们分别是 FeCl 溶液、稀盐酸、KOH 溶液、Ca(OH) 溶液中的一种。
【提出问题】A、B、C、D这四种溶液分别是什么呢
【实验探究】经过观察,A溶液呈黄色,则 A 溶液为 溶液。
为了把剩余三种溶液鉴别出来,化学兴趣小组分别取三种溶液少许于试管中,向其中加入 ,发现 B溶液中产生白色沉淀,B溶液为 ;C溶液中产生气泡,C溶液为 ,D中无明显现象。
【拓展延伸】实验后,兴趣小组同学把 FeCl 溶液放回了药品柜,将其余三种溶液连同废液全部倒入废液杯中,得到无色透明溶液,为了防止废液腐蚀下水道,小明同学向废液中加入了几滴酚酞溶液检测溶液的酸碱性,发现溶液仍为无色,则混合后的溶液中一定不存在的离子为 ,可能存在的物质为 ,怎么证明该物质存在 (用化学方程式表示)。
【反思与评价】若上述物质存在,请你给兴趣小组提出一个建议,怎样处理混合后的废液
。
四、计算题(本题1个小题,共5分)
17.某化学兴趣小组同学将 溶液分五次加入 溶液中,测得实验数据如下表所示。[已知:]
第一次 第二次 第三次 第四次 第五次
Mg(NO ) 溶液质量/g 20 20 20 20 20
沉淀的质量/g 5.6 11.2 16.8 17.4 m
(1)第 次时)Ba(OH) 溶液反应完,表格中m的值为 。
(2)求最终所得溶液中 的溶质质量分数。
一、选择题(每小题 3分,共 30分)
1. C 2. D 3. C 4. C 5. B 6. D 7. A 8. C 9. C10. D
二、填空题(每空1分,共21分)
11.(1)①Ne ②Fe ③NH NO
(2)①26.98 4Al+3O ══2Al O ②4 C、E 四
12.(1)①CO 、H O(答对一个给 0.5分) ②3:22
(2)①合成 ②“内蒙古大草原烤肉串”“长沙臭豆腐”(答对一个给0.5分)
③元素 过滤
13.(1)Na SO 、Na CO (2)37.9%
14.(1)改良酸性土壤(合理即可)
分解反应
三、实验探究题(每空 1分,共14分)
15.(1)长颈漏斗
(3)用一根燃着的木条靠近 m端导管口,若木条熄灭则CO 已满 控制反应的发生与停止
倒置漏斗增大了H S与 NaOH 溶液的接触面积,更有利于吸收 H S(或防止倒吸,答案合理即可)
16.【实验探究】FeCl Na CO 溶液(或 K CO 溶液)
Ca(OH) 稀盐酸
【拓展延伸】CO 、OH 稀盐酸 ↑或酸与金属氧化物、难溶性碱反应的方程式)
【反思与评价】向溶液中加入碱性物质将 pH 调至7 后再倒入下水道(答案合理即可)
四、计算题(共 5分)
17.(1)四17.4…………………………(每空1分,共2分)
(2)解:设生成的Ba(NO ) 的质量为x。
58 261
17.4g x
…(1分)
x=78.3g……………………………………………(1分)
反应后所得到的溶液中Ba(NO ) 的溶质质量分数为: (1分)
中小学教育资源及组卷应用平台
答:最终所得溶液中 Ba(NO ) 的溶质质量分数为 26.1%。
说 明: 1. 全卷满分 70分,考试时间50分钟。
2. 本试卷分为第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共四个大题,17 个小题。
可能用到的相对原子质量: H-1 C-12 N-14 O-16 Na-23 Mg-24 S-32 Cl-35.5 K-39 Ca-40Fe-56 Cu-64 Ag-108 Ba-137
第Ⅰ卷 选择题(共 30 分)
一、选择题(本题共10个小题,每小题只有一个选项符合题意,每小题3分,共30分)
1.结构决定性质,性质决定用途。下列物质的用途主要利用其化学性质的是 ( )
A.用汽油除去衣服上的油污
B.用活性炭除去水中的异味和色素
C.用盐酸除去水壶中的水垢
D.用稀有气体制作霓虹灯
2.化学是一门以实验为基础的科学,下列实验操作正确的是 ( )
3.化学与生活密切相关,下列叙述正确的是 )
A.进入久未开启的菜窖、山洞、沼气池前必须做灯火实验
B.甲醛的水溶液能杀菌消毒,干冰可作制冷剂,都可以用于食品保鲜
C.开发使用可降解塑料,能有效地减少“白色污染”
D.蚊虫叮咬时会在人的皮肤内分泌蚁酸,可以在叮咬处涂抹食醋以减轻痛痒
4.饮酒过量称为醉酒,也称为酒精中毒。饮服适量的柠檬水可以解酒,是因为柠檬里含有柠檬酸,柠檬酸的化学式为C H O ,下列说法不正确的是 ( )
A.柠檬酸是一种有机物
B.柠檬酸是由碳、氢、氧三种元素组成
C.柠檬酸中氢、氧元素的质量比为 8:7
D.19.2g 柠檬酸充分燃烧会生成26.4 g CO 和7.2g H O
5.归纳推理是学习化学的一种重要思维方法,下列归纳推理正确的是 ( )
A.离子是一种带电的粒子,因此带电的粒子一定是离子
B.常温下,pH 大于7 的溶液呈碱性,则呈碱性的溶液 pH一定大于7
C.氧化物中一定含有氧元素,则含有氧元素的化合物一定是氧化物
D.酸能使紫色石蕊溶液变红,将CO 通入紫色石蕊溶液中,紫色石蕊溶液变红,故CO 属于酸
6.根据实验目的,下列实验的方案设计、现象和结论均正确的是 ( )
选项 实验目的 方案设计 现象和结论
A 比较金属 Zn、Mg的活动性强弱 向锌粒和镁条中加入等体积、等浓度的稀盐酸 镁条表面产生的气泡比锌粒产生的多,证明金属活动性:Mg>Zn
B 区 别 NH NO 固 体 和 NaOH固体 分别取等量样品于试管中,向其中加入适量的等质量的水,振荡,触摸试管外壁 试 管 外 壁 温 度 升 高 的 为NH NO 固体,温度降低 的为NaOH 固体
C 除去 CaCO 中的 CaCl 向样品中加入适量的稀盐酸 有气泡产生,待不再产生气泡时表明杂质除尽
D 鉴别羊毛和棉花 将样品分别点燃,闻气味 有烧焦羽毛气味的为羊毛,有烧纸气味的为棉花
7.元素化合价有升降的反应叫做氧化还原反应,反应物中元素化合价升高的物质称为还原剂,元素化合价降低的物质称为氧化剂。常温下铜与稀硫酸不会反应,但是加热情况下铜会与浓硫酸发生反应,其化学方程式为: 下列说法不正确的是 ( )
A.生成物X 的化学式是 H O ,推导依据为化学反应前后原子种类、原子个数不变
B.反应物 Cu的化合价为0价,CuSO 中 Cu的化合价为+2 价,故此反应中 Cu 是还原剂
C.生成物中的 SO 不能随意排放到空气中,因为它是产生酸雨的罪魁祸首之一
D.浓硫酸具有强烈的腐蚀性,不小心弄到皮肤上,应立即用大量清水冲洗,再涂上3%~5%的碳酸氢钠溶液
8.如图是甲、乙、丙三种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是 ( )
A.甲中混有少量的乙,用蒸发结晶的方法提纯甲
B. T ℃时,将20g丙物质投入50g 水中,所得溶液的质量为70g
C.将 T ℃时等质量的甲、乙、丙饱和溶液降温到 T ℃,所得溶液中溶剂由多到少的关系是:丙>乙>甲
D.将 T ℃时甲、乙、丙的饱和溶液升温到 T ℃,所得溶液溶质质量分数由大到小的关系是:甲>乙>丙
9.下列图像对应的变化关系正确的是 ( )
A.甲:向稀硫酸和硫酸铜的混合溶液中加入足量的氢氧化钡溶液
B.乙:将足量的锌和铁投入质量相等的同浓度稀盐酸中
C.丙:将足量的铁粉加入硝酸银和硝酸铜的混合溶液中
D.丁:将足量的碳酸钠溶液逐滴加入盐酸和氯化钙的混合溶液中
10.现有 CaCO 和 CaO的混合物,测得其中钙元素的质量分数为60%,现取 10g 混合物投入一定质量的稀盐酸中恰好完全反应,最终得到100g溶液,所得溶液的溶质质量分数为 ( )
A.17.65% B.18.5% C.6% D.16.65%
第Ⅱ卷 非选择题(共 40 分)
二、填空题(本题共4个小题,每空1分,共21分)
11.(8分)(1)化学用语是学习化学的重要工具。请用化学用语填空:
①保持氖气化学性质的最小粒子: 。
②使溶液显浅绿色的离子: 。
③标出硝酸铵中氮元素的化合价: 。
(2)图1是铝元素在元素周期表中的一些信息,图2是另外几种微粒的结构示意图,根据图示回答下列问题:
①根据图1中信息,铝原子的相对原子质量为 ,铝的化学性质活泼,但是抗腐蚀性能却很强,其原因是 (用化学方程式表示)。
②图2中一共有 种元素,其中化学性质相似的是 (填序号),D元素位于元素周期表中第 周期。
12.(7分)(1)2023年 9 月 23 日,全国首创的绿色零碳甲醇点燃了杭州亚运会主火炬。甲醇可以利用二氧化碳和氢气在一定条件下获得,下面是有关反应的微观示意图,请回答下列问题:
①写出上图中氧化物的化学式: 。
②参加反应的8和 的质量比为 。
(2)一年一度的广元女儿节于2023年9月1日隆重召开,女儿节彰显了广元人民的文化风采。开幕式时虽然天空下起蒙蒙细雨,但丝毫没有阻挡广元人民参与女儿节的热情,大家纷纷穿上了塑料雨衣,去观看游船、划龙舟、品美食……
①塑料雨衣属于 (填“复合”或“合成”)材料。
②此次女儿节“大华1939”美食分会场中涉及的美食众多,有“贵州特色米粉”“内蒙古大草原烤肉串”“长沙臭豆腐”“龙卷风巨型薯塔”“烤糖人”……其中富含蛋白质的食物有 ,制作美食的燃料有木炭、天然气,请写出天然气燃烧的化学方程式: 。
③女儿节中不仅有美食,还有广元“七绝”,其中包含米仓山的富硒富锌绿茶。其中“硒”和“锌”是指 (填“单质”或“元素”),喝茶时茶壶中的金属网起 作用。
13.(2分)有一包 K SO 样品,其中可能含有 中的一种或几种,为了探究其组成,某化学兴趣小组做了如下实验:
(1)该白色粉末中除了 K SO 外,一定还含有 。
(2)样品中导致产生无色气体 C的物质的质量分数为 (保留小数点后一位)。
14.(4分)A~G是初中化学常见的物质(图中每个反应都是一步实现,其中“一”表示两种物质间能发生反应,“→”表示两种物质间的转化关系,反应条件和部分物质已略去)。其中 B是一种红棕色固体,D是人体胃液中所含的酸,F广泛用于玻璃、造纸、纺织和洗涤剂的生产,E 和 G 属于同一类别的物质。请回答下列问题:
(1)写出E的一个用途: 。
(2)写出反应②的化学方程式: ,其基本反应类型为 。
(3)写出反应 的化学方程式: 。
三、实验探究题(本题共 2个小题,每空1分,共 14分)
15.(6分)下图是实验室制取气体的常用装置,请回答下列问题:
(1)写出仪器a的名称: 。
(2)用A、C来制取一瓶氧气,写出有关的化学方程式: 。
(3)若用D来收集一瓶CO ,验满的方法为 。F 装置是某同学用废弃塑料瓶等组装的制取(CO 的发生装置,该装置与 B 比较除了废物利用的优点外,还有的优点为 。
(4)硫化氢(H S)是一种无色、有臭鸡蛋气味的有毒气体,易溶于水,其水溶液显酸性,与盐酸化学性质相似,我们通常选择 E 装置来处理含 H S的尾气,其反应的化学方程式为 ,装置中使用倒置漏斗而没有直接用玻璃管的优点为 。
16.(8分)某化学兴趣小组在整理化学实验室时发现有失去标签的 A、B、C、D 四种溶液,经过了解它们分别是 FeCl 溶液、稀盐酸、KOH 溶液、Ca(OH) 溶液中的一种。
【提出问题】A、B、C、D这四种溶液分别是什么呢
【实验探究】经过观察,A溶液呈黄色,则 A 溶液为 溶液。
为了把剩余三种溶液鉴别出来,化学兴趣小组分别取三种溶液少许于试管中,向其中加入 ,发现 B溶液中产生白色沉淀,B溶液为 ;C溶液中产生气泡,C溶液为 ,D中无明显现象。
【拓展延伸】实验后,兴趣小组同学把 FeCl 溶液放回了药品柜,将其余三种溶液连同废液全部倒入废液杯中,得到无色透明溶液,为了防止废液腐蚀下水道,小明同学向废液中加入了几滴酚酞溶液检测溶液的酸碱性,发现溶液仍为无色,则混合后的溶液中一定不存在的离子为 ,可能存在的物质为 ,怎么证明该物质存在 (用化学方程式表示)。
【反思与评价】若上述物质存在,请你给兴趣小组提出一个建议,怎样处理混合后的废液
。
四、计算题(本题1个小题,共5分)
17.某化学兴趣小组同学将 溶液分五次加入 溶液中,测得实验数据如下表所示。[已知:]
第一次 第二次 第三次 第四次 第五次
Mg(NO ) 溶液质量/g 20 20 20 20 20
沉淀的质量/g 5.6 11.2 16.8 17.4 m
(1)第 次时)Ba(OH) 溶液反应完,表格中m的值为 。
(2)求最终所得溶液中 的溶质质量分数。
一、选择题(每小题 3分,共 30分)
1. C 2. D 3. C 4. C 5. B 6. D 7. A 8. C 9. C10. D
二、填空题(每空1分,共21分)
11.(1)①Ne ②Fe ③NH NO
(2)①26.98 4Al+3O ══2Al O ②4 C、E 四
12.(1)①CO 、H O(答对一个给 0.5分) ②3:22
(2)①合成 ②“内蒙古大草原烤肉串”“长沙臭豆腐”(答对一个给0.5分)
③元素 过滤
13.(1)Na SO 、Na CO (2)37.9%
14.(1)改良酸性土壤(合理即可)
分解反应
三、实验探究题(每空 1分,共14分)
15.(1)长颈漏斗
(3)用一根燃着的木条靠近 m端导管口,若木条熄灭则CO 已满 控制反应的发生与停止
倒置漏斗增大了H S与 NaOH 溶液的接触面积,更有利于吸收 H S(或防止倒吸,答案合理即可)
16.【实验探究】FeCl Na CO 溶液(或 K CO 溶液)
Ca(OH) 稀盐酸
【拓展延伸】CO 、OH 稀盐酸 ↑或酸与金属氧化物、难溶性碱反应的方程式)
【反思与评价】向溶液中加入碱性物质将 pH 调至7 后再倒入下水道(答案合理即可)
四、计算题(共 5分)
17.(1)四17.4…………………………(每空1分,共2分)
(2)解:设生成的Ba(NO ) 的质量为x。
58 261
17.4g x
…(1分)
x=78.3g……………………………………………(1分)
反应后所得到的溶液中Ba(NO ) 的溶质质量分数为: (1分)
中小学教育资源及组卷应用平台
答:最终所得溶液中 Ba(NO ) 的溶质质量分数为 26.1%。
同课章节目录
