7.3乙醇和乙酸同步练习(含解析)2023——2024学年高中化学人教版(2019)必修第二册
文档属性
| 名称 | 7.3乙醇和乙酸同步练习(含解析)2023——2024学年高中化学人教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-14 00:00:00 | ||
图片预览


文档简介
7.3乙醇和乙酸同步练习
姓名()班级()学号()
一、单选题
1.下列有机反应既不属于加成反应也不属于取代反应的是
A.CH2=CH2+H2OCH3CH2OH
B.CH4+Cl2CH3Cl+HCl
C.2CH3CH2OH+O22CH3CHO+2H2O
D.CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
2.下列有关化学用语表示正确的是
A.氮气的电子式: B.的空间填充模型:
C.乙醇的结构式: D.K的原子结构示意图:
3.下列反应中,属于取代反应的是
A.CH2=CH2+HClCH3CH2Cl
B.2CH3CH2OH+O22CH3CHO+2H2O
C.+H2CH3CH2OH
D.CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
4.2021年,我国科学家利用为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程中发生反应:,设为阿伏加德罗常数,下列有关说法正确的是。
A.17 g H2O2中含有过氧键数目为0.5 NA B.标况下,22.4 L CH3OH中含有的羟基数为NA
C.18 g D2O中含有氧原子的数目为1 NA D.1 mol O2参与反应转移电子数为4 NA
5.关于实验室制备、分离乙酸乙酯的装置,说法正确的是
A.图甲用于分离乙酸乙酯
B.乙用于蒸馏纯化乙酸乙酯
C.图丙可从分液漏斗下端放出乙酸乙酯
D.图丁用于制备并收集乙酸乙酯
6.利用柠檬真菌青霉生成的前体,可生产对降低胆固醇有积极作用的他汀类药物,某种他汀类药物M的结构如图。下列关于M的说法正确的是
A.分子中所有碳原子可能共平面
B.通过酯化反应可能获得该分子
C.不存在含苯环结构的同分异构体
D.1molM最多消耗4mol氢气
7.下列说法正确的是
A.含有相同官能团的物质其化学性质全部相同
B.含有的物质不是醛就是酮
C.两种某物质具有相同的化学性质则一定含有相同的官能团
D.含有的物质一定能与在一定条件下发生加成反应
8.化学是一门以实验为基础的学科。下列实验操作能达到目的的是
选项 目的 实验操作
A 验证SO2的漂白性 将SO2气体通入紫色石蕊溶液中
B 制备Fe(OH)3胶体 向沸水中逐滴加入FeCl3饱和溶液继续煮沸至液体呈红褐色
C 检验乙醇中是否有水 向乙醇中加入一小粒金属钠
D 除去Cu粉中混有的CuO 加入稀硝酸溶解,过滤、洗涤、干燥
A.A B.B C.C D.D
9.橙花醇的结构简式如图,根据乙烯和乙醇的有关性质,下列有关橙花醇的说法不正确的是
A.分子式为C10H18O
B.能发生取代反应、加成反应
C.所有的C原子有可能共平面
D.能用酸性高锰酸钾溶液检验其中是否含有碳碳双键
10.设NA为阿伏加德罗常数的值。下列叙述正确的是
A.3.2gS与足量O2在点燃条件下充分反应,转移的电子数为0.6NA
B.1L0.1 mol L-1的乙酸溶液中含有的氧原子数为0.2NA
C.标准状况下,11.2LC3H8中含有C-C键的数目为NA
D.0.2mol硝酸与足量铜反应转移电子数为0.1NA
11.将两块相同的钠分别投入等量的乙醇和水中,下列说法错误的是
A.与甲相比,乙中钠块很快熔化成光亮的小球
B.钠块沉在乙醇液面下,说明乙醇的密度比钠小
C.乙比甲反应缓和,说明乙醇羟基中的氢原子不如水分子中的氢原子活泼
D.触摸甲、乙烧杯外壁均发热,说明两个反应均放热
12.乙酸、乙醇是生活中常见的有机物。下列说法正确的是
A.乙醇和乙酸的官能团相同
B.与足量乙酸反应,生成
C.两者都能与溶液反应
D.一定条件下,乙醇可以被氧化成乙酸
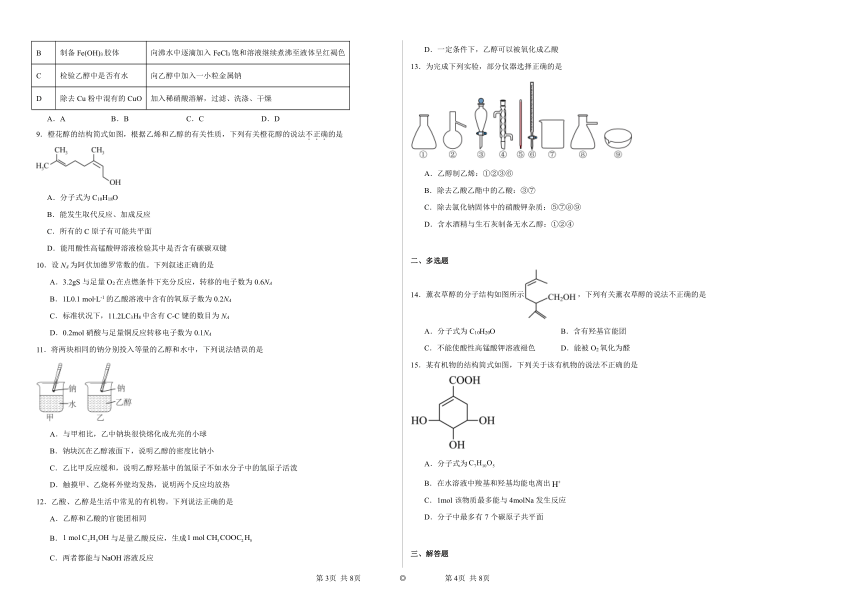
13.为完成下列实验,部分仪器选择正确的是
A.乙醇制乙烯:①②③⑥
B.除去乙酸乙酯中的乙酸:③⑦
C.除去氯化钠固体中的硝酸钾杂质:⑤⑦⑧⑨
D.含水酒精与生石灰制备无水乙醇:①②④
二、多选题
14.薰衣草醇的分子结构如图所示,下列有关薰衣草醇的说法不正确的是
A.分子式为C10H20O B.含有羟基官能团
C.不能使酸性高锰酸钾溶液褪色 D.能被O2氧化为醛
15.某有机物的结构简式如图,下列关于该有机物的说法不正确的是
A.分子式为
B.在水溶液中羧基和羟基均能电离出
C.1mol该物质最多能与4molNa发生反应
D.分子中最多有7个碳原子共平面
三、解答题
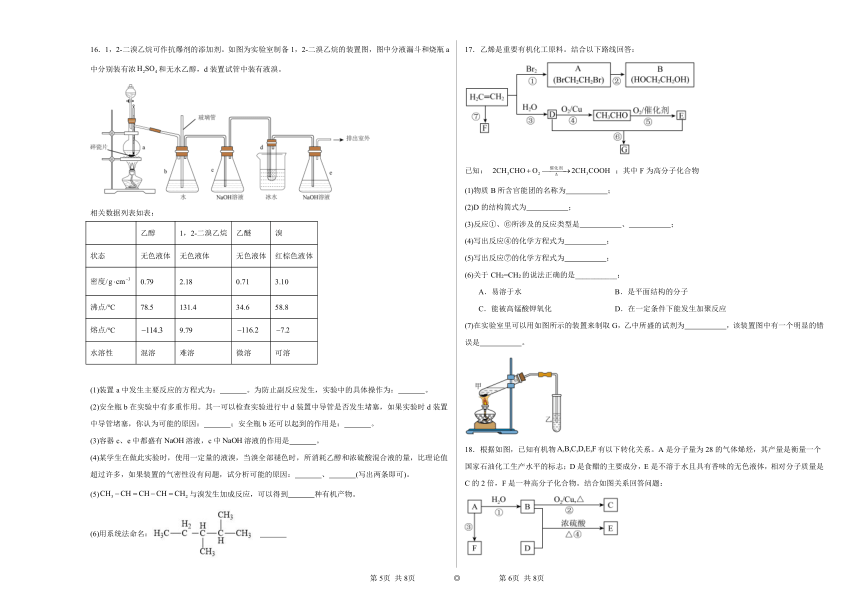
16.1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装置图,图中分液漏斗和烧瓶a中分别装有浓和无水乙醇,d装置试管中装有液溴。
相关数据列表如表:
乙醇 1,2-二溴乙烷 乙醚 溴
状态 无色液体 无色液体 无色液体 红棕色液体
密度/ 0.79 2.18 0.71 3.10
沸点/℃ 78.5 131.4 34.6 58.8
熔点/℃ 9.79
水溶性 混溶 难溶 微溶 可溶
(1)装置a中发生主要反应的方程式为: 。为防止副反应发生,实验中的具体操作为: 。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装置中导管是否发生堵塞,如果实验时d装置中导管堵塞,你认为可能的原因: ;安全瓶b还可以起到的作用是: 。
(3)容器c、e中都盛有溶液,c中溶液的作用是 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比理论值超过许多,如果装置的气密性没有问题,试分析可能的原因: 、 (写出两条即可)。
(5)与溴发生加成反应,可以得到 种有机产物。
(6)用系统法命名:
17.乙烯是重要有机化工原料。结合以下路线回答:
已知: ;其中F为高分子化合物
(1)物质B所含官能团的名称为 ;
(2)D的结构简式为 ;
(3)反应①、⑥所涉及的反应类型是 、 ;
(4)写出反应④的化学方程式为 ;
(5)写出反应⑦的化学方程式为 ;
(6)关于CH2=CH2的说法正确的是___________;
A.易溶于水 B.是平面结构的分子
C.能被高锰酸钾氧化 D.在一定条件下能发生加聚反应
(7)在实验室里可以用如图所示的装置来制取G,乙中所盛的试剂为 ,该装置图中有一个明显的错误是 。
18.根据如图,已知有机物有以下转化关系。A是分子量为28的气体烯烃,其产量是衡量一个国家石油化工生产水平的标志;D是食醋的主要成分,E是不溶于水且具有香味的无色液体,相对分子质量是C的2倍,F是一种高分子化合物。结合如图关系回答问题:
(1)写出中官能团的名称:B 、D ;
(2)写出与B互为同分异构体物质的结构简式 ;
(3)写出与D互为同系物且为该同系物中最简单的一种物质的结构式 。
(4)写出反应②的化学方程式: 。该反应类型是 。
(5)在浓硫酸的作用下实现反应④,实验装置如下图所示,试管1中装入药品后加热。图中X的化学式为 ,其作用是溶解乙醇和 。
19.有机物A~E之间存在如下图所示的转化关系。A的产量是衡量一个国家石油化工产业发展水平的标志。
请回答下列问题:
(1)A→B的化学反应类型为 ,D中官能团的名称为 。
(2)B→C的化学方程式为
(3)石蜡的分解不仅可获得A,还可以得到一种相对分子质量为86的烷烃。写出该烷烃主链碳原子数为4的一种同分异构体的结构简式 。
(4)某化学兴趣小组在实验室利用如图所示装置实现B和D制备E的反应。
①写出甲中反应的化学方程式 。
②试管甲中使用碎瓷片的目的是 ,试管乙中的试剂F为 。
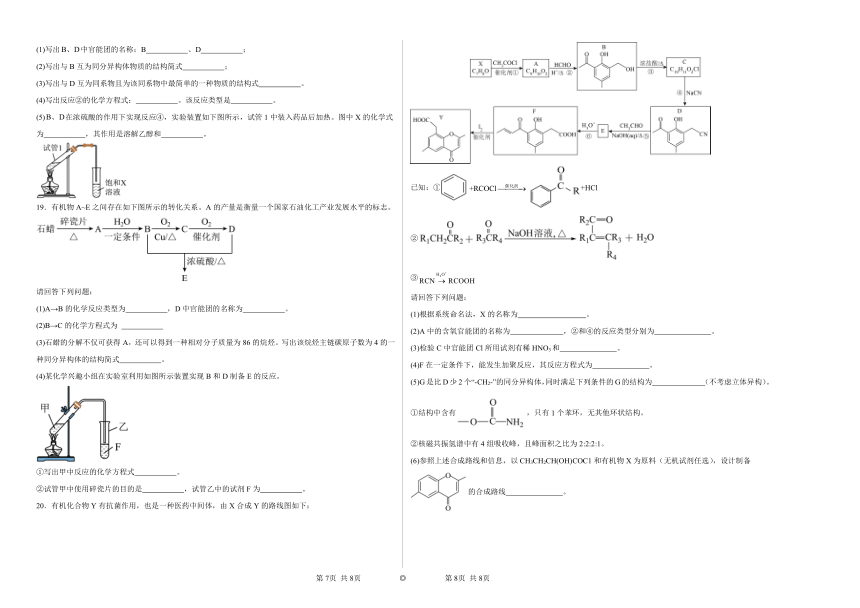
20.有机化合物Y有抗菌作用,也是一种医药中间体,由X合成Y的路线图如下:
已知:① +HCl
②
③
请回答下列问题:
(1)根据系统命名法,X的名称为 。
(2)A中的含氧官能团的名称为 ,②和④的反应类型分别为 。
(3)检验C中官能团Cl所用试剂有稀HNO3和 。
(4)F在一定条件下,能发生加聚反应,其反应方程式为 。
(5)G是比D少2个“-CH2-”的同分异构体,同时满足下列条件的G的结构为 (不考虑立体异构)。
①结构中含有,只有1个苯环,无其他环状结构。
②核磁共振氢谱中有4组吸收峰,且峰面积之比为2:2:2:1。
(6)参照上述合成路线和信息,以CH3CH2CH(OH)COC1和有机物X为原料(无机试剂任选),设计制备的合成路线 。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.C
【详解】A. CH2=CH2+H2OCH3CH2OH,属于加成反应,A不选;
B .CH4+Cl2CH3Cl+HCl,属于取代反应,B不选;
C.2CH3CH2OH+O22CH3CHO+2H2O,属于氧化反应,C选;
D .CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,属于取代反应,D不选;
故选C。
2.B
【详解】A.氮气分子中,两个氮原子间共用3对电子,每个N都达到8电子稳定结构,其电子式是,A项错误;
B.甲烷分子由1个C和4个H构成,的空间填充模型:,B项正确;
C.乙醇的结构式:,C项错误;
D.K为第19号元素,核外电子数为19,其原子结构示意图:,D项错误;
故选B。
3.D
【详解】A.CH2=CH2与HCl反应生成氯乙烷属于加成反应,故A错误;
B.乙醇催化氧化生成乙醛属于氧化反应,故B错误;
C.乙醛与氢气发生加成反应生成乙醇,属于加成反应或还原反应,故C错误;
D.乙酸和乙醇生成乙酸乙酯属于酯化反应,酯化反应为取代反应的一种,故D正确;
故选:D。
4.A
【详解】A.已知H2O2分子中存在1个过氧键,则中含有过氧键数目为,A正确;
B.在标况下CH3OH为液态,密度未知,故无法计算22.4 L CH3OH中含有的羟基数目,B错误;
C.D2O摩尔质量为20g/mol,且一个D2O分子中含1个氧原子,故18gD2O中含有氧原子的数目为,C错误;
D.由反应方程式可知,O2中的O由0价转化到H2O2中的-1价,则参与反应转移电子数为2NA,D错误;
故答案为:A。
5.D
【详解】A.乙酸乙酯中混有乙酸、乙醇,成为液体混合物,图甲用于分离固液混合物,不能用于分离液体混合物中的乙酸乙酯,A不正确;
B.蒸馏操作时,温度计水银球应位于支管口处,不能插入液体中,B不正确;
C.乙酸乙酯密度比水中,浮在水面上,应从分液漏斗上口倒出,C不正确;
D.图丁装置中,反应试管中插入玻璃管,使得试管内外相通,不会产生压强差,能够起到防止倒吸的作用,导管插入碳酸钠溶液中,杂质能与碳酸钠溶液充分接触和反应,有利于杂质的吸收,因此能较好地制备并收集乙酸乙酯,D正确;
故选D。
6.B
【分析】该有机物中含有酯基、碳碳双键、羟基3种官能团,且含有结构“”,则所有碳原子不可能共平面,M的不饱和度大于4,存在含苯环结构的同分异构体,据此回答。
【详解】A.M的分子中含有结构“”,故所有碳原子不可能共平面,A错误;
B.M的结构中含有酯基,酯化反应可引入酯基,B正确;
C.M的不饱和度大于4,存在含苯环结构的同分异构体,C错误;
D.M中的碳碳双键可以与氢气发生加成反应,所以1molM最多消耗2mol氢气,D错误。
故选B。
7.D
【详解】A.有机物的化学性质是通过官能团体现出来的,含有相同的官能团说明具有相似的化学性质,但化学性质不完全相同,故A错误;
B.含有羰基的物质可能是醛、铜或者羧酸、酯、酰胺等,故B错误;
C.某两种物质具有相同的化学性质,不一定含有相同的官能团,如碳碳双键和碳碳三键均可以发生加成反应、加聚反应、氧化反应等,但却是不同的官能团,故C错误;
D.碳碳双键在一定条件下,可以和氢气发生加成反应,故D正确;
故选D。
8.B
【详解】A.验证SO2的漂白性,应将SO2气体通入品红溶液中,而不是通入紫色石蕊溶液中,A不符合题意;
B.向沸水中逐滴加入FeCl3饱和溶液继续煮沸以促进Fe3+水解至液体呈红褐色,可制备Fe(OH)3胶体,B符合题意;
C.向乙醇中加入一小粒金属钠,钠与乙醇也会反应放出无色气泡(H2),会干扰钠与水的反应,则不能检验乙醇中是否有水,C不符合题意;
D.Cu、CuO均可以与稀硝酸反应,导致Cu粉也被溶解,不符合除杂原则,D不符合题意;
故选B。
9.D
【分析】该有机物含有碳碳双键、羟基,能发生取代反应、加成反应,能使高锰酸钾溶液褪色,据此回答。
【详解】A.根据结构式可知,该有机物的分子式为C10H18O,A正确;
B.含有碳碳双键、羟基,能发生取代反应、加成反应,B正确;
C.由于单键可以旋转,所有的C原子有可能共平面,C正确;
D.碳碳双键、羟基都能使高锰酸钾溶液褪色,不能用酸性高锰酸钾溶液检验其中是否含有碳碳双键,D错误;
故选D。
10.C
【详解】A.3.2gS与足量O2在点燃条件下充分反应,生成0.1molSO2,转移的电子数为0.4NA,A不正确;
B.1L0.1 mol L-1的乙酸溶液中,除乙酸中含有0.2molO原子外,水中也含有O原子,则含有的氧原子数大于0.2NA,B不正确;
C. 1个C3H8分子中含有2个C-C键,标准状况下,11.2LC3H8(物质的量为0.5mol)含有C-C键的数目为0.5mol×2×NAmol-1= NA,C正确;
D.0.2mol硝酸与足量铜反应,若只发生转化4HNO3(浓)——2NO2,则转移电子0.1mol,若只发生转化8HNO3(稀)——2NO,则转移电子0.15mol,随着反应的进行,既便起初是浓硝酸,也会转化为稀硝酸,所以转移电子数不是0.1NA,D不正确;
故选C。
11.A
【详解】A.Na的密度比乙醇的密度大,乙中Na沉在底部,且钠的熔点比乙醇的沸点高,钠在乙醇中反应不会熔化成小球,A项错误;
B.Na的密度比乙醇的密度大,故钠块沉在乙醇液面下,B项正确;
C.乙醇羟基中的氢原子不如水分子中的氢原子活泼,故Na与乙醇反应比Na与水反应缓和得多,C项正确;
D.触摸甲、乙烧杯外壁均发热,说明Na与水和乙醇的反应均放热,D项正确;
答案选A。
12.D
【详解】A.乙醇和乙酸的官能团分别为羟基、羧基,则官能团不相同,A错误;
B.C2H5OH与乙酸的酯化反应是可逆反应,不能完全转化,则1molC2H5OH与足量乙酸反应,生成CH3COOC2H5的物质的量小于1mol,B错误;
C.乙酸能与NaOH溶液反应,乙醇不能与NaOH溶液反应,C错误;
D.乙醇可以被酸性KMnO4溶液或酸性K2Cr2O7溶液氧化成乙酸,D正确;
故选D。
13.B
【详解】A.乙醇在170、浓硫酸作用下发生消去反应制备乙烯,主仪器有酒精灯、温度计、圆底烧瓶或者蒸馏烧瓶,不需要锥形瓶,不需要酸式滴定管,A错误;
B.除去乙酸乙酯中的乙酸需要加饱和碳酸钠分液,主要仪器为分液漏斗和烧杯,B正确;
C.除去氯化钠固体中的硝酸钾杂质需要蒸发浓缩,趁热过滤,主要仪器有蒸发皿、玻璃棒、漏斗、烧杯,不需要温度计,C错误;
D.含水酒精与生石灰制备无水乙醇需要酒精灯、蒸馏烧瓶、温度计、直形冷凝管,牛角管、锥形瓶,不用球形冷凝管,D错误;
故选B。
14.AC
【详解】A.分子式为C10H18O,A错误;
B.从结构可以看出,薰衣草醇含有羟基,B正确;
C.含有碳碳双键和,能使酸性高锰酸钾溶液褪色,C错误;
D.结构中含,与羟基直接相连的碳原子上有两个氢原子,能被催化氧化生成醛,D正确;
故选AC。
15.BD
【详解】A.分子式为,A正确;
B.在水溶液中羧基能电离出,羟基不能电离出,B错误;
C.羟基和羧基均能与Na反应,1mol该物质最多能与4molNa发生反应,C正确;
D.该物质碳氧双键和碳碳双键均为平面构型,最多5个碳原子共平面:,D错误;
故选BD。
16.(1) 将温度迅速升高到170℃
(2) 过度冷却,产品1,2-二溴乙烷在装置d中凝固 防止倒吸
(3)吸收乙烯气体中含有的CO2、SO2等酸性气体
(4) 乙醇挥发 乙烯流速过快,未完全发生加成反应
(5)4
(6)2,3-二甲基戊烷
【分析】制备1,2-二溴乙烷,由实验装置可知,分液漏斗和烧瓶a中分别装有浓和无水乙醇,加热时发生,b可防止倒吸,且可吸收乙醇,c中NaOH溶液可除去乙烯中的酸性物质,d中发生CH2=CH2+Br2→CH2BrCH2Br,由信息可知,冷水冷却后试管中无色液体为1,2-二溴乙烷,e可吸收尾气中的溴。
【详解】(1)装置a中为乙醇在浓硫酸条件下反应生成乙烯,方程式为:;因为乙醇加热到140℃时可以反应生成乙醚,所以为了防止副反应发生,实验中具体操作为:将温度迅速升高到170℃;
(2)装置d中发生堵塞,可能是因为过度冷却,产品1,2-二溴乙烷在装置d中凝固;后面的液体可能倒吸到安全瓶b中,但不可能倒吸回反应装置中,所以可以防止倒吸;
(3)氢氧化钠能吸收CO2或SO2等酸性气体,故其作用为:吸收乙烯气体中含有的CO2、SO2等酸性气体;
(4)反应过程中浓硫酸具有强氧化性,可能将部分乙醇氧化;或因为温度控制不当,发生副反应生成乙醚;或因为乙醇挥发造成产物量减少;或因为乙烯流速过快,未完全发生加成反应;
(5)与Br2发生加成反应,可能得到、、、四种产物;
(6)最长碳链为主链,从离支链近的一端开始编号,如图:,该物质名称为:2,3-二甲基戊烷。
17.(1)羟基
(2)CH3CH2OH
(3) 加成反应 酯化反应或(取代反应)
(4)2CH3CH2OH+O22CH3CHO+2H2O
(5)nCH2=CH2
(6)BCD
(7) 饱和碳酸钠溶液 导气管的出口伸入到了液面以下
【分析】乙烯和水发生加成反应生成乙醇,D是CH3CH2OH;乙醇发生催化氧化生成乙醛,乙醛氧化为乙酸,E是CH3COOH,乙醇和乙酸发生酯化反应生成乙酸乙酯,G是CH3COOCH2CH3;乙烯发生加聚反应生成高分子化合物聚乙烯,F是聚乙烯。
【详解】(1)根据物质B的结构简式,可知所含官能团的名称为羟基;
(2)乙烯和水发生加成反应生成乙醇,D是CH3CH2OH;
(3)反应①是乙烯和溴发生加成反应生成1,2-二溴乙烷,反应类型是加成反应;⑥是乙醇和乙酸发生酯化反应生成乙酸乙酯和水,反应类型是取代反应(酯化反应);
(4)反应④是乙醇发生催化氧化生成乙醛和水,反应的化学方程式为2CH3CH2OH+O22CH3CHO+2H2O;
(5)反应⑦是乙烯发生加聚反应生成高分子化合物聚乙烯,反应的化学方程式为nCH2=CH2
(6)A. 乙烯难溶于水,故A错误;
B. CH2=CH2是平面结构的分子,6个原子共平面,故B正确;
C. CH2=CH2含有碳碳双键,能被高锰酸钾氧化,故C正确;
D. CH2=CH2含有碳碳双键,在一定条件下能发生加聚反应生成聚乙烯,故D正确;
选BCD。
(7)饱和碳酸钠溶液能降低乙酸乙酯的溶解度,溶解乙醇,中和乙酸,乙收集乙酸乙酯,所盛的试剂为饱和碳酸钠溶液,为防止倒吸,导气管的出口应在液面以上,该装置图中有一个明显的错误是导气管的出口伸入到了液面以下。
18.(1) 羟基 羧基
(2)CH3OCH3
(3)
(4) 氧化反应
(5) 饱和Na2CO3溶液 反应乙酸,降低乙酸乙酯的溶解度
【分析】A是分子量为28的气体烯烃,其产量是衡量一个国家石油化工生产水平的标志,所以A为乙烯CH2=CH2,A与水发生加成反应生成的B为CH3CH2OH,B被催化氧化生成C为CH3CHO;D是食醋的主要成分,所以D为CH3COOH,D与B发生酯化反应生成E为CH3COOCH2CH3,乙酸乙酯的对分子质量为88,CH3CHO的相对分子质量为44,E相对分子质量是C的2倍符合题意,F为一种高分子化合物,应为乙烯发生聚合反应生成的聚乙烯,据此回答。
【详解】(1)B为CH3CH2OH,其官能团为羟基;D为CH3COOH,其官能团为羧基;故答案为:羟基;羧基;
(2)与B互为同分异构体物质为二甲醚,结构简式为CH3OCH3;故答案为:CH3OCH3;
(3)与D互为同系物且为该同系物中最简单的一种物质为甲酸,其结构式为 ;故答案为:;
(4)反应②为乙醇的催化氧化,化学方程式为,反应类型为氧化反应,故答案为:;氧化反应;
(5)乙醇和乙酸的酯化反应中,浓硫酸的作用是做催化剂和吸水剂;乙酸、乙醇、乙酸乙酯均具有挥发性,反应过程中经挥发冷凝后进入试管X中,故X中液体可以溶解乙醇,反应乙酸,能降低乙酸乙酯的溶解度,便于溶液分层,则X中为饱和碳酸钠溶液;故答案为:饱和Na2CO3溶液;通过反应吸收乙酸,降低乙酸乙酯的溶解度。
19.(1) 加成反应 羧基
(2)
(3)、
(4) 防止暴沸 饱和溶液
【分析】石蜡在加热条件下反应生成A,A的产量是衡量一个国家石油化工产业发展水平的标志,A为CH2=CH2,A和水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C发生氧化反应生成D为CH3COOH,B和D发生酯化反应生成E为CH3COOCH2CH3。
【详解】(1)A和水发生加成反应生成B,D为CH3COOH,D中官能团的名称为羧基;
(2)B发生催化氧化生成C为CH3CHO,化学方程式为;
(3)石蜡的分解不仅可获得A,还可以得到一种相对分子质量为86的烷烃,该烷烃分子中碳原子个数为写出该烷烃主链碳原子数为=6,主链上有4个碳原子的同分异构体为(、;
(4)①甲中反应的化学方程式为;
②试管甲中使用碎瓷片的目的是防暴沸,试管乙中的试剂F为饱和溶液,其作用是吸收乙酸、溶解乙醇、降低乙酸乙酯的溶解度。
20.(1)甲基苯酚(或4-甲基苯酚)
(2) (酚)羟基、羰基(或酮羰基或酮基) 加成反应 取代反应
(3)NaOH溶液、AgNO3溶液
(4)n
(5)
(6)CH3CH2CH(OH)COCl+
【分析】
结合反应②的反应条件、A的分子式以及B的结构简式可得A的结构简式为,结合A的结构简式、X的分子式以及反条件可得X的结构简式为,则X的名称为对甲基苯酚或者4-甲基苯酚;B与浓盐酸在加热条件下发生取代反应生成C(),C与NaCN在一定条件下发生取代反应生成D;结合已知①和D的结构简式可得E的结构简式为,E在酸性条件下水解为F;F在一定条件下反应生成Y;据此分析。
【详解】(1)由分析可知,X的名称为对甲基苯酚或者4-甲基苯酚;
(2)A的结构简式为,则A中的含氧官能团的名称为(酚)羟基、羰基(或酮羰基或酮基);反应②为酚与醛的加成反应,反应④为卤原子的取代反应;
(3)C的结构简式为,想要检验其中的氯原子,应先将C水解加入氢氧化钠水溶液,硝酸酸化后加入硝酸银溶液,若有白色沉淀,则证明为氯原子;
(4)F中含有碳碳双键,能发生加聚反应,方程式为n;
(5)D的不饱和度为7,根据题意,可知G的分子式为C9H7NO2,则符合①结构中含有,只有1个苯环,无其他环状结构;②核磁共振氢谱中有4组吸收峰,且峰面积之比为2:2:2:1的结构的G的结构简式为;
(6)合成路线需要用到信息①及F到Y的成环反应;CH3CH2CH(OH)COCl与反应生成,再经水合氢离子生成,最后在碘单质作用下生成,则路线为:CH3CH2CH(OH)COCl+ 。
答案第1页,共2页
答案第1页,共2页
姓名()班级()学号()
一、单选题
1.下列有机反应既不属于加成反应也不属于取代反应的是
A.CH2=CH2+H2OCH3CH2OH
B.CH4+Cl2CH3Cl+HCl
C.2CH3CH2OH+O22CH3CHO+2H2O
D.CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
2.下列有关化学用语表示正确的是
A.氮气的电子式: B.的空间填充模型:
C.乙醇的结构式: D.K的原子结构示意图:
3.下列反应中,属于取代反应的是
A.CH2=CH2+HClCH3CH2Cl
B.2CH3CH2OH+O22CH3CHO+2H2O
C.+H2CH3CH2OH
D.CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
4.2021年,我国科学家利用为原料人工合成淀粉,在未来具有极高的经济价值。已知合成淀粉过程中发生反应:,设为阿伏加德罗常数,下列有关说法正确的是。
A.17 g H2O2中含有过氧键数目为0.5 NA B.标况下,22.4 L CH3OH中含有的羟基数为NA
C.18 g D2O中含有氧原子的数目为1 NA D.1 mol O2参与反应转移电子数为4 NA
5.关于实验室制备、分离乙酸乙酯的装置,说法正确的是
A.图甲用于分离乙酸乙酯
B.乙用于蒸馏纯化乙酸乙酯
C.图丙可从分液漏斗下端放出乙酸乙酯
D.图丁用于制备并收集乙酸乙酯
6.利用柠檬真菌青霉生成的前体,可生产对降低胆固醇有积极作用的他汀类药物,某种他汀类药物M的结构如图。下列关于M的说法正确的是
A.分子中所有碳原子可能共平面
B.通过酯化反应可能获得该分子
C.不存在含苯环结构的同分异构体
D.1molM最多消耗4mol氢气
7.下列说法正确的是
A.含有相同官能团的物质其化学性质全部相同
B.含有的物质不是醛就是酮
C.两种某物质具有相同的化学性质则一定含有相同的官能团
D.含有的物质一定能与在一定条件下发生加成反应
8.化学是一门以实验为基础的学科。下列实验操作能达到目的的是
选项 目的 实验操作
A 验证SO2的漂白性 将SO2气体通入紫色石蕊溶液中
B 制备Fe(OH)3胶体 向沸水中逐滴加入FeCl3饱和溶液继续煮沸至液体呈红褐色
C 检验乙醇中是否有水 向乙醇中加入一小粒金属钠
D 除去Cu粉中混有的CuO 加入稀硝酸溶解,过滤、洗涤、干燥
A.A B.B C.C D.D
9.橙花醇的结构简式如图,根据乙烯和乙醇的有关性质,下列有关橙花醇的说法不正确的是
A.分子式为C10H18O
B.能发生取代反应、加成反应
C.所有的C原子有可能共平面
D.能用酸性高锰酸钾溶液检验其中是否含有碳碳双键
10.设NA为阿伏加德罗常数的值。下列叙述正确的是
A.3.2gS与足量O2在点燃条件下充分反应,转移的电子数为0.6NA
B.1L0.1 mol L-1的乙酸溶液中含有的氧原子数为0.2NA
C.标准状况下,11.2LC3H8中含有C-C键的数目为NA
D.0.2mol硝酸与足量铜反应转移电子数为0.1NA
11.将两块相同的钠分别投入等量的乙醇和水中,下列说法错误的是
A.与甲相比,乙中钠块很快熔化成光亮的小球
B.钠块沉在乙醇液面下,说明乙醇的密度比钠小
C.乙比甲反应缓和,说明乙醇羟基中的氢原子不如水分子中的氢原子活泼
D.触摸甲、乙烧杯外壁均发热,说明两个反应均放热
12.乙酸、乙醇是生活中常见的有机物。下列说法正确的是
A.乙醇和乙酸的官能团相同
B.与足量乙酸反应,生成
C.两者都能与溶液反应
D.一定条件下,乙醇可以被氧化成乙酸
13.为完成下列实验,部分仪器选择正确的是
A.乙醇制乙烯:①②③⑥
B.除去乙酸乙酯中的乙酸:③⑦
C.除去氯化钠固体中的硝酸钾杂质:⑤⑦⑧⑨
D.含水酒精与生石灰制备无水乙醇:①②④
二、多选题
14.薰衣草醇的分子结构如图所示,下列有关薰衣草醇的说法不正确的是
A.分子式为C10H20O B.含有羟基官能团
C.不能使酸性高锰酸钾溶液褪色 D.能被O2氧化为醛
15.某有机物的结构简式如图,下列关于该有机物的说法不正确的是
A.分子式为
B.在水溶液中羧基和羟基均能电离出
C.1mol该物质最多能与4molNa发生反应
D.分子中最多有7个碳原子共平面
三、解答题
16.1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装置图,图中分液漏斗和烧瓶a中分别装有浓和无水乙醇,d装置试管中装有液溴。
相关数据列表如表:
乙醇 1,2-二溴乙烷 乙醚 溴
状态 无色液体 无色液体 无色液体 红棕色液体
密度/ 0.79 2.18 0.71 3.10
沸点/℃ 78.5 131.4 34.6 58.8
熔点/℃ 9.79
水溶性 混溶 难溶 微溶 可溶
(1)装置a中发生主要反应的方程式为: 。为防止副反应发生,实验中的具体操作为: 。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装置中导管是否发生堵塞,如果实验时d装置中导管堵塞,你认为可能的原因: ;安全瓶b还可以起到的作用是: 。
(3)容器c、e中都盛有溶液,c中溶液的作用是 。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比理论值超过许多,如果装置的气密性没有问题,试分析可能的原因: 、 (写出两条即可)。
(5)与溴发生加成反应,可以得到 种有机产物。
(6)用系统法命名:
17.乙烯是重要有机化工原料。结合以下路线回答:
已知: ;其中F为高分子化合物
(1)物质B所含官能团的名称为 ;
(2)D的结构简式为 ;
(3)反应①、⑥所涉及的反应类型是 、 ;
(4)写出反应④的化学方程式为 ;
(5)写出反应⑦的化学方程式为 ;
(6)关于CH2=CH2的说法正确的是___________;
A.易溶于水 B.是平面结构的分子
C.能被高锰酸钾氧化 D.在一定条件下能发生加聚反应
(7)在实验室里可以用如图所示的装置来制取G,乙中所盛的试剂为 ,该装置图中有一个明显的错误是 。
18.根据如图,已知有机物有以下转化关系。A是分子量为28的气体烯烃,其产量是衡量一个国家石油化工生产水平的标志;D是食醋的主要成分,E是不溶于水且具有香味的无色液体,相对分子质量是C的2倍,F是一种高分子化合物。结合如图关系回答问题:
(1)写出中官能团的名称:B 、D ;
(2)写出与B互为同分异构体物质的结构简式 ;
(3)写出与D互为同系物且为该同系物中最简单的一种物质的结构式 。
(4)写出反应②的化学方程式: 。该反应类型是 。
(5)在浓硫酸的作用下实现反应④,实验装置如下图所示,试管1中装入药品后加热。图中X的化学式为 ,其作用是溶解乙醇和 。
19.有机物A~E之间存在如下图所示的转化关系。A的产量是衡量一个国家石油化工产业发展水平的标志。
请回答下列问题:
(1)A→B的化学反应类型为 ,D中官能团的名称为 。
(2)B→C的化学方程式为
(3)石蜡的分解不仅可获得A,还可以得到一种相对分子质量为86的烷烃。写出该烷烃主链碳原子数为4的一种同分异构体的结构简式 。
(4)某化学兴趣小组在实验室利用如图所示装置实现B和D制备E的反应。
①写出甲中反应的化学方程式 。
②试管甲中使用碎瓷片的目的是 ,试管乙中的试剂F为 。
20.有机化合物Y有抗菌作用,也是一种医药中间体,由X合成Y的路线图如下:
已知:① +HCl
②
③
请回答下列问题:
(1)根据系统命名法,X的名称为 。
(2)A中的含氧官能团的名称为 ,②和④的反应类型分别为 。
(3)检验C中官能团Cl所用试剂有稀HNO3和 。
(4)F在一定条件下,能发生加聚反应,其反应方程式为 。
(5)G是比D少2个“-CH2-”的同分异构体,同时满足下列条件的G的结构为 (不考虑立体异构)。
①结构中含有,只有1个苯环,无其他环状结构。
②核磁共振氢谱中有4组吸收峰,且峰面积之比为2:2:2:1。
(6)参照上述合成路线和信息,以CH3CH2CH(OH)COC1和有机物X为原料(无机试剂任选),设计制备的合成路线 。
第1页 共4页 ◎ 第2页 共4页
第1页 共4页 ◎ 第2页 共4页
参考答案:
1.C
【详解】A. CH2=CH2+H2OCH3CH2OH,属于加成反应,A不选;
B .CH4+Cl2CH3Cl+HCl,属于取代反应,B不选;
C.2CH3CH2OH+O22CH3CHO+2H2O,属于氧化反应,C选;
D .CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O,属于取代反应,D不选;
故选C。
2.B
【详解】A.氮气分子中,两个氮原子间共用3对电子,每个N都达到8电子稳定结构,其电子式是,A项错误;
B.甲烷分子由1个C和4个H构成,的空间填充模型:,B项正确;
C.乙醇的结构式:,C项错误;
D.K为第19号元素,核外电子数为19,其原子结构示意图:,D项错误;
故选B。
3.D
【详解】A.CH2=CH2与HCl反应生成氯乙烷属于加成反应,故A错误;
B.乙醇催化氧化生成乙醛属于氧化反应,故B错误;
C.乙醛与氢气发生加成反应生成乙醇,属于加成反应或还原反应,故C错误;
D.乙酸和乙醇生成乙酸乙酯属于酯化反应,酯化反应为取代反应的一种,故D正确;
故选:D。
4.A
【详解】A.已知H2O2分子中存在1个过氧键,则中含有过氧键数目为,A正确;
B.在标况下CH3OH为液态,密度未知,故无法计算22.4 L CH3OH中含有的羟基数目,B错误;
C.D2O摩尔质量为20g/mol,且一个D2O分子中含1个氧原子,故18gD2O中含有氧原子的数目为,C错误;
D.由反应方程式可知,O2中的O由0价转化到H2O2中的-1价,则参与反应转移电子数为2NA,D错误;
故答案为:A。
5.D
【详解】A.乙酸乙酯中混有乙酸、乙醇,成为液体混合物,图甲用于分离固液混合物,不能用于分离液体混合物中的乙酸乙酯,A不正确;
B.蒸馏操作时,温度计水银球应位于支管口处,不能插入液体中,B不正确;
C.乙酸乙酯密度比水中,浮在水面上,应从分液漏斗上口倒出,C不正确;
D.图丁装置中,反应试管中插入玻璃管,使得试管内外相通,不会产生压强差,能够起到防止倒吸的作用,导管插入碳酸钠溶液中,杂质能与碳酸钠溶液充分接触和反应,有利于杂质的吸收,因此能较好地制备并收集乙酸乙酯,D正确;
故选D。
6.B
【分析】该有机物中含有酯基、碳碳双键、羟基3种官能团,且含有结构“”,则所有碳原子不可能共平面,M的不饱和度大于4,存在含苯环结构的同分异构体,据此回答。
【详解】A.M的分子中含有结构“”,故所有碳原子不可能共平面,A错误;
B.M的结构中含有酯基,酯化反应可引入酯基,B正确;
C.M的不饱和度大于4,存在含苯环结构的同分异构体,C错误;
D.M中的碳碳双键可以与氢气发生加成反应,所以1molM最多消耗2mol氢气,D错误。
故选B。
7.D
【详解】A.有机物的化学性质是通过官能团体现出来的,含有相同的官能团说明具有相似的化学性质,但化学性质不完全相同,故A错误;
B.含有羰基的物质可能是醛、铜或者羧酸、酯、酰胺等,故B错误;
C.某两种物质具有相同的化学性质,不一定含有相同的官能团,如碳碳双键和碳碳三键均可以发生加成反应、加聚反应、氧化反应等,但却是不同的官能团,故C错误;
D.碳碳双键在一定条件下,可以和氢气发生加成反应,故D正确;
故选D。
8.B
【详解】A.验证SO2的漂白性,应将SO2气体通入品红溶液中,而不是通入紫色石蕊溶液中,A不符合题意;
B.向沸水中逐滴加入FeCl3饱和溶液继续煮沸以促进Fe3+水解至液体呈红褐色,可制备Fe(OH)3胶体,B符合题意;
C.向乙醇中加入一小粒金属钠,钠与乙醇也会反应放出无色气泡(H2),会干扰钠与水的反应,则不能检验乙醇中是否有水,C不符合题意;
D.Cu、CuO均可以与稀硝酸反应,导致Cu粉也被溶解,不符合除杂原则,D不符合题意;
故选B。
9.D
【分析】该有机物含有碳碳双键、羟基,能发生取代反应、加成反应,能使高锰酸钾溶液褪色,据此回答。
【详解】A.根据结构式可知,该有机物的分子式为C10H18O,A正确;
B.含有碳碳双键、羟基,能发生取代反应、加成反应,B正确;
C.由于单键可以旋转,所有的C原子有可能共平面,C正确;
D.碳碳双键、羟基都能使高锰酸钾溶液褪色,不能用酸性高锰酸钾溶液检验其中是否含有碳碳双键,D错误;
故选D。
10.C
【详解】A.3.2gS与足量O2在点燃条件下充分反应,生成0.1molSO2,转移的电子数为0.4NA,A不正确;
B.1L0.1 mol L-1的乙酸溶液中,除乙酸中含有0.2molO原子外,水中也含有O原子,则含有的氧原子数大于0.2NA,B不正确;
C. 1个C3H8分子中含有2个C-C键,标准状况下,11.2LC3H8(物质的量为0.5mol)含有C-C键的数目为0.5mol×2×NAmol-1= NA,C正确;
D.0.2mol硝酸与足量铜反应,若只发生转化4HNO3(浓)——2NO2,则转移电子0.1mol,若只发生转化8HNO3(稀)——2NO,则转移电子0.15mol,随着反应的进行,既便起初是浓硝酸,也会转化为稀硝酸,所以转移电子数不是0.1NA,D不正确;
故选C。
11.A
【详解】A.Na的密度比乙醇的密度大,乙中Na沉在底部,且钠的熔点比乙醇的沸点高,钠在乙醇中反应不会熔化成小球,A项错误;
B.Na的密度比乙醇的密度大,故钠块沉在乙醇液面下,B项正确;
C.乙醇羟基中的氢原子不如水分子中的氢原子活泼,故Na与乙醇反应比Na与水反应缓和得多,C项正确;
D.触摸甲、乙烧杯外壁均发热,说明Na与水和乙醇的反应均放热,D项正确;
答案选A。
12.D
【详解】A.乙醇和乙酸的官能团分别为羟基、羧基,则官能团不相同,A错误;
B.C2H5OH与乙酸的酯化反应是可逆反应,不能完全转化,则1molC2H5OH与足量乙酸反应,生成CH3COOC2H5的物质的量小于1mol,B错误;
C.乙酸能与NaOH溶液反应,乙醇不能与NaOH溶液反应,C错误;
D.乙醇可以被酸性KMnO4溶液或酸性K2Cr2O7溶液氧化成乙酸,D正确;
故选D。
13.B
【详解】A.乙醇在170、浓硫酸作用下发生消去反应制备乙烯,主仪器有酒精灯、温度计、圆底烧瓶或者蒸馏烧瓶,不需要锥形瓶,不需要酸式滴定管,A错误;
B.除去乙酸乙酯中的乙酸需要加饱和碳酸钠分液,主要仪器为分液漏斗和烧杯,B正确;
C.除去氯化钠固体中的硝酸钾杂质需要蒸发浓缩,趁热过滤,主要仪器有蒸发皿、玻璃棒、漏斗、烧杯,不需要温度计,C错误;
D.含水酒精与生石灰制备无水乙醇需要酒精灯、蒸馏烧瓶、温度计、直形冷凝管,牛角管、锥形瓶,不用球形冷凝管,D错误;
故选B。
14.AC
【详解】A.分子式为C10H18O,A错误;
B.从结构可以看出,薰衣草醇含有羟基,B正确;
C.含有碳碳双键和,能使酸性高锰酸钾溶液褪色,C错误;
D.结构中含,与羟基直接相连的碳原子上有两个氢原子,能被催化氧化生成醛,D正确;
故选AC。
15.BD
【详解】A.分子式为,A正确;
B.在水溶液中羧基能电离出,羟基不能电离出,B错误;
C.羟基和羧基均能与Na反应,1mol该物质最多能与4molNa发生反应,C正确;
D.该物质碳氧双键和碳碳双键均为平面构型,最多5个碳原子共平面:,D错误;
故选BD。
16.(1) 将温度迅速升高到170℃
(2) 过度冷却,产品1,2-二溴乙烷在装置d中凝固 防止倒吸
(3)吸收乙烯气体中含有的CO2、SO2等酸性气体
(4) 乙醇挥发 乙烯流速过快,未完全发生加成反应
(5)4
(6)2,3-二甲基戊烷
【分析】制备1,2-二溴乙烷,由实验装置可知,分液漏斗和烧瓶a中分别装有浓和无水乙醇,加热时发生,b可防止倒吸,且可吸收乙醇,c中NaOH溶液可除去乙烯中的酸性物质,d中发生CH2=CH2+Br2→CH2BrCH2Br,由信息可知,冷水冷却后试管中无色液体为1,2-二溴乙烷,e可吸收尾气中的溴。
【详解】(1)装置a中为乙醇在浓硫酸条件下反应生成乙烯,方程式为:;因为乙醇加热到140℃时可以反应生成乙醚,所以为了防止副反应发生,实验中具体操作为:将温度迅速升高到170℃;
(2)装置d中发生堵塞,可能是因为过度冷却,产品1,2-二溴乙烷在装置d中凝固;后面的液体可能倒吸到安全瓶b中,但不可能倒吸回反应装置中,所以可以防止倒吸;
(3)氢氧化钠能吸收CO2或SO2等酸性气体,故其作用为:吸收乙烯气体中含有的CO2、SO2等酸性气体;
(4)反应过程中浓硫酸具有强氧化性,可能将部分乙醇氧化;或因为温度控制不当,发生副反应生成乙醚;或因为乙醇挥发造成产物量减少;或因为乙烯流速过快,未完全发生加成反应;
(5)与Br2发生加成反应,可能得到、、、四种产物;
(6)最长碳链为主链,从离支链近的一端开始编号,如图:,该物质名称为:2,3-二甲基戊烷。
17.(1)羟基
(2)CH3CH2OH
(3) 加成反应 酯化反应或(取代反应)
(4)2CH3CH2OH+O22CH3CHO+2H2O
(5)nCH2=CH2
(6)BCD
(7) 饱和碳酸钠溶液 导气管的出口伸入到了液面以下
【分析】乙烯和水发生加成反应生成乙醇,D是CH3CH2OH;乙醇发生催化氧化生成乙醛,乙醛氧化为乙酸,E是CH3COOH,乙醇和乙酸发生酯化反应生成乙酸乙酯,G是CH3COOCH2CH3;乙烯发生加聚反应生成高分子化合物聚乙烯,F是聚乙烯。
【详解】(1)根据物质B的结构简式,可知所含官能团的名称为羟基;
(2)乙烯和水发生加成反应生成乙醇,D是CH3CH2OH;
(3)反应①是乙烯和溴发生加成反应生成1,2-二溴乙烷,反应类型是加成反应;⑥是乙醇和乙酸发生酯化反应生成乙酸乙酯和水,反应类型是取代反应(酯化反应);
(4)反应④是乙醇发生催化氧化生成乙醛和水,反应的化学方程式为2CH3CH2OH+O22CH3CHO+2H2O;
(5)反应⑦是乙烯发生加聚反应生成高分子化合物聚乙烯,反应的化学方程式为nCH2=CH2
(6)A. 乙烯难溶于水,故A错误;
B. CH2=CH2是平面结构的分子,6个原子共平面,故B正确;
C. CH2=CH2含有碳碳双键,能被高锰酸钾氧化,故C正确;
D. CH2=CH2含有碳碳双键,在一定条件下能发生加聚反应生成聚乙烯,故D正确;
选BCD。
(7)饱和碳酸钠溶液能降低乙酸乙酯的溶解度,溶解乙醇,中和乙酸,乙收集乙酸乙酯,所盛的试剂为饱和碳酸钠溶液,为防止倒吸,导气管的出口应在液面以上,该装置图中有一个明显的错误是导气管的出口伸入到了液面以下。
18.(1) 羟基 羧基
(2)CH3OCH3
(3)
(4) 氧化反应
(5) 饱和Na2CO3溶液 反应乙酸,降低乙酸乙酯的溶解度
【分析】A是分子量为28的气体烯烃,其产量是衡量一个国家石油化工生产水平的标志,所以A为乙烯CH2=CH2,A与水发生加成反应生成的B为CH3CH2OH,B被催化氧化生成C为CH3CHO;D是食醋的主要成分,所以D为CH3COOH,D与B发生酯化反应生成E为CH3COOCH2CH3,乙酸乙酯的对分子质量为88,CH3CHO的相对分子质量为44,E相对分子质量是C的2倍符合题意,F为一种高分子化合物,应为乙烯发生聚合反应生成的聚乙烯,据此回答。
【详解】(1)B为CH3CH2OH,其官能团为羟基;D为CH3COOH,其官能团为羧基;故答案为:羟基;羧基;
(2)与B互为同分异构体物质为二甲醚,结构简式为CH3OCH3;故答案为:CH3OCH3;
(3)与D互为同系物且为该同系物中最简单的一种物质为甲酸,其结构式为 ;故答案为:;
(4)反应②为乙醇的催化氧化,化学方程式为,反应类型为氧化反应,故答案为:;氧化反应;
(5)乙醇和乙酸的酯化反应中,浓硫酸的作用是做催化剂和吸水剂;乙酸、乙醇、乙酸乙酯均具有挥发性,反应过程中经挥发冷凝后进入试管X中,故X中液体可以溶解乙醇,反应乙酸,能降低乙酸乙酯的溶解度,便于溶液分层,则X中为饱和碳酸钠溶液;故答案为:饱和Na2CO3溶液;通过反应吸收乙酸,降低乙酸乙酯的溶解度。
19.(1) 加成反应 羧基
(2)
(3)、
(4) 防止暴沸 饱和溶液
【分析】石蜡在加热条件下反应生成A,A的产量是衡量一个国家石油化工产业发展水平的标志,A为CH2=CH2,A和水发生加成反应生成B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C发生氧化反应生成D为CH3COOH,B和D发生酯化反应生成E为CH3COOCH2CH3。
【详解】(1)A和水发生加成反应生成B,D为CH3COOH,D中官能团的名称为羧基;
(2)B发生催化氧化生成C为CH3CHO,化学方程式为;
(3)石蜡的分解不仅可获得A,还可以得到一种相对分子质量为86的烷烃,该烷烃分子中碳原子个数为写出该烷烃主链碳原子数为=6,主链上有4个碳原子的同分异构体为(、;
(4)①甲中反应的化学方程式为;
②试管甲中使用碎瓷片的目的是防暴沸,试管乙中的试剂F为饱和溶液,其作用是吸收乙酸、溶解乙醇、降低乙酸乙酯的溶解度。
20.(1)甲基苯酚(或4-甲基苯酚)
(2) (酚)羟基、羰基(或酮羰基或酮基) 加成反应 取代反应
(3)NaOH溶液、AgNO3溶液
(4)n
(5)
(6)CH3CH2CH(OH)COCl+
【分析】
结合反应②的反应条件、A的分子式以及B的结构简式可得A的结构简式为,结合A的结构简式、X的分子式以及反条件可得X的结构简式为,则X的名称为对甲基苯酚或者4-甲基苯酚;B与浓盐酸在加热条件下发生取代反应生成C(),C与NaCN在一定条件下发生取代反应生成D;结合已知①和D的结构简式可得E的结构简式为,E在酸性条件下水解为F;F在一定条件下反应生成Y;据此分析。
【详解】(1)由分析可知,X的名称为对甲基苯酚或者4-甲基苯酚;
(2)A的结构简式为,则A中的含氧官能团的名称为(酚)羟基、羰基(或酮羰基或酮基);反应②为酚与醛的加成反应,反应④为卤原子的取代反应;
(3)C的结构简式为,想要检验其中的氯原子,应先将C水解加入氢氧化钠水溶液,硝酸酸化后加入硝酸银溶液,若有白色沉淀,则证明为氯原子;
(4)F中含有碳碳双键,能发生加聚反应,方程式为n;
(5)D的不饱和度为7,根据题意,可知G的分子式为C9H7NO2,则符合①结构中含有,只有1个苯环,无其他环状结构;②核磁共振氢谱中有4组吸收峰,且峰面积之比为2:2:2:1的结构的G的结构简式为;
(6)合成路线需要用到信息①及F到Y的成环反应;CH3CH2CH(OH)COCl与反应生成,再经水合氢离子生成,最后在碘单质作用下生成,则路线为:CH3CH2CH(OH)COCl+ 。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
