高中化学同步练习:选择性必修三3.4羧酸 羧酸衍生物 (优生加练)
文档属性
| 名称 | 高中化学同步练习:选择性必修三3.4羧酸 羧酸衍生物 (优生加练) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-16 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
高中化学试卷2024年02月29日9
一、选择题
1.下列离子( 或化学)方程式正确的是( )
A.苯酚钠溶液中通入少量二氧化碳: +CO
B.CH3CO18OC2H5在稀硫酸催化下水解:
C.向 Ba(OH)2溶液中加入稀 H2SO4溶液:
D.用已知浓度的 KMnO4溶液滴定草酸:
2.下列关于有机物的说法正确的是( )
A.糖类、油脂、蛋白质在一定条件下均能水解
B.乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物
C.分子式为C4H8Cl2的有机物共有(不含立体异构)8种
D. 处于同一平面上的原子数最多为18个
3.有机物甲的分子式为C7H14O2,在酸性条件下,甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,则甲的可能结构有 ( )
A.4种 B.6种 C.8种 D.10种
4.氢能是一种重要的清洁能源,由HCOOH可以制得。在催化剂作用下,HCOOH分解生成可能的反应机理如图所示。研究发现,其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳。
下列说法正确的是( )
A.HCOOH催化释氢过程中,有非极性键的断裂与形成
B.HCOOD催化释氢反应除生成外,还生成、HD、
C.其他条件不变时,以HCOOK溶液代替HCOOH不能提高释放氢气的纯度
D.HCOOK溶液代替HCOOH时发生反应:
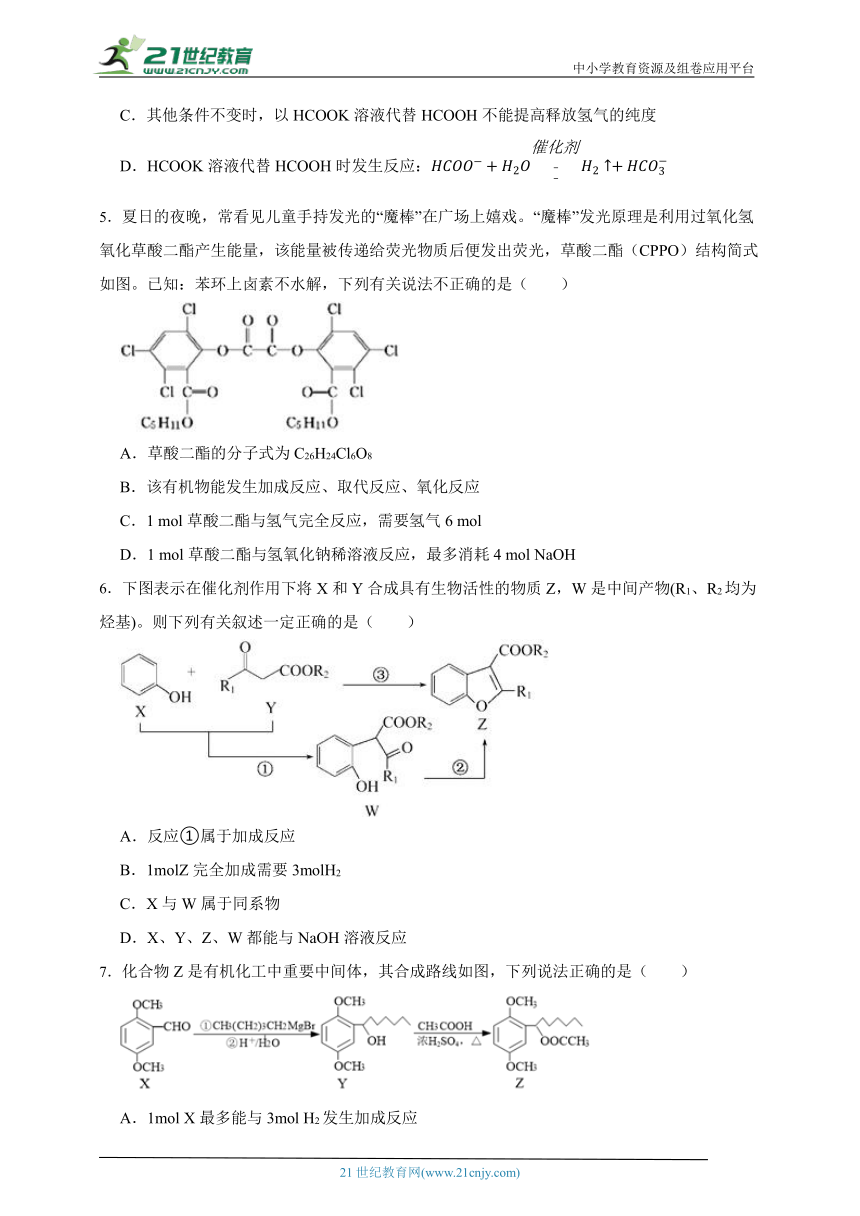
5.夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏。“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图。已知:苯环上卤素不水解,下列有关说法不正确的是( )
A.草酸二酯的分子式为C26H24Cl6O8
B.该有机物能发生加成反应、取代反应、氧化反应
C.1 mol草酸二酯与氢气完全反应,需要氢气6 mol
D.1 mol草酸二酯与氢氧化钠稀溶液反应,最多消耗4 mol NaOH
6.下图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基)。则下列有关叙述一定正确的是( )
A.反应①属于加成反应
B.1molZ完全加成需要3molH2
C.X与W属于同系物
D.X、Y、Z、W都能与NaOH溶液反应
7.化合物Z是有机化工中重要中间体,其合成路线如图,下列说法正确的是( )
A.1mol X最多能与3mol H2发生加成反应
B.可用NaHCO3溶液鉴别反应后Z中是否含有Y
C.可用新制的Cu(OH)2溶液鉴别反应后Z中是否含有X
D.1 mol Z最多可消耗2mol NaOH
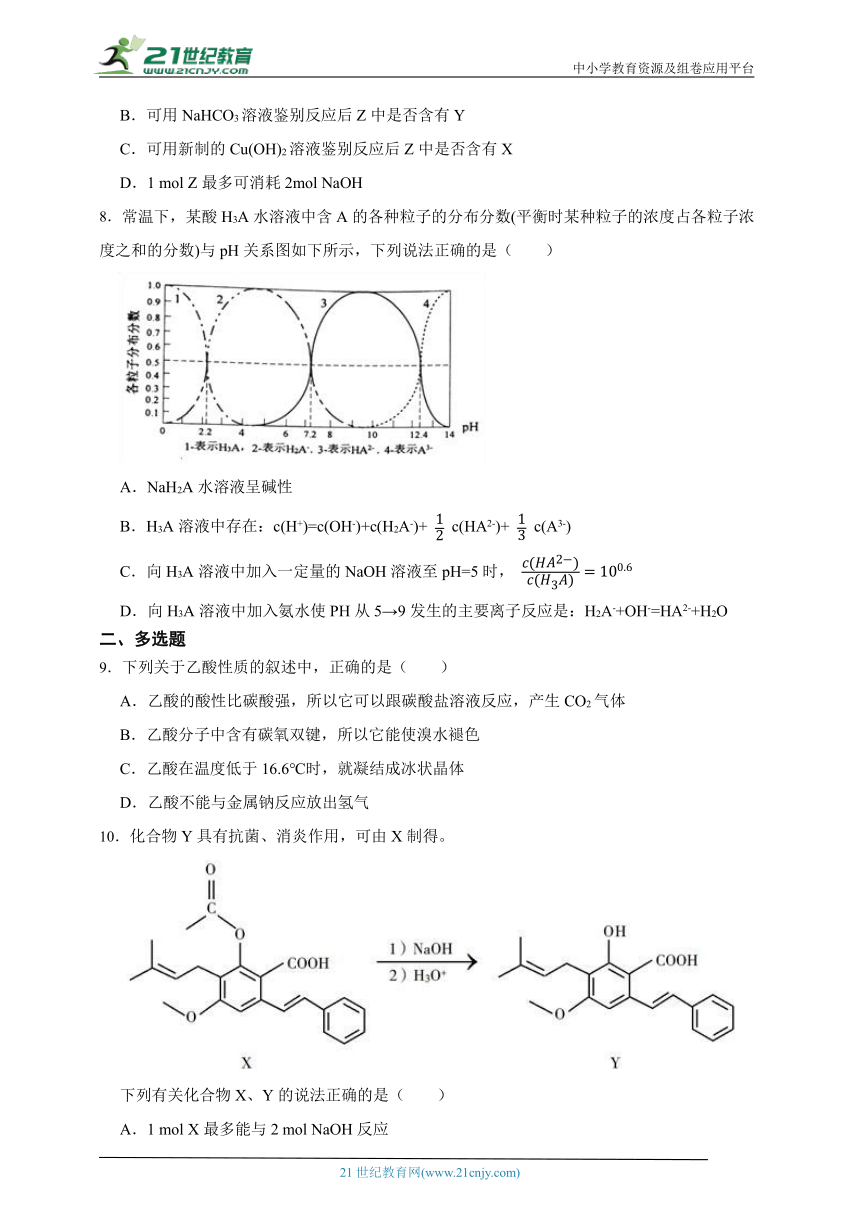
8.常温下,某酸H3A水溶液中含A的各种粒子的分布分数(平衡时某种粒子的浓度占各粒子浓度之和的分数)与pH关系图如下所示,下列说法正确的是( )
A.NaH2A水溶液呈碱性
B.H3A溶液中存在:c(H+)=c(OH-)+c(H2A-)+ c(HA2-)+ c(A3-)
C.向H3A溶液中加入一定量的NaOH溶液至pH=5时,
D.向H3A溶液中加入氨水使PH从5→9发生的主要离子反应是:H2A-+OH-=HA2-+H2O
二、多选题
9.下列关于乙酸性质的叙述中,正确的是( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体
B.乙酸分子中含有碳氧双键,所以它能使溴水褪色
C.乙酸在温度低于16.6℃时,就凝结成冰状晶体
D.乙酸不能与金属钠反应放出氢气
10.化合物Y具有抗菌、消炎作用,可由X制得。
下列有关化合物X、Y的说法正确的是( )
A.1 mol X最多能与2 mol NaOH反应
B.Y与乙醇发生酯化反应可得到X
C.X、Y均能与酸性KMnO4溶液反应
D.室温下X、Y分别与足量Br2加成的产物分子中手性碳原子数目相等
11.有机化合物G是合成抗真菌药物的重要中间体,结构简式如下图。下列说法错误的是( )
A.G的分子式为C11H13O5Cl
B.G分子中含四种官能团
C.G分子含有σ键、π键、大π键、氢键等化学键
D.1molG最多可与3molH2加成,最多与4molNaOH反应
12.在乙醛与氢氧化铜反应生成红色沉淀的实验中,关键操作是( )
A.乙醛要过量 B.CuSO4要过量
C.NaOH要稍微过量 D.氢氧化铜要新制
13.卤代烃R—CH2—CH2—X中的化学键如下图所示,则下列说法正确的是( )
A.当该卤代烃发生水解反应时,被破坏的键是①和②
B.当该卤代烃发生消去反应时,被破坏的键是①和③
C.当该卤代烃发生取代反应时,被破坏的键是①
D.当该卤代烃发生消去反应时,被破坏的键是①和②
14.下列物质中,能发生水解反应,但不能发生消去反应的是( )
A.CH3CH2CH2CH2Cl B.CH3CH2Cl
C.CH3Br D.
15.下列常见的有机反应类型中,能在有机物的分子中引入羟基的是
A.酯化反应 B.取代反应 C.消去反应 D.加成反应
三、非选择题
16.按要求回答下列问题:
(1)写出下列化合物的结构简式:
三乙胺 ; 对甲基苯胺 ;
N,N-二甲基甲酰胺 ;丙烯酰胺 。
(2)按氮原子所连烃基数目分析,环己胺可归为 (填“伯胺”“仲胺”或“叔胺”,下同),三甲胺可归类为 ,二苯胺可归类为 。
(3)苯胺与盐酸反应的化学方程式为 ;甲酰胺在NaOH溶液中水解的化学方程式为 。
17.实验室制备甲基丙烯酸甲酯的反应装置示意图和有关信息如下:
药品 相对分子质量 熔点/℃ 沸点/℃ 溶解性 密度/()
甲醇 32 -98 64.7 与水混溶,易溶于有机溶剂 0.79
甲基丙烯酸 86 15 161 溶于热水,易溶于有机溶剂 1.01
甲基丙烯酸甲酯 100 -48 100 微溶于水,易溶于有机溶剂 0.944
已知甲基丙烯酸甲酯受热易聚合;甲基丙烯酸甲酯在盐溶液中溶解度较小;可与醇结合形成复合物。
实验步骤:
①向烧瓶中依次加入:甲基丙烯酸、2粒沸石、无水甲醇、适量的浓硫酸;
②在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热烧瓶。在反应过程中,通过分水器下部的旋塞放出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中;
③当……..,停止加热;
④冷却后用试剂X洗涤烧瓶中的混合溶液并分离;
⑤取有机层混合液蒸馏,得到较纯净的甲基丙烯酸甲酯。
请回答下列问题:
(1)A装置的名称是 。
(2)请将步骤③填完整: 。
(3)上述实验可能生成的副产物结构简式为 (填两种)。
(4)下列说法错误的是____。
A.在该实验中,浓硫酸的作用之一是作吸水剂,提高了产率
B.酯化反应中若生成的酯的密度比水大,不能用分水器提高反应物的转化率
C.洗涤剂X是一组试剂,产物要依次用饱和、饱和溶液洗涤
D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏
18.烃的含氧衍生物是一类非常重要的有机物。
(1)分子式为C7H16O的饱和一元醇的同分异构体有多种。根据给出的该醇的同分异构体,回答下列问题:
A. B.
C. D.CH3(CH2)5CH2OH
其中,可以发生催化氧化生成酮的是 (填序号)。写出能催化氧化生成醛的化学方程式 。
(2)下列作用不属于水解反应的是_______
A.吃馒头时多咀嚼后有甜味
B.淀粉溶液和稀硫酸共热一段时间后,滴加碘水不显蓝色
C.油脂与氢氧化钠溶液共煮后可以制得肥皂
D.不慎将浓硝酸沾到皮肤上会出现黄色斑痕
(3)请写出能将 转化为 的试剂的化学式 。
(4)共轭二烯烃是含有两个碳碳双键,并且两个双键被一个单键隔开的二烯烃。最简单的共轭二烯烃是1,3-丁二烯。共轭二烯烃比较稳定。共轭二烯烃能以1,4和1,2两种形式发生加成反应,还可发生双烯合成反应(即Diels-Alder反应)等。用于合成橡胶、溶剂,是重要的有机化工原料。
① 与一定量的Br2发生加成反应,生成的产物不可能是 (填序号)。
A. B.
C. D.
②双烯合成反应(即Diels-Alder反应)是一类二烯烃与单烯烃或炔烃作用生成六元环状化合物的反应,例如,最简单的1,3-丁二烯和乙烯的作用表示为: + 。则由1-丁烯和2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物为 。
19.高分子化合物 的合成路线如图:
已知:Ⅰ.
Ⅱ.
回答下列问题:
(1)A的化学名称为 。
(2)由F生成G的反应类型是 。
(3)B→C反应所需试剂,条件分别为 、 。
(4)H的分子式为 。
(5)Ⅰ中官能团的名称是 。
(6)写出一种与F互为同分异构体的酯类芳香族化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为1:2:2:3): 。
(7)分别写出A→B,C→D反应的化学方程式: 、 。
20.3-四氢呋喃甲醇是合成农药呋虫胺的中间体,其一种合成路线如下:
已知:i. R1COOR2+R3OHR1COOR3+R2OH
ii. R1COOR2R1CH2OH+R2OH
iii. R1OH+R2OHR1OR2+H2O
(1)和互为 。的反应类型是 反应。
(2)的分子式 。
(3)不宜选用银氨溶液或新制氢氧化铜的原因是: 。
(4)的结构简式为: 。
(5)3-四氢呋喃甲醇有多种同分异构体,写出1种符合下列条件的有机物的结构简式: 。
①不能与金属钠反应 ②分子中有3种不同化学环境的氢原子
(6)时会生成分子式为的副产物,该副产物的结构简式是 。
(7)已知具有极强还原性,除了还原酯基外(信息ii),还可还原醛基等。请以为原料,利用题中信息及所学知识,选用必要的无机试剂合成。
(合成路线的表示方式为:甲乙……目标产物)
21.某芳香烃A(相对分子质量为78)是一种重要的有机化工原料,以它为初始原料经过如下转化关系图(部分产物和反应条件略去)可以合成阿司匹林(乙酰水杨酸).
已知:Ⅰ.(X为Cl或Br)
Ⅱ.
回答下列问题:
(1)条件X是 ;反应⑤的反应类型是 .
(2)水杨酸中官能团的名称是 .
(3)阿司匹林与足量溶液反应的化学方程式为 .
(4)阿司匹林有多种同分异构体,满足下列条件的同分异构体有 种;其中核磁共振氢谱有四组峰,且峰面积之比为的结构简式为 .
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③该有机物能与完全反应.
22.某化学兴趣小组进行了下列关于氯化铵的课外实验:
(实验操作)
浸过氯化钠溶液的布条很快烧光,浸过氯化铵溶液的布条不燃烧,冒出白烟。
(1)氯化铵饱和溶液中离子浓度由大到小的顺序是 。白烟的成分是 。
(2)请推测浸过氯化铵溶液的布条不燃烧、不易着火的主要原因(写出一条即可) 。
23.按要求写出下列反应方程式(请注明反应条件),并按要求填空
(1)实验室制备乙烯 ,反应类型是 .
(2)乙酸与乙醇的反应 ,反应的无机产物中氧元素的来源是 。
(3)溴乙烷与氢氧化钠水溶液共热 ,此反应将卤代烃类物质转化为 类物质.
(4)苯与浓硫酸、浓硝酸的混合酸在加热时发生反应 ,反应类型是 .
答案解析部分
1.【答案】B
【知识点】苯酚的性质及用途;酯的性质;离子方程式的书写
【解析】【解答】A、由于酸性:H2CO3>苯酚>HCO3-,因此CO2与苯酚钠溶液反应生成苯酚和NaHCO3,该反应的离子方程式为:+H2O+CO2→+HCO3-,A不符合题意。
B、CH3CO18OC2H5在酸性条件下发生水解反应,断裂酯基中的C-O,反应生成CH3COOH和C2H518OH,B符合题意。
C、Ba(OH)2溶液与稀硫酸反应生成BaSO4和H2O,该反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,C不符合题意。
D、KMnO4溶液具有氧化性,H2C2O4中碳元素为+3价,具有还原性,二者可发生氧化还原反应,该反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,D不符合题意。
故答案为:B
【分析】A、苯酚的酸性强于HCO3-,因此反应生成HCO3-,不生成CO32-。
B、酯基水解过程中断裂C-O键。
C、Ba(OH)2与H2SO4反应生成BaSO4和H2O。
D、KMnO4具有氧化性,能将H2C2O4氧化成CO2,自身还原为Mn2+。
2.【答案】B
【知识点】同分异构现象和同分异构体;苯的同系物及其性质;乙醇的化学性质;水解反应
【解析】【解答】A.油脂、蛋白质在一定条件下均能水解,但糖类中的单糖如葡萄糖不水解,故A不符合题意;
B.乙二醇可通过缩聚生成高分子化合物,苯乙烯可通过加聚生成高分子化合物,故B符合题意;
C.C4H8Cl2的同分异构体可以采取“定一移二”法 ,由图可知C4H8Cl2共有9种同分异构体,故C不符合题意;
D.该有机物中含有苯环、碳碳双键、碳碳三键、甲基,甲基中C原子处于乙烯和乙炔中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在乙烯或乙炔的平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故D不符合题意;
故答案为:B。
【分析】该题的难点是有机物共线、共面判断,解答该类试题的判断技巧:①甲烷、乙烯、乙炔、苯、甲醛5种分子中的H原子若被其他原子如
C、O、Cl、N等取代,则取代后的分子空间构型基本不变。②借助C—C键可以旋转而—C≡C—键、 键不能旋转以及立体几何知识判断。③苯分子中苯环可以以任一碳氢键为轴旋转,每个苯分子有三个旋转轴,轴上有四个原子共线。
3.【答案】A
【知识点】同分异构现象和同分异构体;酯的性质
【解析】【解答】在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,这说明二者的相对分子质量是相等的。甲属于酯类,水解生成羧酸和醇。根据质量守恒定律可知,乙和丙的相对分子质量是(130+18)÷2=74,所以饱和一元羧酸CnH2n+1COOH和饱和一元醇的通式CmH2m+2O可知,羧酸是丙酸,醇是丁醇。由于丙酸只有一种,而丁醇有4种,所以甲的结构简式就有4种,答案选A。
【分析】该题的关键是根据阿伏加德罗定律得出乙和丙的相对分子质量相等。然后根据质量守恒定律得出各种的羧酸和醇,最后再分析即可。该属于中等难度的试题。
4.【答案】D
【知识点】极性键和非极性键;催化剂;乙酸的化学性质
【解析】【解答】A.在催化剂作用下,HCOOH分解生成CO2和H2,转化涉及到N-H键的断裂和形成、O-H键的断裂以及H-H键的形成,没有非极性键的断裂,A不符合题意;
B.若用HCOOD代替HCOOH,反应为HCOOD分解,除生成CO2外,还生成HD,无H2 、D2,B不符合题意;
C.若用HCOOK溶液代替HCOOH,HCOOK分解生成CO2和KH,KH与水反应生成KOH和H2,KOH能吸收CO2,CO2的量会减少,能提高释放氢气的纯度,C不符合题意;
D.若用HCOOK溶液代替HCOOH,生成的KOH能吸收CO2转变为HCO3- ,离子反应为 ,D符合题意;
故答案为:D
【分析】A.在催化剂作用下,HCOOH分解生成CO2和H2;
B.若用HCOOD代替HCOOH,反应为HCOOD分解,除生成CO2外,还生成HD,无H2 、D2;
C.KOH能吸收CO2,CO2的量会减少,能提高释放氢气的纯度;
D.若用HCOOK溶液代替HCOOH,生成的KOH能吸收CO2转变为HCO3- 。
5.【答案】D
【知识点】酯的性质;取代反应;加成反应;水解反应
【解析】【解答】A.由结构简式可以看出,草酸二酯的分子中含有26个C、24个H、8个O、6个Cl,分子式为C26H24O8Cl6,故A不符合题意;
B.该有机物中含有苯环,能够与氢气发生加成反应,官能团酯基能够发生水解反应,有机物能够燃烧,发生氧化反应,故B不符合题意;
C.能与氢气发生加成反应的只有2个苯环,则1mol草酸二酯与氢气完全反应,需要氢气6mol,故C不符合题意;
D.1mol草酸二酯含有4个酯基,水解生成4个-COOH和两个酚羟基( ),则最多消耗6molNaOH,故D符合题意。
故答案为:D。
【分析】草酸二酯分子中含有4个酯基和6个氯原子,酯基能够发生水解反应,与氢气发生加成反应时,只有苯环反应。
6.【答案】D
【知识点】苯酚的性质及用途;酯的性质
【解析】【解答】A.X+Y→W变化中没有C=C或C=O生成C-C、C-O键的变化,则反应①为取代反应,故A不符合题意;
B.苯环与3mol氢气发生加成反应,C=C与1mol氢气发生加成反应,但烃基不一定为饱和烃基,则至少需要4mol氢气,故B不符合题意;
C.X与W的结构不同,不是同系物,故C不符合题意;
D.X中含有酚羟基,W含有酚羟基和酯基,Y、Z含有酯基,都能与NaOH反应,故D符合题意;
故答案为:D。
【分析】A.X+Y→W变化中是X酚羟基的邻位上的H被取代;
B.苯环与3mol氢气发生加成反应,C=C与1mol氢气发生加成反应,酯基不与的H2加成,烃基不一定为饱和烃基,所以至少需要4mol氢气;
C.X与W的含的官能团不同,不是同系物;
D.X中含有酚羟基,W含有酚羟基和酯基,Y、Z含有酯基,都能与NaOH反应;
7.【答案】C
【知识点】醛与Cu(OH)2的反应;加成反应;水解反应
【解析】【解答】A. X有苯环可以与3molH2加成,还有1mol的-CHO与1molH2加成,总共耗4molH2, 故A项不符合题意;
B.Y与Z 官能团区别:Y有-OH、Z有酯基,不能用NaHCO3溶液鉴别,-OH与Na反应放出H2,应用Na鉴别,故B项不符合题意;
C. X与Z 官能团区别:X有-CHO、Z有酯基,-CHO与新制的Cu(OH)2共热生成砖红色沉淀,可用新制Cu(OH)2鉴别反应后的Z中是否含有X,故C项符合题意;
D. 1molZ有1mol酯基耗1mol NaOH,故D项不符合题意;
故答案为:C。
【分析】A.苯环中可以看作是三个碳碳双键,X中还有一个醛基,因此1mol的X可以和4molH2发生加成反应;
B.鉴别物质时,所选的试剂应与被鉴别物质产生不同的现象;
C.-CHO可以与新制的Cu(OH)2共热生成砖红色沉淀Cu2O,可以利用这个反应来鉴别-CHO;
D.酯基在碱性条件下会水解生成醇和盐。
8.【答案】C
【知识点】盐类水解的原理;盐类水解的应用;水解反应
【解析】【解答】从图像可知H3A 为弱酸,存在电离平衡,H3A H2A-+H+, Ka1=[c(H2A-).c(H+)]/c(H3A)=10-2.2;H2A- HA2-+H+;Ka2=[ c(HA2-). c(H+)]/ c(H2A-)=10-7,2,H2A-+H2O H3A+OH-水解常数为K= c(H3A).c(OH-)/ c(H2A-),水的离子积常数为KW= c(H+) c(OH-)=10-14,所以K= c(H3A). KW/ c(H2A-). c(H+)=KW/ Ka1=10-11.8Ka2/K=[ c(HA2-). c(H+)]/ c(H2A-)=10-7.2/10-11.8=104.6>1,所以电离大于水解,所以 NaH2A 水溶液呈酸性,故A不符合题意;
B.HA2- A3-+H+;H2O H++OH-,根据电荷守恒c(H+)=c(OH-)+c(H2A-)+2c(HA2-)+3c(A3-),B不符合题意;
C.因为Ka1=[c(H2A-).c(H+)]/c(H3A)=10-2.2;Ka1=[c(HA2-).c(H+)]/c(H2A-)=10-7,2,Ka1. Ka1=[c(HA2-).C2(H+)]/ c(H3A), (Ka1. Ka2)/ C2(H+)=c(HA2-)/ c(H3A),当溶液至pH=5时, c(H+)=10-5 c(HA2-)/ c(H3A)= (10-2.2. 10-7,2)/ 10-10=10-0.6,故C符合题意;
D.因为氨水为弱电解质,所以在离子反应方程式中不能拆,故D 不符合题意。
故答案为:C。
【分析】A.由于NaH2A是弱酸强碱盐,弱酸跟同时存在水解和电离,电离使溶液呈酸性,水解时溶液呈碱性,由于电离程度大于水解,所以NaH2A溶液呈酸性;
B.在体系中存在电荷守恒、质量守恒和物料守恒,电荷守恒的正确表达式应是c(H+)=c(OH-)+c(H2A-)+2c(HA2-)+3c(A3-);
C.根据弱酸的电离平衡常数可以计算出当溶液的pH=5时,二者浓度的比值;
9.【答案】A,C
【知识点】乙酸的化学性质
【解析】【解答】解:A、强酸制备弱酸,乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体,故A正确;
B、乙酸分子中含有碳氧双键,但由于与羟基相连接,形成新的官能团羧基,所以它不能使溴水褪色,故B错误;
C、乙酸的熔点为16.6℃,温度低于熔点时,乙酸凝结成类似冰一样的晶体,故C正确;
D、钠是活泼金属,乙酸具有酸的通性,钠与乙酸反应生成乙酸钠与氢气,故D错误.
故选:AC.
【分析】A、根据强酸制备弱酸原理判断.
B、含有碳氧双键,但由于与羟基相连接,受羟基影响不能与溴水反应.
C、乙酸的熔点为16.6℃,温度低于熔点时,乙酸凝结成类似冰一样的晶体,纯净的乙酸又叫冰醋酸.
D、乙酸具有酸的通性,钠是活泼金属,钠与乙酸反应生成氢气.
10.【答案】C,D
【知识点】“手性分子”在生命科学等方面的应用;羧酸简介;水解反应;酯化反应
【解析】【解答】A、化合物X中能与NaOH溶液反应的官能团有羧基和酯基,其中酯基水解后产物含有羧基和酚羟基,都能与NaOH反应,因此1mol化合物X能与3molNaOH反应,A不符合题意;
B、酯化反应的原理是“酸脱羟基,醇脱氢”,则Y与乙醇发生酯化反应时,Y中的羧基脱去羟基,乙醇的羟基上脱去H原子,所得产物的结构与X不同,B不符合题意;
C、化合物X、Y中都含有碳碳双键,因此都能与KMnO4溶液反应,C符合题意;
D、化合物X与足量的Br2反应后所得产物的结构简式为,其中含有手性碳原子数为3,化合物Y与足量的Br2反应后所得产物的结构简式为:,其中含有手性碳原子数为3,D符合题意;
故答案为:CD
【分析】A、能与NaOH溶液反应的官能团有:卤素原子、羧基、酯基、酚羟基;
B、根据酯化反应的原理“酸脱羟基,醇脱氢”分析;
C、能与KMnO4溶液反应的官能团有:羟基、醛基、碳碳双键、碳碳三键;
D、若碳原子所连的四个原子或原子团不相同,则该碳原子为手性碳原子,结合加成产物的结构简式确定手性碳原子的个数;
11.【答案】C,D
【知识点】共价键的形成及共价键的主要类型;有机物中的官能团;酯的性质
【解析】【解答】A.由图可知其分子式为 C11H13O5Cl ,故A不符合题意;
B.有机物G中含有过氧键、酯基、羟基和氯原子四种官能团,故B不符合题意;
C.氢键不属于化学键,故C符合题意;
D.G只有苯环能与氢气加成,1molG最多能与3mol氢气反应,G中能与NaOH反应的官能团有酯基和卤代烃基,最多可与2mol氢氧化钠反应,故D符合题意;
故答案为:CD。
【分析】A、根据分子结构确定分子中所含原子数,从而得出分子式;
B、分子结构中所含的官能团有过氧键、酯基、羟基和卤素原子;
C、氢键不属于化学键;
D、分子结构中能与H2发生加成反应的苯环,能与NaOH反应的官能团为酯基;
12.【答案】C,D
【知识点】酯化实验
【解析】【解答】乙醛与氢氧化铜反应:在NaOH溶液中加入几滴CuSO4溶液,发生反应的离子方程式是:Cu2++2OH﹣=Cu(OH)2↓,在其中加入乙醛溶液并加热煮沸,可观察到的现象是:溶液中出现砖红色的沉淀,反应的化学方程式为:CH3CHO+2Cu(OH)2 CH3COOH+2H2O+Cu2O↓,此反应可用于检验醛基,
A.乙醛与氢氧化铜反应,实验步骤是在试管里加入10%的氢氧化钠溶液2mL,滴入2%的硫酸铜溶液4~6滴,振荡后加入乙醛溶液0.5mL,乙醛无需过量,故A错误;
B.乙醛与氢氧化铜反应,实验步骤是在试管里加入10%的氢氧化钠溶液2mL,滴入2%的硫酸铜溶液4~6滴,得到新制的氢氧化铜絮状沉淀,无需过量,故B错误;
C.乙醛与氢氧化铜反应,需要在碱溶液中进行,NaOH要稍微过量,故C正确;
D.长期放置的氢氧化铜易形成大颗粒状沉淀吸附试管底部,新制的氢氧化铜沉淀呈絮状,溶于过量的氢氧化钠生成四羟基铜酸钠,使反应顺利进行,故D正确;
故选CD.
【分析】乙醛与氢氧化铜反应生成红色沉淀的实验:首先NaOH溶液中加入几滴CuSO4溶液,发生复分解反应生成氢氧化铜沉淀和硫酸钠,其次氢氧化铜具有氧化性,氧化醛基,本身被还原为砖红色的氧化亚铜,利用该反应也可检验醛基的存在.关键操作是反应要在碱性溶液中进行.从而使醛的氧化加快,同时避免生成大量的氢氧化铜沉淀.
13.【答案】B,C
【知识点】取代反应;消去反应;水解反应
【解析】【解答】A.发生水解反应生成醇,则只断裂C-X,即图中①,故A不符合题意;
B.发生消去反应,断裂C-X和邻位C上的C-H键,则断裂①③,故B符合题意;
C.发生水解反应(取代反应)生成醇时,则只断裂C-X,即图中①,故C符合题意;
D.发生消去反应,断裂C-X和邻位C上的C-H键,则断裂①③,故D不符合题意;
故答案为:BC。
【分析】卤代烃的水解反应实质上就是取代反应,反应中一X被一OH取代了,所以被破坏的只有①;卤代烃的消去反应是相邻两个碳原子上的一个一X和一个一H一同被脱去,而生成不饱和烃和卤化氢的反应,被破坏的键应该是①和③。
14.【答案】C,D
【知识点】消去反应;水解反应
【解析】【解答】解:A.CH3CH2CH2CH2Cl可水解CH3CH2CH2CH2OH,发生消去反应生成CH3CH2CH=CH2,故A不选;
B.CH3CH2Cl可发生水解反应生成CH3CH2OH,发生消去反应生成CH2=CH2,故B不选;
C.CH3Br没有邻位C,不能发生消去反应,CH3Br水解生成CH3OH,故C选;
D. 没有邻位C,不能发生消去反应,可发生水解反应生成醇,故D选;
故选CD.
【分析】由选项可知,均为卤代烃,均可发生水解反应,与﹣X相连C的邻位C上有H可发生消去反应,以此来解答.
15.【答案】B,D
【知识点】取代反应;加成反应;消去反应;酯化反应
【解析】【解答】A.酯化反应的规律是羧酸脱去羟基,醇脱去氢原子,生成酯基,则酯化反应不能引入羟基,故A不符合题意;
B.取代反应可引入羟基,例如卤代烃水解、酯的水解是取代反应,都能引入羟基,故B符合题意;
C.消去反应是消除羟基,不会引入羟基,故C不符合题意;
D.加成反应可引入羟基,如乙烯水化制取乙醇,故D符合题意;
本题答案BD。
【分析】卤代烃的取代可以生成羟基,烯烃的加成也可以生成羟基。
16.【答案】(1)N(CH2CH3)3;CH3— —NH2;;CH2=CHCONH2
(2)伯胺;叔胺;仲胺
(3);
【知识点】酰胺
【解析】【解答】(1)三乙胺的结构简式为N(CH2CH3)3。
对甲基苯胺的结构简式为。
N,N-二甲基甲酰胺的结构简式为。
丙烯酰胺的结构简式为:CH2=CHCONH2。
(2)环己胺的结构简式为,其氮原子上连接有一个烃基,属于伯胺;
三甲胺的结构简式为N(CH3)3,其氮原子上连接有三个烃基,属于叔胺;
二苯胺的结构简式为,其氮原子上连接有两个烃基,属于仲胺。
(3)苯胺与盐酸反应生成,该反应的化学方程式为:。
甲酰胺与NaOH反应生成HCOONa和NH3,该反应的化学方程式为:。
【分析】(1)根据名称书写有机物的结构简式。
(2)氮原子上连接有一个烃基的为伯胺,连接有两个烃基的为仲胺,连接有三个烃基的为叔胺。
(3)苯胺与盐酸反应生成;甲酰胺的结构简式为,与NaOH溶液反应生成HCOONa和NH3,据此写出反应的化学方程式。
17.【答案】(1)球形冷凝管
(2)分水器中液面不再变化
(3)、
(4)C
【知识点】酯化实验;酯化反应
【解析】【解答】甲基丙烯酸与甲醇发生酯化反应生成甲基丙烯酸甲酯和水,当分水器内液面不再变化时说明反应结束;
(1)A装置的名称是球形冷凝管;
(2)当分水器中液面不再变化,停止加热;
(3)已知甲基丙烯酸甲酯受热易聚合,上述实验可能发生加聚反应或甲醇发生分子间发生取代反应,生成的副产物结构简式为 、等。
(4)A.该实验中,浓硫酸的作用之一是作吸水剂,吸收反应生成的水,促进平衡向正反应方向移动,提高了产率,A项正确;B.酯化反应中若生成的酯的密度比水大,则酯沉在分水器中水下,水从分水器中流入圆底烧瓶内,不能提高反应物的转化率,B项正确;C.洗涤剂X是一组试剂,产物要依次用饱和。溶液去除甲基丙烯酸、饱和溶液洗去甲基丙烯酸甲酯中溶解的、饱和溶液吸收甲醇和水,C项不正确;D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏,防止甲基丙烯酸甲酯受热聚合,D项正确;
故答案为:C。
【分析】(1)根据仪器构造可知,A为球形冷凝管;
(2)当分水器内液面不再变化时说明反应结束;
(3)甲基丙烯酸甲酯受热易聚合,则可能发生加聚反应或甲醇发生分子间发生取代反应;
(4)A.浓硫酸具有吸水性;
B.若生成的酯的密度比水大,酯沉在分水器中水下,水从分水器中流入圆底烧瓶内,不能提高反应物的转化率;
C. 饱和Na2CO3去除甲基丙烯酸、饱和NaCl溶液洗去甲基丙烯酸甲酯中溶解的碳酸钠、饱和氯化钙溶液吸收甲醇和水;
D.甲基丙烯酸甲酯受热聚合。
18.【答案】(1)AC;2CH3(CH2)5CH2OH+O2 2CH3(CH2)5CHO+2H2O
(2)D
(3)NaHCO3
(4)A;
【知识点】饱和烃与不饱和烃;同分异构现象和同分异构体;乙醇的化学性质;水解反应
【解析】【解答】(1) A. α-C上有1个H原子,能被氧化为酮; B. α-C上没有H原子,不能发生催化氧化;
C. α-C上有1个H原子,能被氧化为酮;D.CH3(CH2)5CH2OH α-C上有2个H原子,能被氧化为醛;可以发生催化氧化生成酮的是AC。CH3(CH2)5CH2OH能被氧化为醛,反应的化学方程式是2CH3(CH2)5CH2OH+O2 2CH3(CH2)5CHO+2H2O;
(2) A.吃馒头时多咀嚼后有甜味,是淀粉在唾液淀粉酶作用下水解为麦芽糖,故不选A;
B.在酸性环境下,淀粉发生水解变成葡萄糖,加碘不显蓝色,故不选B;
C. 油脂属于酯类,在碱性条件下水解为高级脂肪酸钠和甘油,故不选C;
D.不慎将浓硝酸沾到皮肤上会出现黄色斑痕,发生蛋白质的颜色反应,不是水解,
故答案为:D;
(3)酸性-COOH>H2CO3>酚-OH>HCO3-,能将 转化为 的试剂是NaHCO3;
① 与Br21:2发生加成反应生成 ; 与Br2 1:1发生1,4加成反应生成 ; 与Br2 1:1发生1,2加成反应生成 或 ,不可能生成 ,
故答案为:A;
②根据 + , 和 发生双烯合成反应的产物是 ;
【分析】(1)α-C上有1个H原子的醇能被氧化为酮;
(2)根据糖类、油脂、蛋白质的性质判断;
(3)根据酸性-COOH>H2CO3>酚-OH>HCO3-判断;
(4) ①共轭二烯烃能以1,4和1,2两种形式发生加成反应;
②根据 + 判断1-丁烯和2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物;
19.【答案】(1)苯乙烯
(2)取代反应
(3)NaOH水溶液;加热
(4)C15H14O
(5)羟基、羧基
(6) 或 或
(7) +HBr ;2 +O2 2 +2H2O
【知识点】利用质谱、红外光谱、核磁共振等确定有机物的结构;同分异构现象和同分异构体;取代反应;加成反应;水解反应
【解析】【解答】(1)A的结构简式为 ,名称为苯乙烯,故答案为:苯乙烯;
(2)由F生成G的反应为 与三氯化磷发生取代反应生成 ,故答案为:取代反应;
(3)B→C的反应为 在氢氧化钠溶液中共热发生水解反应生成 ,故答案为:NaOH水溶液;加热;
(4)H的结构简式为 ,分子式为C15H14O,故答案为:C15H14O;
(5)Ⅰ的结构简式为 ,含有的官能团为羟基、羧基,故答案为:羟基、羧基;
(6)F的结构简式为 ,F的同分异构体为酯类芳香族化合物,说明分子中含有酯基,核磁共振氢谱为四组峰说明分子中含有4类氢原子,则符合峰面积比为1:2:2:3的同分异构体的结构简式为 、 、 ,故答案为: 或 或 ;
(7)A→B的反应为在过氧化物作用下, 与溴化氢发生加成反应生成 ,反应的化学方程式为 +HBr ;C→D的反应为在铜做催化剂作用下, 与氧气发生催化氧化反应生成 ,反应的化学方程式为2 +O2 2 +2H2O,故答案为:2 +O2 2 +2H2O。
【分析】由D的结构简式和有机物转化的反应条件可知,C为 ,则B为 、A为 ; 在加热条件下与新制氢氧化铜发生氧化反应生成 ,则E为 ; 经酸化生成 ,则F为 ; 与三氯化磷发生取代反应生成 ,则G为 ;在氯化铝作用下, 与甲苯发生取代反应生成 , 发生信息Ⅱ反应生成 ,则I为 ;在浓硫酸作用下, 共热发生消去反应生成 ,则J为 。
20.【答案】(1)同系物;取代反应
(2)C9H16O5
(3)银氨溶液或新制氢氧化铜都呈碱性,氧化醛基时会使酯基水解
(4)
(5)
(6)
(7)
【知识点】同分异构现象和同分异构体;酯的性质
【解析】【解答】(1)为乙酸乙酯和互为同系物。的反应类型是取代反应反应。故答案为:同系物;取代反应;
(2)的分子式C9H16O5。故答案为:C9H16O5;
(3)不宜选用银氨溶液或新制氢氧化铜的原因是:银氨溶液或新制氢氧化铜都呈碱性,氧化醛基时会使酯基水解。故答案为:银氨溶液或新制氢氧化铜都呈碱性,氧化醛基时会使酯基水解;
(4)根据信息i. R1COOR2+R3OHR1COOR3+R2OH,发生反应生成G和乙醇,的结构简式为:。故答案为:;
(5)3-四氢呋喃甲醇,分子式为C5H10O2 ,不饱和度为1,3-四氢呋喃甲醇有多种同分异构体,符合①不能与金属钠反应,分子中没有羧基和羟基, ②分子中有3种不同化学环境的氢原子,符合条件的有机物的结构简式如:。故答案为:;
(6)E分子的中间碳原子上有2个H原子,均可与环氧乙醚反应,时会生成分子式为的副产物,该副产物的结构简式是。故答案为:;
(7)以为原料,先用将其还原为,在一定条件下脱水得,在铜催化加热条件下将羟基氧化为醛基,得到产物,合成路径为。故答案为:。
【分析】B催化氧化生成D,则D的结构简式为, D与乙醇发生酯化反应生成E,E与环氧乙烷发生开环加成生成F,F发生信息i中酯交换反应脱去1分子CH3CH2OH生成G,G发生信息ii中还原反应生成H,H发生信息iii中反应脱去1分子水生成3-四氢呋喃甲醇,则G为,H为。
21.【答案】(1)(或);取代反应(或酯化反应)
(2)羧基、(酚)羟基
(3)
(4)10;、
【知识点】有机物中的官能团;同分异构现象和同分异构体;酯的性质;取代反应
【解析】【解答】(1)苯与Cl2发生取代反应,其条件为Fe或FeCl3做催化剂,因此条件X是Fe或FeCl3。
反应⑤中与发生反应生成,该反应的反应类型为取代反应。
(2)水杨酸的结构简式为,因此其所含的官能团为羧基、酚羟基。
(3)阿司匹林的结构简式为,其所含的官能团羧基、酯基都能与NaOH溶液反应,且酯基水解产生酚羟基,也能与NaOH溶液反应,因此阿司匹林与NaOH溶液反应的化学方程式为:。
(4)既不能发生水解反应,也不能发生银镜反应,说明分子结构中不含有-COOR和-CHO;1mol该有机物能与2molNaHCO3反应,说明分子结构中含有2mol-COOH。由于一分子阿司匹林中含有9个碳原子,因此其同分异构中含有苯环、2个-COOH,同时还剩余一个碳原子。
若该同分异构体为苯的三取代物,则剩余的碳原子为-CH3,该同分异构体共有6种;
若该同分异构体为苯的二取代物,则苯环上的取代基可以为-COOH、-CH2COOH,该同分异构体共有3种;
若该同分异构体为苯的一取代物,则苯环上的取代基为-CH(COOH)2,则该同分异构体有1种。
因此满足条件的同分异构体共有6+3+1=10种。
核磁共振氢谱有四组峰,且峰面积之比为1:2:2:3,说明分子结构具有对称性,且含有-CH3,2个-COOH处于对称位置,因此满足条件的同分异构体的结构简式为、。
【分析】A为芳香烃,且其相对分子质量为78,由“商余法”,因此A的分子式为C6H6,故A的结构简式为。A与Cl2发生取代反应生成B,因此B的结构简式为。B在NaOH浓溶液的和加热的条件下,发生取代反应,生成C,因此C的结构简式为。C与CO2反应生成。在H+作用下反应生成水杨酸,水杨酸的结构简式为。
22.【答案】(1)c(Cl-)>c(NH4+)>c(H+)>c(OH-);NH4Cl
(2)氯化铵分解吸收热量,降低了温度;氯化铵分解产生的气体隔绝了空气等
【知识点】盐类水解的原理;铵盐;水解反应
【解析】【解答】(1)氯化铵是强酸弱碱盐,在饱和溶液中,NH4+发生水解反应而消耗,所以c(Cl-)>c(NH4+),NH4+水解消耗水电离产生的OH-,最终达到平衡时,溶液中c(H+)>c(OH-),但盐水解产生的离子浓度是微弱的,因此c(NH4+)>c(H+),故溶液中离子浓度由大到小的顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);浸过氯化铵溶液的布条不燃烧,冒出白烟,是由于将布条灼烧时,氯化铵发生分解反应NH4Cl NH3↑+HCl↑,反应产生的气体在空气中相遇,会发生反应:NH3+HCl=NH4Cl,因此看到的白烟为NH4Cl;(2)浸过氯化铵溶液的布条不燃烧、不易着火的主要原因是氯化铵分解吸收热量,降低了布条周围的温度,不能达到相应物质的着火点;而且氯化铵分解产生的氨气和HCl气体充满在布条周围,隔绝了空气,使着火物不能接触空气,不具备着火燃烧的条件。
【分析】(1)氯化铵是强酸弱碱盐,水解呈酸性,即可得出本题答案;根据方程式NH4Cl NH3↑+HCl↑,即可得出本题答案
(2)氯化铵分解产生的氨气和HCl气体充满在布条周围,隔绝了空气,使着火物不能接触空气,不具备着火燃烧的条件
23.【答案】(1)CH3CH2OH CH2=CH2↑+H2O;消去反应
(2)CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;乙酸
(3)CH3CH2Br+NaOH CH3CH2OH+NaBr;醇
(4) +HNO3 +H2O;取代反应
【知识点】乙烯的实验室制法;取代反应;酯化反应
【解析】【解答】(1)乙醇和浓硫酸混合物加热到170℃发生消去反应生成乙烯,方程式是CH3CH2OH CH2=CH2↑+H2O;反应类型是消去反应;
(2)乙酸与乙醇的反应生成乙酸乙酯和水,反应方程式是CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O,发生酯化反应时,酸脱羟基醇脱氢,所以水中氧元素的来源是乙酸;
(3)溴乙烷与氢氧化钠水溶液共热发生取代反应生成乙醇和溴化钠,反应方程式是CH3CH2Br+NaOH CH3CH2OH+NaBr,此反应将卤代烃类物质转化为醇类物质;
(4)苯与浓硫酸、浓硝酸的混合酸在加热时发生反应生成硝基苯和水,反应方程式是 +HNO3 +H2O,反应类型是取代反应。
【分析】(1)乙醇和浓硫酸混合物加热到170℃发生消去反应生成乙烯,结合消去反应的特征分析;
(2)乙酸与乙醇在浓硫酸加热的条件下发生酯化反应,据此分析;
(3)溴乙烷与氢氧化钠水溶液共热发生取代反应生成乙醇和溴化钠;
(4)苯与浓硫酸、浓硝酸的混合酸在加热时发生反应生成硝基苯和水,书写方程式时注意标注反应条件,据此解答。
试题分析部分
1、试卷总体分布分析
总分:85分
分值分布 客观题(占比) 30.0(35.3%)
主观题(占比) 55.0(64.7%)
题量分布 客观题(占比) 15(65.2%)
主观题(占比) 8(34.8%)
2、试卷题量分布分析
大题题型 题目量(占比) 分值(占比)
选择题 8(34.8%) 16.0(18.8%)
非选择题 8(34.8%) 55.0(64.7%)
多选题 7(30.4%) 14.0(16.5%)
3、试卷难度结构分析
序号 难易度 占比
1 普通 (30.4%)
2 困难 (69.6%)
4、试卷知识点分析
序号 知识点(认知水平) 分值(占比) 对应题号
1 极性键和非极性键 2.0(2.4%) 4
2 羧酸简介 2.0(2.4%) 10
3 乙酸的化学性质 4.0(4.7%) 4,9
4 离子方程式的书写 2.0(2.4%) 1
5 “手性分子”在生命科学等方面的应用 2.0(2.4%) 10
6 有机物中的官能团 8.0(9.4%) 11,21
7 苯的同系物及其性质 2.0(2.4%) 2
8 乙醇的化学性质 9.0(10.6%) 2,18
9 醛与Cu(OH)2的反应 2.0(2.4%) 7
10 盐类水解的应用 2.0(2.4%) 8
11 消去反应 6.0(7.1%) 13,14,15
12 利用质谱、红外光谱、核磁共振等确定有机物的结构 9.0(10.6%) 19
13 酰胺 9.0(10.6%) 16
14 共价键的形成及共价键的主要类型 2.0(2.4%) 11
15 同分异构现象和同分异构体 34.0(40.0%) 2,3,18,19,20,21
16 盐类水解的原理 5.0(5.9%) 8,22
17 乙烯的实验室制法 8.0(9.4%) 23
18 加成反应 15.0(17.6%) 5,7,15,19
19 催化剂 2.0(2.4%) 4
20 水解反应 33.0(38.8%) 2,5,7,8,10,13,14,18,19,22
21 铵盐 3.0(3.5%) 22
22 酯化实验 7.0(8.2%) 12,17
23 饱和烃与不饱和烃 7.0(8.2%) 18
24 酯化反应 17.0(20.0%) 10,15,17,23
25 酯的性质 24.0(28.2%) 1,3,5,6,11,20,21
26 苯酚的性质及用途 4.0(4.7%) 1,6
27 取代反应 29.0(34.1%) 5,13,15,19,21,23
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
高中化学试卷2024年02月29日9
一、选择题
1.下列离子( 或化学)方程式正确的是( )
A.苯酚钠溶液中通入少量二氧化碳: +CO
B.CH3CO18OC2H5在稀硫酸催化下水解:
C.向 Ba(OH)2溶液中加入稀 H2SO4溶液:
D.用已知浓度的 KMnO4溶液滴定草酸:
2.下列关于有机物的说法正确的是( )
A.糖类、油脂、蛋白质在一定条件下均能水解
B.乙二醇、苯乙烯在一定条件下均可聚合生成高分子化合物
C.分子式为C4H8Cl2的有机物共有(不含立体异构)8种
D. 处于同一平面上的原子数最多为18个
3.有机物甲的分子式为C7H14O2,在酸性条件下,甲水解为乙和丙两种有机物,在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,则甲的可能结构有 ( )
A.4种 B.6种 C.8种 D.10种
4.氢能是一种重要的清洁能源,由HCOOH可以制得。在催化剂作用下,HCOOH分解生成可能的反应机理如图所示。研究发现,其他条件不变时,以HCOOK溶液代替HCOOH催化释氢的效果更佳。
下列说法正确的是( )
A.HCOOH催化释氢过程中,有非极性键的断裂与形成
B.HCOOD催化释氢反应除生成外,还生成、HD、
C.其他条件不变时,以HCOOK溶液代替HCOOH不能提高释放氢气的纯度
D.HCOOK溶液代替HCOOH时发生反应:
5.夏日的夜晚,常看见儿童手持发光的“魔棒”在广场上嬉戏。“魔棒”发光原理是利用过氧化氢氧化草酸二酯产生能量,该能量被传递给荧光物质后便发出荧光,草酸二酯(CPPO)结构简式如图。已知:苯环上卤素不水解,下列有关说法不正确的是( )
A.草酸二酯的分子式为C26H24Cl6O8
B.该有机物能发生加成反应、取代反应、氧化反应
C.1 mol草酸二酯与氢气完全反应,需要氢气6 mol
D.1 mol草酸二酯与氢氧化钠稀溶液反应,最多消耗4 mol NaOH
6.下图表示在催化剂作用下将X和Y合成具有生物活性的物质Z,W是中间产物(R1、R2均为烃基)。则下列有关叙述一定正确的是( )
A.反应①属于加成反应
B.1molZ完全加成需要3molH2
C.X与W属于同系物
D.X、Y、Z、W都能与NaOH溶液反应
7.化合物Z是有机化工中重要中间体,其合成路线如图,下列说法正确的是( )
A.1mol X最多能与3mol H2发生加成反应
B.可用NaHCO3溶液鉴别反应后Z中是否含有Y
C.可用新制的Cu(OH)2溶液鉴别反应后Z中是否含有X
D.1 mol Z最多可消耗2mol NaOH
8.常温下,某酸H3A水溶液中含A的各种粒子的分布分数(平衡时某种粒子的浓度占各粒子浓度之和的分数)与pH关系图如下所示,下列说法正确的是( )
A.NaH2A水溶液呈碱性
B.H3A溶液中存在:c(H+)=c(OH-)+c(H2A-)+ c(HA2-)+ c(A3-)
C.向H3A溶液中加入一定量的NaOH溶液至pH=5时,
D.向H3A溶液中加入氨水使PH从5→9发生的主要离子反应是:H2A-+OH-=HA2-+H2O
二、多选题
9.下列关于乙酸性质的叙述中,正确的是( )
A.乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体
B.乙酸分子中含有碳氧双键,所以它能使溴水褪色
C.乙酸在温度低于16.6℃时,就凝结成冰状晶体
D.乙酸不能与金属钠反应放出氢气
10.化合物Y具有抗菌、消炎作用,可由X制得。
下列有关化合物X、Y的说法正确的是( )
A.1 mol X最多能与2 mol NaOH反应
B.Y与乙醇发生酯化反应可得到X
C.X、Y均能与酸性KMnO4溶液反应
D.室温下X、Y分别与足量Br2加成的产物分子中手性碳原子数目相等
11.有机化合物G是合成抗真菌药物的重要中间体,结构简式如下图。下列说法错误的是( )
A.G的分子式为C11H13O5Cl
B.G分子中含四种官能团
C.G分子含有σ键、π键、大π键、氢键等化学键
D.1molG最多可与3molH2加成,最多与4molNaOH反应
12.在乙醛与氢氧化铜反应生成红色沉淀的实验中,关键操作是( )
A.乙醛要过量 B.CuSO4要过量
C.NaOH要稍微过量 D.氢氧化铜要新制
13.卤代烃R—CH2—CH2—X中的化学键如下图所示,则下列说法正确的是( )
A.当该卤代烃发生水解反应时,被破坏的键是①和②
B.当该卤代烃发生消去反应时,被破坏的键是①和③
C.当该卤代烃发生取代反应时,被破坏的键是①
D.当该卤代烃发生消去反应时,被破坏的键是①和②
14.下列物质中,能发生水解反应,但不能发生消去反应的是( )
A.CH3CH2CH2CH2Cl B.CH3CH2Cl
C.CH3Br D.
15.下列常见的有机反应类型中,能在有机物的分子中引入羟基的是
A.酯化反应 B.取代反应 C.消去反应 D.加成反应
三、非选择题
16.按要求回答下列问题:
(1)写出下列化合物的结构简式:
三乙胺 ; 对甲基苯胺 ;
N,N-二甲基甲酰胺 ;丙烯酰胺 。
(2)按氮原子所连烃基数目分析,环己胺可归为 (填“伯胺”“仲胺”或“叔胺”,下同),三甲胺可归类为 ,二苯胺可归类为 。
(3)苯胺与盐酸反应的化学方程式为 ;甲酰胺在NaOH溶液中水解的化学方程式为 。
17.实验室制备甲基丙烯酸甲酯的反应装置示意图和有关信息如下:
药品 相对分子质量 熔点/℃ 沸点/℃ 溶解性 密度/()
甲醇 32 -98 64.7 与水混溶,易溶于有机溶剂 0.79
甲基丙烯酸 86 15 161 溶于热水,易溶于有机溶剂 1.01
甲基丙烯酸甲酯 100 -48 100 微溶于水,易溶于有机溶剂 0.944
已知甲基丙烯酸甲酯受热易聚合;甲基丙烯酸甲酯在盐溶液中溶解度较小;可与醇结合形成复合物。
实验步骤:
①向烧瓶中依次加入:甲基丙烯酸、2粒沸石、无水甲醇、适量的浓硫酸;
②在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热烧瓶。在反应过程中,通过分水器下部的旋塞放出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中;
③当……..,停止加热;
④冷却后用试剂X洗涤烧瓶中的混合溶液并分离;
⑤取有机层混合液蒸馏,得到较纯净的甲基丙烯酸甲酯。
请回答下列问题:
(1)A装置的名称是 。
(2)请将步骤③填完整: 。
(3)上述实验可能生成的副产物结构简式为 (填两种)。
(4)下列说法错误的是____。
A.在该实验中,浓硫酸的作用之一是作吸水剂,提高了产率
B.酯化反应中若生成的酯的密度比水大,不能用分水器提高反应物的转化率
C.洗涤剂X是一组试剂,产物要依次用饱和、饱和溶液洗涤
D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏
18.烃的含氧衍生物是一类非常重要的有机物。
(1)分子式为C7H16O的饱和一元醇的同分异构体有多种。根据给出的该醇的同分异构体,回答下列问题:
A. B.
C. D.CH3(CH2)5CH2OH
其中,可以发生催化氧化生成酮的是 (填序号)。写出能催化氧化生成醛的化学方程式 。
(2)下列作用不属于水解反应的是_______
A.吃馒头时多咀嚼后有甜味
B.淀粉溶液和稀硫酸共热一段时间后,滴加碘水不显蓝色
C.油脂与氢氧化钠溶液共煮后可以制得肥皂
D.不慎将浓硝酸沾到皮肤上会出现黄色斑痕
(3)请写出能将 转化为 的试剂的化学式 。
(4)共轭二烯烃是含有两个碳碳双键,并且两个双键被一个单键隔开的二烯烃。最简单的共轭二烯烃是1,3-丁二烯。共轭二烯烃比较稳定。共轭二烯烃能以1,4和1,2两种形式发生加成反应,还可发生双烯合成反应(即Diels-Alder反应)等。用于合成橡胶、溶剂,是重要的有机化工原料。
① 与一定量的Br2发生加成反应,生成的产物不可能是 (填序号)。
A. B.
C. D.
②双烯合成反应(即Diels-Alder反应)是一类二烯烃与单烯烃或炔烃作用生成六元环状化合物的反应,例如,最简单的1,3-丁二烯和乙烯的作用表示为: + 。则由1-丁烯和2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物为 。
19.高分子化合物 的合成路线如图:
已知:Ⅰ.
Ⅱ.
回答下列问题:
(1)A的化学名称为 。
(2)由F生成G的反应类型是 。
(3)B→C反应所需试剂,条件分别为 、 。
(4)H的分子式为 。
(5)Ⅰ中官能团的名称是 。
(6)写出一种与F互为同分异构体的酯类芳香族化合物的结构简式(核磁共振氢谱为四组峰,峰面积比为1:2:2:3): 。
(7)分别写出A→B,C→D反应的化学方程式: 、 。
20.3-四氢呋喃甲醇是合成农药呋虫胺的中间体,其一种合成路线如下:
已知:i. R1COOR2+R3OHR1COOR3+R2OH
ii. R1COOR2R1CH2OH+R2OH
iii. R1OH+R2OHR1OR2+H2O
(1)和互为 。的反应类型是 反应。
(2)的分子式 。
(3)不宜选用银氨溶液或新制氢氧化铜的原因是: 。
(4)的结构简式为: 。
(5)3-四氢呋喃甲醇有多种同分异构体,写出1种符合下列条件的有机物的结构简式: 。
①不能与金属钠反应 ②分子中有3种不同化学环境的氢原子
(6)时会生成分子式为的副产物,该副产物的结构简式是 。
(7)已知具有极强还原性,除了还原酯基外(信息ii),还可还原醛基等。请以为原料,利用题中信息及所学知识,选用必要的无机试剂合成。
(合成路线的表示方式为:甲乙……目标产物)
21.某芳香烃A(相对分子质量为78)是一种重要的有机化工原料,以它为初始原料经过如下转化关系图(部分产物和反应条件略去)可以合成阿司匹林(乙酰水杨酸).
已知:Ⅰ.(X为Cl或Br)
Ⅱ.
回答下列问题:
(1)条件X是 ;反应⑤的反应类型是 .
(2)水杨酸中官能团的名称是 .
(3)阿司匹林与足量溶液反应的化学方程式为 .
(4)阿司匹林有多种同分异构体,满足下列条件的同分异构体有 种;其中核磁共振氢谱有四组峰,且峰面积之比为的结构简式为 .
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③该有机物能与完全反应.
22.某化学兴趣小组进行了下列关于氯化铵的课外实验:
(实验操作)
浸过氯化钠溶液的布条很快烧光,浸过氯化铵溶液的布条不燃烧,冒出白烟。
(1)氯化铵饱和溶液中离子浓度由大到小的顺序是 。白烟的成分是 。
(2)请推测浸过氯化铵溶液的布条不燃烧、不易着火的主要原因(写出一条即可) 。
23.按要求写出下列反应方程式(请注明反应条件),并按要求填空
(1)实验室制备乙烯 ,反应类型是 .
(2)乙酸与乙醇的反应 ,反应的无机产物中氧元素的来源是 。
(3)溴乙烷与氢氧化钠水溶液共热 ,此反应将卤代烃类物质转化为 类物质.
(4)苯与浓硫酸、浓硝酸的混合酸在加热时发生反应 ,反应类型是 .
答案解析部分
1.【答案】B
【知识点】苯酚的性质及用途;酯的性质;离子方程式的书写
【解析】【解答】A、由于酸性:H2CO3>苯酚>HCO3-,因此CO2与苯酚钠溶液反应生成苯酚和NaHCO3,该反应的离子方程式为:+H2O+CO2→+HCO3-,A不符合题意。
B、CH3CO18OC2H5在酸性条件下发生水解反应,断裂酯基中的C-O,反应生成CH3COOH和C2H518OH,B符合题意。
C、Ba(OH)2溶液与稀硫酸反应生成BaSO4和H2O,该反应的离子方程式为:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,C不符合题意。
D、KMnO4溶液具有氧化性,H2C2O4中碳元素为+3价,具有还原性,二者可发生氧化还原反应,该反应的离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,D不符合题意。
故答案为:B
【分析】A、苯酚的酸性强于HCO3-,因此反应生成HCO3-,不生成CO32-。
B、酯基水解过程中断裂C-O键。
C、Ba(OH)2与H2SO4反应生成BaSO4和H2O。
D、KMnO4具有氧化性,能将H2C2O4氧化成CO2,自身还原为Mn2+。
2.【答案】B
【知识点】同分异构现象和同分异构体;苯的同系物及其性质;乙醇的化学性质;水解反应
【解析】【解答】A.油脂、蛋白质在一定条件下均能水解,但糖类中的单糖如葡萄糖不水解,故A不符合题意;
B.乙二醇可通过缩聚生成高分子化合物,苯乙烯可通过加聚生成高分子化合物,故B符合题意;
C.C4H8Cl2的同分异构体可以采取“定一移二”法 ,由图可知C4H8Cl2共有9种同分异构体,故C不符合题意;
D.该有机物中含有苯环、碳碳双键、碳碳三键、甲基,甲基中C原子处于乙烯和乙炔中H原子的位置,甲基通过旋转碳碳单键会有1个H原子处在乙烯或乙炔的平面内,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子(苯环上6个、甲基中2个、碳碳双键上2个、碳碳三键上2个)共面.在甲基上可能还有1个氢原子共平面,则两个甲基有2个氢原子可能共平面,苯环上4个氢原子共平面,双键上2个氢原子共平面,总计得到可能共平面的原子有20个,故D不符合题意;
故答案为:B。
【分析】该题的难点是有机物共线、共面判断,解答该类试题的判断技巧:①甲烷、乙烯、乙炔、苯、甲醛5种分子中的H原子若被其他原子如
C、O、Cl、N等取代,则取代后的分子空间构型基本不变。②借助C—C键可以旋转而—C≡C—键、 键不能旋转以及立体几何知识判断。③苯分子中苯环可以以任一碳氢键为轴旋转,每个苯分子有三个旋转轴,轴上有四个原子共线。
3.【答案】A
【知识点】同分异构现象和同分异构体;酯的性质
【解析】【解答】在相同的温度和压强下,同质量的乙和丙的蒸气所占体积相同,这说明二者的相对分子质量是相等的。甲属于酯类,水解生成羧酸和醇。根据质量守恒定律可知,乙和丙的相对分子质量是(130+18)÷2=74,所以饱和一元羧酸CnH2n+1COOH和饱和一元醇的通式CmH2m+2O可知,羧酸是丙酸,醇是丁醇。由于丙酸只有一种,而丁醇有4种,所以甲的结构简式就有4种,答案选A。
【分析】该题的关键是根据阿伏加德罗定律得出乙和丙的相对分子质量相等。然后根据质量守恒定律得出各种的羧酸和醇,最后再分析即可。该属于中等难度的试题。
4.【答案】D
【知识点】极性键和非极性键;催化剂;乙酸的化学性质
【解析】【解答】A.在催化剂作用下,HCOOH分解生成CO2和H2,转化涉及到N-H键的断裂和形成、O-H键的断裂以及H-H键的形成,没有非极性键的断裂,A不符合题意;
B.若用HCOOD代替HCOOH,反应为HCOOD分解,除生成CO2外,还生成HD,无H2 、D2,B不符合题意;
C.若用HCOOK溶液代替HCOOH,HCOOK分解生成CO2和KH,KH与水反应生成KOH和H2,KOH能吸收CO2,CO2的量会减少,能提高释放氢气的纯度,C不符合题意;
D.若用HCOOK溶液代替HCOOH,生成的KOH能吸收CO2转变为HCO3- ,离子反应为 ,D符合题意;
故答案为:D
【分析】A.在催化剂作用下,HCOOH分解生成CO2和H2;
B.若用HCOOD代替HCOOH,反应为HCOOD分解,除生成CO2外,还生成HD,无H2 、D2;
C.KOH能吸收CO2,CO2的量会减少,能提高释放氢气的纯度;
D.若用HCOOK溶液代替HCOOH,生成的KOH能吸收CO2转变为HCO3- 。
5.【答案】D
【知识点】酯的性质;取代反应;加成反应;水解反应
【解析】【解答】A.由结构简式可以看出,草酸二酯的分子中含有26个C、24个H、8个O、6个Cl,分子式为C26H24O8Cl6,故A不符合题意;
B.该有机物中含有苯环,能够与氢气发生加成反应,官能团酯基能够发生水解反应,有机物能够燃烧,发生氧化反应,故B不符合题意;
C.能与氢气发生加成反应的只有2个苯环,则1mol草酸二酯与氢气完全反应,需要氢气6mol,故C不符合题意;
D.1mol草酸二酯含有4个酯基,水解生成4个-COOH和两个酚羟基( ),则最多消耗6molNaOH,故D符合题意。
故答案为:D。
【分析】草酸二酯分子中含有4个酯基和6个氯原子,酯基能够发生水解反应,与氢气发生加成反应时,只有苯环反应。
6.【答案】D
【知识点】苯酚的性质及用途;酯的性质
【解析】【解答】A.X+Y→W变化中没有C=C或C=O生成C-C、C-O键的变化,则反应①为取代反应,故A不符合题意;
B.苯环与3mol氢气发生加成反应,C=C与1mol氢气发生加成反应,但烃基不一定为饱和烃基,则至少需要4mol氢气,故B不符合题意;
C.X与W的结构不同,不是同系物,故C不符合题意;
D.X中含有酚羟基,W含有酚羟基和酯基,Y、Z含有酯基,都能与NaOH反应,故D符合题意;
故答案为:D。
【分析】A.X+Y→W变化中是X酚羟基的邻位上的H被取代;
B.苯环与3mol氢气发生加成反应,C=C与1mol氢气发生加成反应,酯基不与的H2加成,烃基不一定为饱和烃基,所以至少需要4mol氢气;
C.X与W的含的官能团不同,不是同系物;
D.X中含有酚羟基,W含有酚羟基和酯基,Y、Z含有酯基,都能与NaOH反应;
7.【答案】C
【知识点】醛与Cu(OH)2的反应;加成反应;水解反应
【解析】【解答】A. X有苯环可以与3molH2加成,还有1mol的-CHO与1molH2加成,总共耗4molH2, 故A项不符合题意;
B.Y与Z 官能团区别:Y有-OH、Z有酯基,不能用NaHCO3溶液鉴别,-OH与Na反应放出H2,应用Na鉴别,故B项不符合题意;
C. X与Z 官能团区别:X有-CHO、Z有酯基,-CHO与新制的Cu(OH)2共热生成砖红色沉淀,可用新制Cu(OH)2鉴别反应后的Z中是否含有X,故C项符合题意;
D. 1molZ有1mol酯基耗1mol NaOH,故D项不符合题意;
故答案为:C。
【分析】A.苯环中可以看作是三个碳碳双键,X中还有一个醛基,因此1mol的X可以和4molH2发生加成反应;
B.鉴别物质时,所选的试剂应与被鉴别物质产生不同的现象;
C.-CHO可以与新制的Cu(OH)2共热生成砖红色沉淀Cu2O,可以利用这个反应来鉴别-CHO;
D.酯基在碱性条件下会水解生成醇和盐。
8.【答案】C
【知识点】盐类水解的原理;盐类水解的应用;水解反应
【解析】【解答】从图像可知H3A 为弱酸,存在电离平衡,H3A H2A-+H+, Ka1=[c(H2A-).c(H+)]/c(H3A)=10-2.2;H2A- HA2-+H+;Ka2=[ c(HA2-). c(H+)]/ c(H2A-)=10-7,2,H2A-+H2O H3A+OH-水解常数为K= c(H3A).c(OH-)/ c(H2A-),水的离子积常数为KW= c(H+) c(OH-)=10-14,所以K= c(H3A). KW/ c(H2A-). c(H+)=KW/ Ka1=10-11.8Ka2/K=[ c(HA2-). c(H+)]/ c(H2A-)=10-7.2/10-11.8=104.6>1,所以电离大于水解,所以 NaH2A 水溶液呈酸性,故A不符合题意;
B.HA2- A3-+H+;H2O H++OH-,根据电荷守恒c(H+)=c(OH-)+c(H2A-)+2c(HA2-)+3c(A3-),B不符合题意;
C.因为Ka1=[c(H2A-).c(H+)]/c(H3A)=10-2.2;Ka1=[c(HA2-).c(H+)]/c(H2A-)=10-7,2,Ka1. Ka1=[c(HA2-).C2(H+)]/ c(H3A), (Ka1. Ka2)/ C2(H+)=c(HA2-)/ c(H3A),当溶液至pH=5时, c(H+)=10-5 c(HA2-)/ c(H3A)= (10-2.2. 10-7,2)/ 10-10=10-0.6,故C符合题意;
D.因为氨水为弱电解质,所以在离子反应方程式中不能拆,故D 不符合题意。
故答案为:C。
【分析】A.由于NaH2A是弱酸强碱盐,弱酸跟同时存在水解和电离,电离使溶液呈酸性,水解时溶液呈碱性,由于电离程度大于水解,所以NaH2A溶液呈酸性;
B.在体系中存在电荷守恒、质量守恒和物料守恒,电荷守恒的正确表达式应是c(H+)=c(OH-)+c(H2A-)+2c(HA2-)+3c(A3-);
C.根据弱酸的电离平衡常数可以计算出当溶液的pH=5时,二者浓度的比值;
9.【答案】A,C
【知识点】乙酸的化学性质
【解析】【解答】解:A、强酸制备弱酸,乙酸的酸性比碳酸强,所以它可以跟碳酸盐溶液反应,产生CO2气体,故A正确;
B、乙酸分子中含有碳氧双键,但由于与羟基相连接,形成新的官能团羧基,所以它不能使溴水褪色,故B错误;
C、乙酸的熔点为16.6℃,温度低于熔点时,乙酸凝结成类似冰一样的晶体,故C正确;
D、钠是活泼金属,乙酸具有酸的通性,钠与乙酸反应生成乙酸钠与氢气,故D错误.
故选:AC.
【分析】A、根据强酸制备弱酸原理判断.
B、含有碳氧双键,但由于与羟基相连接,受羟基影响不能与溴水反应.
C、乙酸的熔点为16.6℃,温度低于熔点时,乙酸凝结成类似冰一样的晶体,纯净的乙酸又叫冰醋酸.
D、乙酸具有酸的通性,钠是活泼金属,钠与乙酸反应生成氢气.
10.【答案】C,D
【知识点】“手性分子”在生命科学等方面的应用;羧酸简介;水解反应;酯化反应
【解析】【解答】A、化合物X中能与NaOH溶液反应的官能团有羧基和酯基,其中酯基水解后产物含有羧基和酚羟基,都能与NaOH反应,因此1mol化合物X能与3molNaOH反应,A不符合题意;
B、酯化反应的原理是“酸脱羟基,醇脱氢”,则Y与乙醇发生酯化反应时,Y中的羧基脱去羟基,乙醇的羟基上脱去H原子,所得产物的结构与X不同,B不符合题意;
C、化合物X、Y中都含有碳碳双键,因此都能与KMnO4溶液反应,C符合题意;
D、化合物X与足量的Br2反应后所得产物的结构简式为,其中含有手性碳原子数为3,化合物Y与足量的Br2反应后所得产物的结构简式为:,其中含有手性碳原子数为3,D符合题意;
故答案为:CD
【分析】A、能与NaOH溶液反应的官能团有:卤素原子、羧基、酯基、酚羟基;
B、根据酯化反应的原理“酸脱羟基,醇脱氢”分析;
C、能与KMnO4溶液反应的官能团有:羟基、醛基、碳碳双键、碳碳三键;
D、若碳原子所连的四个原子或原子团不相同,则该碳原子为手性碳原子,结合加成产物的结构简式确定手性碳原子的个数;
11.【答案】C,D
【知识点】共价键的形成及共价键的主要类型;有机物中的官能团;酯的性质
【解析】【解答】A.由图可知其分子式为 C11H13O5Cl ,故A不符合题意;
B.有机物G中含有过氧键、酯基、羟基和氯原子四种官能团,故B不符合题意;
C.氢键不属于化学键,故C符合题意;
D.G只有苯环能与氢气加成,1molG最多能与3mol氢气反应,G中能与NaOH反应的官能团有酯基和卤代烃基,最多可与2mol氢氧化钠反应,故D符合题意;
故答案为:CD。
【分析】A、根据分子结构确定分子中所含原子数,从而得出分子式;
B、分子结构中所含的官能团有过氧键、酯基、羟基和卤素原子;
C、氢键不属于化学键;
D、分子结构中能与H2发生加成反应的苯环,能与NaOH反应的官能团为酯基;
12.【答案】C,D
【知识点】酯化实验
【解析】【解答】乙醛与氢氧化铜反应:在NaOH溶液中加入几滴CuSO4溶液,发生反应的离子方程式是:Cu2++2OH﹣=Cu(OH)2↓,在其中加入乙醛溶液并加热煮沸,可观察到的现象是:溶液中出现砖红色的沉淀,反应的化学方程式为:CH3CHO+2Cu(OH)2 CH3COOH+2H2O+Cu2O↓,此反应可用于检验醛基,
A.乙醛与氢氧化铜反应,实验步骤是在试管里加入10%的氢氧化钠溶液2mL,滴入2%的硫酸铜溶液4~6滴,振荡后加入乙醛溶液0.5mL,乙醛无需过量,故A错误;
B.乙醛与氢氧化铜反应,实验步骤是在试管里加入10%的氢氧化钠溶液2mL,滴入2%的硫酸铜溶液4~6滴,得到新制的氢氧化铜絮状沉淀,无需过量,故B错误;
C.乙醛与氢氧化铜反应,需要在碱溶液中进行,NaOH要稍微过量,故C正确;
D.长期放置的氢氧化铜易形成大颗粒状沉淀吸附试管底部,新制的氢氧化铜沉淀呈絮状,溶于过量的氢氧化钠生成四羟基铜酸钠,使反应顺利进行,故D正确;
故选CD.
【分析】乙醛与氢氧化铜反应生成红色沉淀的实验:首先NaOH溶液中加入几滴CuSO4溶液,发生复分解反应生成氢氧化铜沉淀和硫酸钠,其次氢氧化铜具有氧化性,氧化醛基,本身被还原为砖红色的氧化亚铜,利用该反应也可检验醛基的存在.关键操作是反应要在碱性溶液中进行.从而使醛的氧化加快,同时避免生成大量的氢氧化铜沉淀.
13.【答案】B,C
【知识点】取代反应;消去反应;水解反应
【解析】【解答】A.发生水解反应生成醇,则只断裂C-X,即图中①,故A不符合题意;
B.发生消去反应,断裂C-X和邻位C上的C-H键,则断裂①③,故B符合题意;
C.发生水解反应(取代反应)生成醇时,则只断裂C-X,即图中①,故C符合题意;
D.发生消去反应,断裂C-X和邻位C上的C-H键,则断裂①③,故D不符合题意;
故答案为:BC。
【分析】卤代烃的水解反应实质上就是取代反应,反应中一X被一OH取代了,所以被破坏的只有①;卤代烃的消去反应是相邻两个碳原子上的一个一X和一个一H一同被脱去,而生成不饱和烃和卤化氢的反应,被破坏的键应该是①和③。
14.【答案】C,D
【知识点】消去反应;水解反应
【解析】【解答】解:A.CH3CH2CH2CH2Cl可水解CH3CH2CH2CH2OH,发生消去反应生成CH3CH2CH=CH2,故A不选;
B.CH3CH2Cl可发生水解反应生成CH3CH2OH,发生消去反应生成CH2=CH2,故B不选;
C.CH3Br没有邻位C,不能发生消去反应,CH3Br水解生成CH3OH,故C选;
D. 没有邻位C,不能发生消去反应,可发生水解反应生成醇,故D选;
故选CD.
【分析】由选项可知,均为卤代烃,均可发生水解反应,与﹣X相连C的邻位C上有H可发生消去反应,以此来解答.
15.【答案】B,D
【知识点】取代反应;加成反应;消去反应;酯化反应
【解析】【解答】A.酯化反应的规律是羧酸脱去羟基,醇脱去氢原子,生成酯基,则酯化反应不能引入羟基,故A不符合题意;
B.取代反应可引入羟基,例如卤代烃水解、酯的水解是取代反应,都能引入羟基,故B符合题意;
C.消去反应是消除羟基,不会引入羟基,故C不符合题意;
D.加成反应可引入羟基,如乙烯水化制取乙醇,故D符合题意;
本题答案BD。
【分析】卤代烃的取代可以生成羟基,烯烃的加成也可以生成羟基。
16.【答案】(1)N(CH2CH3)3;CH3— —NH2;;CH2=CHCONH2
(2)伯胺;叔胺;仲胺
(3);
【知识点】酰胺
【解析】【解答】(1)三乙胺的结构简式为N(CH2CH3)3。
对甲基苯胺的结构简式为。
N,N-二甲基甲酰胺的结构简式为。
丙烯酰胺的结构简式为:CH2=CHCONH2。
(2)环己胺的结构简式为,其氮原子上连接有一个烃基,属于伯胺;
三甲胺的结构简式为N(CH3)3,其氮原子上连接有三个烃基,属于叔胺;
二苯胺的结构简式为,其氮原子上连接有两个烃基,属于仲胺。
(3)苯胺与盐酸反应生成,该反应的化学方程式为:。
甲酰胺与NaOH反应生成HCOONa和NH3,该反应的化学方程式为:。
【分析】(1)根据名称书写有机物的结构简式。
(2)氮原子上连接有一个烃基的为伯胺,连接有两个烃基的为仲胺,连接有三个烃基的为叔胺。
(3)苯胺与盐酸反应生成;甲酰胺的结构简式为,与NaOH溶液反应生成HCOONa和NH3,据此写出反应的化学方程式。
17.【答案】(1)球形冷凝管
(2)分水器中液面不再变化
(3)、
(4)C
【知识点】酯化实验;酯化反应
【解析】【解答】甲基丙烯酸与甲醇发生酯化反应生成甲基丙烯酸甲酯和水,当分水器内液面不再变化时说明反应结束;
(1)A装置的名称是球形冷凝管;
(2)当分水器中液面不再变化,停止加热;
(3)已知甲基丙烯酸甲酯受热易聚合,上述实验可能发生加聚反应或甲醇发生分子间发生取代反应,生成的副产物结构简式为 、等。
(4)A.该实验中,浓硫酸的作用之一是作吸水剂,吸收反应生成的水,促进平衡向正反应方向移动,提高了产率,A项正确;B.酯化反应中若生成的酯的密度比水大,则酯沉在分水器中水下,水从分水器中流入圆底烧瓶内,不能提高反应物的转化率,B项正确;C.洗涤剂X是一组试剂,产物要依次用饱和。溶液去除甲基丙烯酸、饱和溶液洗去甲基丙烯酸甲酯中溶解的、饱和溶液吸收甲醇和水,C项不正确;D.为了提高蒸馏速度,最后一步蒸馏可采用减压蒸馏;该步骤一定不能用常压蒸馏,防止甲基丙烯酸甲酯受热聚合,D项正确;
故答案为:C。
【分析】(1)根据仪器构造可知,A为球形冷凝管;
(2)当分水器内液面不再变化时说明反应结束;
(3)甲基丙烯酸甲酯受热易聚合,则可能发生加聚反应或甲醇发生分子间发生取代反应;
(4)A.浓硫酸具有吸水性;
B.若生成的酯的密度比水大,酯沉在分水器中水下,水从分水器中流入圆底烧瓶内,不能提高反应物的转化率;
C. 饱和Na2CO3去除甲基丙烯酸、饱和NaCl溶液洗去甲基丙烯酸甲酯中溶解的碳酸钠、饱和氯化钙溶液吸收甲醇和水;
D.甲基丙烯酸甲酯受热聚合。
18.【答案】(1)AC;2CH3(CH2)5CH2OH+O2 2CH3(CH2)5CHO+2H2O
(2)D
(3)NaHCO3
(4)A;
【知识点】饱和烃与不饱和烃;同分异构现象和同分异构体;乙醇的化学性质;水解反应
【解析】【解答】(1) A. α-C上有1个H原子,能被氧化为酮; B. α-C上没有H原子,不能发生催化氧化;
C. α-C上有1个H原子,能被氧化为酮;D.CH3(CH2)5CH2OH α-C上有2个H原子,能被氧化为醛;可以发生催化氧化生成酮的是AC。CH3(CH2)5CH2OH能被氧化为醛,反应的化学方程式是2CH3(CH2)5CH2OH+O2 2CH3(CH2)5CHO+2H2O;
(2) A.吃馒头时多咀嚼后有甜味,是淀粉在唾液淀粉酶作用下水解为麦芽糖,故不选A;
B.在酸性环境下,淀粉发生水解变成葡萄糖,加碘不显蓝色,故不选B;
C. 油脂属于酯类,在碱性条件下水解为高级脂肪酸钠和甘油,故不选C;
D.不慎将浓硝酸沾到皮肤上会出现黄色斑痕,发生蛋白质的颜色反应,不是水解,
故答案为:D;
(3)酸性-COOH>H2CO3>酚-OH>HCO3-,能将 转化为 的试剂是NaHCO3;
① 与Br21:2发生加成反应生成 ; 与Br2 1:1发生1,4加成反应生成 ; 与Br2 1:1发生1,2加成反应生成 或 ,不可能生成 ,
故答案为:A;
②根据 + , 和 发生双烯合成反应的产物是 ;
【分析】(1)α-C上有1个H原子的醇能被氧化为酮;
(2)根据糖类、油脂、蛋白质的性质判断;
(3)根据酸性-COOH>H2CO3>酚-OH>HCO3-判断;
(4) ①共轭二烯烃能以1,4和1,2两种形式发生加成反应;
②根据 + 判断1-丁烯和2,3-二甲基-1,3-丁二烯发生双烯合成反应的产物;
19.【答案】(1)苯乙烯
(2)取代反应
(3)NaOH水溶液;加热
(4)C15H14O
(5)羟基、羧基
(6) 或 或
(7) +HBr ;2 +O2 2 +2H2O
【知识点】利用质谱、红外光谱、核磁共振等确定有机物的结构;同分异构现象和同分异构体;取代反应;加成反应;水解反应
【解析】【解答】(1)A的结构简式为 ,名称为苯乙烯,故答案为:苯乙烯;
(2)由F生成G的反应为 与三氯化磷发生取代反应生成 ,故答案为:取代反应;
(3)B→C的反应为 在氢氧化钠溶液中共热发生水解反应生成 ,故答案为:NaOH水溶液;加热;
(4)H的结构简式为 ,分子式为C15H14O,故答案为:C15H14O;
(5)Ⅰ的结构简式为 ,含有的官能团为羟基、羧基,故答案为:羟基、羧基;
(6)F的结构简式为 ,F的同分异构体为酯类芳香族化合物,说明分子中含有酯基,核磁共振氢谱为四组峰说明分子中含有4类氢原子,则符合峰面积比为1:2:2:3的同分异构体的结构简式为 、 、 ,故答案为: 或 或 ;
(7)A→B的反应为在过氧化物作用下, 与溴化氢发生加成反应生成 ,反应的化学方程式为 +HBr ;C→D的反应为在铜做催化剂作用下, 与氧气发生催化氧化反应生成 ,反应的化学方程式为2 +O2 2 +2H2O,故答案为:2 +O2 2 +2H2O。
【分析】由D的结构简式和有机物转化的反应条件可知,C为 ,则B为 、A为 ; 在加热条件下与新制氢氧化铜发生氧化反应生成 ,则E为 ; 经酸化生成 ,则F为 ; 与三氯化磷发生取代反应生成 ,则G为 ;在氯化铝作用下, 与甲苯发生取代反应生成 , 发生信息Ⅱ反应生成 ,则I为 ;在浓硫酸作用下, 共热发生消去反应生成 ,则J为 。
20.【答案】(1)同系物;取代反应
(2)C9H16O5
(3)银氨溶液或新制氢氧化铜都呈碱性,氧化醛基时会使酯基水解
(4)
(5)
(6)
(7)
【知识点】同分异构现象和同分异构体;酯的性质
【解析】【解答】(1)为乙酸乙酯和互为同系物。的反应类型是取代反应反应。故答案为:同系物;取代反应;
(2)的分子式C9H16O5。故答案为:C9H16O5;
(3)不宜选用银氨溶液或新制氢氧化铜的原因是:银氨溶液或新制氢氧化铜都呈碱性,氧化醛基时会使酯基水解。故答案为:银氨溶液或新制氢氧化铜都呈碱性,氧化醛基时会使酯基水解;
(4)根据信息i. R1COOR2+R3OHR1COOR3+R2OH,发生反应生成G和乙醇,的结构简式为:。故答案为:;
(5)3-四氢呋喃甲醇,分子式为C5H10O2 ,不饱和度为1,3-四氢呋喃甲醇有多种同分异构体,符合①不能与金属钠反应,分子中没有羧基和羟基, ②分子中有3种不同化学环境的氢原子,符合条件的有机物的结构简式如:。故答案为:;
(6)E分子的中间碳原子上有2个H原子,均可与环氧乙醚反应,时会生成分子式为的副产物,该副产物的结构简式是。故答案为:;
(7)以为原料,先用将其还原为,在一定条件下脱水得,在铜催化加热条件下将羟基氧化为醛基,得到产物,合成路径为。故答案为:。
【分析】B催化氧化生成D,则D的结构简式为, D与乙醇发生酯化反应生成E,E与环氧乙烷发生开环加成生成F,F发生信息i中酯交换反应脱去1分子CH3CH2OH生成G,G发生信息ii中还原反应生成H,H发生信息iii中反应脱去1分子水生成3-四氢呋喃甲醇,则G为,H为。
21.【答案】(1)(或);取代反应(或酯化反应)
(2)羧基、(酚)羟基
(3)
(4)10;、
【知识点】有机物中的官能团;同分异构现象和同分异构体;酯的性质;取代反应
【解析】【解答】(1)苯与Cl2发生取代反应,其条件为Fe或FeCl3做催化剂,因此条件X是Fe或FeCl3。
反应⑤中与发生反应生成,该反应的反应类型为取代反应。
(2)水杨酸的结构简式为,因此其所含的官能团为羧基、酚羟基。
(3)阿司匹林的结构简式为,其所含的官能团羧基、酯基都能与NaOH溶液反应,且酯基水解产生酚羟基,也能与NaOH溶液反应,因此阿司匹林与NaOH溶液反应的化学方程式为:。
(4)既不能发生水解反应,也不能发生银镜反应,说明分子结构中不含有-COOR和-CHO;1mol该有机物能与2molNaHCO3反应,说明分子结构中含有2mol-COOH。由于一分子阿司匹林中含有9个碳原子,因此其同分异构中含有苯环、2个-COOH,同时还剩余一个碳原子。
若该同分异构体为苯的三取代物,则剩余的碳原子为-CH3,该同分异构体共有6种;
若该同分异构体为苯的二取代物,则苯环上的取代基可以为-COOH、-CH2COOH,该同分异构体共有3种;
若该同分异构体为苯的一取代物,则苯环上的取代基为-CH(COOH)2,则该同分异构体有1种。
因此满足条件的同分异构体共有6+3+1=10种。
核磁共振氢谱有四组峰,且峰面积之比为1:2:2:3,说明分子结构具有对称性,且含有-CH3,2个-COOH处于对称位置,因此满足条件的同分异构体的结构简式为、。
【分析】A为芳香烃,且其相对分子质量为78,由“商余法”,因此A的分子式为C6H6,故A的结构简式为。A与Cl2发生取代反应生成B,因此B的结构简式为。B在NaOH浓溶液的和加热的条件下,发生取代反应,生成C,因此C的结构简式为。C与CO2反应生成。在H+作用下反应生成水杨酸,水杨酸的结构简式为。
22.【答案】(1)c(Cl-)>c(NH4+)>c(H+)>c(OH-);NH4Cl
(2)氯化铵分解吸收热量,降低了温度;氯化铵分解产生的气体隔绝了空气等
【知识点】盐类水解的原理;铵盐;水解反应
【解析】【解答】(1)氯化铵是强酸弱碱盐,在饱和溶液中,NH4+发生水解反应而消耗,所以c(Cl-)>c(NH4+),NH4+水解消耗水电离产生的OH-,最终达到平衡时,溶液中c(H+)>c(OH-),但盐水解产生的离子浓度是微弱的,因此c(NH4+)>c(H+),故溶液中离子浓度由大到小的顺序为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);浸过氯化铵溶液的布条不燃烧,冒出白烟,是由于将布条灼烧时,氯化铵发生分解反应NH4Cl NH3↑+HCl↑,反应产生的气体在空气中相遇,会发生反应:NH3+HCl=NH4Cl,因此看到的白烟为NH4Cl;(2)浸过氯化铵溶液的布条不燃烧、不易着火的主要原因是氯化铵分解吸收热量,降低了布条周围的温度,不能达到相应物质的着火点;而且氯化铵分解产生的氨气和HCl气体充满在布条周围,隔绝了空气,使着火物不能接触空气,不具备着火燃烧的条件。
【分析】(1)氯化铵是强酸弱碱盐,水解呈酸性,即可得出本题答案;根据方程式NH4Cl NH3↑+HCl↑,即可得出本题答案
(2)氯化铵分解产生的氨气和HCl气体充满在布条周围,隔绝了空气,使着火物不能接触空气,不具备着火燃烧的条件
23.【答案】(1)CH3CH2OH CH2=CH2↑+H2O;消去反应
(2)CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;乙酸
(3)CH3CH2Br+NaOH CH3CH2OH+NaBr;醇
(4) +HNO3 +H2O;取代反应
【知识点】乙烯的实验室制法;取代反应;酯化反应
【解析】【解答】(1)乙醇和浓硫酸混合物加热到170℃发生消去反应生成乙烯,方程式是CH3CH2OH CH2=CH2↑+H2O;反应类型是消去反应;
(2)乙酸与乙醇的反应生成乙酸乙酯和水,反应方程式是CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O,发生酯化反应时,酸脱羟基醇脱氢,所以水中氧元素的来源是乙酸;
(3)溴乙烷与氢氧化钠水溶液共热发生取代反应生成乙醇和溴化钠,反应方程式是CH3CH2Br+NaOH CH3CH2OH+NaBr,此反应将卤代烃类物质转化为醇类物质;
(4)苯与浓硫酸、浓硝酸的混合酸在加热时发生反应生成硝基苯和水,反应方程式是 +HNO3 +H2O,反应类型是取代反应。
【分析】(1)乙醇和浓硫酸混合物加热到170℃发生消去反应生成乙烯,结合消去反应的特征分析;
(2)乙酸与乙醇在浓硫酸加热的条件下发生酯化反应,据此分析;
(3)溴乙烷与氢氧化钠水溶液共热发生取代反应生成乙醇和溴化钠;
(4)苯与浓硫酸、浓硝酸的混合酸在加热时发生反应生成硝基苯和水,书写方程式时注意标注反应条件,据此解答。
试题分析部分
1、试卷总体分布分析
总分:85分
分值分布 客观题(占比) 30.0(35.3%)
主观题(占比) 55.0(64.7%)
题量分布 客观题(占比) 15(65.2%)
主观题(占比) 8(34.8%)
2、试卷题量分布分析
大题题型 题目量(占比) 分值(占比)
选择题 8(34.8%) 16.0(18.8%)
非选择题 8(34.8%) 55.0(64.7%)
多选题 7(30.4%) 14.0(16.5%)
3、试卷难度结构分析
序号 难易度 占比
1 普通 (30.4%)
2 困难 (69.6%)
4、试卷知识点分析
序号 知识点(认知水平) 分值(占比) 对应题号
1 极性键和非极性键 2.0(2.4%) 4
2 羧酸简介 2.0(2.4%) 10
3 乙酸的化学性质 4.0(4.7%) 4,9
4 离子方程式的书写 2.0(2.4%) 1
5 “手性分子”在生命科学等方面的应用 2.0(2.4%) 10
6 有机物中的官能团 8.0(9.4%) 11,21
7 苯的同系物及其性质 2.0(2.4%) 2
8 乙醇的化学性质 9.0(10.6%) 2,18
9 醛与Cu(OH)2的反应 2.0(2.4%) 7
10 盐类水解的应用 2.0(2.4%) 8
11 消去反应 6.0(7.1%) 13,14,15
12 利用质谱、红外光谱、核磁共振等确定有机物的结构 9.0(10.6%) 19
13 酰胺 9.0(10.6%) 16
14 共价键的形成及共价键的主要类型 2.0(2.4%) 11
15 同分异构现象和同分异构体 34.0(40.0%) 2,3,18,19,20,21
16 盐类水解的原理 5.0(5.9%) 8,22
17 乙烯的实验室制法 8.0(9.4%) 23
18 加成反应 15.0(17.6%) 5,7,15,19
19 催化剂 2.0(2.4%) 4
20 水解反应 33.0(38.8%) 2,5,7,8,10,13,14,18,19,22
21 铵盐 3.0(3.5%) 22
22 酯化实验 7.0(8.2%) 12,17
23 饱和烃与不饱和烃 7.0(8.2%) 18
24 酯化反应 17.0(20.0%) 10,15,17,23
25 酯的性质 24.0(28.2%) 1,3,5,6,11,20,21
26 苯酚的性质及用途 4.0(4.7%) 1,6
27 取代反应 29.0(34.1%) 5,13,15,19,21,23
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
