3.3 醛酮 同步测试题(含解析)2023-2024学年高二下学期化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.3 醛酮 同步测试题(含解析)2023-2024学年高二下学期化学人教版(2019)选择性必修3 |  | |
| 格式 | docx | ||
| 文件大小 | 267.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-15 15:45:26 | ||
图片预览




文档简介
3.3 醛酮 同步测试题
2023-2024学年高二下学期化学人教版(2019)选择性必修3
一、单选题
1.下列说法不正确的是( )
A.液化石油气是纯净物
B.工业酒精中往往含有甲醇
C.福尔马林是甲醛的水溶液
D.许多水果和花卉有芳香气味是因为含有酯
2.化学与科技、社会、生产、生活密切相关。下列有关说祛错误的是()
A.用食醋可除去热水壶内壁的水垢
B.75%(体积分数)的乙醇溶液常用于医疗消毒
C.35%~40%的甲醛溶液俗称福尔马林,可用来浸泡海产品以达到保鲜效果
D.用浸泡过高锰酸钾溶液的硅土吸收水果释放出的乙烯,可达到水果保鲜的目的
3.下列关于乙醇的叙述中,错误的是( )
A.乙醇俗称酒精 B.乙醇可与金属钠反应
C.乙醛经氧化可生成乙醇 D.乙醇能与水任意比例互溶
4.化学与生活密切相关。下列说法错误的是( )
A.乙烯可作水果的催熟剂 B.硅胶可作袋装食品的干燥剂
C.福尔马林可作食品的保鲜剂 D.氢氧化铝可作胃酸的中和剂
5.在医院对某类病人的尿液进行检查时常把氢氧化钠溶液和硫酸铜溶液加入到其尿液中并加热,如果观察到有红色沉淀出现,说明该尿液中含有( )
A.食醋 B.白酒 C.食盐 D.葡萄糖
6.化学与生产、生活息息相关。下列说法错误的是( )
A.甜度仅为蔗糖40%的麦芽糖既能发生水解反应,又能发生银镜反应
B.乙醇的体积分数为75%的医用酒精能使细菌蛋白质发生变性
C.用纤维素制取硝酸纤维的过程中发生了酯化反应
D.5G技术中使用的光导纤维不与任何酸碱反应
7.乙醛与新制氢氧化铜悬浊液反应的实验如下:
步骤1:向试管中加入2mL10%NaOH溶液,边振荡边滴加4~6滴2%CuSO4溶液,观察到有蓝色絮状沉淀产生。
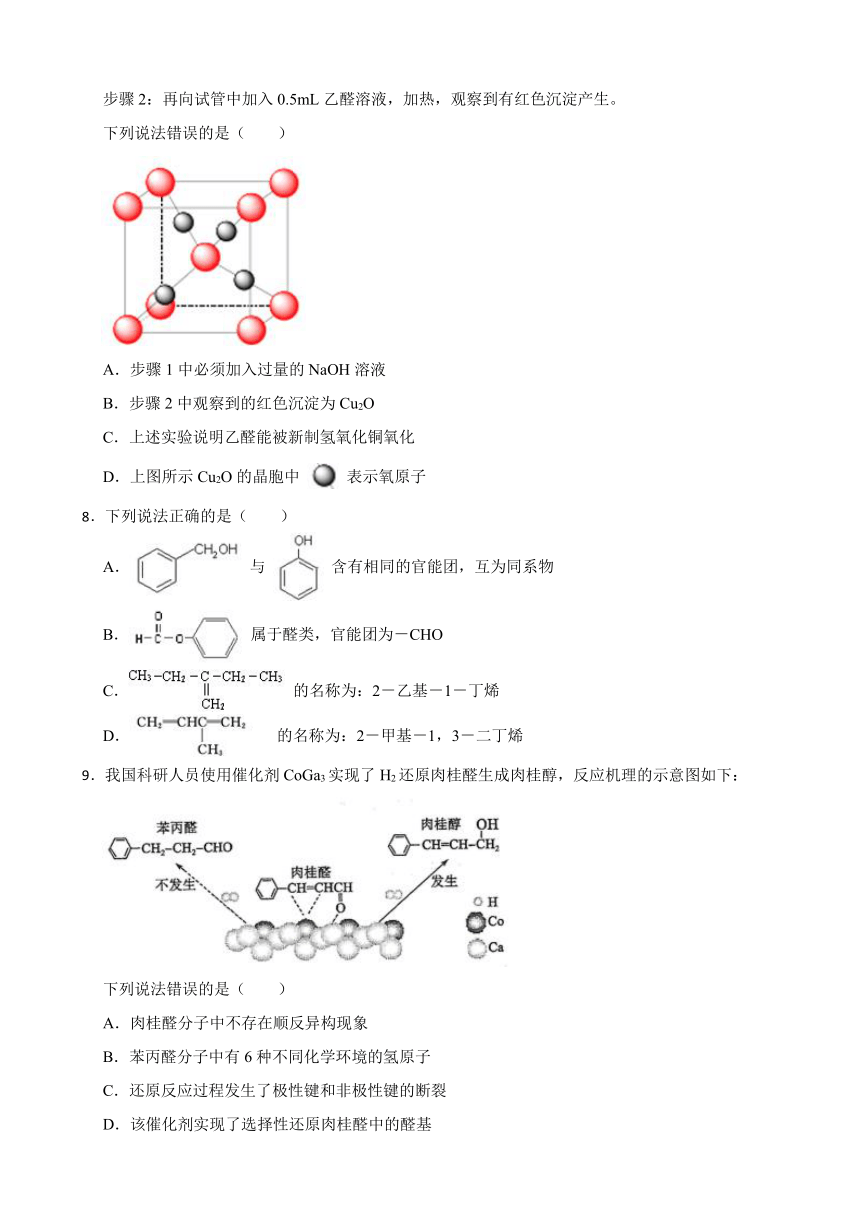
步骤2:再向试管中加入0.5mL乙醛溶液,加热,观察到有红色沉淀产生。
下列说法错误的是( )
A.步骤1中必须加入过量的NaOH溶液
B.步骤2中观察到的红色沉淀为Cu2O
C.上述实验说明乙醛能被新制氢氧化铜氧化
D.上图所示Cu2O的晶胞中 表示氧原子
8.下列说法正确的是( )
A. 与 含有相同的官能团,互为同系物
B. 属于醛类,官能团为-CHO
C. 的名称为:2-乙基-1-丁烯
D. 的名称为:2-甲基-1,3-二丁烯
9.我国科研人员使用催化剂CoGa3实现了H2还原肉桂醛生成肉桂醇,反应机理的示意图如下:
下列说法错误的是( )
A.肉桂醛分子中不存在顺反异构现象
B.苯丙醛分子中有6种不同化学环境的氢原子
C.还原反应过程发生了极性键和非极性键的断裂
D.该催化剂实现了选择性还原肉桂醛中的醛基
10.下列反应中,有机物被还原的是 ( )
A.乙醛的银镜反应 B.乙醛制乙醇
C.乙醇制乙醛 D.乙醇制乙烯
11.具有防腐作用的甲醛 ( )
A.分子中共有12个电子 B.能发生加聚反应
C.难溶于水易溶于酒精 D.比例模型为:
12.用丙醛CH3CH2CHO制取聚丙烯 的过程中发生的反应类型为( )
①取代反应;②消去反应;③加聚反应;④还原反应;⑤氧化反应
A.④②③ B.⑤②③ C.①④③ D.②④⑤
13.化学与日常生活紧密相关.下列说法中,不正确的是( )
A.甲醛可作食品防腐剂 B.氢氧化铝可作抗酸药
C.氯化钠可作食品调味剂 D.生石灰可作食品干燥剂
14.乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为CH2=C=O+HA → CH3-CO-A。乙烯酮在一定条件下可与下列试剂加成,其产物错误的是( )
A.与HCl加成生成CH3COCl
B.与H2O加成生成CH3COOH
C.与CH3COOH加成生成CH3COOCOCH3
D.与CH3OH加成生成CH3COCH2OH
15.对人体健康不会造成危害的是( )
A.用工业酒精(含甲醇)兑制饮用酒
B.用食醋除去水壶内壁的水垢
C.用甲醛溶液浸泡海产品进行防腐保鲜
D.在不通风、无防护的条件下做实验
16.探究甲醛与新制的Cu(OH)2的反应:
⑴向6mL 6mol·L-1NaOH溶液中滴加8滴2%CuSO4溶液,振荡,加入0.5mL15%甲醛溶液,混合均匀,水浴加热,生成红色沉淀同时产生无色气体。
⑵反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解。
已知: ,甲醛是具有强还原性的气体。下列说法错误的是( )
A.如图所示铜的晶胞中Cu原子的配位数为12
B.红色沉淀的主要成分不是Cu2O,可能是Cu
C.将产生的无色气体通过灼热的CuO后得到红色固体,说明生成的气体中一定是CO
D.从甲醛的结构推测,其氧化产物还可能有CO
17.某学生做乙醛还原性的实验,取1mol/L的硫酸铜溶液2mL和0.4mol/L的氢氧化钠溶液4mL,在一个试管内混合后加入0.5mL40%乙醛溶液加热至沸,无红色沉淀。失败的原因是( )
A.氢氧化钠的量不够 B.硫酸铜的量不够
C.乙醛溶液太少 D.加热时间不够
18.某有机物化学式为C5H10O,它能发生银镜反应和加成反应,若将它与H2加成,所得产物的结构简式可能是( )
A.(CH3)3CCH2OH B.(CH3CH2)2CHOH
C.CH3(CH2)2CH(CH3)OH D.CH3CH2C(CH3)2OH
19.某甲酸溶液中可能存在着甲醛,下列操作能正确说明的是( )
A.试液与足量NaOH溶液混合其蒸馏产物可发生银镜反应,则有甲醛
B.能发生银镜反应,证明含甲醛
C.加入新制Cu(OH)2加热,有红色沉淀生成,证明一定存在甲醛
D.先将试液充分进行酯化反应收集生成物进行银镜反应,有银镜产生,则含甲醛
20.“绿色化学”提倡“原子经济性”。理想的“原子经济性”反应中,原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合“原子经济性”的是( )
A.乙烯与氢气在一定条件下制乙烷
B.乙烷与氯气反应制一氯乙烷
C.乙醇催化氧化制乙醛
D.甲苯与浓硝酸、浓硫酸的混合酸制TNT
二、综合题
21.完成方程式。
(1)乙醇的催化氧化方程式:
(2)乙醛和新制的氢氧化铜(氢氧化钠过量)反应方程式:
(3)乙醛和酸性高锰酸钾反应的离子方程式:
(4)苯酚和溴水反应方程式:
(5)乙酸苯酚酯和足量氢氧化钠溶液反应方程式:
22.按要求回答下列问题:
(1)制造烈性炸药TNT的化学方程式是 。
(2)由 生成顺式聚合物的结构简式是 。
(3)由1-氯丁烷制取少量的1,2-丁二醇时,需要经过的反应类型是 反应→ 反应→ 反应。
(4)“一滴香”是一种毒性很强的物质,被人食用后会损伤肝脏,还能致癌.其分子结构如图所示,用该有机物 (填“能”或“不能”)萃取溴水中的溴。
(5)某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
该物质中所含官能团的名称为 。
(6) 和 发生酯化反应的化学方程式是 。
(7)乙醛和新制的 反应的离子方程式是 。
23.按要求书写下列化学方程式:
(1)丙烯的加聚
(2)1,3﹣丁二烯与等物质的量的单质溴在60℃时发生1,4﹣加成
(3)甲苯制备TNT
(4)1,2﹣二溴乙烷与氢氧化钠水溶液共热:
(5)乙醛的还原:
(6)乙二醇和乙二酸脱水成二元环酯 .
24.确定以下各项的n值:
(1)饱和一元醇的通式是 ,醇出现同分异构体时,n的最小值是 ;醇出现同类异构体时,n的最小值是 .n值一定的醇与浓硫酸共热,只能得到一种不饱和烃,符合上述结果的n值是 或 .
(2)饱和一元醛的通式为 ,醛出现稳定的同分异构体时,n的最小值是 ;醛出现同类异构体时,n的最小值是 .
(3)饱和一元脂肪酸的通式为CnH2nO2,羧酸出现同分异构体时,n最小值是 ,羧酸出现同类异构体时,n的最小值是 .
25.有机物M的结构简式为,N的结构简式为。回答下列问题:
(1)M的化学名称为 。
(2)写出M与足量浓溴水反应的化学方程式: 。
(3)写出同时满足下列条件的N的同分异构体的结构简式: 。
①苯环上连有两个取代基
②能发生水解反应
③核磁共振氢谱有两组峰且峰面积比为
(4)写出N在催化和加热条件下发生反应的化学方程式: 。
(5)写出N与足量新制悬浊液加热发生反应的化学方程式: 。
答案解析部分
1.【答案】A
【解析】【解答】A.液化石油气中含有多种物质,属于混合物,选项A符合题意;
B.工业酒精中往往含有甲醇,不能利用工业酒精勾兑白酒,选项B不符合题意;
C.福尔马林是含甲醛37%-40%的水溶液,选项C不符合题意;
D.水果与花卉中存在酯类,具有芳香气味,选项D不符合题意;
故答案为:A。
【分析】A.液化石油气是以丙烷和丁烷为主要成分的混合物;
B.甲醇是工业酒精的原料;
C.甲醛的水溶液俗称福尔马林;
D.酯类具有特殊香味。
2.【答案】C
【解析】【解答】A.食醋中含有醋酸,水垢的主要成分是碳酸钙和氢氧化镁,因此用食醋可除去热水壶内壁的水垢,A不符合题意;
B.75%(体积分数)的乙醇溶液能使蛋白质变性,常用于医疗消毒,B不符合题意;
C.35%~40%的甲醛溶液俗称福尔马林,但甲醛有毒,不能用来浸泡海产品以达到保鲜效果,C符合题意;
D.高锰酸钾能氧化乙烯,因此可用浸泡过高锰酸钾溶液的硅土吸收水果释放出的乙烯,可达到水果保鲜的目的,D不符合题意。
故答案为:C。
【分析】A.醋酸的酸性比碳酸强;
B.消毒用的酒精质量分数是75%;
C.甲醛有毒不能用于海产品的保险;
D.乙烯具有催熟效果,酸性高锰酸钾能够氧化乙烯。
3.【答案】C
【解析】【解答】A.乙醇是一种有机物,俗称酒精,故A不符合题意;
B.乙醇可与金属钠发生置换反应生成乙醇钠和氢气,故B不符合题意
C.乙醛与氢气发生加成反应可生成乙醇,该过程为还原反应,故C符合题意;
D.乙醇分子之间、水分子之间都有氢键,根据相似相溶原理,乙醇能与水任意比例互溶,故D不符合题意;
故答案为:C。
【分析】乙醇俗名叫酒精,乙醇具有羟基可发生取代、消去以及与钠发生置换反应,与水形成氢键可以与水互溶
4.【答案】C
【解析】【解答】A、乙烯是一种植物生长调节剂,可作水果的催熟剂,A不符合题意;
B、硅胶多孔,吸收水分能力强,可作袋装食品的干燥剂,B不符合题意;
C、福尔马林是甲醛的水溶液,甲醛有毒,不能作食品的保鲜剂,C符合题意;
D、氢氧化铝属于两性氢氧化物能与酸反应,可作胃酸的中和剂,D不符合题意,
故答案为:C。
【分析】A.乙烯是一种植物生长调节剂;
B.硅胶的表面积较大,可作干燥剂;
C.福尔马林是甲醛的水溶液,有毒;
D.氢氧化铝是两性氢氧化物,能够中和胃酸中的盐酸。
5.【答案】D
【解析】【解答】A.食醋的化学式CH3COOH,分子结构中不含有-CHO,A不符合题意;
B.白酒的化学式为CH3CH2OH,分子结构中不含有-CHO,B不符合题意;
C.食盐的化学式为NaCl,不含有-CHO,C不符合题意;
D.葡萄糖结构简式为CH2OH(CHOH)4CHO,分子结构中含有-CHO,D符合题意;
故答案为:D
【分析】能与新制Cu(OH)2悬浊液反应产生砖红色沉淀,则说明尿液中所含物质含有-CHO,据此结合选项所给物质进行分析。
6.【答案】D
【解析】【解答】A.麦芽糖分子结构中有醛基,具有还原性是一种还原糖。因此可以与银氨溶液发生银镜反应,也可以与新制碱性氢氧化铜反应生成砖红色沉淀。可以在一定条件下水解,生成两分子葡萄糖,故A不符合题意;
B.乙醇可以提供自己的羟基或羰基上的氢或氧去形成氢键,从而破坏了蛋白质中原有的氢键,使蛋白质变性,故B不符合题意;
C.纤维素分子中有羟基,能够与硝酸发生反应生成酯硝酸纤维和水,发生的是酯化反应,故C不符合题意;
D.D光导纤维成分是二氧化硅,可以和氢氧化钠反应SiO2+2NaOH=Na2SiO3+H2O,故D符合题意;
故答案为:D。
【分析】光导纤维中的物质是二氧化硅,可以和氢氟酸和氢氧化钠强碱反应,其他选项均正确
7.【答案】D
【解析】【解答】A.醛基和新制的氢氧化铜悬浊液反应时需要碱过量,故必须加入过量的氢氧化钠溶液,A不符合题意;
B.乙醛和新制的氢氧化铜悬浊液反应生成红色的氧化亚铜沉淀,B不符合题意;
C.实验生成乙酸铵,说明乙醛被氢氧化铜氧化,C不符合题意;
D.晶胞中红色球有 ,黑色球有4个,所以结合氧化亚铜的化学式分析,黑色球表示铜原子,D符合题意;
故答案为:D。
【分析】根据红球和黑球的占位计算出晶胞中铜原子和氧原子的个数比即可
8.【答案】C
【解析】【解答】A. 前者—OH与苯环的侧链相连,属于醇类,后者—OH直接与苯环相连,属于酚类,尽管分子构成相差了1个CH2,但是二者不是同一类物质,所以它们不互为同系物,A不符合题意;
B. 该物质属于酯类(甲酸酯,含有醛基),官能团为酯基, B不符合题意;
C. 该物质的官能团为碳碳双键,含有官能团的最长的碳链有4个C,因此主链含有4个C,为丁烯;编号时官能团的编号要小,因此碳碳双键的编号为1,乙基的编号为2,命名为2-乙基-1-丁烯,C符合题意;
D. 该物质中含有2个碳碳双键,且含有碳碳双键最长的碳链有4个碳原子,因此该物质为丁二烯。编号时,不管是从左端还是右端,碳碳双键的编号均为1、3,因此编号的选择,让甲基的编号的编号小,甲基的编号为2,则该物质的名称应为:2-甲基-1,3-丁二烯,D不符合题意。
故答案为:C
【分析】A. 注意属于醇,属于酚;
B. 该物质为甲酸和苯酚形成的酯类;
C. 该物质按烯烃来命名;
D. 该物质按双烯烃来命名。
9.【答案】A
【解析】【解答】A.肉桂醛分子中每个双键碳原子所连接的原子或原子团都不同,所以存在顺反异构现象,A符合题意;
B.苯丙醛分子中,苯环上有3种不同化学环境的氢原子,另外还有3种不同的氢原子,所以共有6种不同化学环境的氢原子,B不符合题意;
C.还原反应过程,发生了醛基上极性键的断裂和氢分子中非极性键的断裂,C不符合题意;
D.在该催化剂作用下,只有醛基被还原,碳碳双键和苯基没有被还原,所以实现了选择性还原肉桂醛中的醛基,D不符合题意;
故答案为:A。
【分析】A.肉桂醛中存在碳碳双键,碳碳双键中的碳原子连接的有相同的原子,因此存在顺反异构
B.找出苯丙醛分子中的氢原子的种类,苯环高度对称,故有3种不同种类的氢原子,在支链上有3种氢原子
C.还原反应时,氢气的非极性键的断裂,碳氧键的断裂是极性键的断裂
D.根据图示发现,只有醛基被还原,双键没有被还原故具有选择性
10.【答案】B
【解析】【解答】乙醛的银镜反应被氧化,乙醇制乙醛氧化反应,乙醇加水加成制乙烯。乙醛制乙醇是还原反应,加氢还原。
【分析】有机反应中还原反应判断方法一:“加氢或去氧”有机物的变化是氢原子多了或者氧原子少了,即是还原反应。
方法二:根据有机物中碳元素的化合价的变化进行判断,注意标化合价的原则是氢元素是+1,O是-1价。最后标碳元素。
11.【答案】B
【解析】【解答】解:A.甲醛的电子式为: ,核外共有电子数=8+6+2=16,故A错误;
B.甲醛的结构式为 ,含有碳氧双键能发生加聚反应,故B正确;
C.甲醛是极性分子,水是极性分子,乙醇是极性分子,根据相似相溶原理,甲醛易溶于水,也易溶于酒精,故C错误;
D.比例模型中氧原子半径应大于氢原子的半径,故D错误;
故选B.
【分析】A.甲醛的分子式为CH2O,电子式为 ;
B.根据甲醛的结构式为 以及双键能发生加聚反应来分析;
C.根据相似相溶原理来解答;
D.根据比例模型中氧原子半径应大于氢原子的半径.
12.【答案】A
【解析】【解答】用CH3CH2CHO制取聚丙烯,可用逆推法: CH3CH=CH2 CH3CH2CH2OH CH3CH2CHO;第一步CH3CH2CHO与氢气发生加成反应得到CH3CH2CH2OH,该反应又可称为还原反应;第二步CH3CH2CH2OH发生消去反应得到丙烯;第三步丙烯发生加聚反应得到聚丙烯;
故答案为:A。
【分析】采用逆推法即可判断反应所有的产物以及发生法反应类型
13.【答案】A
【解析】【解答】解:A.甲醛有毒,能破坏蛋白质的结构,使之失去生理功能,所以不能用甲醛作食品防腐剂,故A错误;
B.抗酸药的有效成分为:碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等,氢氧化铝能与胃液中的盐酸反应,且自身对人无害,故B正确;
C.Na为人体不可缺少的元素,食盐可用于食品调味剂,具有咸味,故C正确;
D.生石灰能和水反应,所以可用生石灰作食品干燥剂,故D正确.
故选A.
【分析】A.甲醛有毒性,能使蛋白质发生变性;
B.氢氧化铝能与盐酸反应,且自身对人无害;
C.氯化钠具有咸味,常用作调味品;
D.生石灰能和水反应生成微溶于水的氢氧化钙.
14.【答案】D
【解析】【解答】A. 乙烯酮(CH2=C=O)与HCl加成,端点碳原子连氢,另一个碳原子连Cl,得到CH3COCl,故A不选;
B. 乙烯酮(CH2=C=O)与H2O加成,端点碳原子连氢,另一个碳原子连-OH,得到CH3COOH,故B不选;
C. 乙烯酮(CH2=C=O)与CH3COOH加成,端点碳原子连氢,另一个碳原子连CH3COO-,得到CH3COOCOCH3,故C不选;
D. 乙烯酮(CH2=C=O)与CH3OH加成,端点碳原子连氢,另一个碳原子连CH3O-,得到CH3COOCH3,故D选。
故答案为:D。
【分析】乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,碳碳双键断开,端点碳原子连氢,另一个碳原子连除了氢原子之外的另一个原子或原子团。
15.【答案】B
【解析】【解答】解:A.甲醇有毒,会危害人体健康,饮用工业酒精(含甲醇)兑制饮用酒会导致失明或死亡,故A错误;
B.醋酸对人体无害,而且醋酸能溶解水垢,所以可以用食醋除去水壶内壁的水垢,故B正确;
C.甲醛有毒,用甲醛保鲜海产品会危害人类健康,故C错误;
D.有些化学药品具有毒性,应该在通风、有防护的条件下做实验,否则会引起实验人员中毒,故D错误.
故选B.
【分析】A.甲醇有毒,会危害人体健康;
B.醋酸能溶解水垢;
C.甲醛有毒,会危害人体健康;
D.有些化学药品具有毒性.
16.【答案】C
【解析】【解答】A.根据铜的晶胞结构,铜为面心立方晶胞, Cu原子的配位数为12,故A不符合题意;
B. ,沉淀洗净后加入浓盐酸,不溶解,可知红色沉淀的主要成分不是Cu2O,可能是Cu,故B不符合题意;
C.将产生的无色气体通过灼热的CuO后得到红色固体,生成的气体中可能含有CO、HCHO,故C符合题意;
D.从甲醛的结构推测,甲醛可以氧化为甲酸,在碱溶液中生成甲酸盐,或被氧化为碳酸,碱溶液中反应生成碳酸盐,所以氧化产物还可能有CO ,故D不符合题意;
故答案为:C。
【分析】A.与铜原子的距离最近的铜原子有3层,每层有4个共12个
B.红色沉淀不溶于盐酸,可能是氧化亚铜或铜单质或者是混合物
C.甲醛易挥发,甲醛是具有强还原性的气体
D.根据甲醛的结构,即可判断产物可能是羧酸类,羧酸类继续反应
17.【答案】A
【解析】【解答】乙醛和新制氢氧化铜悬浊液发生反应的环境是在碱性条件下进行的,而根据题意可判断氢氧化钠溶液是不足的,硫酸铜过量,
故答案为:A。
【分析】此题考查醛的还原性的实验,根据醛还原的条件是碱性环境进行判断。
18.【答案】A
【解析】【解答】由题意知该物质的饱和的一元醛,-CHO加氢后为-CH2OH,只有A项符合要求
【分析】该有机物可以发生银镜反应,因此是醛类,在根据分子式和加成反应,可得出该醛的结构简式。
19.【答案】A
【解析】【解答】解:甲酸和甲醛都含有醛基,则直接加入新制备氢氧化铜浊液或银氨溶液不能鉴别是否含有甲醛,应先加入足量NaOH溶液混合,甲酸与氢氧化钠溶液反应生成难挥发的甲酸钠,然后蒸馏,可得到甲醛,再用银氨溶液或新制备氢氧化铜浊液鉴别,D中先将试液充分进行酯化反应,甲酸酯也可发生银镜反应,不能鉴别,所以B、C、D错误,故选A.
【分析】甲酸中含有醛基和羧基,甲醛中只含醛基,不能直接用银氨溶液鉴别,应先分离后再鉴别,以此解答.
20.【答案】A
【解析】【解答】A.乙烯和氢气在一定条件下制乙烷,是加成反应,原子利用率100%,A符合题意;
B.乙烷和氯气反应制一氯乙烷,是取代反应,原子利用率不是100%,B不符合题意;
C.乙醇催化氧化制乙醛,是氧化反应,原子利用率不是100%,C不符合题意;
D.甲苯和浓硝酸、浓硫酸的混合酸制TNT,是取代反应,原子利用率不是100%,D不符合题意;
故答案为:A
【分析】A.乙烯和氢气是加成反应;
B.乙烷和氯气是取代反应;
C.乙醇催化氧化是氧化反应;
D.甲苯和浓硝酸、浓硫酸的混合酸制TNT是取代反应。
21.【答案】(1)2CH3CH2OH+O2 2CH3CHO+2H2O
(2)CH3CHO+NaOH+2Cu(OH)2 Cu2O↓+CH3COONa+ 3H2O
(3)
(4)
(5)
【解析】【解答】(1)方程式为2CH3CH2OH+O2 2CH3CHO+2H2O;
(2)方程式为CH3CHO+NaOH+2Cu(OH)2 Cu2O↓+CH3COONa+ 3H2O;
(3)反应的离子方程式为 ;
(4)方程式为 ;
(5)方程式为 。
【分析】(1)乙醇的催化氧化生成乙醛
(2)乙醛和新制的氢氧化铜(氢氧化钠过量)反应生成乙酸钠和氧化亚铜和水
(3)乙醛被酸性高锰酸钾氧化生成乙酸
(4)苯酚和溴水反应生成三溴苯酚和溴化氢
(5)乙酸苯酚酯和足量氢氧化钠溶液反应生成乙酸钠和苯酚钠和水
22.【答案】(1) +3HNO3 3H2O+
(2)
(3)消去;加成;水解
(4)不能
(5)碳碳双键、羧基
(6) + +H2O
(7)
【解析】【解答】(1)甲苯和浓硝酸在浓硫酸、加热下发生取代反应可生成烈性炸药TNT,化学方程式是 +3H2O。
(2) 发生加聚反应得到聚异戊二烯,顺式聚合物的结构简式是 。
(3)由1-氯丁烷制取少量的1,2-丁二醇时,需要消除氯原子,可通过消去反应转变为含碳碳双键的1-丁烯、1-丁烯可与氯气反应得到1,2-二氯丁烷,加热下,1,2-二氯丁烷在氢氧化钠溶液中水解可得到1,2-丁二醇,故需要经过的反应类型是消去反应→加成反应→水解或取代反应。
(4)由“一滴香”分子结构知,分子内含有碳碳双键,能与溴水发生加成反应,故该有机物不能萃取溴水中的溴。
(5)某物质只含C、H、O三种元素, 能形成2个共价键,则为O, 形成1个共价键,则为H, 能形成4个共价键,则为C,分子中共有12个原子、由其分子模型可知其结构简式为CH2=CH(CH3)COOH, 故所含官能团的名称为碳碳双键、羧基。
(6) 和 发生酯化反应生成 和水,化学方程式是 + +H2O。
(7)加热下,乙醛和新制的 碱性悬浊液反应生成乙酸钠、氧化亚铜和水,离子方程式是 。
【分析】(1)TNT是三硝基甲苯根据反应物和生成物以及反应条件即可写出方程式
(2)含有连续两个双键进行加聚时发生1,4加聚即可写出结构简式
(3)先将氯元素进行消去反应再进行加成再进行水解反应得到产物即可
(4)根据此有机物中含有的双键即可判断不能与溴水作用
(5)根据结构模型即可找出官能团即可
(6)根据酯化反应发生的原理即可写出方程式
(7)根据醛基的性质即可写出方程式
23.【答案】(1)
(2)CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br
(3)
(4)CH2BrCH2Br+2NaOH CH2OHCH2OH+2NaBr
(5)CH3CHO+H2 CH3CH2OH
(6)HOCH2CH2OH+HOOCCOOH +2H2O
【解析】【解答】解:(1)丙烯发生加聚反应生成聚丙烯,化学方程式为: ;
故答案为: ;(2)60℃时1,3﹣丁二烯与溴1:1发生1,4加成反应生成1,4﹣二溴﹣2﹣丁烯,反应方程式为CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br,
故答案为:CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br;(3)甲苯与浓硝酸、浓硫酸发生取代反应生成TNT,反应为 ,
故答案为: ;(4)卤代烃在碱性水溶液加热条件下发生取代反应,由1,2﹣二溴乙烷变成乙二醇,方程式为CH2BrCH2Br+2NaOH CH2OHCH2OH+2NaBr,
故答案为:CH2BrCH2Br+2NaOH CH2OHCH2OH+2NaBr;(5)乙醛与氢气在催化剂条件下发生加成反应生成乙醇,方程式:CH3CHO+H2 CH3CH2OH;
故答案为:CH3CHO+H2 CH3CH2OH;(6)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯,方程式:HOCH2CH2OH+HOOCCOOH +2H2O;
故答案为:HOCH2CH2OH+HOOCCOOH +2H2O;
【分析】(1)丙烯发生加聚反应生成聚丙烯;(2)60℃时1,3﹣丁二烯与溴1:1发生1,4加成反应生成1,4﹣二溴﹣2﹣丁烯;(3)甲苯与浓硝酸、浓硫酸发生取代反应生成TNT;(4)根据卤代烃水解的条件解答,1,2﹣二溴乙烷与氢氧化钠水溶液共热发生水解反应生成乙二醇;(5)乙醛与氢气在催化剂条件下发生加成反应生成乙醇;(6)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯.
24.【答案】(1)CnH(2n+2)O;2;3;2;3
(2)CnH2nO;3;4
(3)2;4
【解析】【解答】解:(1)饱和一元醇在形式上由羟基﹣OH取代烷烃的一个氢原子形成,故饱和一元醇的通式为:CnH(2n+2)O;
醇类和醚类存在同分异构关系,最简单的醚类是甲醚CH3﹣O﹣CH3,故最小的n值为2;
﹣CH3、﹣C2H5结构均只有1种,﹣C3H7结构有2种,故出现醇类同分异构体从n=3开始,有1﹣丙醇、2﹣丙醇之分;
醇与浓硫酸发生消去反应生成烯烃,不存在同类异构体的烯烃有乙烯、丙烯,故n值为2或3;
故答案为:CnH(2n+2)O;2;3;2或3;(2)由醛基(﹣CHO)和烷基相连而构成的化合物为饱和一元醛,饱和一元醛含有一个碳氧双键,故通式为CnH2nO;
醛类和酮类存在同分异构现象,最简单的酮类为丙酮CH3COCH3,故最小的n值为3;醛类是烷基和醛基(含有1个碳原子)构成的有机物,有同分异构现象的最小烷基是丙基(含有3个碳原子),故最小的n值为:4;
故答案为:CnH2nO;3;4;(3)由羧基(﹣COOH)和烷基相连而构成的化合物为饱和一元脂肪酸,饱和一元脂肪酸含有一个碳氧双键,故通式为CnH2nO2;
羧酸和酯类存在同分异构现象,最简单的酯类为乙酸乙酯(HCOOCH3),故最小的n值为2;
羧酸是烷基和羧基(含有1个碳原子)构成的有机物,有同分异构现象的最小烷基是丙基(含有3个碳原子),故最小的n值为:4;
故答案为:CnH2nO2;2;4.
【分析】(1)根据饱和一元醇的结构特点写成通式,根据有机物同分异构体的概念完成;根据醇的同分异构体进行分析;根据与羟基相邻的碳原子上氢原子位置判断;(2)根据饱和一元醛的结构完成其通式,根据官能团醛基进行分析存在同分异构体至少的碳原子数;(3)根据饱和一元脂肪酸的通式为CnH2nO2,找出羧酸出现同分异构体、羧酸出现同类异构体
25.【答案】(1)对苯二酚
(2)+4Br2↓+4HBr
(3)
(4)2+O22+2H2O
(5)+2Cu(OH)2+2NaOH+Cu2O↓+4H2O
【解析】【解答】(1)由结构简式可知,M的名称为对苯二酚,故答案为:对苯二酚;
(2)对苯二酚与足量浓溴水发生取代反应生成四溴对苯二酚沉淀和溴化氢,反应的化学方程式为+4Br2↓+4HBr,故答案为:+4Br2↓+4HBr;
(3)N的同分异构体的苯环上连有两个取代基,能发生水解反应说明分子中含有酯基结构,核磁共振氢谱有两组峰且峰面积比为3:2说明分子结构对称,分子中含有2个处于对位的—OOCCH3的取代基,结构简式为,故答案为:;
(4)在铜做催化剂作用下,与氧气共热发生催化氧化反应生成,反应的化学方程式为2+O22+2H2O,故答案为:2+O22+2H2O;
(5)
与足量新制氢氧化铜悬浊液加热反应生成、氧化亚铜沉淀和水,反应的化学方程式为+2Cu(OH)2+2NaOH+Cu2O↓+4H2O,故答案为:+2Cu(OH)2+2NaOH+Cu2O↓+4H2O。
【分析】(1)M含有两个酚羟基,且位于对位;
(2)M中酚羟基的邻位和对位均能被浓溴水取代;
(3)根据题意可知,N的同分异构体中含有酯基,且含有两种不同环境的氢原子;
(4)N含有醛基,在Cu、加热的条件下被氧化成羧基;
(5)N与新制氢氧化铜反应,被氧化成羧基,同时生成砖红色沉淀。
2023-2024学年高二下学期化学人教版(2019)选择性必修3
一、单选题
1.下列说法不正确的是( )
A.液化石油气是纯净物
B.工业酒精中往往含有甲醇
C.福尔马林是甲醛的水溶液
D.许多水果和花卉有芳香气味是因为含有酯
2.化学与科技、社会、生产、生活密切相关。下列有关说祛错误的是()
A.用食醋可除去热水壶内壁的水垢
B.75%(体积分数)的乙醇溶液常用于医疗消毒
C.35%~40%的甲醛溶液俗称福尔马林,可用来浸泡海产品以达到保鲜效果
D.用浸泡过高锰酸钾溶液的硅土吸收水果释放出的乙烯,可达到水果保鲜的目的
3.下列关于乙醇的叙述中,错误的是( )
A.乙醇俗称酒精 B.乙醇可与金属钠反应
C.乙醛经氧化可生成乙醇 D.乙醇能与水任意比例互溶
4.化学与生活密切相关。下列说法错误的是( )
A.乙烯可作水果的催熟剂 B.硅胶可作袋装食品的干燥剂
C.福尔马林可作食品的保鲜剂 D.氢氧化铝可作胃酸的中和剂
5.在医院对某类病人的尿液进行检查时常把氢氧化钠溶液和硫酸铜溶液加入到其尿液中并加热,如果观察到有红色沉淀出现,说明该尿液中含有( )
A.食醋 B.白酒 C.食盐 D.葡萄糖
6.化学与生产、生活息息相关。下列说法错误的是( )
A.甜度仅为蔗糖40%的麦芽糖既能发生水解反应,又能发生银镜反应
B.乙醇的体积分数为75%的医用酒精能使细菌蛋白质发生变性
C.用纤维素制取硝酸纤维的过程中发生了酯化反应
D.5G技术中使用的光导纤维不与任何酸碱反应
7.乙醛与新制氢氧化铜悬浊液反应的实验如下:
步骤1:向试管中加入2mL10%NaOH溶液,边振荡边滴加4~6滴2%CuSO4溶液,观察到有蓝色絮状沉淀产生。
步骤2:再向试管中加入0.5mL乙醛溶液,加热,观察到有红色沉淀产生。
下列说法错误的是( )
A.步骤1中必须加入过量的NaOH溶液
B.步骤2中观察到的红色沉淀为Cu2O
C.上述实验说明乙醛能被新制氢氧化铜氧化
D.上图所示Cu2O的晶胞中 表示氧原子
8.下列说法正确的是( )
A. 与 含有相同的官能团,互为同系物
B. 属于醛类,官能团为-CHO
C. 的名称为:2-乙基-1-丁烯
D. 的名称为:2-甲基-1,3-二丁烯
9.我国科研人员使用催化剂CoGa3实现了H2还原肉桂醛生成肉桂醇,反应机理的示意图如下:
下列说法错误的是( )
A.肉桂醛分子中不存在顺反异构现象
B.苯丙醛分子中有6种不同化学环境的氢原子
C.还原反应过程发生了极性键和非极性键的断裂
D.该催化剂实现了选择性还原肉桂醛中的醛基
10.下列反应中,有机物被还原的是 ( )
A.乙醛的银镜反应 B.乙醛制乙醇
C.乙醇制乙醛 D.乙醇制乙烯
11.具有防腐作用的甲醛 ( )
A.分子中共有12个电子 B.能发生加聚反应
C.难溶于水易溶于酒精 D.比例模型为:
12.用丙醛CH3CH2CHO制取聚丙烯 的过程中发生的反应类型为( )
①取代反应;②消去反应;③加聚反应;④还原反应;⑤氧化反应
A.④②③ B.⑤②③ C.①④③ D.②④⑤
13.化学与日常生活紧密相关.下列说法中,不正确的是( )
A.甲醛可作食品防腐剂 B.氢氧化铝可作抗酸药
C.氯化钠可作食品调味剂 D.生石灰可作食品干燥剂
14.乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,反应可表示为CH2=C=O+HA → CH3-CO-A。乙烯酮在一定条件下可与下列试剂加成,其产物错误的是( )
A.与HCl加成生成CH3COCl
B.与H2O加成生成CH3COOH
C.与CH3COOH加成生成CH3COOCOCH3
D.与CH3OH加成生成CH3COCH2OH
15.对人体健康不会造成危害的是( )
A.用工业酒精(含甲醇)兑制饮用酒
B.用食醋除去水壶内壁的水垢
C.用甲醛溶液浸泡海产品进行防腐保鲜
D.在不通风、无防护的条件下做实验
16.探究甲醛与新制的Cu(OH)2的反应:
⑴向6mL 6mol·L-1NaOH溶液中滴加8滴2%CuSO4溶液,振荡,加入0.5mL15%甲醛溶液,混合均匀,水浴加热,生成红色沉淀同时产生无色气体。
⑵反应停止后分离出沉淀,将所得沉淀洗净后加入浓盐酸,不溶解。
已知: ,甲醛是具有强还原性的气体。下列说法错误的是( )
A.如图所示铜的晶胞中Cu原子的配位数为12
B.红色沉淀的主要成分不是Cu2O,可能是Cu
C.将产生的无色气体通过灼热的CuO后得到红色固体,说明生成的气体中一定是CO
D.从甲醛的结构推测,其氧化产物还可能有CO
17.某学生做乙醛还原性的实验,取1mol/L的硫酸铜溶液2mL和0.4mol/L的氢氧化钠溶液4mL,在一个试管内混合后加入0.5mL40%乙醛溶液加热至沸,无红色沉淀。失败的原因是( )
A.氢氧化钠的量不够 B.硫酸铜的量不够
C.乙醛溶液太少 D.加热时间不够
18.某有机物化学式为C5H10O,它能发生银镜反应和加成反应,若将它与H2加成,所得产物的结构简式可能是( )
A.(CH3)3CCH2OH B.(CH3CH2)2CHOH
C.CH3(CH2)2CH(CH3)OH D.CH3CH2C(CH3)2OH
19.某甲酸溶液中可能存在着甲醛,下列操作能正确说明的是( )
A.试液与足量NaOH溶液混合其蒸馏产物可发生银镜反应,则有甲醛
B.能发生银镜反应,证明含甲醛
C.加入新制Cu(OH)2加热,有红色沉淀生成,证明一定存在甲醛
D.先将试液充分进行酯化反应收集生成物进行银镜反应,有银镜产生,则含甲醛
20.“绿色化学”提倡“原子经济性”。理想的“原子经济性”反应中,原料分子中的所有原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合“原子经济性”的是( )
A.乙烯与氢气在一定条件下制乙烷
B.乙烷与氯气反应制一氯乙烷
C.乙醇催化氧化制乙醛
D.甲苯与浓硝酸、浓硫酸的混合酸制TNT
二、综合题
21.完成方程式。
(1)乙醇的催化氧化方程式:
(2)乙醛和新制的氢氧化铜(氢氧化钠过量)反应方程式:
(3)乙醛和酸性高锰酸钾反应的离子方程式:
(4)苯酚和溴水反应方程式:
(5)乙酸苯酚酯和足量氢氧化钠溶液反应方程式:
22.按要求回答下列问题:
(1)制造烈性炸药TNT的化学方程式是 。
(2)由 生成顺式聚合物的结构简式是 。
(3)由1-氯丁烷制取少量的1,2-丁二醇时,需要经过的反应类型是 反应→ 反应→ 反应。
(4)“一滴香”是一种毒性很强的物质,被人食用后会损伤肝脏,还能致癌.其分子结构如图所示,用该有机物 (填“能”或“不能”)萃取溴水中的溴。
(5)某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键)。
该物质中所含官能团的名称为 。
(6) 和 发生酯化反应的化学方程式是 。
(7)乙醛和新制的 反应的离子方程式是 。
23.按要求书写下列化学方程式:
(1)丙烯的加聚
(2)1,3﹣丁二烯与等物质的量的单质溴在60℃时发生1,4﹣加成
(3)甲苯制备TNT
(4)1,2﹣二溴乙烷与氢氧化钠水溶液共热:
(5)乙醛的还原:
(6)乙二醇和乙二酸脱水成二元环酯 .
24.确定以下各项的n值:
(1)饱和一元醇的通式是 ,醇出现同分异构体时,n的最小值是 ;醇出现同类异构体时,n的最小值是 .n值一定的醇与浓硫酸共热,只能得到一种不饱和烃,符合上述结果的n值是 或 .
(2)饱和一元醛的通式为 ,醛出现稳定的同分异构体时,n的最小值是 ;醛出现同类异构体时,n的最小值是 .
(3)饱和一元脂肪酸的通式为CnH2nO2,羧酸出现同分异构体时,n最小值是 ,羧酸出现同类异构体时,n的最小值是 .
25.有机物M的结构简式为,N的结构简式为。回答下列问题:
(1)M的化学名称为 。
(2)写出M与足量浓溴水反应的化学方程式: 。
(3)写出同时满足下列条件的N的同分异构体的结构简式: 。
①苯环上连有两个取代基
②能发生水解反应
③核磁共振氢谱有两组峰且峰面积比为
(4)写出N在催化和加热条件下发生反应的化学方程式: 。
(5)写出N与足量新制悬浊液加热发生反应的化学方程式: 。
答案解析部分
1.【答案】A
【解析】【解答】A.液化石油气中含有多种物质,属于混合物,选项A符合题意;
B.工业酒精中往往含有甲醇,不能利用工业酒精勾兑白酒,选项B不符合题意;
C.福尔马林是含甲醛37%-40%的水溶液,选项C不符合题意;
D.水果与花卉中存在酯类,具有芳香气味,选项D不符合题意;
故答案为:A。
【分析】A.液化石油气是以丙烷和丁烷为主要成分的混合物;
B.甲醇是工业酒精的原料;
C.甲醛的水溶液俗称福尔马林;
D.酯类具有特殊香味。
2.【答案】C
【解析】【解答】A.食醋中含有醋酸,水垢的主要成分是碳酸钙和氢氧化镁,因此用食醋可除去热水壶内壁的水垢,A不符合题意;
B.75%(体积分数)的乙醇溶液能使蛋白质变性,常用于医疗消毒,B不符合题意;
C.35%~40%的甲醛溶液俗称福尔马林,但甲醛有毒,不能用来浸泡海产品以达到保鲜效果,C符合题意;
D.高锰酸钾能氧化乙烯,因此可用浸泡过高锰酸钾溶液的硅土吸收水果释放出的乙烯,可达到水果保鲜的目的,D不符合题意。
故答案为:C。
【分析】A.醋酸的酸性比碳酸强;
B.消毒用的酒精质量分数是75%;
C.甲醛有毒不能用于海产品的保险;
D.乙烯具有催熟效果,酸性高锰酸钾能够氧化乙烯。
3.【答案】C
【解析】【解答】A.乙醇是一种有机物,俗称酒精,故A不符合题意;
B.乙醇可与金属钠发生置换反应生成乙醇钠和氢气,故B不符合题意
C.乙醛与氢气发生加成反应可生成乙醇,该过程为还原反应,故C符合题意;
D.乙醇分子之间、水分子之间都有氢键,根据相似相溶原理,乙醇能与水任意比例互溶,故D不符合题意;
故答案为:C。
【分析】乙醇俗名叫酒精,乙醇具有羟基可发生取代、消去以及与钠发生置换反应,与水形成氢键可以与水互溶
4.【答案】C
【解析】【解答】A、乙烯是一种植物生长调节剂,可作水果的催熟剂,A不符合题意;
B、硅胶多孔,吸收水分能力强,可作袋装食品的干燥剂,B不符合题意;
C、福尔马林是甲醛的水溶液,甲醛有毒,不能作食品的保鲜剂,C符合题意;
D、氢氧化铝属于两性氢氧化物能与酸反应,可作胃酸的中和剂,D不符合题意,
故答案为:C。
【分析】A.乙烯是一种植物生长调节剂;
B.硅胶的表面积较大,可作干燥剂;
C.福尔马林是甲醛的水溶液,有毒;
D.氢氧化铝是两性氢氧化物,能够中和胃酸中的盐酸。
5.【答案】D
【解析】【解答】A.食醋的化学式CH3COOH,分子结构中不含有-CHO,A不符合题意;
B.白酒的化学式为CH3CH2OH,分子结构中不含有-CHO,B不符合题意;
C.食盐的化学式为NaCl,不含有-CHO,C不符合题意;
D.葡萄糖结构简式为CH2OH(CHOH)4CHO,分子结构中含有-CHO,D符合题意;
故答案为:D
【分析】能与新制Cu(OH)2悬浊液反应产生砖红色沉淀,则说明尿液中所含物质含有-CHO,据此结合选项所给物质进行分析。
6.【答案】D
【解析】【解答】A.麦芽糖分子结构中有醛基,具有还原性是一种还原糖。因此可以与银氨溶液发生银镜反应,也可以与新制碱性氢氧化铜反应生成砖红色沉淀。可以在一定条件下水解,生成两分子葡萄糖,故A不符合题意;
B.乙醇可以提供自己的羟基或羰基上的氢或氧去形成氢键,从而破坏了蛋白质中原有的氢键,使蛋白质变性,故B不符合题意;
C.纤维素分子中有羟基,能够与硝酸发生反应生成酯硝酸纤维和水,发生的是酯化反应,故C不符合题意;
D.D光导纤维成分是二氧化硅,可以和氢氧化钠反应SiO2+2NaOH=Na2SiO3+H2O,故D符合题意;
故答案为:D。
【分析】光导纤维中的物质是二氧化硅,可以和氢氟酸和氢氧化钠强碱反应,其他选项均正确
7.【答案】D
【解析】【解答】A.醛基和新制的氢氧化铜悬浊液反应时需要碱过量,故必须加入过量的氢氧化钠溶液,A不符合题意;
B.乙醛和新制的氢氧化铜悬浊液反应生成红色的氧化亚铜沉淀,B不符合题意;
C.实验生成乙酸铵,说明乙醛被氢氧化铜氧化,C不符合题意;
D.晶胞中红色球有 ,黑色球有4个,所以结合氧化亚铜的化学式分析,黑色球表示铜原子,D符合题意;
故答案为:D。
【分析】根据红球和黑球的占位计算出晶胞中铜原子和氧原子的个数比即可
8.【答案】C
【解析】【解答】A. 前者—OH与苯环的侧链相连,属于醇类,后者—OH直接与苯环相连,属于酚类,尽管分子构成相差了1个CH2,但是二者不是同一类物质,所以它们不互为同系物,A不符合题意;
B. 该物质属于酯类(甲酸酯,含有醛基),官能团为酯基, B不符合题意;
C. 该物质的官能团为碳碳双键,含有官能团的最长的碳链有4个C,因此主链含有4个C,为丁烯;编号时官能团的编号要小,因此碳碳双键的编号为1,乙基的编号为2,命名为2-乙基-1-丁烯,C符合题意;
D. 该物质中含有2个碳碳双键,且含有碳碳双键最长的碳链有4个碳原子,因此该物质为丁二烯。编号时,不管是从左端还是右端,碳碳双键的编号均为1、3,因此编号的选择,让甲基的编号的编号小,甲基的编号为2,则该物质的名称应为:2-甲基-1,3-丁二烯,D不符合题意。
故答案为:C
【分析】A. 注意属于醇,属于酚;
B. 该物质为甲酸和苯酚形成的酯类;
C. 该物质按烯烃来命名;
D. 该物质按双烯烃来命名。
9.【答案】A
【解析】【解答】A.肉桂醛分子中每个双键碳原子所连接的原子或原子团都不同,所以存在顺反异构现象,A符合题意;
B.苯丙醛分子中,苯环上有3种不同化学环境的氢原子,另外还有3种不同的氢原子,所以共有6种不同化学环境的氢原子,B不符合题意;
C.还原反应过程,发生了醛基上极性键的断裂和氢分子中非极性键的断裂,C不符合题意;
D.在该催化剂作用下,只有醛基被还原,碳碳双键和苯基没有被还原,所以实现了选择性还原肉桂醛中的醛基,D不符合题意;
故答案为:A。
【分析】A.肉桂醛中存在碳碳双键,碳碳双键中的碳原子连接的有相同的原子,因此存在顺反异构
B.找出苯丙醛分子中的氢原子的种类,苯环高度对称,故有3种不同种类的氢原子,在支链上有3种氢原子
C.还原反应时,氢气的非极性键的断裂,碳氧键的断裂是极性键的断裂
D.根据图示发现,只有醛基被还原,双键没有被还原故具有选择性
10.【答案】B
【解析】【解答】乙醛的银镜反应被氧化,乙醇制乙醛氧化反应,乙醇加水加成制乙烯。乙醛制乙醇是还原反应,加氢还原。
【分析】有机反应中还原反应判断方法一:“加氢或去氧”有机物的变化是氢原子多了或者氧原子少了,即是还原反应。
方法二:根据有机物中碳元素的化合价的变化进行判断,注意标化合价的原则是氢元素是+1,O是-1价。最后标碳元素。
11.【答案】B
【解析】【解答】解:A.甲醛的电子式为: ,核外共有电子数=8+6+2=16,故A错误;
B.甲醛的结构式为 ,含有碳氧双键能发生加聚反应,故B正确;
C.甲醛是极性分子,水是极性分子,乙醇是极性分子,根据相似相溶原理,甲醛易溶于水,也易溶于酒精,故C错误;
D.比例模型中氧原子半径应大于氢原子的半径,故D错误;
故选B.
【分析】A.甲醛的分子式为CH2O,电子式为 ;
B.根据甲醛的结构式为 以及双键能发生加聚反应来分析;
C.根据相似相溶原理来解答;
D.根据比例模型中氧原子半径应大于氢原子的半径.
12.【答案】A
【解析】【解答】用CH3CH2CHO制取聚丙烯,可用逆推法: CH3CH=CH2 CH3CH2CH2OH CH3CH2CHO;第一步CH3CH2CHO与氢气发生加成反应得到CH3CH2CH2OH,该反应又可称为还原反应;第二步CH3CH2CH2OH发生消去反应得到丙烯;第三步丙烯发生加聚反应得到聚丙烯;
故答案为:A。
【分析】采用逆推法即可判断反应所有的产物以及发生法反应类型
13.【答案】A
【解析】【解答】解:A.甲醛有毒,能破坏蛋白质的结构,使之失去生理功能,所以不能用甲醛作食品防腐剂,故A错误;
B.抗酸药的有效成分为:碳酸氢钠、碳酸钙、碳酸镁、氢氧化铝、氢氧化镁等,氢氧化铝能与胃液中的盐酸反应,且自身对人无害,故B正确;
C.Na为人体不可缺少的元素,食盐可用于食品调味剂,具有咸味,故C正确;
D.生石灰能和水反应,所以可用生石灰作食品干燥剂,故D正确.
故选A.
【分析】A.甲醛有毒性,能使蛋白质发生变性;
B.氢氧化铝能与盐酸反应,且自身对人无害;
C.氯化钠具有咸味,常用作调味品;
D.生石灰能和水反应生成微溶于水的氢氧化钙.
14.【答案】D
【解析】【解答】A. 乙烯酮(CH2=C=O)与HCl加成,端点碳原子连氢,另一个碳原子连Cl,得到CH3COCl,故A不选;
B. 乙烯酮(CH2=C=O)与H2O加成,端点碳原子连氢,另一个碳原子连-OH,得到CH3COOH,故B不选;
C. 乙烯酮(CH2=C=O)与CH3COOH加成,端点碳原子连氢,另一个碳原子连CH3COO-,得到CH3COOCOCH3,故C不选;
D. 乙烯酮(CH2=C=O)与CH3OH加成,端点碳原子连氢,另一个碳原子连CH3O-,得到CH3COOCH3,故D选。
故答案为:D。
【分析】乙烯酮(CH2=C=O)在一定条件下能与含活泼氢的化合物发生加成反应,碳碳双键断开,端点碳原子连氢,另一个碳原子连除了氢原子之外的另一个原子或原子团。
15.【答案】B
【解析】【解答】解:A.甲醇有毒,会危害人体健康,饮用工业酒精(含甲醇)兑制饮用酒会导致失明或死亡,故A错误;
B.醋酸对人体无害,而且醋酸能溶解水垢,所以可以用食醋除去水壶内壁的水垢,故B正确;
C.甲醛有毒,用甲醛保鲜海产品会危害人类健康,故C错误;
D.有些化学药品具有毒性,应该在通风、有防护的条件下做实验,否则会引起实验人员中毒,故D错误.
故选B.
【分析】A.甲醇有毒,会危害人体健康;
B.醋酸能溶解水垢;
C.甲醛有毒,会危害人体健康;
D.有些化学药品具有毒性.
16.【答案】C
【解析】【解答】A.根据铜的晶胞结构,铜为面心立方晶胞, Cu原子的配位数为12,故A不符合题意;
B. ,沉淀洗净后加入浓盐酸,不溶解,可知红色沉淀的主要成分不是Cu2O,可能是Cu,故B不符合题意;
C.将产生的无色气体通过灼热的CuO后得到红色固体,生成的气体中可能含有CO、HCHO,故C符合题意;
D.从甲醛的结构推测,甲醛可以氧化为甲酸,在碱溶液中生成甲酸盐,或被氧化为碳酸,碱溶液中反应生成碳酸盐,所以氧化产物还可能有CO ,故D不符合题意;
故答案为:C。
【分析】A.与铜原子的距离最近的铜原子有3层,每层有4个共12个
B.红色沉淀不溶于盐酸,可能是氧化亚铜或铜单质或者是混合物
C.甲醛易挥发,甲醛是具有强还原性的气体
D.根据甲醛的结构,即可判断产物可能是羧酸类,羧酸类继续反应
17.【答案】A
【解析】【解答】乙醛和新制氢氧化铜悬浊液发生反应的环境是在碱性条件下进行的,而根据题意可判断氢氧化钠溶液是不足的,硫酸铜过量,
故答案为:A。
【分析】此题考查醛的还原性的实验,根据醛还原的条件是碱性环境进行判断。
18.【答案】A
【解析】【解答】由题意知该物质的饱和的一元醛,-CHO加氢后为-CH2OH,只有A项符合要求
【分析】该有机物可以发生银镜反应,因此是醛类,在根据分子式和加成反应,可得出该醛的结构简式。
19.【答案】A
【解析】【解答】解:甲酸和甲醛都含有醛基,则直接加入新制备氢氧化铜浊液或银氨溶液不能鉴别是否含有甲醛,应先加入足量NaOH溶液混合,甲酸与氢氧化钠溶液反应生成难挥发的甲酸钠,然后蒸馏,可得到甲醛,再用银氨溶液或新制备氢氧化铜浊液鉴别,D中先将试液充分进行酯化反应,甲酸酯也可发生银镜反应,不能鉴别,所以B、C、D错误,故选A.
【分析】甲酸中含有醛基和羧基,甲醛中只含醛基,不能直接用银氨溶液鉴别,应先分离后再鉴别,以此解答.
20.【答案】A
【解析】【解答】A.乙烯和氢气在一定条件下制乙烷,是加成反应,原子利用率100%,A符合题意;
B.乙烷和氯气反应制一氯乙烷,是取代反应,原子利用率不是100%,B不符合题意;
C.乙醇催化氧化制乙醛,是氧化反应,原子利用率不是100%,C不符合题意;
D.甲苯和浓硝酸、浓硫酸的混合酸制TNT,是取代反应,原子利用率不是100%,D不符合题意;
故答案为:A
【分析】A.乙烯和氢气是加成反应;
B.乙烷和氯气是取代反应;
C.乙醇催化氧化是氧化反应;
D.甲苯和浓硝酸、浓硫酸的混合酸制TNT是取代反应。
21.【答案】(1)2CH3CH2OH+O2 2CH3CHO+2H2O
(2)CH3CHO+NaOH+2Cu(OH)2 Cu2O↓+CH3COONa+ 3H2O
(3)
(4)
(5)
【解析】【解答】(1)方程式为2CH3CH2OH+O2 2CH3CHO+2H2O;
(2)方程式为CH3CHO+NaOH+2Cu(OH)2 Cu2O↓+CH3COONa+ 3H2O;
(3)反应的离子方程式为 ;
(4)方程式为 ;
(5)方程式为 。
【分析】(1)乙醇的催化氧化生成乙醛
(2)乙醛和新制的氢氧化铜(氢氧化钠过量)反应生成乙酸钠和氧化亚铜和水
(3)乙醛被酸性高锰酸钾氧化生成乙酸
(4)苯酚和溴水反应生成三溴苯酚和溴化氢
(5)乙酸苯酚酯和足量氢氧化钠溶液反应生成乙酸钠和苯酚钠和水
22.【答案】(1) +3HNO3 3H2O+
(2)
(3)消去;加成;水解
(4)不能
(5)碳碳双键、羧基
(6) + +H2O
(7)
【解析】【解答】(1)甲苯和浓硝酸在浓硫酸、加热下发生取代反应可生成烈性炸药TNT,化学方程式是 +3H2O。
(2) 发生加聚反应得到聚异戊二烯,顺式聚合物的结构简式是 。
(3)由1-氯丁烷制取少量的1,2-丁二醇时,需要消除氯原子,可通过消去反应转变为含碳碳双键的1-丁烯、1-丁烯可与氯气反应得到1,2-二氯丁烷,加热下,1,2-二氯丁烷在氢氧化钠溶液中水解可得到1,2-丁二醇,故需要经过的反应类型是消去反应→加成反应→水解或取代反应。
(4)由“一滴香”分子结构知,分子内含有碳碳双键,能与溴水发生加成反应,故该有机物不能萃取溴水中的溴。
(5)某物质只含C、H、O三种元素, 能形成2个共价键,则为O, 形成1个共价键,则为H, 能形成4个共价键,则为C,分子中共有12个原子、由其分子模型可知其结构简式为CH2=CH(CH3)COOH, 故所含官能团的名称为碳碳双键、羧基。
(6) 和 发生酯化反应生成 和水,化学方程式是 + +H2O。
(7)加热下,乙醛和新制的 碱性悬浊液反应生成乙酸钠、氧化亚铜和水,离子方程式是 。
【分析】(1)TNT是三硝基甲苯根据反应物和生成物以及反应条件即可写出方程式
(2)含有连续两个双键进行加聚时发生1,4加聚即可写出结构简式
(3)先将氯元素进行消去反应再进行加成再进行水解反应得到产物即可
(4)根据此有机物中含有的双键即可判断不能与溴水作用
(5)根据结构模型即可找出官能团即可
(6)根据酯化反应发生的原理即可写出方程式
(7)根据醛基的性质即可写出方程式
23.【答案】(1)
(2)CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br
(3)
(4)CH2BrCH2Br+2NaOH CH2OHCH2OH+2NaBr
(5)CH3CHO+H2 CH3CH2OH
(6)HOCH2CH2OH+HOOCCOOH +2H2O
【解析】【解答】解:(1)丙烯发生加聚反应生成聚丙烯,化学方程式为: ;
故答案为: ;(2)60℃时1,3﹣丁二烯与溴1:1发生1,4加成反应生成1,4﹣二溴﹣2﹣丁烯,反应方程式为CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br,
故答案为:CH2=CH﹣CH=CH2+Br2→CH2Br﹣CH=CH﹣CH2Br;(3)甲苯与浓硝酸、浓硫酸发生取代反应生成TNT,反应为 ,
故答案为: ;(4)卤代烃在碱性水溶液加热条件下发生取代反应,由1,2﹣二溴乙烷变成乙二醇,方程式为CH2BrCH2Br+2NaOH CH2OHCH2OH+2NaBr,
故答案为:CH2BrCH2Br+2NaOH CH2OHCH2OH+2NaBr;(5)乙醛与氢气在催化剂条件下发生加成反应生成乙醇,方程式:CH3CHO+H2 CH3CH2OH;
故答案为:CH3CHO+H2 CH3CH2OH;(6)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯,方程式:HOCH2CH2OH+HOOCCOOH +2H2O;
故答案为:HOCH2CH2OH+HOOCCOOH +2H2O;
【分析】(1)丙烯发生加聚反应生成聚丙烯;(2)60℃时1,3﹣丁二烯与溴1:1发生1,4加成反应生成1,4﹣二溴﹣2﹣丁烯;(3)甲苯与浓硝酸、浓硫酸发生取代反应生成TNT;(4)根据卤代烃水解的条件解答,1,2﹣二溴乙烷与氢氧化钠水溶液共热发生水解反应生成乙二醇;(5)乙醛与氢气在催化剂条件下发生加成反应生成乙醇;(6)乙二酸和乙二醇之间可以发生酯化反应得到乙二酸乙二醇酯.
24.【答案】(1)CnH(2n+2)O;2;3;2;3
(2)CnH2nO;3;4
(3)2;4
【解析】【解答】解:(1)饱和一元醇在形式上由羟基﹣OH取代烷烃的一个氢原子形成,故饱和一元醇的通式为:CnH(2n+2)O;
醇类和醚类存在同分异构关系,最简单的醚类是甲醚CH3﹣O﹣CH3,故最小的n值为2;
﹣CH3、﹣C2H5结构均只有1种,﹣C3H7结构有2种,故出现醇类同分异构体从n=3开始,有1﹣丙醇、2﹣丙醇之分;
醇与浓硫酸发生消去反应生成烯烃,不存在同类异构体的烯烃有乙烯、丙烯,故n值为2或3;
故答案为:CnH(2n+2)O;2;3;2或3;(2)由醛基(﹣CHO)和烷基相连而构成的化合物为饱和一元醛,饱和一元醛含有一个碳氧双键,故通式为CnH2nO;
醛类和酮类存在同分异构现象,最简单的酮类为丙酮CH3COCH3,故最小的n值为3;醛类是烷基和醛基(含有1个碳原子)构成的有机物,有同分异构现象的最小烷基是丙基(含有3个碳原子),故最小的n值为:4;
故答案为:CnH2nO;3;4;(3)由羧基(﹣COOH)和烷基相连而构成的化合物为饱和一元脂肪酸,饱和一元脂肪酸含有一个碳氧双键,故通式为CnH2nO2;
羧酸和酯类存在同分异构现象,最简单的酯类为乙酸乙酯(HCOOCH3),故最小的n值为2;
羧酸是烷基和羧基(含有1个碳原子)构成的有机物,有同分异构现象的最小烷基是丙基(含有3个碳原子),故最小的n值为:4;
故答案为:CnH2nO2;2;4.
【分析】(1)根据饱和一元醇的结构特点写成通式,根据有机物同分异构体的概念完成;根据醇的同分异构体进行分析;根据与羟基相邻的碳原子上氢原子位置判断;(2)根据饱和一元醛的结构完成其通式,根据官能团醛基进行分析存在同分异构体至少的碳原子数;(3)根据饱和一元脂肪酸的通式为CnH2nO2,找出羧酸出现同分异构体、羧酸出现同类异构体
25.【答案】(1)对苯二酚
(2)+4Br2↓+4HBr
(3)
(4)2+O22+2H2O
(5)+2Cu(OH)2+2NaOH+Cu2O↓+4H2O
【解析】【解答】(1)由结构简式可知,M的名称为对苯二酚,故答案为:对苯二酚;
(2)对苯二酚与足量浓溴水发生取代反应生成四溴对苯二酚沉淀和溴化氢,反应的化学方程式为+4Br2↓+4HBr,故答案为:+4Br2↓+4HBr;
(3)N的同分异构体的苯环上连有两个取代基,能发生水解反应说明分子中含有酯基结构,核磁共振氢谱有两组峰且峰面积比为3:2说明分子结构对称,分子中含有2个处于对位的—OOCCH3的取代基,结构简式为,故答案为:;
(4)在铜做催化剂作用下,与氧气共热发生催化氧化反应生成,反应的化学方程式为2+O22+2H2O,故答案为:2+O22+2H2O;
(5)
与足量新制氢氧化铜悬浊液加热反应生成、氧化亚铜沉淀和水,反应的化学方程式为+2Cu(OH)2+2NaOH+Cu2O↓+4H2O,故答案为:+2Cu(OH)2+2NaOH+Cu2O↓+4H2O。
【分析】(1)M含有两个酚羟基,且位于对位;
(2)M中酚羟基的邻位和对位均能被浓溴水取代;
(3)根据题意可知,N的同分异构体中含有酯基,且含有两种不同环境的氢原子;
(4)N含有醛基,在Cu、加热的条件下被氧化成羧基;
(5)N与新制氢氧化铜反应,被氧化成羧基,同时生成砖红色沉淀。
