7.2 乙烯与有机高分子材料练习(含解析)高中化学苏教版(2019)必修第二册
文档属性
| 名称 | 7.2 乙烯与有机高分子材料练习(含解析)高中化学苏教版(2019)必修第二册 |

|
|
| 格式 | docx | ||
| 文件大小 | 286.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-15 00:00:00 | ||
图片预览



文档简介
7.2 乙烯与有机高分子材料 同步练习
2023-2024学年高一下学期化学人教版(2019)必修第二册
一、单选题
1.下列化合物的分子中,所有原子都处于同一平面的有( )
A.乙烷 B.乙醇 C.丙烯 D.乙烯
2.化学创造美好生活。下列生产活动中,没有运用相应化学原理的是( )
选项 生产活动 化学原理
A 乙烯水化法制工业酒精 乙烯可发生加成反应
B 利用明矾净水 Al3+有氧化性
C 利用硅做太阳能电池 硅是半导体材料
D 轮船铁护栏上绑一块锌 牺牲阳极保护阴极
A.A B.B C.C D.D
3.下列说法正确的是( )
A.乙烯和乙炔都是直线形分子
B.乙烯分子中含有极性键和非极性键
C.乙炔分子中含有1个σ键和2个π键
D.乙烯与分子式为C4H8的烃一定互为同系物
4.2022年2月,第24届冬奥会在北京成功举办。下列有关说法正确的是( )
A.为保证食物的口感和安全性,不能在食品中添加任何食品添加剂
B.北京冬奥会上,礼仪服饰采用高科技石墨烯发热材料,石墨烯属于有机高分子材料
C.冰的密度比水小,是因为水分子内存在氢键
D.“绿色奥运”是本届奥运会的理念之一,采用风能和太阳能为奥运服务体现了这一理念
5.化学与生产生活密切相关。下列说法错误的是( )
A.多糖、蛋白质都是高分子化合物,一定条件下都能水解
B.具有特殊的光学性能,可用于制作光导纤维
C.尼龙绳、羊绒衫和棉衬衣等生活用品都是由合成纤维制造的
D.不溶于水和酸,可用于胃肠X射线造影检查
6.化学与生活密切相关,下列说法正确的是( )
A.聚乙烯塑料的老化是由于发生了加成反应
B.煤经过气化和液化等物理变化可以转化为清洁燃料
C.合成纤维、人造纤维及碳纤维都属于有机高分子材料
D.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程
7.2023年5月10日,最强太空“快递小哥”天舟六号货运飞船由长征七号运载火箭发射升空,体现了我国强大科技力量。下列说法正确的是( )
A.“天舟六号”为空间站送去电推进氙气瓶,与互为同位素
B.“天舟六号”配有半刚性太阳电池阵“翅膀”,电池板主要成分是
C.“长征七号”采用液氧、煤油等作为推进剂,液氧、煤油是纯净物
D.“长征七号”使用碳纤维材料减轻火箭质量,碳纤维属于有机高分子材料
8.下列说法中正确的是( )
A.制造N95口罩的聚丙烯树脂中含有碳碳双键
B.C6H14有4种同分异构体
C.乙烯能使溴水和酸性高锰酸钾溶液褪色,且褪色原理也相同
D.C2H6完全燃烧生成的CO2和H2O的质量可能是4.4 g和2.7 g
9.新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述错误的是( )
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面方案等处的油墨中所含有的Fe3O4是一种磁性物质
C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
10.以下3种有机物是一些食用香精和精油的主要成分,下列说法不正确的是( )
A.桂醛分子中所有原子均可能处于同一平面上
B.1mol桂醛最多与4mol H2发生加成反应
C.香茅醇的分子式为C10H20O
D.可用银氨溶液鉴别桂醛和D-香芹酮
11.下列关于丁烷的叙述不正确的是( )
A.常温下,C4H10是气体
B.丁烷有正丁烷写异丁烷两种同分异构体
C.C4H10与CH4互为同系物
D.C4H10进行一氯取代时最多生成两种沸点不同的产物
12.欲制取较纯净的CH2ClCH2Cl(即1,2-二氯乙烷),最合理的方法是( )
A.CH3CH3与Cl2取代 B.CH2=CH2与 HCl加成
C.CH2=CH2与Cl2加成 D.CH3CH2Cl与Cl2取代
13.下列说法错误的是
A.从分子结构上看糖类都是多羟基醛及其缩合产物
B.蛋白质溶液与浓硝酸作用产生白色沉淀,加热后沉淀变黄色
C.水果中因含有低级酯类物质而具有特殊香味
D.聚乙烯、聚氯乙烯是热塑性塑料
14.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯,得到纯净乙烷的方法是( )
A.通入足量溴水中 B.与足量溴蒸气反应
C.在一定条件下通入氢气 D.通入酸性KMnO4溶液中
15.通常用来衡量一个国家石油化工发展水平标志的是( )
A.甲烷的产量 B.苯的产量 C.乙醇的产量 D.乙烯的产量
16.石油被誉为“工业的血液”,乙烯和苯都是重要的石油化工产品,也是重要的有机化工原料。下列关于乙烯和苯的叙述正确的是( )
A.乙烯和苯都是平面型分子,分子结构中都含有碳碳双键,都属于不饱和烃
B.乙烯和苯都可以来自于石油,石油的产量是衡量一个国家石油化工发展水平的标志
C.乙烯易发生加成反应,苯不能发生加成反应
D.乙烯和苯都可以发生氧化反应
17.下列“类比”合理的是( )
A.常温下, Zn 和浓硫酸反应可以得到 SO2 ,则常温下 Al 和浓硫酸反应也可以得到 SO2
B.H2O 的沸点比H2S 的沸点高,则 CH4 的沸点比 SiH4 的沸点高
C.乙烯使溴水褪色发生加成反应,则乙烯使酸性高锰酸钾褪色也发生加成反应
D.加热条件下,和能直接化合生成,则加热条件下和也能直接化合生成
18.四氯乙烯()是一种衣物干洗剂,聚四氟乙烯()是家用不粘锅内侧涂层的主要成分,下列说法正确的是( )
A.它们都能发生加成反应,都能使酸性高锰酸钾溶液褪色
B.它们的分子中C原子的杂化类型均为sp3杂化
C.四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较活泼
D.Cl和F为同主族元素,由于电负性F大于Cl,因此C-F键极性大于C-Cl键极性
19.《本草纲目》果部第三十卷中提到“山楂化饮食,消肉积、症瘕、痰饮、痞满吞酸、滞血痛胀。”山楂中的有效成分枸橼酸又称柠檬酸,结构如下,下列说法中正确的是
A.柠檬酸的酸性比碳酸弱
B.柠檬酸易溶于水,可与水分子形成氢键
C.1mol 柠檬酸可与4molNaOH反应
D.柠檬酸可发生取代反应、加成反应和氧化反应
20.下列变化是通过加成反应来实现的是( )
A.CH3CH3→CH3-CH2Br B.CH3COOH→CH3COOC2H5
C. → D.CH2=CH2→CH3CH2OH
二、综合题
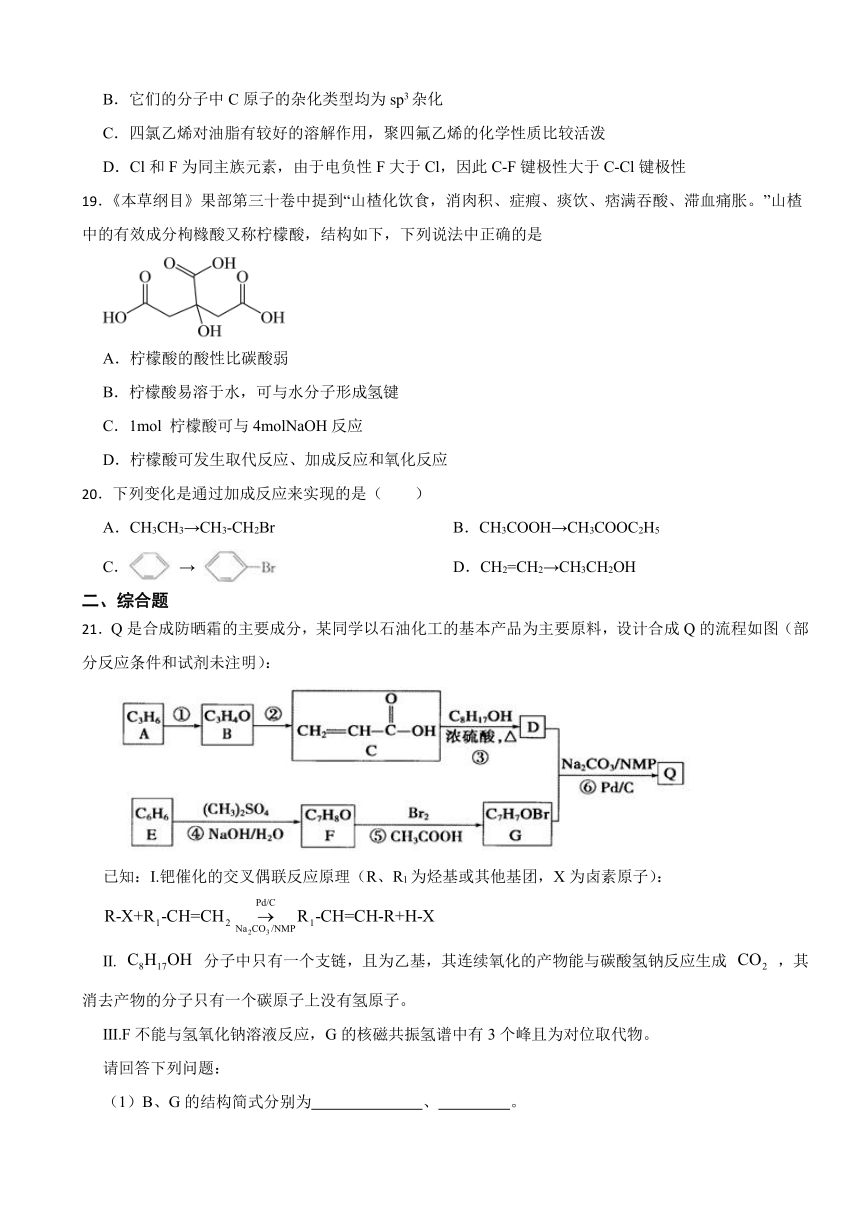
21.Q是合成防晒霜的主要成分,某同学以石油化工的基本产品为主要原料,设计合成Q的流程如图(部分反应条件和试剂未注明):
已知:Ⅰ.钯催化的交叉偶联反应原理(R、R1为烃基或其他基团,X为卤素原子):
Ⅱ. 分子中只有一个支链,且为乙基,其连续氧化的产物能与碳酸氢钠反应生成 ,其消去产物的分子只有一个碳原子上没有氢原子。
Ⅲ.F不能与氢氧化钠溶液反应,G的核磁共振氢谱中有3个峰且为对位取代物。
请回答下列问题:
(1)B、G的结构简式分别为 、 。
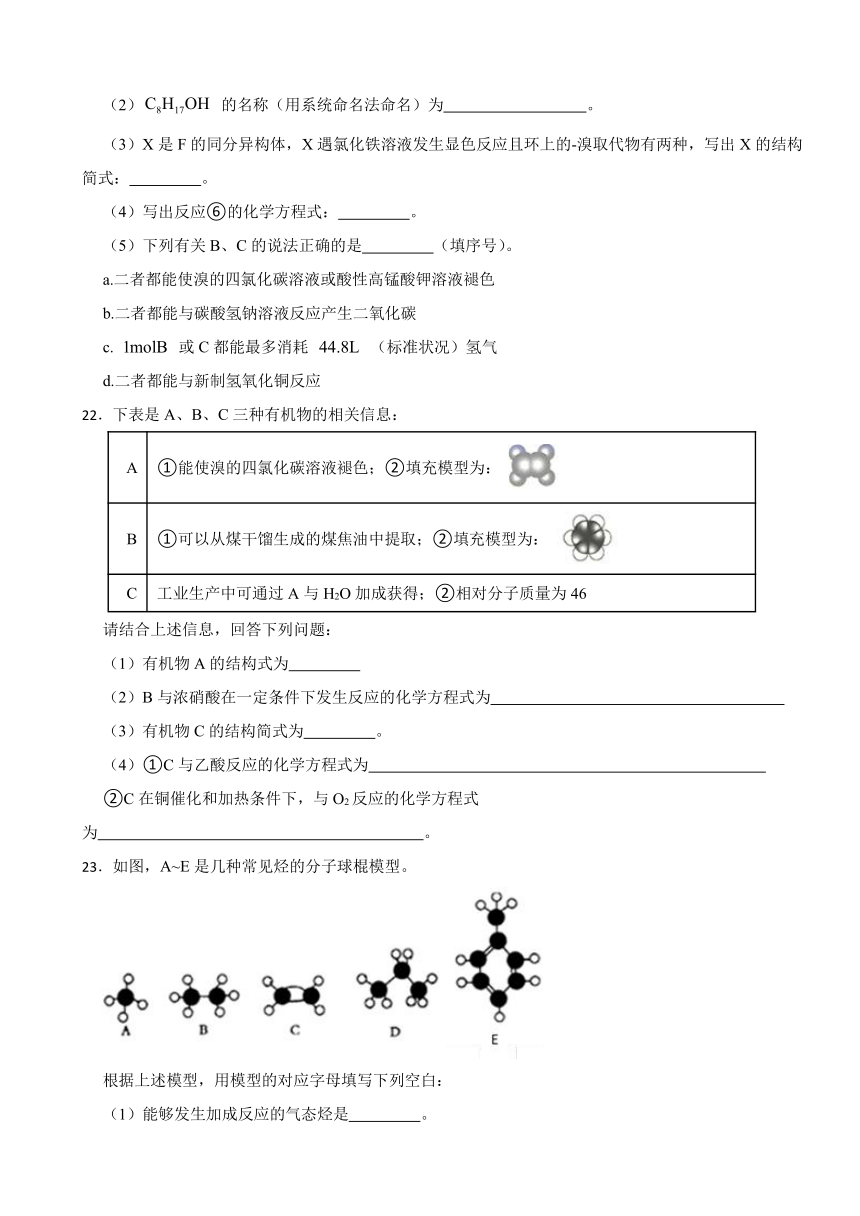
(2) 的名称(用系统命名法命名)为 。
(3)X是F的同分异构体,X遇氯化铁溶液发生显色反应且环上的-溴取代物有两种,写出X的结构简式: 。
(4)写出反应⑥的化学方程式: 。
(5)下列有关B、C的说法正确的是 (填序号)。
a.二者都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色
b.二者都能与碳酸氢钠溶液反应产生二氧化碳
c. 或C都能最多消耗 (标准状况)氢气
d.二者都能与新制氢氧化铜反应
22.下表是A、B、C三种有机物的相关信息:
A ①能使溴的四氯化碳溶液褪色;②填充模型为:
B ①可以从煤干馏生成的煤焦油中提取;②填充模型为:
C 工业生产中可通过A与H2O加成获得;②相对分子质量为46
请结合上述信息,回答下列问题:
(1)有机物A的结构式为
(2)B与浓硝酸在一定条件下发生反应的化学方程式为
(3)有机物C的结构简式为 。
(4)①C与乙酸反应的化学方程式为
②C在铜催化和加热条件下,与O2反应的化学方程式为 。
23.如图,A~E是几种常见烃的分子球棍模型。
根据上述模型,用模型的对应字母填写下列空白:
(1)能够发生加成反应的气态烃是 。
(2)一氯代物的同分异构体最多的是 。
(3)所有原子均在同一平面上的是 。
(4)能使酸性高锰酸钾溶液褪色的是 。
24.写出下列反应的化学方程式,并注明反应类型
(1)由丙烯制备聚丙烯的反应 反应类型
(2)用甲苯制TNT的反应 反应类型
(3)苯制溴苯 反应类型
(4)乙烯通入溴水中 反应类型 .
25.从石油中获取乙烯已成为生产乙烯的重要途径。如图表示几种有机物的相互转化关系:
(1)以石油为原料,获取大量乙烯的主要方法是 (填标号)。
a.水解 b.裂解 c.分馏 d.干馏
(2)C中官能团的名称是 ,D的结构简式是 。
(3)反应①的化学方程式为 。
(4)A是一种高分子化合物,可用于食品包装,②的反应类型为 。
(5)CH3COOCH2CH3是种油状的液体,实验室制取CH3COOCH2CH3的装置如图所示:
①A中发生反应的化学方程式为 。
②试管B中盛放的溶液是 ,B中分离出的CH3COOCH2CH3中常含有少量的水,最好加入 作吸水剂(填标号)。
a.碱石灰 b.氢氧化钾 c.无水硫酸钠
答案解析部分
1.【答案】D
【解析】【解答】乙烷、乙醇和丙烯均含有甲基,分子中所有原子不可能处于同一平面上,乙烯为平面结构,所有原子都处于同一平面,
故答案为:D。
【分析】在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,甲基具有甲烷的结构特点,分子中所有原子不可能处于同一平面上。
2.【答案】B
【解析】【解答】A.乙烯能与水发生加成反应生成乙醇,A不符合题意;
B.明矾净水是因为铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中杂质使其沉降,从而达到净水的目的,B符合题意;
C.硅为半导体材料,能用于制作太阳能电池,C不符合题意;
D.轮船铁护栏上绑一块锌,形成原电池,锌作负极被腐蚀,铁作正极被保护,为牺牲阳极的阴极保护法,D不符合题意;
故答案为:B。
【分析】A、乙烯和水加成生成乙醇;
B、明矾在水中生成氢氧化铝胶体;
C、硅是半导体材料,可以制作太阳能电池板和芯片;
D、锌比铁活泼,作为负极,为牺牲阳极的阴极保护法。
3.【答案】B
【解析】【解答】A.乙烯分子中键角是120°,所有原子在同一平面上,因此乙烯分子属于平面分子,C2H4分子中各个原子不在同一条直线上,而乙炔分子是直线形分子,A不符合题意;
B.乙烯分子中C原子之间以共价双键结合,两个C原子再与4个H原子形成4个C-H共价键,碳碳双键是非极性键,C-H键是极性键,因此乙烯分子中含有极性键和非极性键,B符合题意;
C.乙炔分子中2个C原子之间以共价三键结合,每个C原子分别与1个H原子形成C-H共价键,共价单键都是σ键,共价三键中含有1个σ键和2个π键,因此乙炔分子中含有3个σ键和2个π键,C不符合题意;
D.乙烯分子式是C2H4,属于烯烃;而分子式为C4H8的烃与C2H4在分子组成上相差2个CH2原子团,但C4H8可能是烯烃,也可能是环烷烃,因此二者不一定互为同系物,D不符合题意;
故答案为:B。
【分析】A、乙烯分子不是直线分子;
C、乙炔分子中含有3个σ键和2个π键;
D、两者不一定互为同系物,因为C4H8可以是烯烃,也可以是环烷烃。
4.【答案】D
【解析】【解答】A.为保证食物的口感和安全性,可以符合题意选择合适的食品添加剂并适量添加,A项不符合题意;
B.石墨烯是一种无机碳单质,不属于有机高分子材料,B项不符合题意;
C.冰的密度比水小,是因为固态水分子间存在的氢键数目更多,且氢键具有方向性,空间体积更大,所以冰的密度更小,C项不符合题意;
D.风能和太阳能属于新型能源,同时也属于清洁能源,采用风能和太阳能为奥运服务体现了绿色化学、绿色奥运这一理念,D项符合题意;
故答案为:D。
【分析】A.食品添加剂合理添加即可;
B.石墨烯为碳单质,属于无机非金属材料;
C.水蒸气中水分子主要以单个分子的形式存在,液态水中多个水分子通过氢键结合在一起,形成(H2O)n,冰中所有水分子以氢键互相联结成晶体,氢键的形成使水分子之间的间隙增大,从而导致冰的密度比水的密度小。
5.【答案】C
【解析】【解答】A.相对分子质量在一万以上的是高分子化合物,而多糖和蛋白质均为高分子化合物,且均能水解,故A不符合题意;
B.光导纤维主要成分是二氧化硅,利用的导光性,具有特殊的光学性能,故B不符合题意;
C.羊绒衫主要成分是蛋白质;棉村衣主要成分是纤维素,蛋白质和纤维素都是天然高分子化合物,不是合成纤维,故C符合题意;
D.BaSO4不溶于水和酸,在X光的照射下显示出白色光点,对人体无害,可用于肠胃X射线造影检查,故D不符合题意;
故答案为:C。
【分析】A、多糖和蛋白质都是高分子化合物,可以发生水解;
B、二氧化硅可以制作光导纤维,单质硅可以制作芯片和太阳能电池板;
C、尼龙属于合成纤维,羊毛衫和棉衬衣属于天然纤维;
D、钡餐指的是硫酸钡。
6.【答案】D
【解析】【解答】解:A.乙烯含碳碳双键其中1根键断裂,相互加成生成聚乙烯,聚乙烯中不存在双键,聚乙烯塑料的老化是由于长链断裂等原因,故A错误;
B.煤的气化是煤在氧气不足的条件下进行部分氧化形成H2、CO等气体的过程,煤的液化是将煤与H2在催化剂作用下转化为液体燃料或利用煤产生的H2和CO通过化学合成产生液体燃料或其他液体化工产品的过程,所以煤经过气化和液化等变化是化学变化,故B错误;
C.合成纤维、人造纤维都属于有机高分子材料,碳纤维是碳的单质,不属于有机高分子材料,故C错误;
D.用粮食酿酒时,先在糖化酶作用下水解为葡萄糖,然后在酵母作用下转变为酒精,都是化学变化,故D正确;故选D.
【分析】A.聚乙烯塑料是乙烯发生加成反应生成的高分子聚合物,聚乙烯的单体是乙烯;
B.煤的气化、液化都是化学变化;
C.碳纤维是碳的单质;
D.淀粉→葡萄糖→乙醇都是化学变化;
7.【答案】A
【解析】【解答】A.同位素是质子数相同在,中子数不同,故A符合题意;
B.电池板主要用的硅单质,故B不符合题意;
C.煤油是混合物,故C不符合题意;
D.碳纤维属于无机非金属材料,故D不符合题意;
故答案为:A
【分析】A.考查的是同位素的概念;
B.电池板主要是硅单质;
C.煤油是混合物;
D.考查的碳纤维属于无机非金属材料。
8.【答案】D
【解析】【解答】A.制造N95口罩的聚丙烯树脂中没有碳碳双键,故A不符合题意;
B.C6H14为己烷,有5种同分异构体,分别为正己烷、2-甲基戊烷、3-甲基戊烷、2,2-二甲基丁烷、2,3-二甲基丁烷,故B不符合题意;
C.乙烯与溴水发生加成反应使溴水褪色,乙烯使酸性高锰酸钾溶液褪色是因为被高锰酸钾溶液氧化,褪色原理不同,故C不符合题意;
D.C2H6完全燃烧,若生成水的质量为2.7 g,则n(H2O)= =0.15mol,n(H) =0.3mol,根据乙烷的分子式可知,n(C) =0.1mol,则完全燃烧生成CO2的物质的量为0.1mol,质量为4.4g,故D符合题意。
故答案为:D。
【分析】A.丙烯发生加聚反应生成聚丙烯树脂,都是单键
B.烷烃一般都是支链异构,根据碳原子个数定主链,再定支链即可
C.褪色原理不同,溴水是发生加成反应,而高锰酸钾是发生氧化还原反应而褪色
D.根据方程式可以进行计算
9.【答案】D
【解析】【解答】A.棉花、优质针叶木等原料的主要成分是纤维素,A不符合题意;
B.Fe3O4是磁性物质,有磁性,B不符合题意;
C.树脂相对分子质量很大,属于有机高分子材料,C不符合题意;
D.葡萄糖遇碘不变蓝,D符合题意;
故答案为:D。
【分析】A.纤维素属于糖类;
B.Fe3O4 俗称氧化铁黑、吸铁石、黑氧化铁,为具有磁性的黑色晶体,故又称为磁性氧化铁 ;
C.高分子化合物相对分子质量很大,一般在10000以上,可高达几百万;
D.碘单质遇碘变蓝。
10.【答案】B
【解析】【解答】A. 桂醛分子中所有原子均可能处于同一平面上 ,A选项是正确的;
B.1mol苯环上可以加成3molH2,碳碳双键可以与1molH2加成,1mol-CHO发生加成反应,所以1mol桂醛分子可以与5molH2发生加成反应,B选项是错误的;
C. 香茅醇的分子式为C10H20O ,C选项是错误的;
D. 桂醛有醛基,而 D-香芹酮 没有醛基,所以可以用银氨溶液来鉴别二者,D选项是正确的。
故答案为:B。
【分析】A.苯环和碳碳双键都是平面结构,因此桂醛分子中所有原子均可能处于同一平面上;
B.1mol苯环上可以加成3molH2,碳碳双键可以与1molH2加成,1mol-CHO发生加成反应,所以1mol桂醛分子可以与5molH2发生加成反应;
C.香茅醇的分子式为C10H20O ;
D.醛基可以与银氨溶液发生氧化还原反应,得到银镜,即银单质。
11.【答案】D
【解析】【解答】解:A.常温下,C4H10是气体,故A正确;
B.丁烷有CH3CH2CH2CH3、CH3CH(CH3)2两种同分异构体,前者为正丁烷、后者为异丁烷,故B正确;
C.C4H10与CH4都属于烷烃,结构相似,在组成上相差3个CH2原子团,二者互为同系物,故C正确;
D.丁烷有正丁烷与异丁烷两种同分异构体,正丁烷分子种有2种H原子,其一氯代物有2种,异丁烷分子种有2种H原子,其一氯代物有2种,故丁烷的一氯代物有4种,即有4种沸点不同的产物一氯代物,故D错误,
故选D.
【分析】A.常温下,碳原子数目小于或等于4的烃为气体;
B.利用减少碳原子作取代基书写丁烷的同分异构体;
C.结构相似,在组成上相差1个或若干个CH2原子团的化合物互称同系物;
D.判断丁烷的同分异构体,再根据等效氢确定一氯代物的同分异构体,据此判断.
12.【答案】B
【解析】【解答】A.CH3CH3与Cl2取代产物有多种,得不到纯净的CH2ClCH2Cl,故A不符合题意;
B.CH2=CH2与HCl加成只生成CH3CH2Cl,得不到CH2ClCH2Cl,故B不符合题意;
C.CH2=CH2与Cl2加成只生成CH2ClCH2Cl,故C符合题意;
D.CH3CH2Cl与Cl2取代产物有多种,得不到纯净的CH2ClCH2Cl,故D不符合题意。
【分析】制备纯净的1,2-二氯乙烷一般采用加成反应可以得到纯净的产物,而取代反应会混有杂质,据此解答即可。
13.【答案】A
【解析】【解答】A.从分子结构上,糖是多羟基醛、多羟基酮或它们的脱水缩合物,故A符合题意;
B.某些含有苯环的蛋白质溶液与浓硝酸作用,先变性生成白色沉淀,加热后沉淀发生显色反应变为黄色,故B不符合题意;
C.酯是易挥发而具有芳香气味的有机化合物,所以含有酯类的水果会因含有低级酯类物质而具有特殊香味,故C不符合题意;
D.聚乙烯、聚氯乙烯的是具有优良性能的热塑性塑料,故D不符合题意;
故答案为:A。
【分析】A.糖是多羟基醛、多羟基酮或它们的脱水缩合物;
B.蛋白质溶液与浓硝酸作用,先变性生成白色沉淀,加热后沉淀变黄色;
C.酯类具有特殊香味;
D.聚乙烯、聚氯乙烯是常见的热塑性塑料。
14.【答案】A
【解析】【解答】A. 因为乙烷不和溴水反应,而乙烯能和溴水发生加成反应而使溴水退色,且生成的CH2BrCH2Br为液态,便于分离,故A符合题意;
B. 乙烷和乙烯均是无色气体,但前者易发生取代反应,后者易发生加成反应,若与足量溴蒸气反应,乙烷可以发生取代反应,乙烯则发生加成反应生成CH2BrCH2Br,不仅不易鉴别,还会损失大量的乙烷且混入大量的溴蒸气杂质,故B不符合题意;
C. 若在一定条件下通入氢气,虽可将乙烯转变为乙烷,但通入氢气的量不易控制,很难得到纯净的乙烷,且用氢气无法鉴别它们,故C不符合题意;
D. 乙烯被酸性高锰酸钾溶液氧化生成二氧化碳,会引入新杂质二氧化碳,故D不符合题意;
故答案为:A。
【分析】鉴别乙烷和乙烯可根据乙烯含有不饱和键,能使溴水褪色分析,除去乙烷中混有的少量乙烯时注意不能引入新的杂质,并且不能影响乙烷的量。
15.【答案】D
【解析】【解答】解:乙烯可有石油裂解生成,且乙烯用途广泛,可用于制造塑料、合成纤维、有机溶剂等,带动了其他以石油为原料的石油化工的发展.因此一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志,
故选D.
【分析】乙烯主要用于制造塑料、合成纤维、有机溶剂等,是石油化工发展的标志.
16.【答案】D
【解析】【解答】A.乙烯分子中的2个C原子和4个氢原子处于同一平面,苯是平面正六边形结构,都属于不饱和烃,但苯分子中的碳碳键完全相同,没有碳碳双键,A选项不符合题意;
B.乙烯和苯都可以来自于石油,石油的裂解可获得乙烯、石油的催化重整可获得苯,乙烯工业的发展,带动了其他以石油为原料的石油化工的发展,因此,乙烯的产量是衡量一个国家石油化工发展水平的标志,B选项不符合题意;
C.乙烯含有碳碳双键能够发生加成反应,苯的不饱和度很大,也能与氢气、氯气等发生加成反应,C选项不符合题意;
D.乙烯和苯都可以在氧气中燃烧,发生氧化反应,D选项符合题意;
故答案为:D。
【分析】A.苯环中不存在碳碳双键;
B.苯来自于煤的加工;
C.苯既能发生取代又能发生加成反应;
D.乙烯和苯都能和氧气发生氧化反应。
17.【答案】D
【解析】【解答】A.常温下, Zn 和浓硫酸反应可以得到 SO2 ,而 Al 和浓硫酸发生钝化得不到 SO2,A不符合题意;
B.H2O、H2S、CH4、SiH4均属于分子晶体,H2O的沸点比 H2S 的沸点高,是因为H2O中含有氢键,B不符合题意;
C.乙烯使溴水褪色发生加成反应,而乙烯使酸性高锰酸钾褪色发生的是氧化还原反应,C不符合题意;
D.铁元素化合价有+2、+3,铜元素化合价有+1、+2,由分析可知, 加热条件下,和能直接化合生成,则加热条件下和也能直接化合生成 ,D符合题意;
故答案为:D。
【分析】A.常温下,铝遇浓硫酸发生钝化。
B.一般分子晶体的熔沸点随相对分子质量的增大而升高,含有氢键的分子晶体熔沸点较高。
C.注意乙烯使酸性高锰酸钾褪色的原理是二者发生了氧化还原反应。
D.S氧化性较弱,与变价金属反应生成低价态的硫化物。
18.【答案】D
【解析】【解答】聚四氟乙烯不含不饱和键,不能发生加成反应,也不能使酸性高锰酸钾溶液褪色,故A不符合题意;
四氯乙烯中C原子的杂化类型为sp2杂化,故B不符合题意;
聚四氟乙烯具有高度的化学稳定性,故C不符合题意;
Cl和F为同主族元素,由于电负性F大于Cl,因此C-F键极性大于C-Cl键极性,故D符合题意。
【分析】
A.后者不含双键,不可加成;
B.杂化类型是sp2杂化;
C.其化学性质稳定;
D.氟元素电负性大于氯元素,故键的极性较大。
19.【答案】B
【解析】【解答】A.柠檬酸分子中有三个羧基,酸性比碳酸强,A不符合题意;
B.柠檬酸分子中有羟基,可与水分子形成氢键,B符合题意;
C.柠檬酸分子中含有三个羧基,1mol 柠檬酸可与3molNaOH反应,C不符合题意;
D.柠檬酸分子中含有三个羧基和一个醇羟基,可发生取代反应、氧化反应,不能发生加成反应,D不符合题意;
故答案为:B
【分析】A.三个羧基,酸性比碳酸强;
B.有羟基,可与水分子形成氢键;
C.羧基和NaOH反应;
D.羧基和醇羟基,可发生取代反应、氧化反应,不能发生加成反应。
20.【答案】D
【解析】【解答】A.CH3CH3与溴发生取代反应生成CH3-CH2Br,故A不符合要求;
B.CH3COOH与乙醇发生酯化反应生成水和CH3COOC2H5,故B不符合要求;
C.苯与液溴在铁催化作用下发生取代反应生成溴苯和溴化氢,故C不符合要求;
D.乙烯含碳碳双键与水发生加成反应生成乙醇,故D符合要求;
故答案为:D。
【分析】发生加成的前提是含有不饱和键,一般是碳碳双键、碳碳三键、醛基等等,D中发生的是双键的加成,其他均是取代反应
21.【答案】(1);
(2)2-乙基-1-己醇
(3)
(4)
(5)d
【解析】【解答】(1)由分析可知B的结构简式为CH2=CHCHO,G的结构简式为 ;故答案为:CH2=CHCHO; ;
(2)C8H17OH为 ,与-OH相连的C原子为第1位碳原子编号来命名,其名称为2-乙基-1-己醇;故答案为:2-乙基-1-己醇;
(3)F为苯甲醚,X遇氯化铁溶液发生显色反应且环上的一溴取代物有两种,X为酚,甲基与酚羟基处于对位,则X为 ;故答案为: ;
(4)由信息Ⅰ,D与G合成Q,并生成HBr,反应⑥的化学方程式为 ;故答案为: ;
(5)B为烯醛,C为烯酸,均含C=C键,但羧基中的C=O不能与氢气发生加成反应;
a.均含C=C键,则二者都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色,故a正确;
b.C中含-COOH,能与碳酸氢钠溶液反应产生二氧化碳,而B不能,故b不正确;
c.1mol B最多消耗44.8L(标准状况)氢气,而C消耗22.4L氢气,故c不正确;
d.B中含-CHO,C中含-COOH,二者都能与新制氢氧化铜悬浊液反应,故d正确;
故答案为ad。
【分析】由A、B的分子式及的结构简式C可知,A为CH3CH=CH2,B为CH2=CHCHO,由信息Ⅱ可知,C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与碳酸氢钠反应生成CO2,其消去产物的分子中只有一个碳原子上没有氢原子,则C8H17OH为 ,与丙烯酸发生酯化反应生成D,由流程图可知,F为 等,因F不能与NaOH溶液反应,所以F为苯甲醇或苯甲醚,由F和G的分子式可知,F与溴发生取代反应,又G的核磁共振氢谱中有3组峰,说明G中有3种位置的H原子,所以G为 。
22.【答案】(1)
(2) +HO-NO2 +H2O
(3)C2H5OH
(4)CH3COOH +HOCH2CH3 CH3COOCH2CH3+ H2O;2CH3CH2OH + O2 2CH3CHO + 2H2O
【解析】【解答】(1)A为乙烯,其结构式为 ;
(2)苯与浓硝酸在浓硫酸、加热(50℃~60℃)的条件下发生取代反应生成硝基苯和水,化学方程式为 +HO-NO2 +H2O;
(3)C为乙醇,结构简式为C2H5OH;
(4)①乙醇和乙酸在浓硫酸加热的条件下可以发生酯化反应生成乙酸乙酯,化学方程式为CH3COOH +HOCH2CH3 CH3COOCH2CH3+ H2O;
②C在铜催化和加热条件下被氧气氧化成乙醛,化学方程式为2CH3CH2OH + O2 2CH3CHO + 2H2O。
【分析】A能使溴的四氯化碳溶液褪色,结合其填充模型可知应含有碳碳双键,A为CH2=CH2;B可以可以从煤干馏生成的煤焦油中提取,结合其填充模型可知为苯;C可通过A与H2O加成获得,相对分子质量为46,所以C为CH3CH2OH。
23.【答案】(1)C
(2)E
(3)C
(4)CE
【解析】【解答】(1)能够发生加成的烃为:乙烯和甲苯,其中气态的烃为乙烯,故答案为:C;
(2) 甲烷、乙烷、乙烯、丙烷、甲苯中分别含有1种、1种、1种、2种、4种环境的氢原子,因此一卤代物种类最多的是甲苯,共有4种一氯代物,故答案为:E;
(3)所有原子均在同一平面上的是乙烯,故答案为:C;
(4)乙烯和甲苯能够使酸性高锰酸钾溶液褪色,故答案为:CE。
【分析】根据分子的球棍模型可知:A为甲烷,B为乙烷,C为乙烯,D为丙烷,E为甲苯,根据物质的结构和性质分析解答。
24.【答案】(1);加聚反应
(2);取代反应
(3);取代反应
(4)CH2=CH2+Br2→BrCH2CH2Br;加成反应
【解析】【解答】解:(1)丙烯能发生加聚反应得到聚丙烯,方程式为 ,属于加聚反应,
故答案为: ;加聚反应;(2)甲苯可以和浓硝酸之间发生取代反应生成2,4,6﹣三硝基甲苯,即TNT,化学反应方程式为 ,属于取代反应;
故答案为: ;取代反应;(3)苯与液溴反应苯环上的氢原子被溴原子代替生成溴苯和溴化氢,化学方程式为: ,属于取代反应;
故答案为: ;取代反应;(4)乙烯含碳碳双键,与溴水发生加成反应,反应为CH2=CH2+Br2→BrCH2CH2Br,故答案为:CH2=CH2+Br2→BrCH2CH2Br;加成反应.
【分析】(1)丙烯分子含有碳碳双键,发生加聚反应生成聚丙烯;(2)甲苯与浓硝酸发生取代反应可生成TNT,即三硝基甲苯;(3)苯与液溴发生取代反应生成溴苯;(4)乙烯含碳碳双键,与溴水发生加成反应.
25.【答案】(1)b
(2)羟基;CH3CHO
(3)
(4)加聚反应
(5);饱和Na2CO3;c
【解析】【解答】(1)工业上通过石油裂解可以获得大量乙烯,b正确,故答案为:b;
(2)C的结构简式为CH3CH2OH,官能团为羟基;D的结构简式为CH3CHO,故答案为:羟基;CH3CHO;
(3)反应①为乙烯与溴水发生加成反应生成BrCH2CH2Br,反应的化学方程式为 ,故答案为: ;
(4)反应②为一定条件下,乙烯发生加聚反应生成聚乙烯,故答案为:加聚反应;
(5)①装置A中发生的反应为在浓硫酸作用下,CH3CH2OH和CH3COOH共热发生酯化反应生成CH3COOCH2CH3,反应的化学方程式为 ,故答案为: ;
②试管B中盛放的溶液是饱和碳酸钠溶液,目的是除去乙酸,吸收乙醇,降低乙酸乙酯的溶解度,便于分层;乙酸乙酯在碱溶液中会发生水解反应,所以除去CH3COOCH2CH3中含有少量的水不能加入碱石灰和氢氧化钾,应该加入无水硫酸钠,c正确,故答案为:饱和Na2CO3;c。
【分析】由题给有机物的转化关系可知,通过石油裂解可以获得大量乙烯;一定条件下,乙烯发生加聚反应生成聚乙烯,则A为聚乙烯;乙烯与溴水发生加成反应生成BrCH2CH2Br,则B为BrCH2CH2Br;在催化剂作用下,乙烯与水发生加成反应生成CH3CH2OH,则C为CH3CH2OH;在Cu或Ag做催化剂作用下,CH3CH2OH与氧气共热发生催化氧化反应生成CH3CHO,则D为CH3CHO;在催化剂作用下,CH3CHO与氧气共热发生催化氧化反应生成CH3COOH,在浓硫酸作用下,CH3CH2OH和CH3COOH共热发生酯化反应生成CH3COOCH2CH3。
2023-2024学年高一下学期化学人教版(2019)必修第二册
一、单选题
1.下列化合物的分子中,所有原子都处于同一平面的有( )
A.乙烷 B.乙醇 C.丙烯 D.乙烯
2.化学创造美好生活。下列生产活动中,没有运用相应化学原理的是( )
选项 生产活动 化学原理
A 乙烯水化法制工业酒精 乙烯可发生加成反应
B 利用明矾净水 Al3+有氧化性
C 利用硅做太阳能电池 硅是半导体材料
D 轮船铁护栏上绑一块锌 牺牲阳极保护阴极
A.A B.B C.C D.D
3.下列说法正确的是( )
A.乙烯和乙炔都是直线形分子
B.乙烯分子中含有极性键和非极性键
C.乙炔分子中含有1个σ键和2个π键
D.乙烯与分子式为C4H8的烃一定互为同系物
4.2022年2月,第24届冬奥会在北京成功举办。下列有关说法正确的是( )
A.为保证食物的口感和安全性,不能在食品中添加任何食品添加剂
B.北京冬奥会上,礼仪服饰采用高科技石墨烯发热材料,石墨烯属于有机高分子材料
C.冰的密度比水小,是因为水分子内存在氢键
D.“绿色奥运”是本届奥运会的理念之一,采用风能和太阳能为奥运服务体现了这一理念
5.化学与生产生活密切相关。下列说法错误的是( )
A.多糖、蛋白质都是高分子化合物,一定条件下都能水解
B.具有特殊的光学性能,可用于制作光导纤维
C.尼龙绳、羊绒衫和棉衬衣等生活用品都是由合成纤维制造的
D.不溶于水和酸,可用于胃肠X射线造影检查
6.化学与生活密切相关,下列说法正确的是( )
A.聚乙烯塑料的老化是由于发生了加成反应
B.煤经过气化和液化等物理变化可以转化为清洁燃料
C.合成纤维、人造纤维及碳纤维都属于有机高分子材料
D.利用粮食酿酒经过了淀粉→葡萄糖→乙醇的化学变化过程
7.2023年5月10日,最强太空“快递小哥”天舟六号货运飞船由长征七号运载火箭发射升空,体现了我国强大科技力量。下列说法正确的是( )
A.“天舟六号”为空间站送去电推进氙气瓶,与互为同位素
B.“天舟六号”配有半刚性太阳电池阵“翅膀”,电池板主要成分是
C.“长征七号”采用液氧、煤油等作为推进剂,液氧、煤油是纯净物
D.“长征七号”使用碳纤维材料减轻火箭质量,碳纤维属于有机高分子材料
8.下列说法中正确的是( )
A.制造N95口罩的聚丙烯树脂中含有碳碳双键
B.C6H14有4种同分异构体
C.乙烯能使溴水和酸性高锰酸钾溶液褪色,且褪色原理也相同
D.C2H6完全燃烧生成的CO2和H2O的质量可能是4.4 g和2.7 g
9.新版人民币的发行,引发了人们对有关人民币中化学知识的关注。下列表述错误的是( )
A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素
B.用于人民币票面方案等处的油墨中所含有的Fe3O4是一种磁性物质
C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料
D.某种验钞笔中含有碘酒,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖
10.以下3种有机物是一些食用香精和精油的主要成分,下列说法不正确的是( )
A.桂醛分子中所有原子均可能处于同一平面上
B.1mol桂醛最多与4mol H2发生加成反应
C.香茅醇的分子式为C10H20O
D.可用银氨溶液鉴别桂醛和D-香芹酮
11.下列关于丁烷的叙述不正确的是( )
A.常温下,C4H10是气体
B.丁烷有正丁烷写异丁烷两种同分异构体
C.C4H10与CH4互为同系物
D.C4H10进行一氯取代时最多生成两种沸点不同的产物
12.欲制取较纯净的CH2ClCH2Cl(即1,2-二氯乙烷),最合理的方法是( )
A.CH3CH3与Cl2取代 B.CH2=CH2与 HCl加成
C.CH2=CH2与Cl2加成 D.CH3CH2Cl与Cl2取代
13.下列说法错误的是
A.从分子结构上看糖类都是多羟基醛及其缩合产物
B.蛋白质溶液与浓硝酸作用产生白色沉淀,加热后沉淀变黄色
C.水果中因含有低级酯类物质而具有特殊香味
D.聚乙烯、聚氯乙烯是热塑性塑料
14.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯,得到纯净乙烷的方法是( )
A.通入足量溴水中 B.与足量溴蒸气反应
C.在一定条件下通入氢气 D.通入酸性KMnO4溶液中
15.通常用来衡量一个国家石油化工发展水平标志的是( )
A.甲烷的产量 B.苯的产量 C.乙醇的产量 D.乙烯的产量
16.石油被誉为“工业的血液”,乙烯和苯都是重要的石油化工产品,也是重要的有机化工原料。下列关于乙烯和苯的叙述正确的是( )
A.乙烯和苯都是平面型分子,分子结构中都含有碳碳双键,都属于不饱和烃
B.乙烯和苯都可以来自于石油,石油的产量是衡量一个国家石油化工发展水平的标志
C.乙烯易发生加成反应,苯不能发生加成反应
D.乙烯和苯都可以发生氧化反应
17.下列“类比”合理的是( )
A.常温下, Zn 和浓硫酸反应可以得到 SO2 ,则常温下 Al 和浓硫酸反应也可以得到 SO2
B.H2O 的沸点比H2S 的沸点高,则 CH4 的沸点比 SiH4 的沸点高
C.乙烯使溴水褪色发生加成反应,则乙烯使酸性高锰酸钾褪色也发生加成反应
D.加热条件下,和能直接化合生成,则加热条件下和也能直接化合生成
18.四氯乙烯()是一种衣物干洗剂,聚四氟乙烯()是家用不粘锅内侧涂层的主要成分,下列说法正确的是( )
A.它们都能发生加成反应,都能使酸性高锰酸钾溶液褪色
B.它们的分子中C原子的杂化类型均为sp3杂化
C.四氯乙烯对油脂有较好的溶解作用,聚四氟乙烯的化学性质比较活泼
D.Cl和F为同主族元素,由于电负性F大于Cl,因此C-F键极性大于C-Cl键极性
19.《本草纲目》果部第三十卷中提到“山楂化饮食,消肉积、症瘕、痰饮、痞满吞酸、滞血痛胀。”山楂中的有效成分枸橼酸又称柠檬酸,结构如下,下列说法中正确的是
A.柠檬酸的酸性比碳酸弱
B.柠檬酸易溶于水,可与水分子形成氢键
C.1mol 柠檬酸可与4molNaOH反应
D.柠檬酸可发生取代反应、加成反应和氧化反应
20.下列变化是通过加成反应来实现的是( )
A.CH3CH3→CH3-CH2Br B.CH3COOH→CH3COOC2H5
C. → D.CH2=CH2→CH3CH2OH
二、综合题
21.Q是合成防晒霜的主要成分,某同学以石油化工的基本产品为主要原料,设计合成Q的流程如图(部分反应条件和试剂未注明):
已知:Ⅰ.钯催化的交叉偶联反应原理(R、R1为烃基或其他基团,X为卤素原子):
Ⅱ. 分子中只有一个支链,且为乙基,其连续氧化的产物能与碳酸氢钠反应生成 ,其消去产物的分子只有一个碳原子上没有氢原子。
Ⅲ.F不能与氢氧化钠溶液反应,G的核磁共振氢谱中有3个峰且为对位取代物。
请回答下列问题:
(1)B、G的结构简式分别为 、 。
(2) 的名称(用系统命名法命名)为 。
(3)X是F的同分异构体,X遇氯化铁溶液发生显色反应且环上的-溴取代物有两种,写出X的结构简式: 。
(4)写出反应⑥的化学方程式: 。
(5)下列有关B、C的说法正确的是 (填序号)。
a.二者都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色
b.二者都能与碳酸氢钠溶液反应产生二氧化碳
c. 或C都能最多消耗 (标准状况)氢气
d.二者都能与新制氢氧化铜反应
22.下表是A、B、C三种有机物的相关信息:
A ①能使溴的四氯化碳溶液褪色;②填充模型为:
B ①可以从煤干馏生成的煤焦油中提取;②填充模型为:
C 工业生产中可通过A与H2O加成获得;②相对分子质量为46
请结合上述信息,回答下列问题:
(1)有机物A的结构式为
(2)B与浓硝酸在一定条件下发生反应的化学方程式为
(3)有机物C的结构简式为 。
(4)①C与乙酸反应的化学方程式为
②C在铜催化和加热条件下,与O2反应的化学方程式为 。
23.如图,A~E是几种常见烃的分子球棍模型。
根据上述模型,用模型的对应字母填写下列空白:
(1)能够发生加成反应的气态烃是 。
(2)一氯代物的同分异构体最多的是 。
(3)所有原子均在同一平面上的是 。
(4)能使酸性高锰酸钾溶液褪色的是 。
24.写出下列反应的化学方程式,并注明反应类型
(1)由丙烯制备聚丙烯的反应 反应类型
(2)用甲苯制TNT的反应 反应类型
(3)苯制溴苯 反应类型
(4)乙烯通入溴水中 反应类型 .
25.从石油中获取乙烯已成为生产乙烯的重要途径。如图表示几种有机物的相互转化关系:
(1)以石油为原料,获取大量乙烯的主要方法是 (填标号)。
a.水解 b.裂解 c.分馏 d.干馏
(2)C中官能团的名称是 ,D的结构简式是 。
(3)反应①的化学方程式为 。
(4)A是一种高分子化合物,可用于食品包装,②的反应类型为 。
(5)CH3COOCH2CH3是种油状的液体,实验室制取CH3COOCH2CH3的装置如图所示:
①A中发生反应的化学方程式为 。
②试管B中盛放的溶液是 ,B中分离出的CH3COOCH2CH3中常含有少量的水,最好加入 作吸水剂(填标号)。
a.碱石灰 b.氢氧化钾 c.无水硫酸钠
答案解析部分
1.【答案】D
【解析】【解答】乙烷、乙醇和丙烯均含有甲基,分子中所有原子不可能处于同一平面上,乙烯为平面结构,所有原子都处于同一平面,
故答案为:D。
【分析】在常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,甲基具有甲烷的结构特点,分子中所有原子不可能处于同一平面上。
2.【答案】B
【解析】【解答】A.乙烯能与水发生加成反应生成乙醇,A不符合题意;
B.明矾净水是因为铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有吸附性,能吸附水中杂质使其沉降,从而达到净水的目的,B符合题意;
C.硅为半导体材料,能用于制作太阳能电池,C不符合题意;
D.轮船铁护栏上绑一块锌,形成原电池,锌作负极被腐蚀,铁作正极被保护,为牺牲阳极的阴极保护法,D不符合题意;
故答案为:B。
【分析】A、乙烯和水加成生成乙醇;
B、明矾在水中生成氢氧化铝胶体;
C、硅是半导体材料,可以制作太阳能电池板和芯片;
D、锌比铁活泼,作为负极,为牺牲阳极的阴极保护法。
3.【答案】B
【解析】【解答】A.乙烯分子中键角是120°,所有原子在同一平面上,因此乙烯分子属于平面分子,C2H4分子中各个原子不在同一条直线上,而乙炔分子是直线形分子,A不符合题意;
B.乙烯分子中C原子之间以共价双键结合,两个C原子再与4个H原子形成4个C-H共价键,碳碳双键是非极性键,C-H键是极性键,因此乙烯分子中含有极性键和非极性键,B符合题意;
C.乙炔分子中2个C原子之间以共价三键结合,每个C原子分别与1个H原子形成C-H共价键,共价单键都是σ键,共价三键中含有1个σ键和2个π键,因此乙炔分子中含有3个σ键和2个π键,C不符合题意;
D.乙烯分子式是C2H4,属于烯烃;而分子式为C4H8的烃与C2H4在分子组成上相差2个CH2原子团,但C4H8可能是烯烃,也可能是环烷烃,因此二者不一定互为同系物,D不符合题意;
故答案为:B。
【分析】A、乙烯分子不是直线分子;
C、乙炔分子中含有3个σ键和2个π键;
D、两者不一定互为同系物,因为C4H8可以是烯烃,也可以是环烷烃。
4.【答案】D
【解析】【解答】A.为保证食物的口感和安全性,可以符合题意选择合适的食品添加剂并适量添加,A项不符合题意;
B.石墨烯是一种无机碳单质,不属于有机高分子材料,B项不符合题意;
C.冰的密度比水小,是因为固态水分子间存在的氢键数目更多,且氢键具有方向性,空间体积更大,所以冰的密度更小,C项不符合题意;
D.风能和太阳能属于新型能源,同时也属于清洁能源,采用风能和太阳能为奥运服务体现了绿色化学、绿色奥运这一理念,D项符合题意;
故答案为:D。
【分析】A.食品添加剂合理添加即可;
B.石墨烯为碳单质,属于无机非金属材料;
C.水蒸气中水分子主要以单个分子的形式存在,液态水中多个水分子通过氢键结合在一起,形成(H2O)n,冰中所有水分子以氢键互相联结成晶体,氢键的形成使水分子之间的间隙增大,从而导致冰的密度比水的密度小。
5.【答案】C
【解析】【解答】A.相对分子质量在一万以上的是高分子化合物,而多糖和蛋白质均为高分子化合物,且均能水解,故A不符合题意;
B.光导纤维主要成分是二氧化硅,利用的导光性,具有特殊的光学性能,故B不符合题意;
C.羊绒衫主要成分是蛋白质;棉村衣主要成分是纤维素,蛋白质和纤维素都是天然高分子化合物,不是合成纤维,故C符合题意;
D.BaSO4不溶于水和酸,在X光的照射下显示出白色光点,对人体无害,可用于肠胃X射线造影检查,故D不符合题意;
故答案为:C。
【分析】A、多糖和蛋白质都是高分子化合物,可以发生水解;
B、二氧化硅可以制作光导纤维,单质硅可以制作芯片和太阳能电池板;
C、尼龙属于合成纤维,羊毛衫和棉衬衣属于天然纤维;
D、钡餐指的是硫酸钡。
6.【答案】D
【解析】【解答】解:A.乙烯含碳碳双键其中1根键断裂,相互加成生成聚乙烯,聚乙烯中不存在双键,聚乙烯塑料的老化是由于长链断裂等原因,故A错误;
B.煤的气化是煤在氧气不足的条件下进行部分氧化形成H2、CO等气体的过程,煤的液化是将煤与H2在催化剂作用下转化为液体燃料或利用煤产生的H2和CO通过化学合成产生液体燃料或其他液体化工产品的过程,所以煤经过气化和液化等变化是化学变化,故B错误;
C.合成纤维、人造纤维都属于有机高分子材料,碳纤维是碳的单质,不属于有机高分子材料,故C错误;
D.用粮食酿酒时,先在糖化酶作用下水解为葡萄糖,然后在酵母作用下转变为酒精,都是化学变化,故D正确;故选D.
【分析】A.聚乙烯塑料是乙烯发生加成反应生成的高分子聚合物,聚乙烯的单体是乙烯;
B.煤的气化、液化都是化学变化;
C.碳纤维是碳的单质;
D.淀粉→葡萄糖→乙醇都是化学变化;
7.【答案】A
【解析】【解答】A.同位素是质子数相同在,中子数不同,故A符合题意;
B.电池板主要用的硅单质,故B不符合题意;
C.煤油是混合物,故C不符合题意;
D.碳纤维属于无机非金属材料,故D不符合题意;
故答案为:A
【分析】A.考查的是同位素的概念;
B.电池板主要是硅单质;
C.煤油是混合物;
D.考查的碳纤维属于无机非金属材料。
8.【答案】D
【解析】【解答】A.制造N95口罩的聚丙烯树脂中没有碳碳双键,故A不符合题意;
B.C6H14为己烷,有5种同分异构体,分别为正己烷、2-甲基戊烷、3-甲基戊烷、2,2-二甲基丁烷、2,3-二甲基丁烷,故B不符合题意;
C.乙烯与溴水发生加成反应使溴水褪色,乙烯使酸性高锰酸钾溶液褪色是因为被高锰酸钾溶液氧化,褪色原理不同,故C不符合题意;
D.C2H6完全燃烧,若生成水的质量为2.7 g,则n(H2O)= =0.15mol,n(H) =0.3mol,根据乙烷的分子式可知,n(C) =0.1mol,则完全燃烧生成CO2的物质的量为0.1mol,质量为4.4g,故D符合题意。
故答案为:D。
【分析】A.丙烯发生加聚反应生成聚丙烯树脂,都是单键
B.烷烃一般都是支链异构,根据碳原子个数定主链,再定支链即可
C.褪色原理不同,溴水是发生加成反应,而高锰酸钾是发生氧化还原反应而褪色
D.根据方程式可以进行计算
9.【答案】D
【解析】【解答】A.棉花、优质针叶木等原料的主要成分是纤维素,A不符合题意;
B.Fe3O4是磁性物质,有磁性,B不符合题意;
C.树脂相对分子质量很大,属于有机高分子材料,C不符合题意;
D.葡萄糖遇碘不变蓝,D符合题意;
故答案为:D。
【分析】A.纤维素属于糖类;
B.Fe3O4 俗称氧化铁黑、吸铁石、黑氧化铁,为具有磁性的黑色晶体,故又称为磁性氧化铁 ;
C.高分子化合物相对分子质量很大,一般在10000以上,可高达几百万;
D.碘单质遇碘变蓝。
10.【答案】B
【解析】【解答】A. 桂醛分子中所有原子均可能处于同一平面上 ,A选项是正确的;
B.1mol苯环上可以加成3molH2,碳碳双键可以与1molH2加成,1mol-CHO发生加成反应,所以1mol桂醛分子可以与5molH2发生加成反应,B选项是错误的;
C. 香茅醇的分子式为C10H20O ,C选项是错误的;
D. 桂醛有醛基,而 D-香芹酮 没有醛基,所以可以用银氨溶液来鉴别二者,D选项是正确的。
故答案为:B。
【分析】A.苯环和碳碳双键都是平面结构,因此桂醛分子中所有原子均可能处于同一平面上;
B.1mol苯环上可以加成3molH2,碳碳双键可以与1molH2加成,1mol-CHO发生加成反应,所以1mol桂醛分子可以与5molH2发生加成反应;
C.香茅醇的分子式为C10H20O ;
D.醛基可以与银氨溶液发生氧化还原反应,得到银镜,即银单质。
11.【答案】D
【解析】【解答】解:A.常温下,C4H10是气体,故A正确;
B.丁烷有CH3CH2CH2CH3、CH3CH(CH3)2两种同分异构体,前者为正丁烷、后者为异丁烷,故B正确;
C.C4H10与CH4都属于烷烃,结构相似,在组成上相差3个CH2原子团,二者互为同系物,故C正确;
D.丁烷有正丁烷与异丁烷两种同分异构体,正丁烷分子种有2种H原子,其一氯代物有2种,异丁烷分子种有2种H原子,其一氯代物有2种,故丁烷的一氯代物有4种,即有4种沸点不同的产物一氯代物,故D错误,
故选D.
【分析】A.常温下,碳原子数目小于或等于4的烃为气体;
B.利用减少碳原子作取代基书写丁烷的同分异构体;
C.结构相似,在组成上相差1个或若干个CH2原子团的化合物互称同系物;
D.判断丁烷的同分异构体,再根据等效氢确定一氯代物的同分异构体,据此判断.
12.【答案】B
【解析】【解答】A.CH3CH3与Cl2取代产物有多种,得不到纯净的CH2ClCH2Cl,故A不符合题意;
B.CH2=CH2与HCl加成只生成CH3CH2Cl,得不到CH2ClCH2Cl,故B不符合题意;
C.CH2=CH2与Cl2加成只生成CH2ClCH2Cl,故C符合题意;
D.CH3CH2Cl与Cl2取代产物有多种,得不到纯净的CH2ClCH2Cl,故D不符合题意。
【分析】制备纯净的1,2-二氯乙烷一般采用加成反应可以得到纯净的产物,而取代反应会混有杂质,据此解答即可。
13.【答案】A
【解析】【解答】A.从分子结构上,糖是多羟基醛、多羟基酮或它们的脱水缩合物,故A符合题意;
B.某些含有苯环的蛋白质溶液与浓硝酸作用,先变性生成白色沉淀,加热后沉淀发生显色反应变为黄色,故B不符合题意;
C.酯是易挥发而具有芳香气味的有机化合物,所以含有酯类的水果会因含有低级酯类物质而具有特殊香味,故C不符合题意;
D.聚乙烯、聚氯乙烯的是具有优良性能的热塑性塑料,故D不符合题意;
故答案为:A。
【分析】A.糖是多羟基醛、多羟基酮或它们的脱水缩合物;
B.蛋白质溶液与浓硝酸作用,先变性生成白色沉淀,加热后沉淀变黄色;
C.酯类具有特殊香味;
D.聚乙烯、聚氯乙烯是常见的热塑性塑料。
14.【答案】A
【解析】【解答】A. 因为乙烷不和溴水反应,而乙烯能和溴水发生加成反应而使溴水退色,且生成的CH2BrCH2Br为液态,便于分离,故A符合题意;
B. 乙烷和乙烯均是无色气体,但前者易发生取代反应,后者易发生加成反应,若与足量溴蒸气反应,乙烷可以发生取代反应,乙烯则发生加成反应生成CH2BrCH2Br,不仅不易鉴别,还会损失大量的乙烷且混入大量的溴蒸气杂质,故B不符合题意;
C. 若在一定条件下通入氢气,虽可将乙烯转变为乙烷,但通入氢气的量不易控制,很难得到纯净的乙烷,且用氢气无法鉴别它们,故C不符合题意;
D. 乙烯被酸性高锰酸钾溶液氧化生成二氧化碳,会引入新杂质二氧化碳,故D不符合题意;
故答案为:A。
【分析】鉴别乙烷和乙烯可根据乙烯含有不饱和键,能使溴水褪色分析,除去乙烷中混有的少量乙烯时注意不能引入新的杂质,并且不能影响乙烷的量。
15.【答案】D
【解析】【解答】解:乙烯可有石油裂解生成,且乙烯用途广泛,可用于制造塑料、合成纤维、有机溶剂等,带动了其他以石油为原料的石油化工的发展.因此一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志,
故选D.
【分析】乙烯主要用于制造塑料、合成纤维、有机溶剂等,是石油化工发展的标志.
16.【答案】D
【解析】【解答】A.乙烯分子中的2个C原子和4个氢原子处于同一平面,苯是平面正六边形结构,都属于不饱和烃,但苯分子中的碳碳键完全相同,没有碳碳双键,A选项不符合题意;
B.乙烯和苯都可以来自于石油,石油的裂解可获得乙烯、石油的催化重整可获得苯,乙烯工业的发展,带动了其他以石油为原料的石油化工的发展,因此,乙烯的产量是衡量一个国家石油化工发展水平的标志,B选项不符合题意;
C.乙烯含有碳碳双键能够发生加成反应,苯的不饱和度很大,也能与氢气、氯气等发生加成反应,C选项不符合题意;
D.乙烯和苯都可以在氧气中燃烧,发生氧化反应,D选项符合题意;
故答案为:D。
【分析】A.苯环中不存在碳碳双键;
B.苯来自于煤的加工;
C.苯既能发生取代又能发生加成反应;
D.乙烯和苯都能和氧气发生氧化反应。
17.【答案】D
【解析】【解答】A.常温下, Zn 和浓硫酸反应可以得到 SO2 ,而 Al 和浓硫酸发生钝化得不到 SO2,A不符合题意;
B.H2O、H2S、CH4、SiH4均属于分子晶体,H2O的沸点比 H2S 的沸点高,是因为H2O中含有氢键,B不符合题意;
C.乙烯使溴水褪色发生加成反应,而乙烯使酸性高锰酸钾褪色发生的是氧化还原反应,C不符合题意;
D.铁元素化合价有+2、+3,铜元素化合价有+1、+2,由分析可知, 加热条件下,和能直接化合生成,则加热条件下和也能直接化合生成 ,D符合题意;
故答案为:D。
【分析】A.常温下,铝遇浓硫酸发生钝化。
B.一般分子晶体的熔沸点随相对分子质量的增大而升高,含有氢键的分子晶体熔沸点较高。
C.注意乙烯使酸性高锰酸钾褪色的原理是二者发生了氧化还原反应。
D.S氧化性较弱,与变价金属反应生成低价态的硫化物。
18.【答案】D
【解析】【解答】聚四氟乙烯不含不饱和键,不能发生加成反应,也不能使酸性高锰酸钾溶液褪色,故A不符合题意;
四氯乙烯中C原子的杂化类型为sp2杂化,故B不符合题意;
聚四氟乙烯具有高度的化学稳定性,故C不符合题意;
Cl和F为同主族元素,由于电负性F大于Cl,因此C-F键极性大于C-Cl键极性,故D符合题意。
【分析】
A.后者不含双键,不可加成;
B.杂化类型是sp2杂化;
C.其化学性质稳定;
D.氟元素电负性大于氯元素,故键的极性较大。
19.【答案】B
【解析】【解答】A.柠檬酸分子中有三个羧基,酸性比碳酸强,A不符合题意;
B.柠檬酸分子中有羟基,可与水分子形成氢键,B符合题意;
C.柠檬酸分子中含有三个羧基,1mol 柠檬酸可与3molNaOH反应,C不符合题意;
D.柠檬酸分子中含有三个羧基和一个醇羟基,可发生取代反应、氧化反应,不能发生加成反应,D不符合题意;
故答案为:B
【分析】A.三个羧基,酸性比碳酸强;
B.有羟基,可与水分子形成氢键;
C.羧基和NaOH反应;
D.羧基和醇羟基,可发生取代反应、氧化反应,不能发生加成反应。
20.【答案】D
【解析】【解答】A.CH3CH3与溴发生取代反应生成CH3-CH2Br,故A不符合要求;
B.CH3COOH与乙醇发生酯化反应生成水和CH3COOC2H5,故B不符合要求;
C.苯与液溴在铁催化作用下发生取代反应生成溴苯和溴化氢,故C不符合要求;
D.乙烯含碳碳双键与水发生加成反应生成乙醇,故D符合要求;
故答案为:D。
【分析】发生加成的前提是含有不饱和键,一般是碳碳双键、碳碳三键、醛基等等,D中发生的是双键的加成,其他均是取代反应
21.【答案】(1);
(2)2-乙基-1-己醇
(3)
(4)
(5)d
【解析】【解答】(1)由分析可知B的结构简式为CH2=CHCHO,G的结构简式为 ;故答案为:CH2=CHCHO; ;
(2)C8H17OH为 ,与-OH相连的C原子为第1位碳原子编号来命名,其名称为2-乙基-1-己醇;故答案为:2-乙基-1-己醇;
(3)F为苯甲醚,X遇氯化铁溶液发生显色反应且环上的一溴取代物有两种,X为酚,甲基与酚羟基处于对位,则X为 ;故答案为: ;
(4)由信息Ⅰ,D与G合成Q,并生成HBr,反应⑥的化学方程式为 ;故答案为: ;
(5)B为烯醛,C为烯酸,均含C=C键,但羧基中的C=O不能与氢气发生加成反应;
a.均含C=C键,则二者都能使溴的四氯化碳溶液或酸性高锰酸钾溶液褪色,故a正确;
b.C中含-COOH,能与碳酸氢钠溶液反应产生二氧化碳,而B不能,故b不正确;
c.1mol B最多消耗44.8L(标准状况)氢气,而C消耗22.4L氢气,故c不正确;
d.B中含-CHO,C中含-COOH,二者都能与新制氢氧化铜悬浊液反应,故d正确;
故答案为ad。
【分析】由A、B的分子式及的结构简式C可知,A为CH3CH=CH2,B为CH2=CHCHO,由信息Ⅱ可知,C8H17OH分子中只有一个支链,且为乙基,其连续氧化的产物能与碳酸氢钠反应生成CO2,其消去产物的分子中只有一个碳原子上没有氢原子,则C8H17OH为 ,与丙烯酸发生酯化反应生成D,由流程图可知,F为 等,因F不能与NaOH溶液反应,所以F为苯甲醇或苯甲醚,由F和G的分子式可知,F与溴发生取代反应,又G的核磁共振氢谱中有3组峰,说明G中有3种位置的H原子,所以G为 。
22.【答案】(1)
(2) +HO-NO2 +H2O
(3)C2H5OH
(4)CH3COOH +HOCH2CH3 CH3COOCH2CH3+ H2O;2CH3CH2OH + O2 2CH3CHO + 2H2O
【解析】【解答】(1)A为乙烯,其结构式为 ;
(2)苯与浓硝酸在浓硫酸、加热(50℃~60℃)的条件下发生取代反应生成硝基苯和水,化学方程式为 +HO-NO2 +H2O;
(3)C为乙醇,结构简式为C2H5OH;
(4)①乙醇和乙酸在浓硫酸加热的条件下可以发生酯化反应生成乙酸乙酯,化学方程式为CH3COOH +HOCH2CH3 CH3COOCH2CH3+ H2O;
②C在铜催化和加热条件下被氧气氧化成乙醛,化学方程式为2CH3CH2OH + O2 2CH3CHO + 2H2O。
【分析】A能使溴的四氯化碳溶液褪色,结合其填充模型可知应含有碳碳双键,A为CH2=CH2;B可以可以从煤干馏生成的煤焦油中提取,结合其填充模型可知为苯;C可通过A与H2O加成获得,相对分子质量为46,所以C为CH3CH2OH。
23.【答案】(1)C
(2)E
(3)C
(4)CE
【解析】【解答】(1)能够发生加成的烃为:乙烯和甲苯,其中气态的烃为乙烯,故答案为:C;
(2) 甲烷、乙烷、乙烯、丙烷、甲苯中分别含有1种、1种、1种、2种、4种环境的氢原子,因此一卤代物种类最多的是甲苯,共有4种一氯代物,故答案为:E;
(3)所有原子均在同一平面上的是乙烯,故答案为:C;
(4)乙烯和甲苯能够使酸性高锰酸钾溶液褪色,故答案为:CE。
【分析】根据分子的球棍模型可知:A为甲烷,B为乙烷,C为乙烯,D为丙烷,E为甲苯,根据物质的结构和性质分析解答。
24.【答案】(1);加聚反应
(2);取代反应
(3);取代反应
(4)CH2=CH2+Br2→BrCH2CH2Br;加成反应
【解析】【解答】解:(1)丙烯能发生加聚反应得到聚丙烯,方程式为 ,属于加聚反应,
故答案为: ;加聚反应;(2)甲苯可以和浓硝酸之间发生取代反应生成2,4,6﹣三硝基甲苯,即TNT,化学反应方程式为 ,属于取代反应;
故答案为: ;取代反应;(3)苯与液溴反应苯环上的氢原子被溴原子代替生成溴苯和溴化氢,化学方程式为: ,属于取代反应;
故答案为: ;取代反应;(4)乙烯含碳碳双键,与溴水发生加成反应,反应为CH2=CH2+Br2→BrCH2CH2Br,故答案为:CH2=CH2+Br2→BrCH2CH2Br;加成反应.
【分析】(1)丙烯分子含有碳碳双键,发生加聚反应生成聚丙烯;(2)甲苯与浓硝酸发生取代反应可生成TNT,即三硝基甲苯;(3)苯与液溴发生取代反应生成溴苯;(4)乙烯含碳碳双键,与溴水发生加成反应.
25.【答案】(1)b
(2)羟基;CH3CHO
(3)
(4)加聚反应
(5);饱和Na2CO3;c
【解析】【解答】(1)工业上通过石油裂解可以获得大量乙烯,b正确,故答案为:b;
(2)C的结构简式为CH3CH2OH,官能团为羟基;D的结构简式为CH3CHO,故答案为:羟基;CH3CHO;
(3)反应①为乙烯与溴水发生加成反应生成BrCH2CH2Br,反应的化学方程式为 ,故答案为: ;
(4)反应②为一定条件下,乙烯发生加聚反应生成聚乙烯,故答案为:加聚反应;
(5)①装置A中发生的反应为在浓硫酸作用下,CH3CH2OH和CH3COOH共热发生酯化反应生成CH3COOCH2CH3,反应的化学方程式为 ,故答案为: ;
②试管B中盛放的溶液是饱和碳酸钠溶液,目的是除去乙酸,吸收乙醇,降低乙酸乙酯的溶解度,便于分层;乙酸乙酯在碱溶液中会发生水解反应,所以除去CH3COOCH2CH3中含有少量的水不能加入碱石灰和氢氧化钾,应该加入无水硫酸钠,c正确,故答案为:饱和Na2CO3;c。
【分析】由题给有机物的转化关系可知,通过石油裂解可以获得大量乙烯;一定条件下,乙烯发生加聚反应生成聚乙烯,则A为聚乙烯;乙烯与溴水发生加成反应生成BrCH2CH2Br,则B为BrCH2CH2Br;在催化剂作用下,乙烯与水发生加成反应生成CH3CH2OH,则C为CH3CH2OH;在Cu或Ag做催化剂作用下,CH3CH2OH与氧气共热发生催化氧化反应生成CH3CHO,则D为CH3CHO;在催化剂作用下,CH3CHO与氧气共热发生催化氧化反应生成CH3COOH,在浓硫酸作用下,CH3CH2OH和CH3COOH共热发生酯化反应生成CH3COOCH2CH3。
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
