第五单元 化学方程式试卷(含答案)2023-2024学年九年级上册化学
文档属性
| 名称 | 第五单元 化学方程式试卷(含答案)2023-2024学年九年级上册化学 |

|
|
| 格式 | docx | ||
| 文件大小 | 195.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-15 00:00:00 | ||
图片预览




文档简介
第五单元 化学方程式
(时间:65分钟 分值:70分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 P-31 K-39 Mn-55 Fe-56
一、单项选择题(本大题包括10小题,每小题有四个选项,其中只有一个选项符合题意,请将符合题意的选项代号填在相应位置上。1~5题每小题1分,6~10题每小题2分,共15分)
1.下列对历史上几项重要化学研究成果的介绍错误的是 ( )
A.波义耳发现了质量守恒定律 B.居里夫妇发现了钋和镭
C.门捷列夫编制了元素周期表 D.侯德榜创新了纯碱制法
2.下图是某化学反应的微观模型示意图,其中“”表示氧原子、“”表示碳原子。下列从图中获得的信息不正确的是 ( )
A.反应前后原子种类没有变化
B.该反应是化合反应
C.分子是由原子构成的
D.反应前后的物质都是氧化物
3.小林和小明在学习合作中讨论:相同质量的下列物质分别在氧气中完全燃烧,哪种物质消耗氧气最多 请你也参与讨论,你认为消耗氧气最多的物质是 ( )
A.C B.H2 C.Fe D.P
4.物质混合、反应等过程中,存在着“1+1≠2”的有趣现象。通常情况下,下列选项符合“1+1=2”的是 ( )
A.1 mL酒精与1 mL水混合后的总体积
B.1 g碳和1 g氧气反应后生成物的质量
C.1 g氧气和1 g氢气混合后的气体体积
D.1 g氯化钠饱和溶液中加入1 g水后所得溶液的质量
5.中国科学院天津工业生物技术研究所在淀粉人工合成方面取得突破性进展,在国际上首次实现二氧化碳到淀粉的从头合成,其核心步骤:先将氢气和二氧化碳合成甲醇,再由甲醇合成淀粉。第一步反应的化学方程式为CO2+3H2甲醇+H2O,则甲醇的化学式为 ( )
A.CH4 B.CO C.CH4O D.C2H6O
6.化学方程式是描述化学反应的语言,下列化学方程式中书写正确的是 ( )
A.2S+3O22SO3
B.Mg+O2MgO2
C.2KClO3+MnO22KCl+MnO2+3O2↑
D.2H2+O22H2O
7.常用燃烧法测定有机物的组成。现取3.2 g某有机物在足量的氧气中充分燃烧,生成了 8.8 g CO2 和7.2 g H2O,则该有机物中 ( )
A.一定含C、H两种元素,可能含O元素
B.只含有C、H两种元素,不含O元素
C.一定含有C、H、O元素
D.一定含C、O两种元素,可能含H元素
8.一定条件下,在密闭容器中发生某反应,反应前后各物质的质量如下图所示。下列说法正确的是 ( )
A.x的值为22
B.该反应为置换反应
C.W由碳、氢两种元素组成
D.W中碳元素的质量分数为85%
9.已知2A+3BC+3D,足量的A和49 g B恰好完全反应,生成57 g C和1 g D,若B的相对分子质量为98,则A的相对分子质量为 ( )
A.27 B.16 C.44 D.54
10.白磷在耐高温的密闭容器中(内含空气)加热,下图中能正确表示容器内所有物质总质量(m)与时间(t)的变化关系的是 ( )
二、选择填充题(本大题包括3小题,先在A、B、C中选择一个正确选项,将正确选项的代号填在相应位置上,然后在D处补充一个符合题意的答案。每小题2分,其中选择1分,填充1分,共6分)
11.根据化学方程式2H2O2H2↑+O2↑,可获取的信息是 ( )
A.反应所需条件
B.氧气可助燃
C.水由氢气和氧气构成
D.
12.2022年6月5日,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭在酒泉卫星发射中心成功发射。其在轨运行过程中,发生的一种反应的微观示意图如下,下列说法正确的是 ( )
A.甲和乙都是氧化物
B.该反应属于置换反应
C.丙的化学式为N2
D.反应中丙与丁的化学计量数之比为
13.现有 A、B、C三种物质各30 g,它们化合时只能生成60 g新物质D。若增加20 g A,则反应停止后,原反应物中只剩余C。根据上述条件推断,下列说法中正确的是 ( )
A.第一次反应停止后,B剩余18 g
B.第二次反应后,D的质量为100 g
C.反应中A和B的质量比是3∶2
D.反应中A和C的质量比是
三、填空与说明题(本大题包括4小题,共23分)
14.(3分)请用化学用语填空。
(1)2个氢氧根离子: 。
(2)高铁酸钠(Na2FeO4)是一种净水剂,请标出高铁酸钠中铁元素的化合价: 。
(3)过氧乙酸的结构式如图所示,其化学式为 。
15.(7分)“嫦娥五号”月球采样返回、“天问一号”成功着陆火星等一系列航天壮举,标志着我国航天事业取得突破性进展。
(1)月壤含CaAl2Si2Ox以及可作为核聚变燃料的氦-3等物质。
①已知CaAl2Si2Ox中Si显+4价,则x的值为 。
②氦-3原子的相对原子质量为3,则其中子数为 ,氦原子的符号是 。
(2)月球上可能存在大量的水,光催化分解水技术对人类在月球上活动意义重大,应用该技术发生反应的化学方程式为 。
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.70 1.60 0.13 0.25
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是 。
②为了满足人类未来在火星上生活的条件,下列研究设想不合理的是 (填字母)。
A.将CO2分解转化为N2,提高N2含量
B.将CO2转化为O2,提高O2含量
C.寻找水的存在和开发水循环技术
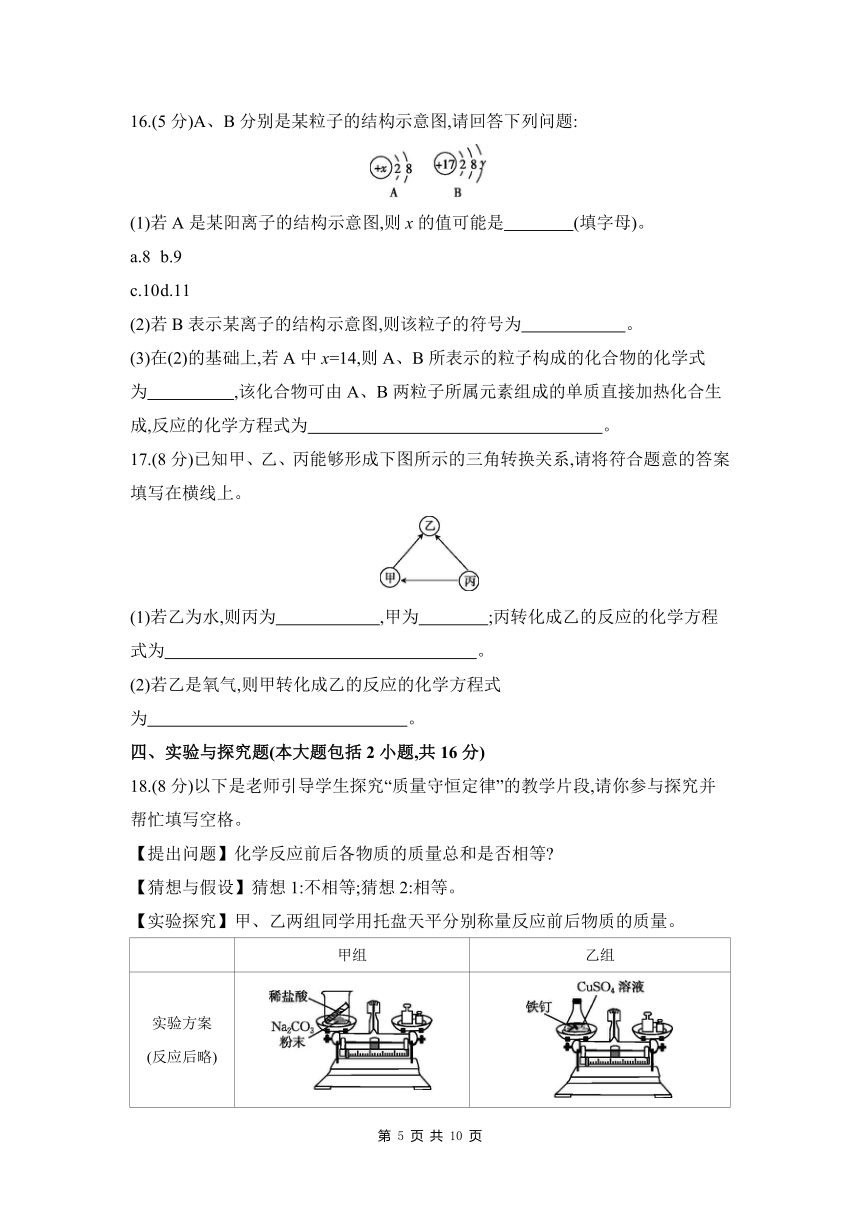
16.(5分)A、B分别是某粒子的结构示意图,请回答下列问题:
(1)若A是某阳离子的结构示意图,则x的值可能是 (填字母)。
a.8 b.9
c.10 d.11
(2)若B表示某离子的结构示意图,则该粒子的符号为 。
(3)在(2)的基础上,若A中x=14,则A、B所表示的粒子构成的化合物的化学式为 ,该化合物可由A、B两粒子所属元素组成的单质直接加热化合生成,反应的化学方程式为 。
17.(8分)已知甲、乙、丙能够形成下图所示的三角转换关系,请将符合题意的答案填写在横线上。
(1)若乙为水,则丙为 ,甲为 ;丙转化成乙的反应的化学方程式为 。
(2)若乙是氧气,则甲转化成乙的反应的化学方程式为 。
四、实验与探究题(本大题包括2小题,共16分)
18.(8分)以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格。
【提出问题】化学反应前后各物质的质量总和是否相等
【猜想与假设】猜想1:不相等;猜想2:相等。
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 乙组
实验方案 (反应后略)
实验现象 有气泡产生,天平指针向右偏转 铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转
结论 猜想1正确 猜想2正确
【反思评价】究竟哪种猜想正确 通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在 中进行。
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进(提示: NaOH溶液可吸收反应产生的CO2气体),你认为最佳装置是 (填字母)。
【得出结论】同学们利用改进后的最佳装置再次进行探究,得出猜想二正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论: 的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】请从原子的角度分析,化学反应前后质量守恒的原因是 。
质量守恒定律的应用:
①某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由 种元素组成。
②某同学进行右图所示的实验,在一根用细铜丝吊着的长玻璃棒两端分别绕上粗铜丝,并使玻璃棒保持水平。用酒精灯给a端铜丝加热数分钟,停止加热后冷却,他观察到的现象是 ,发生反应的化学方程式为 。
19.(8分)某课外小组同学进一步对铁与氧气反应的实验现象和生成物进行探究。
(一)产生“火星四射”的原因
【提出问题】铁丝燃烧时为什么与镁条燃烧不一样,出现“火星四射”的现象
【查阅资料】铁丝燃烧时“火星四射”现象与铁丝含碳量有关。
【进行实验】探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系。
实验 现象 解释与结论
实验1:取直径为0.15 mm、含碳0.2%的铁丝,在氧气中点燃 零星的火星四射 (1)铁丝燃烧的化学方程式是 ; (2)直径为0.15 mm的铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为
实验2:取直径为0.15 mm、含碳0.4%的铁丝,在氧气中点燃 较明显的火星四射
实验3:取直径为0.15 mm、含碳0.6%的铁丝,在氧气中点燃 (3)
(二)溅落的“黑色固体”的成分
【提出问题】纯铁在氧气中燃烧溅落的“黑色固体”是什么
【查阅资料】①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO易被氧化,不能稳定存在);②铁的氧化物均能溶于酸溶液,但没有气泡产生,而铁溶于酸会产生气泡;③Fe3O4是黑色固体,Fe2O3是红棕色粉末。
【进行实验】测定黑色固体的成分
实验 现象 解释与结论
实验4:将冷却后的黑色固体碾碎,装入试管,加入稀盐酸 (4) 铁燃烧时溅落下来的黑色固体中含有铁
实验5:收集实验4残留的固体观察 只存在黑色固体 (5)黑色固体的组成为
(三)确定具体的质量
(6)实验前称得纯铁质量是26.6 g,燃烧后称得黑色固体质量为33.0 g,则33.0 g黑色固体的具体成分及对应的质量为 。
五、综合计算题(本大题包括1小题,共10分)
20.(10分)如下图所示,为了测定实验室中高锰酸钾样品的纯度(假设杂质不参加反应),小亮称取4.0 g该样品于试管中,加热,用量筒收集生成的气体。高锰酸钾完全分解后,移去酒精灯。待装置冷却到室温后,得到0.23 L氧气(常温下氧气的密度约为1.4 g/L)。
请回答下列问题:
(1)图中小亮收集氧气采用的方法是 法,收集的氧气的质量为 (保留2位小数)。
(2)求该样品中高锰酸钾的质量分数。(写出计算过程)
(3)下列有关本实验的描述中正确的是 (填字母)。
A.酒精灯加热时间过短,会导致所测高锰酸钾的质量分数偏小
B.导管不伸入量筒底部,气体无法顺利进入量筒
C.导管伸入量筒底部,可使测得的氧气体积更准确
D.导管伸入量筒底部,可以避免先移去酒精灯而导致水倒吸入试管
参考答案
1.A 2.D 3.B 4.D 5.C 6.D 7.B 8.C 9.A 10.B
11.A 反应物是水,生成物是氢气和氧气(合理即可)
12.C 3∶4
13.B 5∶2
14.(3分)(1)2OH-
(2)Na2O4
(3)CH3COOOH(或C2H4O3)
15.(7分)(1)①8 ②1 He
(2)2H2O2H2↑+O2↑ (2分)
(3)①伸入燃着的木条(或倒入澄清石灰水)
②A
16.(5分)(1)d
(2)Cl-
(3)SiCl4 Si+2Cl2SiCl4(2分)
17.(8分)(1)H2O2(2分) O2(2分) 2H2O22H2O+O2↑(2分)
(2)2H2O2H2↑+O2↑(2分)(此题答案合理即可)
18.(8分)【反思评价】密闭容器(或封闭体系)
【优化装置】B
【得出结论】参加化学反应
【解释应用】化学反应前后,原子的种类、数目、质量均不变,所以质量守恒 ①4(或四) ②a端铜丝表面变黑,玻璃棒向a端倾斜 2Cu+O22CuO(2分)
19.(8分)(1)3Fe+2O2Fe3O4(2分)
(2)铁丝含碳量越多,火星四射现象越明显
(3)明显的火星四射
(4)有气泡产生
(5)铁、四氧化三铁
(6)铁9.8 g、四氧化三铁23.2 g(2分)
20.(10分)(1)排水(1分) 0.32 g(2分)
(2)解:设该样品中高锰酸钾的质量为x。
2KMnO4K2MnO4+MnO2+O2↑(1分)
316 32
x 0.32 g(1分)
=(1分)
x=3.16 g(1分)
样品中高锰酸钾的质量分数=×100%=79%(1分)
答:该样品中高锰酸钾的质量分数是79%。
(3)ACD(2分)
(时间:65分钟 分值:70分)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 P-31 K-39 Mn-55 Fe-56
一、单项选择题(本大题包括10小题,每小题有四个选项,其中只有一个选项符合题意,请将符合题意的选项代号填在相应位置上。1~5题每小题1分,6~10题每小题2分,共15分)
1.下列对历史上几项重要化学研究成果的介绍错误的是 ( )
A.波义耳发现了质量守恒定律 B.居里夫妇发现了钋和镭
C.门捷列夫编制了元素周期表 D.侯德榜创新了纯碱制法
2.下图是某化学反应的微观模型示意图,其中“”表示氧原子、“”表示碳原子。下列从图中获得的信息不正确的是 ( )
A.反应前后原子种类没有变化
B.该反应是化合反应
C.分子是由原子构成的
D.反应前后的物质都是氧化物
3.小林和小明在学习合作中讨论:相同质量的下列物质分别在氧气中完全燃烧,哪种物质消耗氧气最多 请你也参与讨论,你认为消耗氧气最多的物质是 ( )
A.C B.H2 C.Fe D.P
4.物质混合、反应等过程中,存在着“1+1≠2”的有趣现象。通常情况下,下列选项符合“1+1=2”的是 ( )
A.1 mL酒精与1 mL水混合后的总体积
B.1 g碳和1 g氧气反应后生成物的质量
C.1 g氧气和1 g氢气混合后的气体体积
D.1 g氯化钠饱和溶液中加入1 g水后所得溶液的质量
5.中国科学院天津工业生物技术研究所在淀粉人工合成方面取得突破性进展,在国际上首次实现二氧化碳到淀粉的从头合成,其核心步骤:先将氢气和二氧化碳合成甲醇,再由甲醇合成淀粉。第一步反应的化学方程式为CO2+3H2甲醇+H2O,则甲醇的化学式为 ( )
A.CH4 B.CO C.CH4O D.C2H6O
6.化学方程式是描述化学反应的语言,下列化学方程式中书写正确的是 ( )
A.2S+3O22SO3
B.Mg+O2MgO2
C.2KClO3+MnO22KCl+MnO2+3O2↑
D.2H2+O22H2O
7.常用燃烧法测定有机物的组成。现取3.2 g某有机物在足量的氧气中充分燃烧,生成了 8.8 g CO2 和7.2 g H2O,则该有机物中 ( )
A.一定含C、H两种元素,可能含O元素
B.只含有C、H两种元素,不含O元素
C.一定含有C、H、O元素
D.一定含C、O两种元素,可能含H元素
8.一定条件下,在密闭容器中发生某反应,反应前后各物质的质量如下图所示。下列说法正确的是 ( )
A.x的值为22
B.该反应为置换反应
C.W由碳、氢两种元素组成
D.W中碳元素的质量分数为85%
9.已知2A+3BC+3D,足量的A和49 g B恰好完全反应,生成57 g C和1 g D,若B的相对分子质量为98,则A的相对分子质量为 ( )
A.27 B.16 C.44 D.54
10.白磷在耐高温的密闭容器中(内含空气)加热,下图中能正确表示容器内所有物质总质量(m)与时间(t)的变化关系的是 ( )
二、选择填充题(本大题包括3小题,先在A、B、C中选择一个正确选项,将正确选项的代号填在相应位置上,然后在D处补充一个符合题意的答案。每小题2分,其中选择1分,填充1分,共6分)
11.根据化学方程式2H2O2H2↑+O2↑,可获取的信息是 ( )
A.反应所需条件
B.氧气可助燃
C.水由氢气和氧气构成
D.
12.2022年6月5日,搭载神舟十四号载人飞船的长征二号F遥十四运载火箭在酒泉卫星发射中心成功发射。其在轨运行过程中,发生的一种反应的微观示意图如下,下列说法正确的是 ( )
A.甲和乙都是氧化物
B.该反应属于置换反应
C.丙的化学式为N2
D.反应中丙与丁的化学计量数之比为
13.现有 A、B、C三种物质各30 g,它们化合时只能生成60 g新物质D。若增加20 g A,则反应停止后,原反应物中只剩余C。根据上述条件推断,下列说法中正确的是 ( )
A.第一次反应停止后,B剩余18 g
B.第二次反应后,D的质量为100 g
C.反应中A和B的质量比是3∶2
D.反应中A和C的质量比是
三、填空与说明题(本大题包括4小题,共23分)
14.(3分)请用化学用语填空。
(1)2个氢氧根离子: 。
(2)高铁酸钠(Na2FeO4)是一种净水剂,请标出高铁酸钠中铁元素的化合价: 。
(3)过氧乙酸的结构式如图所示,其化学式为 。
15.(7分)“嫦娥五号”月球采样返回、“天问一号”成功着陆火星等一系列航天壮举,标志着我国航天事业取得突破性进展。
(1)月壤含CaAl2Si2Ox以及可作为核聚变燃料的氦-3等物质。
①已知CaAl2Si2Ox中Si显+4价,则x的值为 。
②氦-3原子的相对原子质量为3,则其中子数为 ,氦原子的符号是 。
(2)月球上可能存在大量的水,光催化分解水技术对人类在月球上活动意义重大,应用该技术发生反应的化学方程式为 。
(3)火星拥有丰富的金属矿物和二氧化碳等资源。火星低层大气的主要成分如下表。
气体成分 CO2 N2 Ar O2 其他
体积分数/% 95.32 2.70 1.60 0.13 0.25
①为鉴别一瓶模拟“火星低层大气”组成的气体和一瓶空气,可采用的化学方法是 。
②为了满足人类未来在火星上生活的条件,下列研究设想不合理的是 (填字母)。
A.将CO2分解转化为N2,提高N2含量
B.将CO2转化为O2,提高O2含量
C.寻找水的存在和开发水循环技术
16.(5分)A、B分别是某粒子的结构示意图,请回答下列问题:
(1)若A是某阳离子的结构示意图,则x的值可能是 (填字母)。
a.8 b.9
c.10 d.11
(2)若B表示某离子的结构示意图,则该粒子的符号为 。
(3)在(2)的基础上,若A中x=14,则A、B所表示的粒子构成的化合物的化学式为 ,该化合物可由A、B两粒子所属元素组成的单质直接加热化合生成,反应的化学方程式为 。
17.(8分)已知甲、乙、丙能够形成下图所示的三角转换关系,请将符合题意的答案填写在横线上。
(1)若乙为水,则丙为 ,甲为 ;丙转化成乙的反应的化学方程式为 。
(2)若乙是氧气,则甲转化成乙的反应的化学方程式为 。
四、实验与探究题(本大题包括2小题,共16分)
18.(8分)以下是老师引导学生探究“质量守恒定律”的教学片段,请你参与探究并帮忙填写空格。
【提出问题】化学反应前后各物质的质量总和是否相等
【猜想与假设】猜想1:不相等;猜想2:相等。
【实验探究】甲、乙两组同学用托盘天平分别称量反应前后物质的质量。
甲组 乙组
实验方案 (反应后略)
实验现象 有气泡产生,天平指针向右偏转 铁钉表面有红色物质析出,溶液颜色发生改变,天平指针没有偏转
结论 猜想1正确 猜想2正确
【反思评价】究竟哪种猜想正确 通过讨论,同学们发现甲组中有气体溢出,导致指针向右偏转。得到启示:在探究化学反应前后各物质的质量总和是否相等时,凡是有气体生成或参加的反应一定要在 中进行。
【优化装置】同学们对甲组左盘中的反应装置进行了如下三种改进(提示: NaOH溶液可吸收反应产生的CO2气体),你认为最佳装置是 (填字母)。
【得出结论】同学们利用改进后的最佳装置再次进行探究,得出猜想二正确。进一步分析发现,反应体系中器材和未参加反应的物质的质量在反应前后保持不变,最终得出结论: 的各物质的质量总和等于反应后生成的各物质的质量总和。
【解释应用】请从原子的角度分析,化学反应前后质量守恒的原因是 。
质量守恒定律的应用:
①某固体物质受热会发生分解反应,生成氧化铜、水和二氧化碳三种物质,则该固体物质一定由 种元素组成。
②某同学进行右图所示的实验,在一根用细铜丝吊着的长玻璃棒两端分别绕上粗铜丝,并使玻璃棒保持水平。用酒精灯给a端铜丝加热数分钟,停止加热后冷却,他观察到的现象是 ,发生反应的化学方程式为 。
19.(8分)某课外小组同学进一步对铁与氧气反应的实验现象和生成物进行探究。
(一)产生“火星四射”的原因
【提出问题】铁丝燃烧时为什么与镁条燃烧不一样,出现“火星四射”的现象
【查阅资料】铁丝燃烧时“火星四射”现象与铁丝含碳量有关。
【进行实验】探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系。
实验 现象 解释与结论
实验1:取直径为0.15 mm、含碳0.2%的铁丝,在氧气中点燃 零星的火星四射 (1)铁丝燃烧的化学方程式是 ; (2)直径为0.15 mm的铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为
实验2:取直径为0.15 mm、含碳0.4%的铁丝,在氧气中点燃 较明显的火星四射
实验3:取直径为0.15 mm、含碳0.6%的铁丝,在氧气中点燃 (3)
(二)溅落的“黑色固体”的成分
【提出问题】纯铁在氧气中燃烧溅落的“黑色固体”是什么
【查阅资料】①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO易被氧化,不能稳定存在);②铁的氧化物均能溶于酸溶液,但没有气泡产生,而铁溶于酸会产生气泡;③Fe3O4是黑色固体,Fe2O3是红棕色粉末。
【进行实验】测定黑色固体的成分
实验 现象 解释与结论
实验4:将冷却后的黑色固体碾碎,装入试管,加入稀盐酸 (4) 铁燃烧时溅落下来的黑色固体中含有铁
实验5:收集实验4残留的固体观察 只存在黑色固体 (5)黑色固体的组成为
(三)确定具体的质量
(6)实验前称得纯铁质量是26.6 g,燃烧后称得黑色固体质量为33.0 g,则33.0 g黑色固体的具体成分及对应的质量为 。
五、综合计算题(本大题包括1小题,共10分)
20.(10分)如下图所示,为了测定实验室中高锰酸钾样品的纯度(假设杂质不参加反应),小亮称取4.0 g该样品于试管中,加热,用量筒收集生成的气体。高锰酸钾完全分解后,移去酒精灯。待装置冷却到室温后,得到0.23 L氧气(常温下氧气的密度约为1.4 g/L)。
请回答下列问题:
(1)图中小亮收集氧气采用的方法是 法,收集的氧气的质量为 (保留2位小数)。
(2)求该样品中高锰酸钾的质量分数。(写出计算过程)
(3)下列有关本实验的描述中正确的是 (填字母)。
A.酒精灯加热时间过短,会导致所测高锰酸钾的质量分数偏小
B.导管不伸入量筒底部,气体无法顺利进入量筒
C.导管伸入量筒底部,可使测得的氧气体积更准确
D.导管伸入量筒底部,可以避免先移去酒精灯而导致水倒吸入试管
参考答案
1.A 2.D 3.B 4.D 5.C 6.D 7.B 8.C 9.A 10.B
11.A 反应物是水,生成物是氢气和氧气(合理即可)
12.C 3∶4
13.B 5∶2
14.(3分)(1)2OH-
(2)Na2O4
(3)CH3COOOH(或C2H4O3)
15.(7分)(1)①8 ②1 He
(2)2H2O2H2↑+O2↑ (2分)
(3)①伸入燃着的木条(或倒入澄清石灰水)
②A
16.(5分)(1)d
(2)Cl-
(3)SiCl4 Si+2Cl2SiCl4(2分)
17.(8分)(1)H2O2(2分) O2(2分) 2H2O22H2O+O2↑(2分)
(2)2H2O2H2↑+O2↑(2分)(此题答案合理即可)
18.(8分)【反思评价】密闭容器(或封闭体系)
【优化装置】B
【得出结论】参加化学反应
【解释应用】化学反应前后,原子的种类、数目、质量均不变,所以质量守恒 ①4(或四) ②a端铜丝表面变黑,玻璃棒向a端倾斜 2Cu+O22CuO(2分)
19.(8分)(1)3Fe+2O2Fe3O4(2分)
(2)铁丝含碳量越多,火星四射现象越明显
(3)明显的火星四射
(4)有气泡产生
(5)铁、四氧化三铁
(6)铁9.8 g、四氧化三铁23.2 g(2分)
20.(10分)(1)排水(1分) 0.32 g(2分)
(2)解:设该样品中高锰酸钾的质量为x。
2KMnO4K2MnO4+MnO2+O2↑(1分)
316 32
x 0.32 g(1分)
=(1分)
x=3.16 g(1分)
样品中高锰酸钾的质量分数=×100%=79%(1分)
答:该样品中高锰酸钾的质量分数是79%。
(3)ACD(2分)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
