化学人教版选修五 2.1 脂肪烃 课件(共62张PPT)
文档属性
| 名称 | 化学人教版选修五 2.1 脂肪烃 课件(共62张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-10-23 00:00:00 | ||
图片预览









文档简介
课件62张PPT。1.烷烃CnH2n+2 单键、 价键饱和、四面体
2.烯烃CnH2n 碳碳双键 、不饱和、平面型
3.炔烃CnH2n-2 H-C≡C-、不饱和、直线型碳原子排列呈锯齿状,主链上的碳可能共面。双键碳原子上的所有原子一定共面.叁键碳原子上的所有原子一定共线.一、烷烃、烯烃、炔烃的结构1.CH≡C─CH=CHC(CH3)3中:在一条直线上的原子有 个,
至少 个有碳原子共面,最多有 个碳原子共面。456 练 习2.对CH3—CH = CH—C≡C—CF3的叙述下列正确的是 A.6个碳原子有可能都在一条直线上
B.6个碳原子不可能都在一条直线上
C.6个碳原子有可能都在同一平面上
D.6个碳原子不可能都在同一平面上 1.黑色的金子、工业的血液是什么?它的主要组成元素是什么?
2.什么是烃的衍生物?
什么是卤代径?
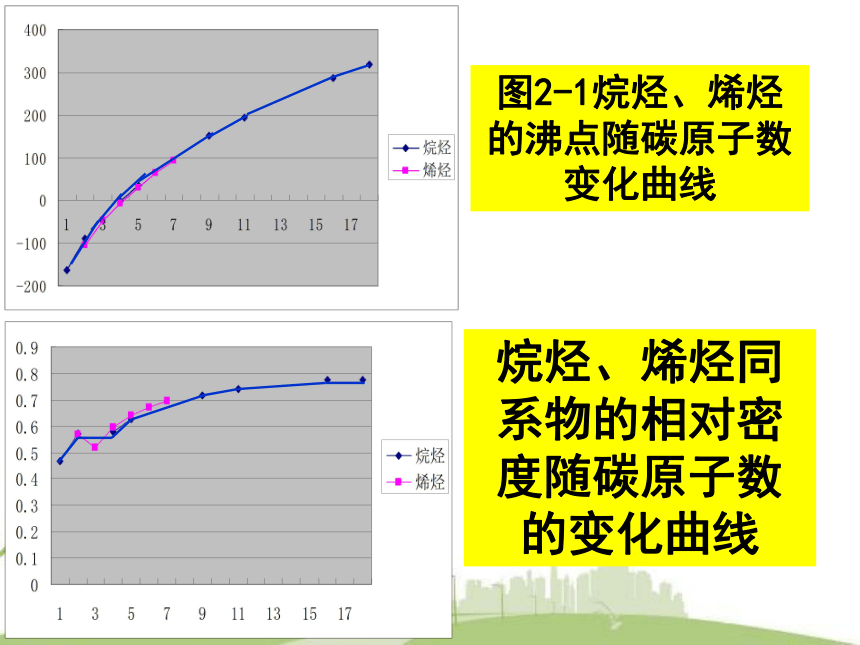
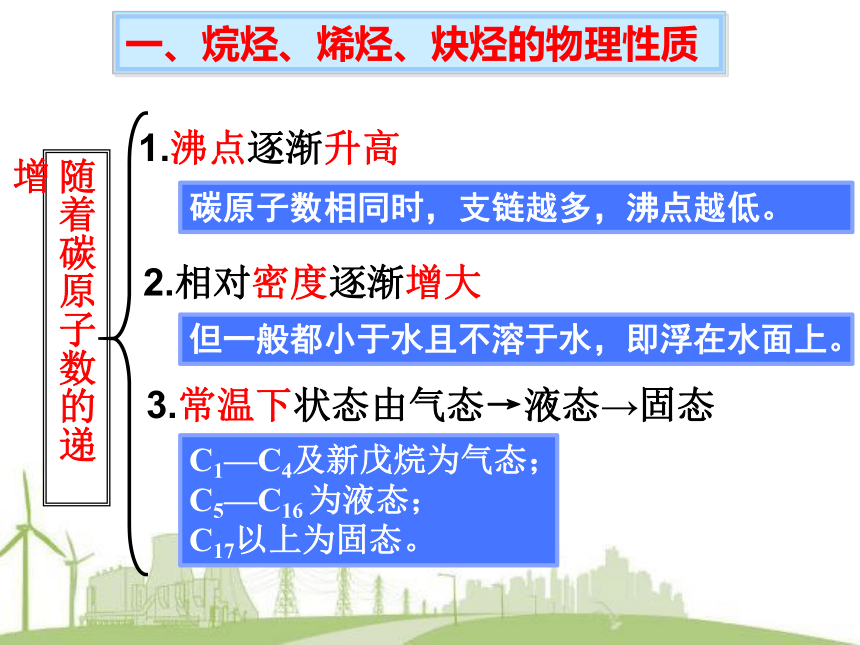
3.有机物的反应与无机物反应相比有何特点? 链状烃包括烷烃、烯烃、炔烃等。环状烃脂环烃芳香烃脂肪烃烃按碳的骨架给烃分类?【复习】第一节 脂肪烃——烷烃、烯烃、炔烃图2-1烷烃、烯烃的沸点随碳原子数变化曲线烷烃、烯烃同系物的相对密度随碳原子数的变化曲线同碳原子数的烷烃,支链越多熔沸点越低3.常温下状态由气态→液态→固态2.相对密度逐渐增大1.沸点逐渐升高碳原子数相同时,支链越多,沸点越低。C1—C4及新戊烷为气态;C5—C16 为液态;
C17以上为固态。一、烷烃、烯烃、炔烃的物理性质随着碳原子数的递增但一般都小于水且不溶于水,即浮在水面上。1.由下列数据:可判断丙烷的沸点可能是( )
A.高于-0.5℃ B.约是+30℃
C.约是-40℃ D.低于-89℃
2.下列烷烃沸点最高的是( )
A.CH3CH2CH3 B.CH3CH2CH2CH3
C.CH3(CH2)3CH3 D.(CH3)2CHCH2CH3
CC3.下列物质 ①丁烷 ②2-甲基丙烷 ③正戊烷
④2-甲基丁烷 ⑤2,2-二甲基丙烷 沸点由高到低的顺序应为 。 ③>④>⑤>①>②
——可燃性:二、烷烃、烯烃、炔烃的化学性质(一)共性1.等物质的量的下列烃完全燃烧时,消耗O2最多的是( )
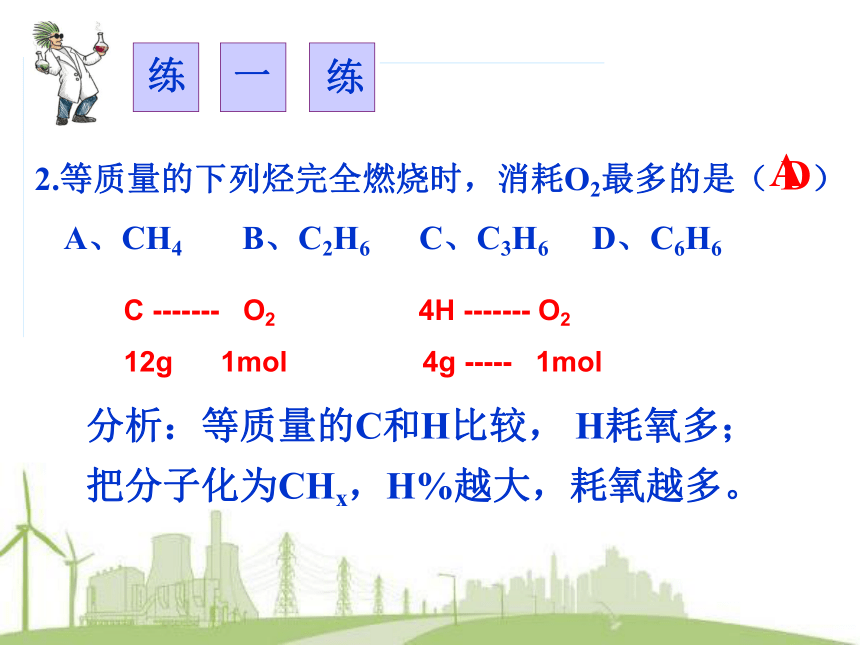
A、CH4 B、C2H6 C、C3H6 D、C6H62.等质量的下列烃完全燃烧时,消耗O2最多的是( )DC ------- O2 4H ------- O2
12g 1mol 4g ----- 1mol分析:等质量的C和H比较, H耗氧多;把分子化为CHx,H%越大,耗氧越多。A——可燃性:【常识】二、烷烃、烯烃、炔烃的化学性质(一)共性?2.甲烷——天然气主要成分;丙烷——液化石油气主要成分3.乙烯——衡量国家石油化工发展水平4.乙炔——氧炔焰用于切割、焊接金属(二)烷烃的性质二、烷烃、烯烃、炔烃的化学性质1、取代反应(光照、卤素单质)、 N (Cl2) :N(H) = 1:12、热分解3、稳定性:不能使酸性高锰酸钾溶液褪色——有进有出制炭黑甲烷与氯气反应CH2=CH2+Br2→CH2BrCH2Br(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质、N (H2) :N(C=C) = 1:11、加成反应(与H2、Br2、HX、H2O等)(1)乙烯加成:可使溴的四氯化碳溶液(或溴水)褪色——有进无出乙烯加成反应乙烯能使溴的CCl4褪色,甲同学认为发生了取代反应,乙同学认为发生了加成反应,
哪一位同学正确呢?试设计实验验证。 方法:向反应后溶液中加AgNO3溶液或石蕊
现象:若发生取代反应则生成HBr,则有淡黄色沉淀或加石蕊会变红;
若发生加成反应,则无此现象。按马氏规则,即氢多加氢。(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质1、加成反应丙烯CH2=CH-CH3CH2-CH-CH3
| |
H BrCH2-CH-CH3
| |
Br H主要产物(2)不对称烯烃和HX加成:+ HBr(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质(3)共轭二烯烃和1molBr2的1,2加成与1,4加成:1、加成反应CH2=CH-CH=CH2+Br2 CH2-CH-CH=CH2
| |
Br BrCH2-CH=CH-CH2
| |
Br Br1,2 加成1,4 加成1,2 Br1,4 Br(中间体)3,4-二溴-1-丁烯1,4-二溴-2-丁烯1 2 3 4(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质2、加聚反应单体链节聚合度加聚产物是由简单的结构单元即链节重复n次连接而成分别写出下列烯烃发生加聚反应的产物A. CH2=CHCH2CH3;B. CH3CH=CHCH2CH3;2-甲基-1,3-丁二烯
或异戊二烯 C. CH2=CH-CH=CH2 分别写出下列烯烃发生加聚反应的产物聚异戊二烯
或(天然橡胶)(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质3、氧化反应:能使酸性高锰酸钾溶液褪色并生成CO2能用于鉴别甲烷与乙烯两种气体的试剂或方法是( )
A、点燃 B、溴水
C、氯气 D、氢气B(四)炔烃的性质二、烷烃、烯烃、炔烃的化学性质1、加成反应:能使溴的四氯化碳溶液(或溴水)褪色——与烯烃类似但三键比双键稳定聚氯乙烯聚氯乙烯在使用的过程中,易发生老化,变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。2、氧化反应:能使酸性高锰酸钾褪色并生成CO21, 2—二溴乙烯1, 1, 2, 2—四溴乙烷CH≡CH + 2Br2 → CHBr2CHBr21mol乙炔最多能与2mol Br2发生加成反应练习2、某气态烃0.5mol能与1mol HCl氯化氢完全加成,加成产物分子上的氢原子又可被3mol Cl2取代,则气态烃可能是
A、CH ≡CH B、CH2=CH2
C、CH≡C—CH3 D、CH2=C(CH3)CH3 练习3、含一叁键的炔烃,氢化后的产物结构简式为
此炔烃可能有的结构有( )
A.1种 B.2种 C.3种 D.4种CnH2n+2CnH2n、CnH2n-2单键、饱和碳碳双键、三键、不饱和取代反应
氧化反应
分解反应加成
加聚反应
氧化反应小 结酸性高锰酸钾溶液或
溴水或溴的四氯化碳溶液 1.反应原理: 2.装置:
3.收集方法:
4.注意事项:
固+液不加热排水法收集三、乙炔的实验室制法注意事项:
(1)使用前要检验装置气密性。
(2)制取时在导气管口附近塞入少量棉花
目的:为防止产生的泡沫进入导管。
(3)常用饱和食盐水代替水,并用分液漏斗控制水流的速度,逐滴慢慢地滴入。电石与水反应很剧烈。
(4)纯净的乙炔气体是无色无味的气体。
用电石和水反应制取的乙炔,常闻到有恶臭气味。是因为在电石中含有少量硫化钙、砷化钙、磷化钙等杂质,跟水作用生成H2S、ASH3、PH3等有特殊气味气体所致。
常用盛有CuSO4溶液的洗气瓶除去。习题1.
鉴别甲烷、乙烯、乙炔三种气体可采用的方法是( )
A. 通入溴水中,观察溴水是否褪色。
B. 通入酸化的高锰酸钾溶液中,观察颜色是否变化。
C. 点燃,检验燃烧产物。
D. 点燃,观察火焰明亮程度及产生黑烟量的多少。D习题2. 下列说法正确的是( )
乙烯和乙炔都能使溴水褪色,但乙炔反应时要比等物质的量的乙烯消耗溴 单质要少。
B.纯净的乙炔没有难闻的臭味。
C.乙炔可用电石和水反应制得,所以可选用长颈漏斗加水。
D.乙炔含碳量高于乙烯,等物质的量的乙炔和乙烯充分燃烧时,乙炔耗氧多。BDBADC6.7.找出下列高聚物的单体(并命名有关产物)四、脂肪烃的来源及其应用脂肪烃的来源有石油、天然气和煤等。 石油通过常压分馏可以得到石油气、汽油、煤油、柴油等;减压分馏可以得到润滑油、石蜡等分子量较大的烷烃;气态烯烃是最基本的化工原料;催化重整是获得芳香烃的主要途径。 煤也是获得有机化合物的源泉。通过煤焦油的分馏可以获得各种芳香烃;通过煤矿直接或间接液化,可以获得燃料油及多种化工原料。天然气是高效清洁燃料,主要是烃类气体,以甲烷为主。原油的分馏及裂化的产品和用途石油的常压分馏产物:汽油、煤油、柴油等仍然是混合物。减压分馏润滑油石蜡沥青学与问 石油分馏是利用石油中各组分的沸点不同而加以分离的技术。
分为常压分馏和减压分馏,
常压分馏可以得到石油气、汽油、煤油、柴油和重油;重油再进行减压分馏可以得到润滑油、凡士林、石蜡等。
减压分馏是利用低压时液体的沸点降低的原理,使重油中各成分的沸点降低而进行分馏,避免高温下有机物的炭化。 石油催化重整的目的有两个:提高汽油的辛烷值和制取芳香烃。 石油裂解是深度的裂化,使短链的烷烃进一步分解生成乙烷、丙烷、丁烯等重要石油化工原料。 石油的催化裂化是将重油成分(如石油)在催化剂存在下,在460~520℃及100kPa~ 200kPa的压强下,长链烷烃断裂成短链烷烃和烯烃,从而大大提高汽油的产量。六、烃的来源及其应用知识回顾1、烃的主要来源是什么?2、石油、天然气和煤都是古代 经过一系列复杂变化而成的,它们是人们生活中经常使用的主要燃料,因此人们常称它们为 燃料,是 资源。动植物遗骸化石不可再生1、石油的炼制 石油主要是由多种碳氢化合物组成的混合物,主要含有烷烃及环烷烃。 利用原油中各组分沸点的不同,将复杂的混合物分离成简单和更有用的混合物的过程叫做分馏,该过程是物理变化。(1)石油的分馏 石油的分馏分为常压分馏和减压分馏两个过程。(2)石油的裂化 石油的裂化是将碳原子数较多、沸点较高的烃断裂为碳原子数较少、沸点较低的烃的过程。 裂化的目的:提高轻质液体燃料的产量C16H34→C8H18+C8H16C8H18→C4H10+C4H8(3)石油的裂解 石油的裂解同样是将碳原子数较多、沸点较高的烃断裂为碳原子数较少、沸点较低的烃的过程。 裂解是深度裂化,其目的是: 获得乙烯、丙烯、甲烷等重要化工基本原料。C4H10→C2H4+C2H6C4H10→CH4+C3H6气态烃经催化重整可获得芳香烃。2、天然气的综合利用 天然气是一种高效清洁的化石燃料,更是一种重要的化工原料,主要用于合成氨和生产甲醇等。 还可以利用甲烷合成含有两个或多个碳原子的其他有机物。3、煤的组成及综合利用(1)煤的组成:煤是由 和
组成的复杂混合物,主要含 元素,还含有少量的氢、氧、氮、硫等元素。 有机物少量无机物碳(2)煤综合利用的途径:_________、
__________、__________。 煤的干馏煤的气化煤的液化(3)煤的干馏煤干馏得到焦炭、煤焦油、焦炉气等,属于化学变化。 原理:将煤隔绝空气加强热使它分解的过程,也叫煤的焦化。焦炉气成分:氢气、甲烷、乙烯、一氧化碳(4)煤的气化原理:将其中的有机物转化为可燃性气体的过程。(5)煤的液化使煤先汽化为一氧化碳和氢气,再催化合成甲醇等 使煤与氢气作用生成液体燃料。间接液化:直接液化:考点三、烃的燃烧规律及有关计算1、烃完全燃烧前后体积的变化(1)燃烧后温度高于100℃时,水为气态:(2)燃烧后温度低于100℃时,水为液态:体积总是减小(3)无论水为气态,还是液态,燃烧前后体积的变化都只与烃分
子中的氢原子数有关,而与烃分子中的碳原子数无关.1、两种气态烃以任意比例混合,在105℃时1L该混合烃与9LO2混合,充分燃烧后恢复到原状态,所得气体体积仍为10L。下列各组混合烃中不符合此条件的是( )
A、CH4、C2H4 B、CH4、C3H6
C、C2H4、C3H4 D、C2H2、C3H6
2、a mL三种气态烃的混合物与足量的氧气混合点燃爆炸后,恢复到原来的状态(常温常压),体积共缩小2a mL。则三种烃可能是( )
A、CH4、C2H4、 、C3H4 B、C2H6、C3H6、C4H6
C、CH4、C2H6 C3H8 D、C2H4、C2H2、CH4
3、25℃时,某气态烃与O2混合充入密闭容器中,点燃爆炸后又恢复到25℃,此时容器内压强为原来的一半,再经NaOH溶液处理,容器内几乎成真空,该烃的分子式为( )
A、C2H4 B、C2H2 C、C3H6 D、C3H8A、DB、DA练习:Cu+ HO-NO2浓H2SO455℃~60℃-NO2+ H2O+ HO-SO3H 70℃~80℃-SO3H+ H2OABCDE下列反应属于取代反应的是+ HBr浓硫酸△二、烯烃的顺反异构 由于碳碳双键不能旋转而导致分子
中的原子或原子团在空间的排列方式不
同所产生的异构现象,称为顺反异构.顺反异构的概念: 两个相同的原子或原子团排列在双键的同一侧的称为顺式结构。 两个相同的原子或原子团排列在双键的两侧的称为反式结构。反-2-丁烯顺-2-丁烯化学性质基本相同,但物理性质有差异。练习1
下列哪些物质存在顺反异构?
A .1,2-二氯丙烯 B . 2-丁烯
C . 丙烯 D . 1-丁烯练习2. AB思考题:下列物质中没有顺反异构的是哪些?
1、 1,2-二氯乙烯
2、 1,2-二氯丙烯
3、 2-甲基-2-丁烯
4、 2-氯-2-丁烯 顺反异构的条件:形成顺反异构的条件:
1.具有碳碳双键
2.组成双键的每个碳原子必须连接
两个不同的原子或原子团.烯烃的同分异构现象(1)碳链异构(2)官能团位置异构(4)顺反异构(3)官能团异构以C4H8为例写出其烯烃类的同分异构体,
并用系统命名法命名思考:2-丁烯中与碳碳双键相连的两个碳原子、两个氢原子是否处于同一平面?若处于同一平面,与碳碳双键相连的两个碳原子是处于双键的同侧还是异侧?CH2=CHCH2CH3CH3CH=CHCH32-丁烯2-甲基-1-丙烯1-丁烯能否用启普发生器作乙炔气体发生装置?1.等物质的量的下列烃完全燃烧,消耗氧气最多的是( )
A.CH4 B.C5H12 C.C3H8 D.C2H6
2.下列各种有机物无论二者以何种比例混合,只要总的物质的量一定,则在完全燃烧时消耗的氧气的物质的量为一恒量的是 ( )
A.C3H6 C3H8 B. C4H6 C3H8
C. C8H10 C6H6 D. C10H8 C8H16DB聚氯乙烯聚氯乙烯在使用的过程中,易发生老化,变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。
2.烯烃CnH2n 碳碳双键 、不饱和、平面型
3.炔烃CnH2n-2 H-C≡C-、不饱和、直线型碳原子排列呈锯齿状,主链上的碳可能共面。双键碳原子上的所有原子一定共面.叁键碳原子上的所有原子一定共线.一、烷烃、烯烃、炔烃的结构1.CH≡C─CH=CHC(CH3)3中:在一条直线上的原子有 个,
至少 个有碳原子共面,最多有 个碳原子共面。456 练 习2.对CH3—CH = CH—C≡C—CF3的叙述下列正确的是 A.6个碳原子有可能都在一条直线上
B.6个碳原子不可能都在一条直线上
C.6个碳原子有可能都在同一平面上
D.6个碳原子不可能都在同一平面上 1.黑色的金子、工业的血液是什么?它的主要组成元素是什么?
2.什么是烃的衍生物?
什么是卤代径?
3.有机物的反应与无机物反应相比有何特点? 链状烃包括烷烃、烯烃、炔烃等。环状烃脂环烃芳香烃脂肪烃烃按碳的骨架给烃分类?【复习】第一节 脂肪烃——烷烃、烯烃、炔烃图2-1烷烃、烯烃的沸点随碳原子数变化曲线烷烃、烯烃同系物的相对密度随碳原子数的变化曲线同碳原子数的烷烃,支链越多熔沸点越低3.常温下状态由气态→液态→固态2.相对密度逐渐增大1.沸点逐渐升高碳原子数相同时,支链越多,沸点越低。C1—C4及新戊烷为气态;C5—C16 为液态;
C17以上为固态。一、烷烃、烯烃、炔烃的物理性质随着碳原子数的递增但一般都小于水且不溶于水,即浮在水面上。1.由下列数据:可判断丙烷的沸点可能是( )
A.高于-0.5℃ B.约是+30℃
C.约是-40℃ D.低于-89℃
2.下列烷烃沸点最高的是( )
A.CH3CH2CH3 B.CH3CH2CH2CH3
C.CH3(CH2)3CH3 D.(CH3)2CHCH2CH3
CC3.下列物质 ①丁烷 ②2-甲基丙烷 ③正戊烷
④2-甲基丁烷 ⑤2,2-二甲基丙烷 沸点由高到低的顺序应为 。 ③>④>⑤>①>②
——可燃性:二、烷烃、烯烃、炔烃的化学性质(一)共性1.等物质的量的下列烃完全燃烧时,消耗O2最多的是( )
A、CH4 B、C2H6 C、C3H6 D、C6H62.等质量的下列烃完全燃烧时,消耗O2最多的是( )DC ------- O2 4H ------- O2
12g 1mol 4g ----- 1mol分析:等质量的C和H比较, H耗氧多;把分子化为CHx,H%越大,耗氧越多。A——可燃性:【常识】二、烷烃、烯烃、炔烃的化学性质(一)共性?2.甲烷——天然气主要成分;丙烷——液化石油气主要成分3.乙烯——衡量国家石油化工发展水平4.乙炔——氧炔焰用于切割、焊接金属(二)烷烃的性质二、烷烃、烯烃、炔烃的化学性质1、取代反应(光照、卤素单质)、 N (Cl2) :N(H) = 1:12、热分解3、稳定性:不能使酸性高锰酸钾溶液褪色——有进有出制炭黑甲烷与氯气反应CH2=CH2+Br2→CH2BrCH2Br(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质、N (H2) :N(C=C) = 1:11、加成反应(与H2、Br2、HX、H2O等)(1)乙烯加成:可使溴的四氯化碳溶液(或溴水)褪色——有进无出乙烯加成反应乙烯能使溴的CCl4褪色,甲同学认为发生了取代反应,乙同学认为发生了加成反应,
哪一位同学正确呢?试设计实验验证。 方法:向反应后溶液中加AgNO3溶液或石蕊
现象:若发生取代反应则生成HBr,则有淡黄色沉淀或加石蕊会变红;
若发生加成反应,则无此现象。按马氏规则,即氢多加氢。(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质1、加成反应丙烯CH2=CH-CH3CH2-CH-CH3
| |
H BrCH2-CH-CH3
| |
Br H主要产物(2)不对称烯烃和HX加成:+ HBr(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质(3)共轭二烯烃和1molBr2的1,2加成与1,4加成:1、加成反应CH2=CH-CH=CH2+Br2 CH2-CH-CH=CH2
| |
Br BrCH2-CH=CH-CH2
| |
Br Br1,2 加成1,4 加成1,2 Br1,4 Br(中间体)3,4-二溴-1-丁烯1,4-二溴-2-丁烯1 2 3 4(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质2、加聚反应单体链节聚合度加聚产物是由简单的结构单元即链节重复n次连接而成分别写出下列烯烃发生加聚反应的产物A. CH2=CHCH2CH3;B. CH3CH=CHCH2CH3;2-甲基-1,3-丁二烯
或异戊二烯 C. CH2=CH-CH=CH2 分别写出下列烯烃发生加聚反应的产物聚异戊二烯
或(天然橡胶)(三)烯烃的性质二、烷烃、烯烃、炔烃的化学性质3、氧化反应:能使酸性高锰酸钾溶液褪色并生成CO2能用于鉴别甲烷与乙烯两种气体的试剂或方法是( )
A、点燃 B、溴水
C、氯气 D、氢气B(四)炔烃的性质二、烷烃、烯烃、炔烃的化学性质1、加成反应:能使溴的四氯化碳溶液(或溴水)褪色——与烯烃类似但三键比双键稳定聚氯乙烯聚氯乙烯在使用的过程中,易发生老化,变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。2、氧化反应:能使酸性高锰酸钾褪色并生成CO21, 2—二溴乙烯1, 1, 2, 2—四溴乙烷CH≡CH + 2Br2 → CHBr2CHBr21mol乙炔最多能与2mol Br2发生加成反应练习2、某气态烃0.5mol能与1mol HCl氯化氢完全加成,加成产物分子上的氢原子又可被3mol Cl2取代,则气态烃可能是
A、CH ≡CH B、CH2=CH2
C、CH≡C—CH3 D、CH2=C(CH3)CH3 练习3、含一叁键的炔烃,氢化后的产物结构简式为
此炔烃可能有的结构有( )
A.1种 B.2种 C.3种 D.4种CnH2n+2CnH2n、CnH2n-2单键、饱和碳碳双键、三键、不饱和取代反应
氧化反应
分解反应加成
加聚反应
氧化反应小 结酸性高锰酸钾溶液或
溴水或溴的四氯化碳溶液 1.反应原理: 2.装置:
3.收集方法:
4.注意事项:
固+液不加热排水法收集三、乙炔的实验室制法注意事项:
(1)使用前要检验装置气密性。
(2)制取时在导气管口附近塞入少量棉花
目的:为防止产生的泡沫进入导管。
(3)常用饱和食盐水代替水,并用分液漏斗控制水流的速度,逐滴慢慢地滴入。电石与水反应很剧烈。
(4)纯净的乙炔气体是无色无味的气体。
用电石和水反应制取的乙炔,常闻到有恶臭气味。是因为在电石中含有少量硫化钙、砷化钙、磷化钙等杂质,跟水作用生成H2S、ASH3、PH3等有特殊气味气体所致。
常用盛有CuSO4溶液的洗气瓶除去。习题1.
鉴别甲烷、乙烯、乙炔三种气体可采用的方法是( )
A. 通入溴水中,观察溴水是否褪色。
B. 通入酸化的高锰酸钾溶液中,观察颜色是否变化。
C. 点燃,检验燃烧产物。
D. 点燃,观察火焰明亮程度及产生黑烟量的多少。D习题2. 下列说法正确的是( )
乙烯和乙炔都能使溴水褪色,但乙炔反应时要比等物质的量的乙烯消耗溴 单质要少。
B.纯净的乙炔没有难闻的臭味。
C.乙炔可用电石和水反应制得,所以可选用长颈漏斗加水。
D.乙炔含碳量高于乙烯,等物质的量的乙炔和乙烯充分燃烧时,乙炔耗氧多。BDBADC6.7.找出下列高聚物的单体(并命名有关产物)四、脂肪烃的来源及其应用脂肪烃的来源有石油、天然气和煤等。 石油通过常压分馏可以得到石油气、汽油、煤油、柴油等;减压分馏可以得到润滑油、石蜡等分子量较大的烷烃;气态烯烃是最基本的化工原料;催化重整是获得芳香烃的主要途径。 煤也是获得有机化合物的源泉。通过煤焦油的分馏可以获得各种芳香烃;通过煤矿直接或间接液化,可以获得燃料油及多种化工原料。天然气是高效清洁燃料,主要是烃类气体,以甲烷为主。原油的分馏及裂化的产品和用途石油的常压分馏产物:汽油、煤油、柴油等仍然是混合物。减压分馏润滑油石蜡沥青学与问 石油分馏是利用石油中各组分的沸点不同而加以分离的技术。
分为常压分馏和减压分馏,
常压分馏可以得到石油气、汽油、煤油、柴油和重油;重油再进行减压分馏可以得到润滑油、凡士林、石蜡等。
减压分馏是利用低压时液体的沸点降低的原理,使重油中各成分的沸点降低而进行分馏,避免高温下有机物的炭化。 石油催化重整的目的有两个:提高汽油的辛烷值和制取芳香烃。 石油裂解是深度的裂化,使短链的烷烃进一步分解生成乙烷、丙烷、丁烯等重要石油化工原料。 石油的催化裂化是将重油成分(如石油)在催化剂存在下,在460~520℃及100kPa~ 200kPa的压强下,长链烷烃断裂成短链烷烃和烯烃,从而大大提高汽油的产量。六、烃的来源及其应用知识回顾1、烃的主要来源是什么?2、石油、天然气和煤都是古代 经过一系列复杂变化而成的,它们是人们生活中经常使用的主要燃料,因此人们常称它们为 燃料,是 资源。动植物遗骸化石不可再生1、石油的炼制 石油主要是由多种碳氢化合物组成的混合物,主要含有烷烃及环烷烃。 利用原油中各组分沸点的不同,将复杂的混合物分离成简单和更有用的混合物的过程叫做分馏,该过程是物理变化。(1)石油的分馏 石油的分馏分为常压分馏和减压分馏两个过程。(2)石油的裂化 石油的裂化是将碳原子数较多、沸点较高的烃断裂为碳原子数较少、沸点较低的烃的过程。 裂化的目的:提高轻质液体燃料的产量C16H34→C8H18+C8H16C8H18→C4H10+C4H8(3)石油的裂解 石油的裂解同样是将碳原子数较多、沸点较高的烃断裂为碳原子数较少、沸点较低的烃的过程。 裂解是深度裂化,其目的是: 获得乙烯、丙烯、甲烷等重要化工基本原料。C4H10→C2H4+C2H6C4H10→CH4+C3H6气态烃经催化重整可获得芳香烃。2、天然气的综合利用 天然气是一种高效清洁的化石燃料,更是一种重要的化工原料,主要用于合成氨和生产甲醇等。 还可以利用甲烷合成含有两个或多个碳原子的其他有机物。3、煤的组成及综合利用(1)煤的组成:煤是由 和
组成的复杂混合物,主要含 元素,还含有少量的氢、氧、氮、硫等元素。 有机物少量无机物碳(2)煤综合利用的途径:_________、
__________、__________。 煤的干馏煤的气化煤的液化(3)煤的干馏煤干馏得到焦炭、煤焦油、焦炉气等,属于化学变化。 原理:将煤隔绝空气加强热使它分解的过程,也叫煤的焦化。焦炉气成分:氢气、甲烷、乙烯、一氧化碳(4)煤的气化原理:将其中的有机物转化为可燃性气体的过程。(5)煤的液化使煤先汽化为一氧化碳和氢气,再催化合成甲醇等 使煤与氢气作用生成液体燃料。间接液化:直接液化:考点三、烃的燃烧规律及有关计算1、烃完全燃烧前后体积的变化(1)燃烧后温度高于100℃时,水为气态:(2)燃烧后温度低于100℃时,水为液态:体积总是减小(3)无论水为气态,还是液态,燃烧前后体积的变化都只与烃分
子中的氢原子数有关,而与烃分子中的碳原子数无关.1、两种气态烃以任意比例混合,在105℃时1L该混合烃与9LO2混合,充分燃烧后恢复到原状态,所得气体体积仍为10L。下列各组混合烃中不符合此条件的是( )
A、CH4、C2H4 B、CH4、C3H6
C、C2H4、C3H4 D、C2H2、C3H6
2、a mL三种气态烃的混合物与足量的氧气混合点燃爆炸后,恢复到原来的状态(常温常压),体积共缩小2a mL。则三种烃可能是( )
A、CH4、C2H4、 、C3H4 B、C2H6、C3H6、C4H6
C、CH4、C2H6 C3H8 D、C2H4、C2H2、CH4
3、25℃时,某气态烃与O2混合充入密闭容器中,点燃爆炸后又恢复到25℃,此时容器内压强为原来的一半,再经NaOH溶液处理,容器内几乎成真空,该烃的分子式为( )
A、C2H4 B、C2H2 C、C3H6 D、C3H8A、DB、DA练习:Cu+ HO-NO2浓H2SO455℃~60℃-NO2+ H2O+ HO-SO3H 70℃~80℃-SO3H+ H2OABCDE下列反应属于取代反应的是+ HBr浓硫酸△二、烯烃的顺反异构 由于碳碳双键不能旋转而导致分子
中的原子或原子团在空间的排列方式不
同所产生的异构现象,称为顺反异构.顺反异构的概念: 两个相同的原子或原子团排列在双键的同一侧的称为顺式结构。 两个相同的原子或原子团排列在双键的两侧的称为反式结构。反-2-丁烯顺-2-丁烯化学性质基本相同,但物理性质有差异。练习1
下列哪些物质存在顺反异构?
A .1,2-二氯丙烯 B . 2-丁烯
C . 丙烯 D . 1-丁烯练习2. AB思考题:下列物质中没有顺反异构的是哪些?
1、 1,2-二氯乙烯
2、 1,2-二氯丙烯
3、 2-甲基-2-丁烯
4、 2-氯-2-丁烯 顺反异构的条件:形成顺反异构的条件:
1.具有碳碳双键
2.组成双键的每个碳原子必须连接
两个不同的原子或原子团.烯烃的同分异构现象(1)碳链异构(2)官能团位置异构(4)顺反异构(3)官能团异构以C4H8为例写出其烯烃类的同分异构体,
并用系统命名法命名思考:2-丁烯中与碳碳双键相连的两个碳原子、两个氢原子是否处于同一平面?若处于同一平面,与碳碳双键相连的两个碳原子是处于双键的同侧还是异侧?CH2=CHCH2CH3CH3CH=CHCH32-丁烯2-甲基-1-丙烯1-丁烯能否用启普发生器作乙炔气体发生装置?1.等物质的量的下列烃完全燃烧,消耗氧气最多的是( )
A.CH4 B.C5H12 C.C3H8 D.C2H6
2.下列各种有机物无论二者以何种比例混合,只要总的物质的量一定,则在完全燃烧时消耗的氧气的物质的量为一恒量的是 ( )
A.C3H6 C3H8 B. C4H6 C3H8
C. C8H10 C6H6 D. C10H8 C8H16DB聚氯乙烯聚氯乙烯在使用的过程中,易发生老化,变硬、发脆、开裂等,并释放出对人体有害的氯化氢,故不宜使用聚氯乙烯制品直接盛装食物。
