3.2.1乙醇课件(共24张ppt)化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.2.1乙醇课件(共24张ppt)化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-17 00:00:00 | ||
图片预览





文档简介
(共24张PPT)
第三章 烃的衍生物
3.2.1 醇
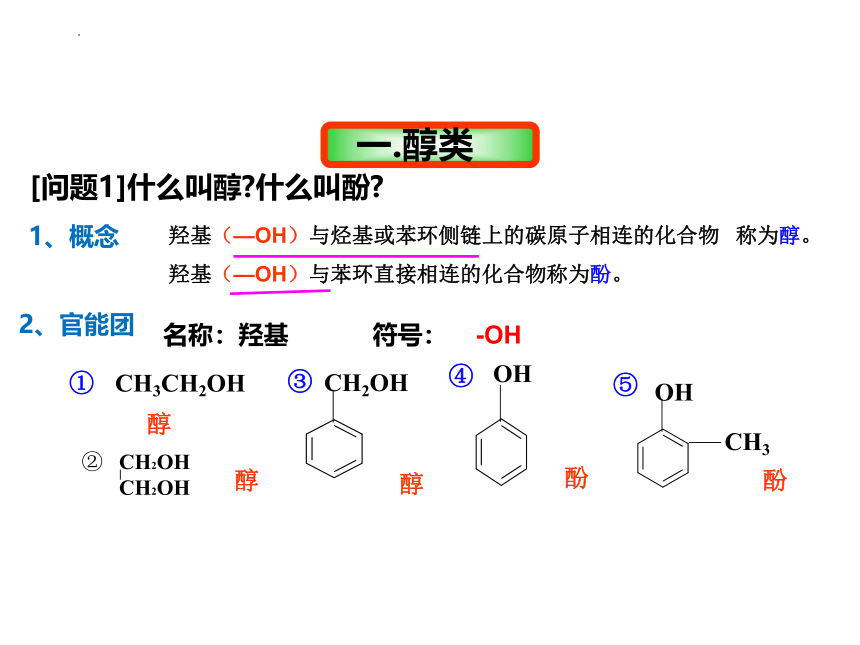
羟基(—OH)与烃基或苯环侧链上的碳原子相连的化合物 称为醇。
羟基(—OH)与苯环直接相连的化合物称为酚。
醇
酚
醇
OH
① CH3CH2OH
CH2OH
OH
CH3
酚
③
④
⑤
② CH2OH
CH2OH
醇
[问题1]什么叫醇 什么叫酚
1、概念
2、官能团
名称:羟基 符号: -OH
一.醇类
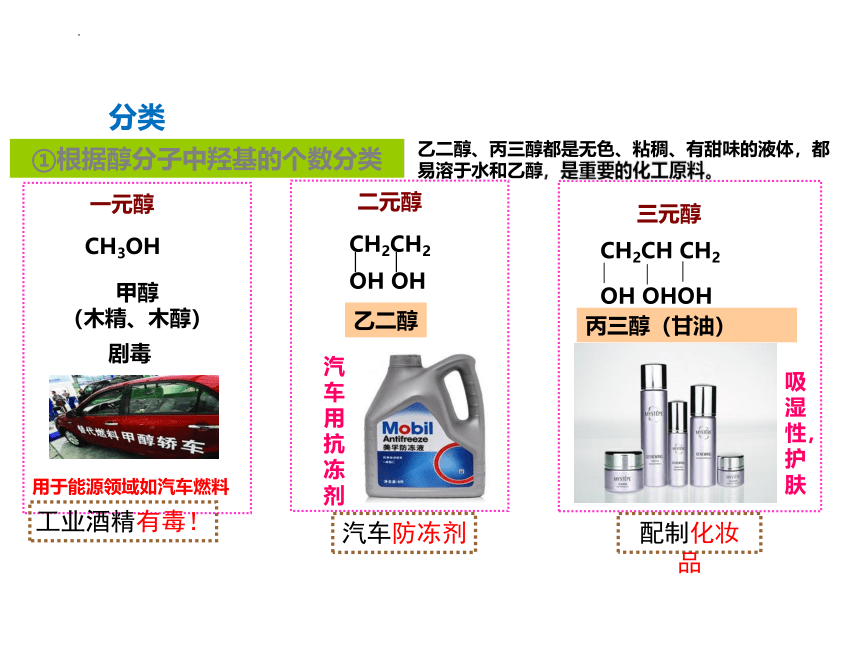
①根据醇分子中羟基的个数分类
CH2CH2
OH OH
乙二醇
汽车用抗冻剂
二元醇
CH2CH CH2
OH OHOH
丙三醇(甘油)
吸湿性,护肤
三元醇
一元醇
CH3OH
甲醇
(木精、木醇)
剧毒
用于能源领域如汽车燃料
乙二醇、丙三醇都是无色、粘稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。
工业酒精有毒!
汽车防冻剂
配制化妆品
分类
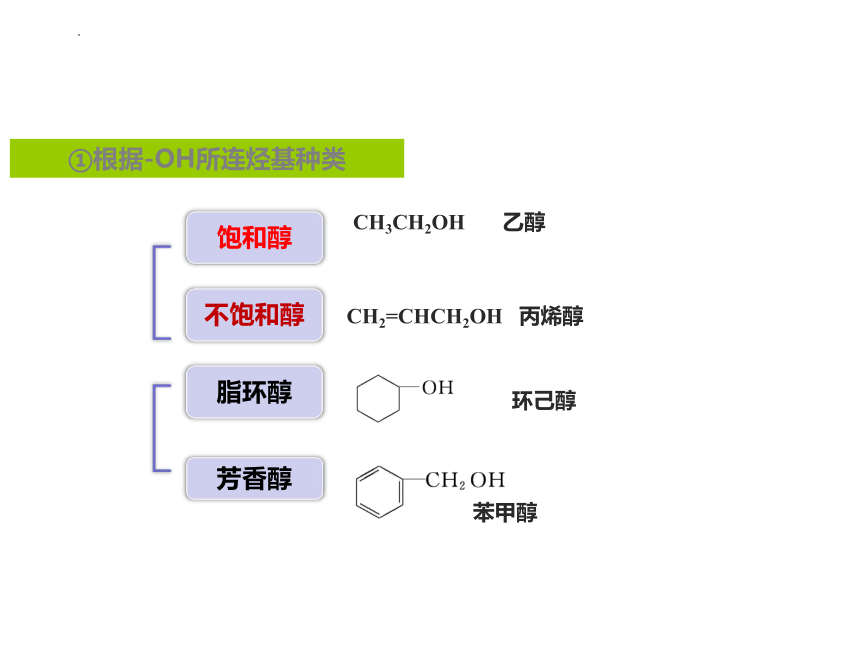
饱和醇
不饱和醇
脂环醇
芳香醇
CH3CH2OH 乙醇
CH2=CHCH2OH 丙烯醇
苯甲醇
环己醇
①根据-OH所连烃基种类
相对分子质量相近的醇与烷烃的沸点比较
名称 相对分子质量 沸点/℃
甲醇 32 64.7
乙烷 30 -88.6
乙醇 46 78.5
丙烷 44 -42.1
丙醇 60 97.2
丁烷 58 -0.5
结论:P60
醇分子间形成氢键
氢键
物理性质
(2)溶解性:
(1)沸点:
(3)密度:
饱和一元醇随碳原子数增多,沸点增大,醇的沸点远高于相对分子质量相近的烷烃。
醇的密度小于水。
①甲醇、乙醇和丙醇均可与水互溶,因为醇分子与水分子间形成了氢键。
②醇在水中的溶解度一般随碳原子数的增加而减小。
③碳原子数相同时,羟基个数越多,醇的水溶性越好。
(淡蓝色火焰)
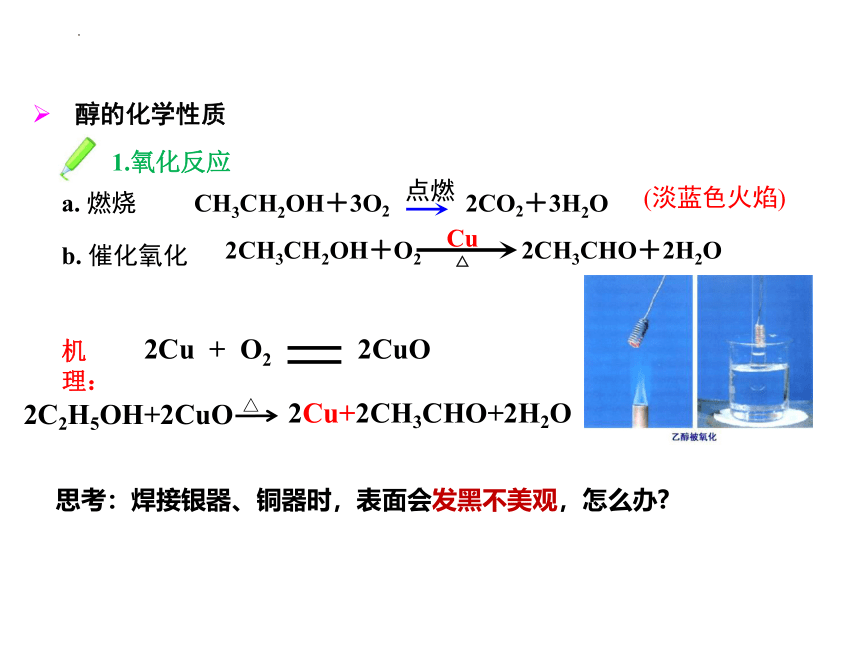
a. 燃烧
b. 催化氧化
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
△
醇的化学性质
CH3CH2OH+3O2 2CO2+3H2O
点燃
△
2Cu + O2 2CuO
2Cu+2CH3CHO+2H2O
机理:
1.氧化反应
2C2H5OH+2CuO
思考:焊接银器、铜器时,表面会发黑不美观,怎么办
CH3CH2OH
CH3COOH
酸性K2Cr2O7
或 酸性KMnO4
(乙酸)
酸性K2Cr2O7溶液
橙色
Cr3+
绿色
酒驾
①羟基所在碳上有两个氢可氧化生成酸
②羟基所在碳上有一个氢可氧化生成酮
③羟基所在碳上没有氢不能被氧化
R CH2OH
R COOH
KMnO4(H+)或
K2Cr2O7(H+)
R1 CH R2
OH
KMnO4(H+)或
K2Cr2O7(H+)
R1 C R2
O
小结:醇与强氧化剂反应
2.取代反应
醇
(1)酯化反应
酸脱羟基、醇脱羟基上的氢原子
18
18
O O
CH3—C—OH+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
H C C O H
H
H
H
H
2.取代反应
醇
(2)与氢卤酸HX反应
C2H5 OH + H Br C2H5 Br + H2O
△
乙醇与浓氢溴酸混合加热
H C C O H
H
H
H
H
2.取代反应
醇
(3)分子间脱水
C2H5 OH + HO C2H5 C2H5 O C2H5 + H2O
浓H2SO4
140 ℃
一分子脱羟基,另一分子脱羟基氢
乙醚
醚类物质可用作溶剂和麻醉剂
3.消去反应
醇
1700C
浓H2SO4
H C C H CH2=CH2 +H2O
H
H
H
OH
分子内脱水
相邻碳原子上有氢原子
乙烯的实验室制法
1.实验原理
CH2=CH2 ↑ +H2O
1700C
浓H2SO4
CH3CH2OH
酸性KMnO4溶液
NaOH溶液
溴的四氯化碳溶液
混合液
碎瓷片
温度计
2.实验装置
液体逐渐变黑
溶液褪色
乙烯的实验室制法
3.实验注意事项
(1)放入几片碎瓷片作用
(2) 浓硫酸的作用
温度计水银球要置于反应物的液面下,因为需要测量的是反应物的温度。
防止暴沸
催化剂和脱水剂
(3)温度计的位置
(4)加药品顺序
浓硫酸缓慢加入乙醇中
(5)反应所得气体要除杂质气体
(6)温度要迅速升高并稳定在170℃
防止140℃时发生副反应,生成乙醚
乙烯的实验室制法
3.实验注意事项
反应制得的乙烯中往往混有CO2、SO2等气体。其中SO2会干扰后续实验现象,可将气体通过NaOH溶液除去。
(6)温度要迅速升高并稳定在170℃
乙醇和浓硫酸混合物在170℃的温度下主要生成乙烯和水,而在140℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚。
醇
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应 断键位置
分子间脱水
与HX反应
②④
②
①③
①②
与金属反应
消去反应
催化氧化
①
1.等物质的量的乙醇、乙二醇、丙三醇中分别加入足量的金属钠产生等体积的氢气(相同条件),则产生氢气的体积之比是 ( )A.2∶3∶6 B.6∶3∶2 C.3∶2∶1 D.1∶2∶3
课堂检测
D
2 、二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO—CH2CH2—O—CH2CH2—OH。下列有关二甘醇的叙述正确的是 ( )
A.不能发生消去反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D. 不能氧化为醛
B
3.某有机物的结构简式为:
则此有机物可发生的反应类型有:
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚 ⑧中和 ( )
A.①②④⑤⑥⑦⑧ B.②③④⑤⑥⑧
C.②③④⑤⑥⑦⑧ D.①②③④⑤⑥⑦⑧
课堂检测
D
课堂检测
写出下列醇发生消去反应的化学反应方程式
① CH3CH2CH2OH
④ (CH3)3COH
② CH3CHCH2CH3
OH
③ CH2OH
CH2OH
(1)选择包含官能团的最长碳链作为主链
(2)从靠近官能团的一端开始编号
CH3—CH—CH2—OH
CH3
CH2—OH
CH2—OH
CH2—OH
CH—OH
CH2—OH
CH3 CH CH
HO CH CH3
CH3
CH3
3,4-二甲基-2-戊醇
1,2,3-丙三醇
2-甲基-1-丙醇
1,2-乙二醇
醇的命名
2CH3CH2CH2OH+O2
Cu
△
(CH3)3COH
Cu
△
+O2
【例】写出下列有机物催化氧化的反应方程式:
Cu
△
2CH3CHCH3+O2
OH
Cu
△
+O2
CH2OH
CH2OH
不可被氧化
2CH3CH2CHO+2H2O
2CH3—C—CH3+2H2O
O
+2H2O
CHO
CHO
生活中的醇
聚会时酒必不可少
但不是所有人酒量都好
在日常生活中,我们看到有些人喝酒后,会产生脸部变红、呕吐、昏迷等醉酒症状;有些人喝了一定量的酒,却并不会出现上述症状。这是什么原因造成的呢
第三章 烃的衍生物
3.2.1 醇
羟基(—OH)与烃基或苯环侧链上的碳原子相连的化合物 称为醇。
羟基(—OH)与苯环直接相连的化合物称为酚。
醇
酚
醇
OH
① CH3CH2OH
CH2OH
OH
CH3
酚
③
④
⑤
② CH2OH
CH2OH
醇
[问题1]什么叫醇 什么叫酚
1、概念
2、官能团
名称:羟基 符号: -OH
一.醇类
①根据醇分子中羟基的个数分类
CH2CH2
OH OH
乙二醇
汽车用抗冻剂
二元醇
CH2CH CH2
OH OHOH
丙三醇(甘油)
吸湿性,护肤
三元醇
一元醇
CH3OH
甲醇
(木精、木醇)
剧毒
用于能源领域如汽车燃料
乙二醇、丙三醇都是无色、粘稠、有甜味的液体,都易溶于水和乙醇,是重要的化工原料。
工业酒精有毒!
汽车防冻剂
配制化妆品
分类
饱和醇
不饱和醇
脂环醇
芳香醇
CH3CH2OH 乙醇
CH2=CHCH2OH 丙烯醇
苯甲醇
环己醇
①根据-OH所连烃基种类
相对分子质量相近的醇与烷烃的沸点比较
名称 相对分子质量 沸点/℃
甲醇 32 64.7
乙烷 30 -88.6
乙醇 46 78.5
丙烷 44 -42.1
丙醇 60 97.2
丁烷 58 -0.5
结论:P60
醇分子间形成氢键
氢键
物理性质
(2)溶解性:
(1)沸点:
(3)密度:
饱和一元醇随碳原子数增多,沸点增大,醇的沸点远高于相对分子质量相近的烷烃。
醇的密度小于水。
①甲醇、乙醇和丙醇均可与水互溶,因为醇分子与水分子间形成了氢键。
②醇在水中的溶解度一般随碳原子数的增加而减小。
③碳原子数相同时,羟基个数越多,醇的水溶性越好。
(淡蓝色火焰)
a. 燃烧
b. 催化氧化
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu
△
醇的化学性质
CH3CH2OH+3O2 2CO2+3H2O
点燃
△
2Cu + O2 2CuO
2Cu+2CH3CHO+2H2O
机理:
1.氧化反应
2C2H5OH+2CuO
思考:焊接银器、铜器时,表面会发黑不美观,怎么办
CH3CH2OH
CH3COOH
酸性K2Cr2O7
或 酸性KMnO4
(乙酸)
酸性K2Cr2O7溶液
橙色
Cr3+
绿色
酒驾
①羟基所在碳上有两个氢可氧化生成酸
②羟基所在碳上有一个氢可氧化生成酮
③羟基所在碳上没有氢不能被氧化
R CH2OH
R COOH
KMnO4(H+)或
K2Cr2O7(H+)
R1 CH R2
OH
KMnO4(H+)或
K2Cr2O7(H+)
R1 C R2
O
小结:醇与强氧化剂反应
2.取代反应
醇
(1)酯化反应
酸脱羟基、醇脱羟基上的氢原子
18
18
O O
CH3—C—OH+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
H C C O H
H
H
H
H
2.取代反应
醇
(2)与氢卤酸HX反应
C2H5 OH + H Br C2H5 Br + H2O
△
乙醇与浓氢溴酸混合加热
H C C O H
H
H
H
H
2.取代反应
醇
(3)分子间脱水
C2H5 OH + HO C2H5 C2H5 O C2H5 + H2O
浓H2SO4
140 ℃
一分子脱羟基,另一分子脱羟基氢
乙醚
醚类物质可用作溶剂和麻醉剂
3.消去反应
醇
1700C
浓H2SO4
H C C H CH2=CH2 +H2O
H
H
H
OH
分子内脱水
相邻碳原子上有氢原子
乙烯的实验室制法
1.实验原理
CH2=CH2 ↑ +H2O
1700C
浓H2SO4
CH3CH2OH
酸性KMnO4溶液
NaOH溶液
溴的四氯化碳溶液
混合液
碎瓷片
温度计
2.实验装置
液体逐渐变黑
溶液褪色
乙烯的实验室制法
3.实验注意事项
(1)放入几片碎瓷片作用
(2) 浓硫酸的作用
温度计水银球要置于反应物的液面下,因为需要测量的是反应物的温度。
防止暴沸
催化剂和脱水剂
(3)温度计的位置
(4)加药品顺序
浓硫酸缓慢加入乙醇中
(5)反应所得气体要除杂质气体
(6)温度要迅速升高并稳定在170℃
防止140℃时发生副反应,生成乙醚
乙烯的实验室制法
3.实验注意事项
反应制得的乙烯中往往混有CO2、SO2等气体。其中SO2会干扰后续实验现象,可将气体通过NaOH溶液除去。
(6)温度要迅速升高并稳定在170℃
乙醇和浓硫酸混合物在170℃的温度下主要生成乙烯和水,而在140℃时乙醇将以另一种方式脱水,即分子间脱水,生成乙醚。
醇
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应 断键位置
分子间脱水
与HX反应
②④
②
①③
①②
与金属反应
消去反应
催化氧化
①
1.等物质的量的乙醇、乙二醇、丙三醇中分别加入足量的金属钠产生等体积的氢气(相同条件),则产生氢气的体积之比是 ( )A.2∶3∶6 B.6∶3∶2 C.3∶2∶1 D.1∶2∶3
课堂检测
D
2 、二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO—CH2CH2—O—CH2CH2—OH。下列有关二甘醇的叙述正确的是 ( )
A.不能发生消去反应 B.能发生取代反应
C.能溶于水,不溶于乙醇 D. 不能氧化为醛
B
3.某有机物的结构简式为:
则此有机物可发生的反应类型有:
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化 ⑦加聚 ⑧中和 ( )
A.①②④⑤⑥⑦⑧ B.②③④⑤⑥⑧
C.②③④⑤⑥⑦⑧ D.①②③④⑤⑥⑦⑧
课堂检测
D
课堂检测
写出下列醇发生消去反应的化学反应方程式
① CH3CH2CH2OH
④ (CH3)3COH
② CH3CHCH2CH3
OH
③ CH2OH
CH2OH
(1)选择包含官能团的最长碳链作为主链
(2)从靠近官能团的一端开始编号
CH3—CH—CH2—OH
CH3
CH2—OH
CH2—OH
CH2—OH
CH—OH
CH2—OH
CH3 CH CH
HO CH CH3
CH3
CH3
3,4-二甲基-2-戊醇
1,2,3-丙三醇
2-甲基-1-丙醇
1,2-乙二醇
醇的命名
2CH3CH2CH2OH+O2
Cu
△
(CH3)3COH
Cu
△
+O2
【例】写出下列有机物催化氧化的反应方程式:
Cu
△
2CH3CHCH3+O2
OH
Cu
△
+O2
CH2OH
CH2OH
不可被氧化
2CH3CH2CHO+2H2O
2CH3—C—CH3+2H2O
O
+2H2O
CHO
CHO
生活中的醇
聚会时酒必不可少
但不是所有人酒量都好
在日常生活中,我们看到有些人喝酒后,会产生脸部变红、呕吐、昏迷等醉酒症状;有些人喝了一定量的酒,却并不会出现上述症状。这是什么原因造成的呢
