5.1硫及其化合物 课件(20张PPT)高中化学人教版(2019)必修 第二册
文档属性
| 名称 | 5.1硫及其化合物 课件(20张PPT)高中化学人教版(2019)必修 第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1009.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-17 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
硫及其化合物
【思考】
1.亮蓝色的火焰来自于什么化学过程?
2.火山附近气体冷却后,会得到哪种物质?
3.吸入火山喷发的气体,人会中毒,该气体是什么?
(1)游离态:
存在于火山喷口附近或地壳的岩层里
(2)化合态:
硫化物
硫酸盐
有机物
硫铁矿(FeS2),黄铜矿(CuFeS2)
石膏(CaSO4·2H2O)
芒硝(Na2SO4·10H2O)
石油、天然气、煤、蛋白质等
一、硫的存在及性质
1.存在
2. 硫单质的性质
(1)物理性质
黄色晶体,俗称硫黄,质脆,易研成粉末。难溶于水,微溶于酒精,易溶于二硫化碳(CS2);熔沸点低,密度比水大(2.06 g/cm3 )。
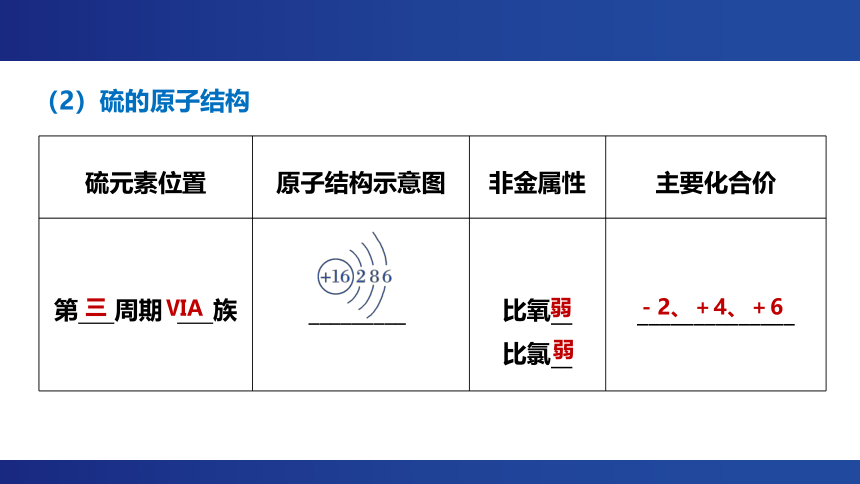
(2)硫的原子结构
一、硫
硫元素位置 原子结构示意图 非金属性 主要化合价
第 周期 族 _________ 比氧__ 比氯__ ______________
三
ⅥA
弱
-2、+4、+6
弱
(3)化学性质
①氧化性:
2Cu + S = Cu2S
△
H2 + S = H2S
△
与Na、Fe、Cu、Hg等金属及H2反应
单质硫的氧化性较弱,与变价金属反应时,一般只生成低价金属硫化物(如FeS、Cu2S)。
Fe + S = FeS
△
2Na + S = Na2S
△
无色、有刺激性气味的有毒气体,密度大于空气,溶解度???
【实验1】 观察矿泉水瓶中的SO2气体,并描述其物理性质。
【实验2】 向充有约400mLSO2的矿泉水瓶快速倒入20mL蒸馏水,然后迅速将盖子旋紧,振荡,观察瓶子的变化。
任务一:SO2的物理性质
二、二氧化硫的性质
【实验3】 用pH试纸检验SO2水溶液的酸碱性。
任务二:SO2溶于水有没有发生化学反应?能否设计实验验证你的猜测?
任务二:SO2的化学性质
(1)SO2具有酸性氧化物的通性
①写出下列反应的化学方程式:
a.和水反应:___________________________。
b.和澄清石灰水反应:_____________________________。
c.和CaO反应:___________________。
②可逆反应:在 条件下,既能向 方向进行, 又能向______方向进行的反应。
在可逆反应的化学方程式中用“_____”代替“_____”。
SO2+Ca(OH)2=CaSO3↓+H2O
SO2+CaO=CaSO3
=
同一
正反应
同时
逆反应
【思考】从元素化合价变化的角度推测SO2可能具有哪些性质?
(2)从元素化合价变化的角度分析SO2性质
H2SO4+2HCl
2SO3
3S+2H2O
3.漂白性
某些有机色素+SO2
无色的物质
△
【实验4】观察课本P3演示实验,思考该实验体现出SO2的什么性质?
它能与某些有色物质(如品红溶液)生成不稳定的无色物质。这些无色物质容易分解而使有色物质恢复原来的颜色。
类型 漂白原理 漂白特点 变化类型 举例
氧化型 具有强氧化性,因与有色物质发生氧化还原反应而使其褪色 褪色后不会恢复原色 化学变化 HClO、Na2O2、O3、H2O2等
化合型 与某些有色物质发生化合反应而使其褪色 一定条件下分解,又恢复原色 化学变化 SO2
吸附型 某些固体物质具有疏松多孔结构,能吸附有色物质 物理变化 活性炭等
天然银耳
SO2熏制的银耳
4.SO2的用途
肉类防腐
食品保鲜
4.SO2的用途
二氧化硫常用作漂白剂、杀菌消毒剂、食品添加剂。
【思考】
1.下列反应是可逆反应吗?
(1)CO2+H2O = H2CO3,H2CO3 = CO2↑+H2O
(2)2H2+O2 == 2H2O,2H2O == 2H2↑+O2 ↑
点燃
通电
3.SO2有漂白作用,氯水也有漂白作用,如果把SO2和氯水
混合,漂白效果会增强吗?
2.SO2使酸性KMnO4溶液褪色,能体现SO2的漂白作用吗?
同学们,再见
硫及其化合物
【思考】
1.亮蓝色的火焰来自于什么化学过程?
2.火山附近气体冷却后,会得到哪种物质?
3.吸入火山喷发的气体,人会中毒,该气体是什么?
(1)游离态:
存在于火山喷口附近或地壳的岩层里
(2)化合态:
硫化物
硫酸盐
有机物
硫铁矿(FeS2),黄铜矿(CuFeS2)
石膏(CaSO4·2H2O)
芒硝(Na2SO4·10H2O)
石油、天然气、煤、蛋白质等
一、硫的存在及性质
1.存在
2. 硫单质的性质
(1)物理性质
黄色晶体,俗称硫黄,质脆,易研成粉末。难溶于水,微溶于酒精,易溶于二硫化碳(CS2);熔沸点低,密度比水大(2.06 g/cm3 )。
(2)硫的原子结构
一、硫
硫元素位置 原子结构示意图 非金属性 主要化合价
第 周期 族 _________ 比氧__ 比氯__ ______________
三
ⅥA
弱
-2、+4、+6
弱
(3)化学性质
①氧化性:
2Cu + S = Cu2S
△
H2 + S = H2S
△
与Na、Fe、Cu、Hg等金属及H2反应
单质硫的氧化性较弱,与变价金属反应时,一般只生成低价金属硫化物(如FeS、Cu2S)。
Fe + S = FeS
△
2Na + S = Na2S
△
无色、有刺激性气味的有毒气体,密度大于空气,溶解度???
【实验1】 观察矿泉水瓶中的SO2气体,并描述其物理性质。
【实验2】 向充有约400mLSO2的矿泉水瓶快速倒入20mL蒸馏水,然后迅速将盖子旋紧,振荡,观察瓶子的变化。
任务一:SO2的物理性质
二、二氧化硫的性质
【实验3】 用pH试纸检验SO2水溶液的酸碱性。
任务二:SO2溶于水有没有发生化学反应?能否设计实验验证你的猜测?
任务二:SO2的化学性质
(1)SO2具有酸性氧化物的通性
①写出下列反应的化学方程式:
a.和水反应:___________________________。
b.和澄清石灰水反应:_____________________________。
c.和CaO反应:___________________。
②可逆反应:在 条件下,既能向 方向进行, 又能向______方向进行的反应。
在可逆反应的化学方程式中用“_____”代替“_____”。
SO2+Ca(OH)2=CaSO3↓+H2O
SO2+CaO=CaSO3
=
同一
正反应
同时
逆反应
【思考】从元素化合价变化的角度推测SO2可能具有哪些性质?
(2)从元素化合价变化的角度分析SO2性质
H2SO4+2HCl
2SO3
3S+2H2O
3.漂白性
某些有机色素+SO2
无色的物质
△
【实验4】观察课本P3演示实验,思考该实验体现出SO2的什么性质?
它能与某些有色物质(如品红溶液)生成不稳定的无色物质。这些无色物质容易分解而使有色物质恢复原来的颜色。
类型 漂白原理 漂白特点 变化类型 举例
氧化型 具有强氧化性,因与有色物质发生氧化还原反应而使其褪色 褪色后不会恢复原色 化学变化 HClO、Na2O2、O3、H2O2等
化合型 与某些有色物质发生化合反应而使其褪色 一定条件下分解,又恢复原色 化学变化 SO2
吸附型 某些固体物质具有疏松多孔结构,能吸附有色物质 物理变化 活性炭等
天然银耳
SO2熏制的银耳
4.SO2的用途
肉类防腐
食品保鲜
4.SO2的用途
二氧化硫常用作漂白剂、杀菌消毒剂、食品添加剂。
【思考】
1.下列反应是可逆反应吗?
(1)CO2+H2O = H2CO3,H2CO3 = CO2↑+H2O
(2)2H2+O2 == 2H2O,2H2O == 2H2↑+O2 ↑
点燃
通电
3.SO2有漂白作用,氯水也有漂白作用,如果把SO2和氯水
混合,漂白效果会增强吗?
2.SO2使酸性KMnO4溶液褪色,能体现SO2的漂白作用吗?
同学们,再见
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
