7.1认识有机化合物 课件(16张PPT)高中化学人教版(2019)必修 第二册
文档属性
| 名称 | 7.1认识有机化合物 课件(16张PPT)高中化学人教版(2019)必修 第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-17 00:00:00 | ||
图片预览




文档简介
(共16张PPT)
厨房中的有机物—烷烃
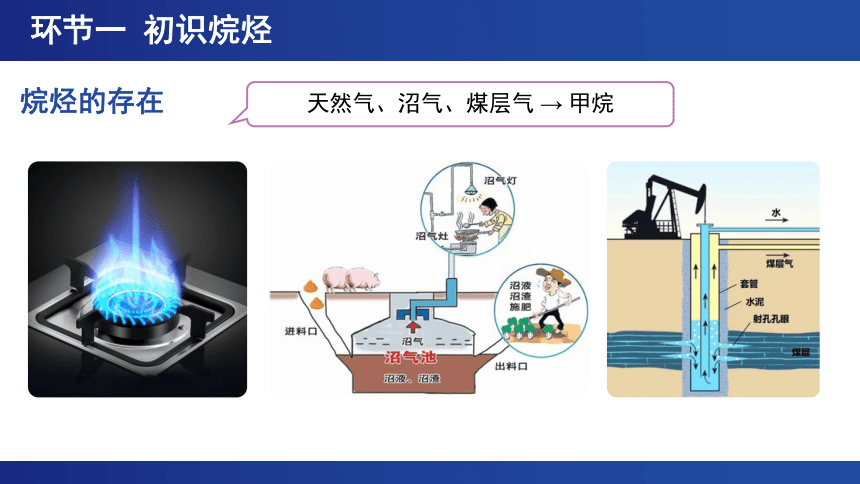
烷烃的存在
环节一 初识烷烃
天然气、沼气、煤层气 → 甲烷
环节一 初识烷烃
结合生活经验以及所学知识,想想烷烃可能有哪些性质。
烷烃的存在
蜡烛、蜡笔、凡士林 → 含碳原子数较多的烷烃
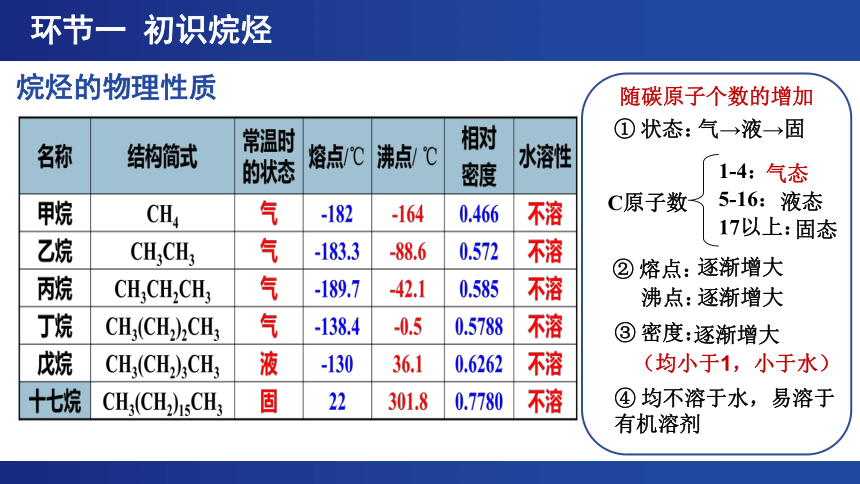
烷烃的物理性质
① 状态:
C原子数
1-4:
5-16:
17以上:
随碳原子个数的增加
③ 密度:
② 熔点:
沸点:
④ 均不溶于水,易溶于有机溶剂
气→液→固
气态
液态
固态
逐渐增大
逐渐增大
逐渐增大
(均小于1,小于水)
环节一 初识烷烃
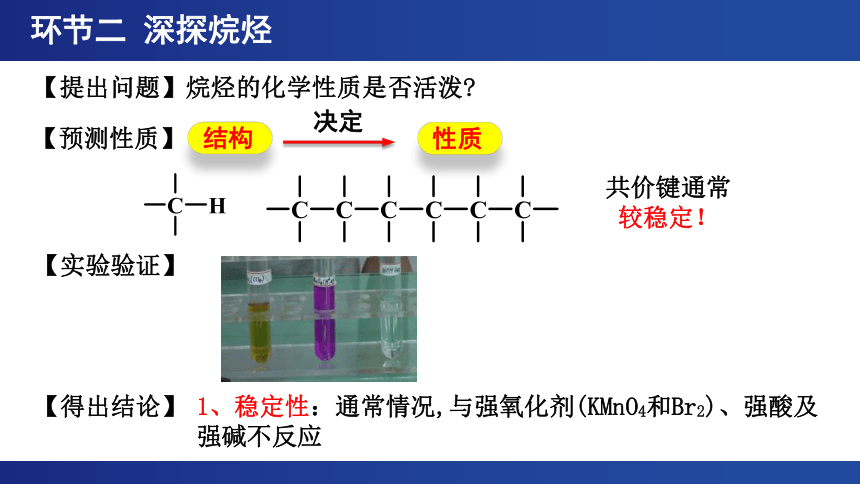
环节二 深探烷烃
【提出问题】烷烃的化学性质是否活泼
结构
决定
性质
【预测性质】
共价键通常
较稳定!
【实验验证】
【得出结论】
1、稳定性:通常情况,与强氧化剂(KMnO4和Br2)、强酸及强碱不反应
环节二 深探烷烃
【生活知识】煤矿中的爆炸事故多与甲烷气体爆炸有关。为了保证安全生产,必须采取通风、严禁烟火等措施。
2、可燃性: 可做燃料
CH4 + 2O2 CO2 + 2H2O
点燃
现象:放出大量的热,产生淡蓝色火焰
C3H8 + 5O2 3CO2 + 4H2O
点燃
注意: 点燃甲烷前必须验纯
否则会爆炸。
烷烃燃烧通式为:
CnH2n+2+(3n+1)/2O2 nCO2+(n+1)H2O
点燃
3.分解反应
烷烃在较高温度下会发生分解。
CH4 C + 2H2
高温
高温
应用于石油化工和天然气化工生产
从烷烃 → 化工基本原料和燃料
C18H38 C10H22 + C8H16
十八烷
癸烷
催化剂
加热、加压
C4H10 CH2== CH2 + CH3CH3
(乙烯)
制造颜料、油墨、油漆等
合成氨
环节二 深探烷烃
1883年法国巴黎王室一次舞会上,新买的巨大的蜡烛(含C、H)燃烧时,冒出一股刺鼻的气体,呛走了宾客。巴黎大学化学教授杜马在调查中发现,蜡烛是经氯气漂白过的,并发现了一个新的反应类型。
“蜡烛冒烟”事件
【提出问题】这是什么气体
HCl
【预测原因】
氯取代了蜡烛中的H
【实验验证】
环节二 深探烷烃
【实验7-1】
注意:暗处不反应 强光会爆炸
现象:
试管内黄绿色逐渐变浅
试管内液面上升
试管壁出现油状液滴
有少量白雾
Cl2发生反应
气体体积减小
生成难溶于水的物质
气体体积减小
实验探究
CH4 + Cl2 CH3Cl +HCl
光照
4.取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。
一上一下取而代之
一氯甲烷,沸点:-24.2℃
环节二 深探烷烃
H
C
H
Cl
Cl
H Cl
光
H
C
H
H
Cl
Cl Cl
+
+
H
C
Cl
Cl
Cl
H Cl
光
H
C
H
Cl
Cl
Cl Cl
+
+
Cl
C
Cl
Cl
Cl
H Cl
光
H
C
Cl
Cl
Cl
Cl Cl
+
+
二氯甲烷
三氯甲烷
氯仿
四氯化碳
四氯甲烷
液态
环节二 深探烷烃
环节二 深探烷烃
1、甲烷与氯气发生取代反应后产物可能有几种?
2、乙烷与氯气发生取代反应后产物可能有几种? 哪种产物最多?
5种 CH3Cl CH2Cl2 CHCl3 CCl4 HCl
7种 HCl一定是最多的
3、计算1mol甲烷与4mol氯气在光照条件下反应足够长时间后得到的产物的物质的量。
最终得到 1mol CCl4 和 4mol HCl
逐步取代
CH4分子中的H原子.
同时发生
反应不停留在某一步
得到混合物
氯化氢最多
【思考】
烷烃(以甲烷为例)发生取代反应的有关规律
(1)反应条件:反应条件为光照,其光照为漫射光,强光直射易发生爆炸。
(2)反应物:反应物为卤素单质,如甲烷与氯水、溴水不反应,但可以与氯气、溴蒸气发生取代反应。
(3)反应产物:虽然反应物的比例、反应的时间长短等因素会造成各种产物的比例不同,但甲烷与氯气反应生成的产物都是CH3Cl、CH2Cl2、CHCl3和CCl4四种有机物与HCl形成的混合物。反应产物中HCl的物质的量最多。
环节二 深探烷烃
【总结】
1.烃的概念:仅含碳和氢两种元素的有机化合物称为碳氢化合物,也称为烃。
2.烃的分类
烃
饱和烃(烷烃)
不饱和烃
链状烷烃
环状烷烃
烯烃
炔烃
芳香烃
甲烷CH4 乙烷CH3CH3
环己烷
乙烯CH2=CH2
乙炔CH≡CH
苯
环节三 总结烃
烷烃
物理性质
化学性质
难溶于水
熔点、沸点和密度随分子中碳原子数的增加而升高
气态→液态→固态
可燃性
热分解
取代反应
小结
稳定性
环节三 总结烃
同学们,再见
厨房中的有机物—烷烃
烷烃的存在
环节一 初识烷烃
天然气、沼气、煤层气 → 甲烷
环节一 初识烷烃
结合生活经验以及所学知识,想想烷烃可能有哪些性质。
烷烃的存在
蜡烛、蜡笔、凡士林 → 含碳原子数较多的烷烃
烷烃的物理性质
① 状态:
C原子数
1-4:
5-16:
17以上:
随碳原子个数的增加
③ 密度:
② 熔点:
沸点:
④ 均不溶于水,易溶于有机溶剂
气→液→固
气态
液态
固态
逐渐增大
逐渐增大
逐渐增大
(均小于1,小于水)
环节一 初识烷烃
环节二 深探烷烃
【提出问题】烷烃的化学性质是否活泼
结构
决定
性质
【预测性质】
共价键通常
较稳定!
【实验验证】
【得出结论】
1、稳定性:通常情况,与强氧化剂(KMnO4和Br2)、强酸及强碱不反应
环节二 深探烷烃
【生活知识】煤矿中的爆炸事故多与甲烷气体爆炸有关。为了保证安全生产,必须采取通风、严禁烟火等措施。
2、可燃性: 可做燃料
CH4 + 2O2 CO2 + 2H2O
点燃
现象:放出大量的热,产生淡蓝色火焰
C3H8 + 5O2 3CO2 + 4H2O
点燃
注意: 点燃甲烷前必须验纯
否则会爆炸。
烷烃燃烧通式为:
CnH2n+2+(3n+1)/2O2 nCO2+(n+1)H2O
点燃
3.分解反应
烷烃在较高温度下会发生分解。
CH4 C + 2H2
高温
高温
应用于石油化工和天然气化工生产
从烷烃 → 化工基本原料和燃料
C18H38 C10H22 + C8H16
十八烷
癸烷
催化剂
加热、加压
C4H10 CH2== CH2 + CH3CH3
(乙烯)
制造颜料、油墨、油漆等
合成氨
环节二 深探烷烃
1883年法国巴黎王室一次舞会上,新买的巨大的蜡烛(含C、H)燃烧时,冒出一股刺鼻的气体,呛走了宾客。巴黎大学化学教授杜马在调查中发现,蜡烛是经氯气漂白过的,并发现了一个新的反应类型。
“蜡烛冒烟”事件
【提出问题】这是什么气体
HCl
【预测原因】
氯取代了蜡烛中的H
【实验验证】
环节二 深探烷烃
【实验7-1】
注意:暗处不反应 强光会爆炸
现象:
试管内黄绿色逐渐变浅
试管内液面上升
试管壁出现油状液滴
有少量白雾
Cl2发生反应
气体体积减小
生成难溶于水的物质
气体体积减小
实验探究
CH4 + Cl2 CH3Cl +HCl
光照
4.取代反应:有机物分子里的某些原子或原子团被其他原子或原子团所代替的反应。
一上一下取而代之
一氯甲烷,沸点:-24.2℃
环节二 深探烷烃
H
C
H
Cl
Cl
H Cl
光
H
C
H
H
Cl
Cl Cl
+
+
H
C
Cl
Cl
Cl
H Cl
光
H
C
H
Cl
Cl
Cl Cl
+
+
Cl
C
Cl
Cl
Cl
H Cl
光
H
C
Cl
Cl
Cl
Cl Cl
+
+
二氯甲烷
三氯甲烷
氯仿
四氯化碳
四氯甲烷
液态
环节二 深探烷烃
环节二 深探烷烃
1、甲烷与氯气发生取代反应后产物可能有几种?
2、乙烷与氯气发生取代反应后产物可能有几种? 哪种产物最多?
5种 CH3Cl CH2Cl2 CHCl3 CCl4 HCl
7种 HCl一定是最多的
3、计算1mol甲烷与4mol氯气在光照条件下反应足够长时间后得到的产物的物质的量。
最终得到 1mol CCl4 和 4mol HCl
逐步取代
CH4分子中的H原子.
同时发生
反应不停留在某一步
得到混合物
氯化氢最多
【思考】
烷烃(以甲烷为例)发生取代反应的有关规律
(1)反应条件:反应条件为光照,其光照为漫射光,强光直射易发生爆炸。
(2)反应物:反应物为卤素单质,如甲烷与氯水、溴水不反应,但可以与氯气、溴蒸气发生取代反应。
(3)反应产物:虽然反应物的比例、反应的时间长短等因素会造成各种产物的比例不同,但甲烷与氯气反应生成的产物都是CH3Cl、CH2Cl2、CHCl3和CCl4四种有机物与HCl形成的混合物。反应产物中HCl的物质的量最多。
环节二 深探烷烃
【总结】
1.烃的概念:仅含碳和氢两种元素的有机化合物称为碳氢化合物,也称为烃。
2.烃的分类
烃
饱和烃(烷烃)
不饱和烃
链状烷烃
环状烷烃
烯烃
炔烃
芳香烃
甲烷CH4 乙烷CH3CH3
环己烷
乙烯CH2=CH2
乙炔CH≡CH
苯
环节三 总结烃
烷烃
物理性质
化学性质
难溶于水
熔点、沸点和密度随分子中碳原子数的增加而升高
气态→液态→固态
可燃性
热分解
取代反应
小结
稳定性
环节三 总结烃
同学们,再见
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
