第三节 醛 酮 课件(18张PPT)
文档属性
| 名称 | 第三节 醛 酮 课件(18张PPT) |  | |
| 格式 | pptx | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-17 18:49:54 | ||
图片预览


文档简介
(共18张PPT)
酮
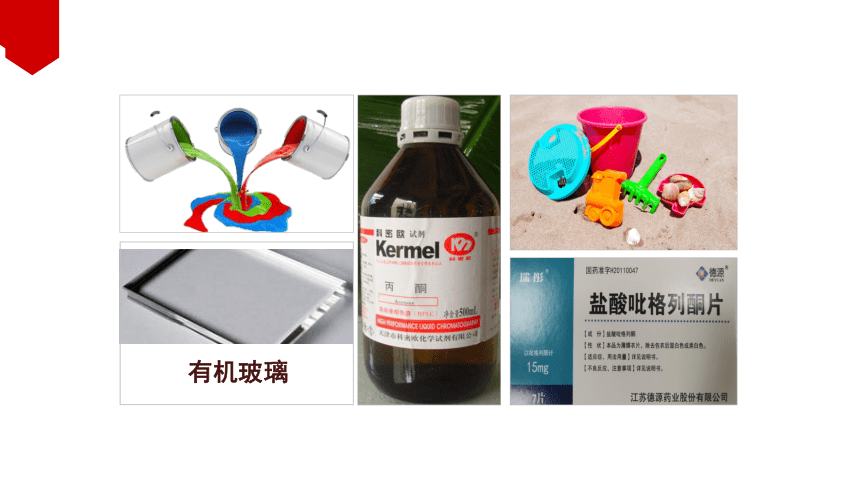
有机玻璃
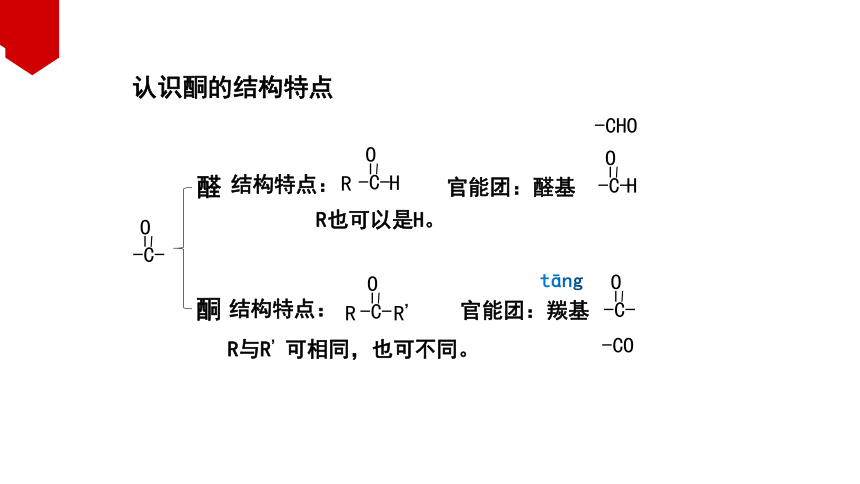
醛
结构特点:
酮
官能团:醛基
R与R’可相同,也可不同。
结构特点:
官能团:羰基
tāng
认识酮的结构特点
R也可以是H。
-C-
O
-C-
O
R
H
R
-C-
O
R’
-C-
O
H
-CHO
-C-
O
-CO
认识酮的结构特点
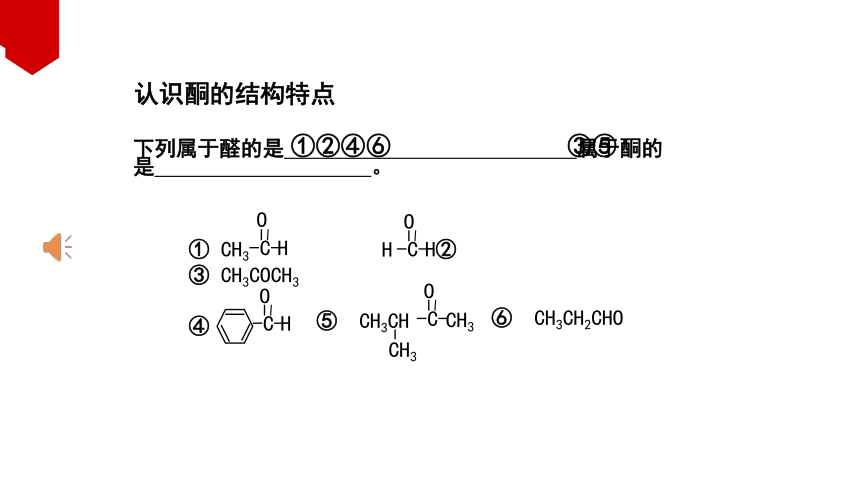
下列属于醛的是 属于酮的是 。
①②④⑥
③⑤
⑥ CH3CH2CHO
① CH3 ② ③ CH3COCH3
-C-
O
H
-C-
O
H
H
-C-
O
H
④
⑤ CH3CH
CH3
-C-
O
CH3
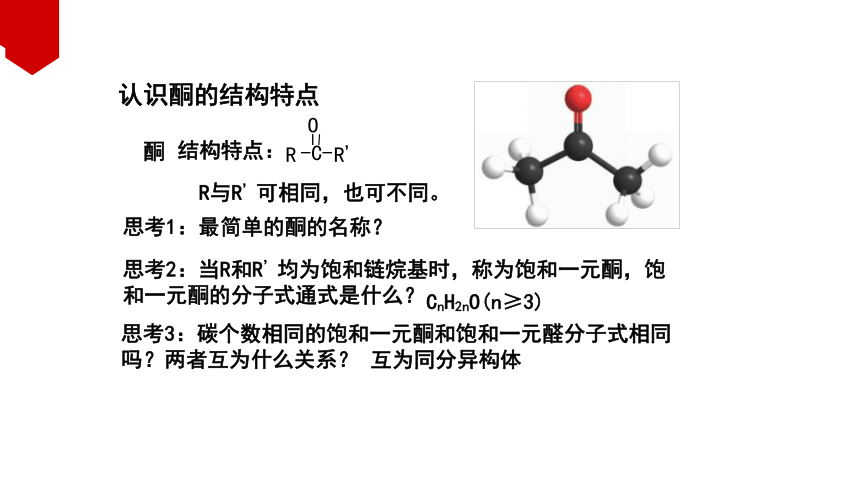
认识酮的结构特点
思考1:最简单的酮的名称?
思考2:当R和R’均为饱和链烷基时,称为饱和一元酮,饱和一元酮的分子式通式是什么?
思考3:碳个数相同的饱和一元酮和饱和一元醛分子式相同吗?两者互为什么关系?
酮
R与R’可相同,也可不同。
结构特点:
CnH2nO(n≥3)
互为同分异构体
R
-C-
O
R’
实验一:打开试剂瓶塞用扇闻法闻一闻丙酮的气味,取4mL丙酮于试管,观察。分装在两支试管中,分别加入2mL水和2mL乙醇观察。(温馨提示:由于丙酮蒸气有毒,应在通风环境或通风橱进行实验)
一、丙酮的物理性质
无色透明的液体,有特殊气味,与水、乙醇等互溶。
思考4:为什么丙烷难溶于水 ,而丙酮能与水互溶呢?
丙酮羰基上的氧与水分子中的氢形成氢键,
增加了丙酮在水中的溶解度。
H
H
O
“裸露”的H
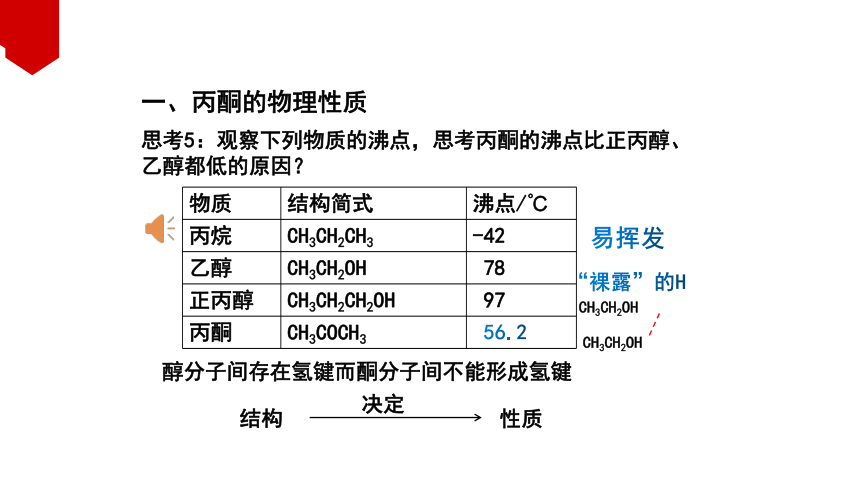
思考5:观察下列物质的沸点,思考丙酮的沸点比正丙醇、乙醇都低的原因?
易挥发
醇分子间存在氢键而酮分子间不能形成氢键
物质 结构简式 沸点/℃
丙烷 CH3CH2CH3 -42
乙醇 CH3CH2OH 78
正丙醇 CH3CH2CH2OH 97
丙酮 CH3COCH3 56.2
一、丙酮的物理性质
CH3CH2OH
CH3CH2OH
“裸露”的H
决定
结构 性质
二、丙酮的化学性质
实验二:在洁净的试管里加入2mL2%AgNO3溶液,边振荡试管边逐滴滴2%氨水,使最初产生的沉淀溶解,制得银氨溶液,再滴入5滴丙酮,热水浴加热。观察实验现象。
试从结构上分析,乙醛能和银氨反应而丙酮不能的原因。
现象:无明显现象
结论:丙酮不能被银氨溶液或新制Cu(OH)2等弱氧化剂氧化。
-C—
O
R
H
-C C-
-C-
O
O
根据酮的官能团,推测酮的性质
不饱和
易加成
结论:酮和烯烃、炔烃、苯环及醛都能和H2在镍作催化剂下发生加成,也叫还原反应。
二、丙酮的化学性质
-C-
O
(2—丙醇)
Ni
CH3CHCH3
OH
+H2
根据酮的官能团,推测酮的性质
δ-
δ+
羰基中,由于氧原子的电负性较大,吸电子能力较强,使羰基具有较强的极性。丙酮也能和一些极性试剂发生加成反应。
二、丙酮的化学性质
-C-
O
根据酮的官能团,推测酮的性质
当极性分子与羰基发生加成反应时,
带正电荷的原子或原子团连接在 上,
带负电荷的原子或原子团连接在 上。
δ-
+ H-CN
δ+
二、丙酮的化学性质
羰基的氧原子
羰基的碳原子
CH3CCH3
O
+H-CN
CH3CCH3
OH
CN
C=O
δ-
δ+
+ H-CN
δ-
δ+
写出丙酮和NH3反应的化学方程式
二、丙酮的化学性质
H-NH2
CH3CCH3
O
+H-NH2
CH3CCH3
OH
NH2
C=O
δ-
δ+
构建学习有机物的一般思路
确定
分子式
确定
结构式
研究典型
代表物的性质
结构分析
实验探究
一类物质的性质
推广
实验法+现代仪器法
反映
决定
结构 性质
(官能团)
银氨溶液或新制Cu(OH)2溶液
学以致用
你有哪些方法鉴别丙醛和丙酮?
思考6:丙酮能作涂料、用于生产有机玻璃的原因?
酮的用途1 —— 有机溶剂
指甲油难溶于水,洗甲水可以轻松地洗去指甲油,洗甲水的主要成份是丙酮。
丙酮是一种很好的有机溶剂,工业上丙酮可用作化学纤维、钢瓶储存乙炔等的溶剂。
乙炔气瓶内装有浸入丙酮的多孔填料,使乙炔能安全地储存在瓶内。
还能用于生产农药和涂料。
有机玻璃是甲基丙烯酸甲酯通过加聚反应制得的,丙酮是制备有机玻璃单体的原料。
有机玻璃又可以用来制造学生用的直尺、三角绘图尺、电风扇的扇片等。
CH3CCH3
O
HCN
CH3CCH3
OH
CN
CH3OH
H2SO4
CH2=C-C-OCH3
CH3
O
酮的用途2 —— 化工原料
拓展视野
蜜蜂传递警戒信息的激素含有2-庚酮( )。
它是昆虫之间进行化学通信的物质之一。
O
课堂小结
酮( )
代表物:丙酮( )
官能团( )
性质
决定
反映
物理性质
(颜色、状态、熔沸点、溶解性等 )
化学性质
与H2加成生成醇
(也叫还原反应)
与极性分子加成(正负电荷作用形成新键,如和HCN、NH3等加成)
决定用途
学化学 用化学 爱化学
CH3CCH3
O
R
-C-
O
R’
-C-
O
有机溶剂
化工原料
酮
有机玻璃
醛
结构特点:
酮
官能团:醛基
R与R’可相同,也可不同。
结构特点:
官能团:羰基
tāng
认识酮的结构特点
R也可以是H。
-C-
O
-C-
O
R
H
R
-C-
O
R’
-C-
O
H
-CHO
-C-
O
-CO
认识酮的结构特点
下列属于醛的是 属于酮的是 。
①②④⑥
③⑤
⑥ CH3CH2CHO
① CH3 ② ③ CH3COCH3
-C-
O
H
-C-
O
H
H
-C-
O
H
④
⑤ CH3CH
CH3
-C-
O
CH3
认识酮的结构特点
思考1:最简单的酮的名称?
思考2:当R和R’均为饱和链烷基时,称为饱和一元酮,饱和一元酮的分子式通式是什么?
思考3:碳个数相同的饱和一元酮和饱和一元醛分子式相同吗?两者互为什么关系?
酮
R与R’可相同,也可不同。
结构特点:
CnH2nO(n≥3)
互为同分异构体
R
-C-
O
R’
实验一:打开试剂瓶塞用扇闻法闻一闻丙酮的气味,取4mL丙酮于试管,观察。分装在两支试管中,分别加入2mL水和2mL乙醇观察。(温馨提示:由于丙酮蒸气有毒,应在通风环境或通风橱进行实验)
一、丙酮的物理性质
无色透明的液体,有特殊气味,与水、乙醇等互溶。
思考4:为什么丙烷难溶于水 ,而丙酮能与水互溶呢?
丙酮羰基上的氧与水分子中的氢形成氢键,
增加了丙酮在水中的溶解度。
H
H
O
“裸露”的H
思考5:观察下列物质的沸点,思考丙酮的沸点比正丙醇、乙醇都低的原因?
易挥发
醇分子间存在氢键而酮分子间不能形成氢键
物质 结构简式 沸点/℃
丙烷 CH3CH2CH3 -42
乙醇 CH3CH2OH 78
正丙醇 CH3CH2CH2OH 97
丙酮 CH3COCH3 56.2
一、丙酮的物理性质
CH3CH2OH
CH3CH2OH
“裸露”的H
决定
结构 性质
二、丙酮的化学性质
实验二:在洁净的试管里加入2mL2%AgNO3溶液,边振荡试管边逐滴滴2%氨水,使最初产生的沉淀溶解,制得银氨溶液,再滴入5滴丙酮,热水浴加热。观察实验现象。
试从结构上分析,乙醛能和银氨反应而丙酮不能的原因。
现象:无明显现象
结论:丙酮不能被银氨溶液或新制Cu(OH)2等弱氧化剂氧化。
-C—
O
R
H
-C C-
-C-
O
O
根据酮的官能团,推测酮的性质
不饱和
易加成
结论:酮和烯烃、炔烃、苯环及醛都能和H2在镍作催化剂下发生加成,也叫还原反应。
二、丙酮的化学性质
-C-
O
(2—丙醇)
Ni
CH3CHCH3
OH
+H2
根据酮的官能团,推测酮的性质
δ-
δ+
羰基中,由于氧原子的电负性较大,吸电子能力较强,使羰基具有较强的极性。丙酮也能和一些极性试剂发生加成反应。
二、丙酮的化学性质
-C-
O
根据酮的官能团,推测酮的性质
当极性分子与羰基发生加成反应时,
带正电荷的原子或原子团连接在 上,
带负电荷的原子或原子团连接在 上。
δ-
+ H-CN
δ+
二、丙酮的化学性质
羰基的氧原子
羰基的碳原子
CH3CCH3
O
+H-CN
CH3CCH3
OH
CN
C=O
δ-
δ+
+ H-CN
δ-
δ+
写出丙酮和NH3反应的化学方程式
二、丙酮的化学性质
H-NH2
CH3CCH3
O
+H-NH2
CH3CCH3
OH
NH2
C=O
δ-
δ+
构建学习有机物的一般思路
确定
分子式
确定
结构式
研究典型
代表物的性质
结构分析
实验探究
一类物质的性质
推广
实验法+现代仪器法
反映
决定
结构 性质
(官能团)
银氨溶液或新制Cu(OH)2溶液
学以致用
你有哪些方法鉴别丙醛和丙酮?
思考6:丙酮能作涂料、用于生产有机玻璃的原因?
酮的用途1 —— 有机溶剂
指甲油难溶于水,洗甲水可以轻松地洗去指甲油,洗甲水的主要成份是丙酮。
丙酮是一种很好的有机溶剂,工业上丙酮可用作化学纤维、钢瓶储存乙炔等的溶剂。
乙炔气瓶内装有浸入丙酮的多孔填料,使乙炔能安全地储存在瓶内。
还能用于生产农药和涂料。
有机玻璃是甲基丙烯酸甲酯通过加聚反应制得的,丙酮是制备有机玻璃单体的原料。
有机玻璃又可以用来制造学生用的直尺、三角绘图尺、电风扇的扇片等。
CH3CCH3
O
HCN
CH3CCH3
OH
CN
CH3OH
H2SO4
CH2=C-C-OCH3
CH3
O
酮的用途2 —— 化工原料
拓展视野
蜜蜂传递警戒信息的激素含有2-庚酮( )。
它是昆虫之间进行化学通信的物质之一。
O
课堂小结
酮( )
代表物:丙酮( )
官能团( )
性质
决定
反映
物理性质
(颜色、状态、熔沸点、溶解性等 )
化学性质
与H2加成生成醇
(也叫还原反应)
与极性分子加成(正负电荷作用形成新键,如和HCN、NH3等加成)
决定用途
学化学 用化学 爱化学
CH3CCH3
O
R
-C-
O
R’
-C-
O
有机溶剂
化工原料
