高二化学选修5第三章第二节 醛(共49张PPT)
文档属性
| 名称 | 高二化学选修5第三章第二节 醛(共49张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-10-26 00:00:00 | ||
图片预览







文档简介
课件49张PPT。第三章 烃的含氧衍生物第二节 醛第一课时 乙醛顺德华侨中学
陈焕龙人喝酒后会产生恶心呕吐、昏迷不适等醉酒症状。你知道吗?乙醛的毒性是乙醇的10倍。高浓度
乙醛有麻醉作用,使体内某些反应
停止,部分组织坏死,从而令人头晕
头痛、嗜睡昏迷, 伤及肝脏、心脑血
管及脑神经系统。是乙醇在体内氧化后的产物乙醛!你知道酒精中毒的罪魁祸首是什么吗?写出乙醇催化氧化成乙醛的化学方程式乙醛乙醛是一种____色,有刺激性气味
的____体,密度比水____,易挥发、
易燃烧、易溶于水及乙醇、乙醚、
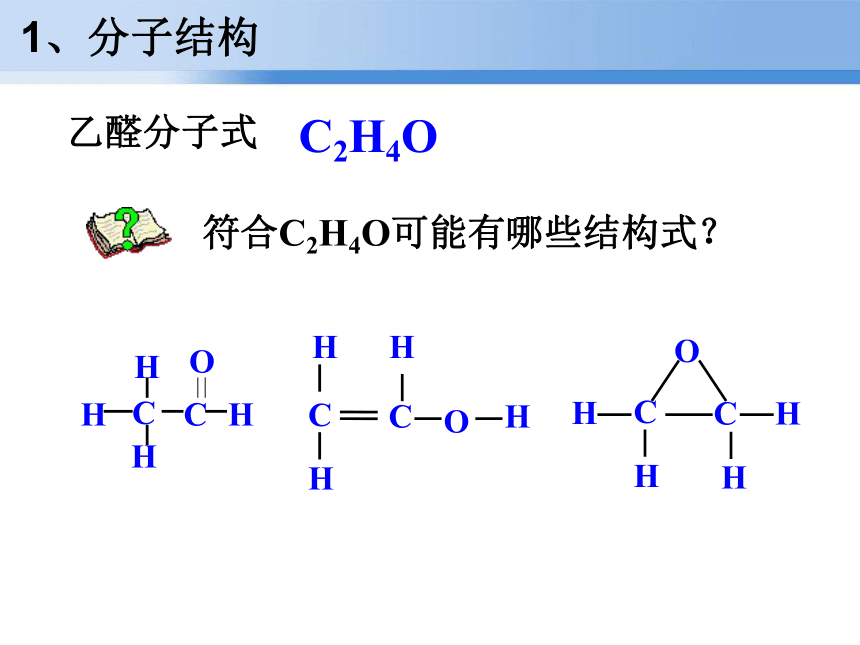
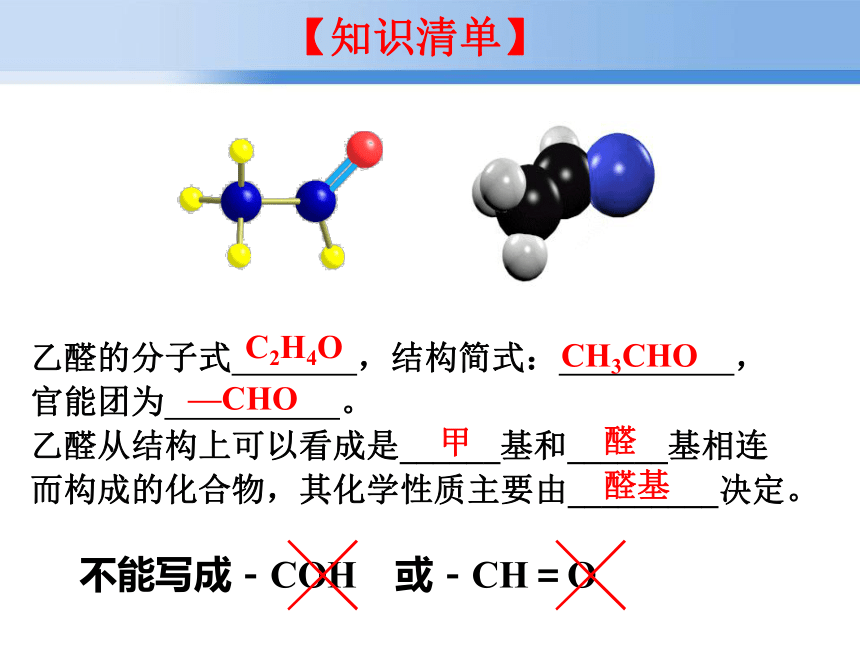
氯仿等溶剂。乙醛无液小【知识清单】乙醛、苯、CCl4均为无色液体,如何用最简便的方法鉴别?乙醛分子式符合C2H4O可能有哪些结构式?C2H4O1、分子结构乙醛的核磁共振氢谱图—CHO—CH3乙醛的分子式 ,结构简式: ,
官能团为 。
乙醛从结构上可以看成是______基和______基相连
而构成的化合物,其化学性质主要由_________决定。C2H4OCH3CHO甲醛醛基【知识清单】不能写成-COH 或-CH=O╳ ╳—CHO由烃基跟醛基相连而构成的化合物醛苯甲醛肉桂醛 H O
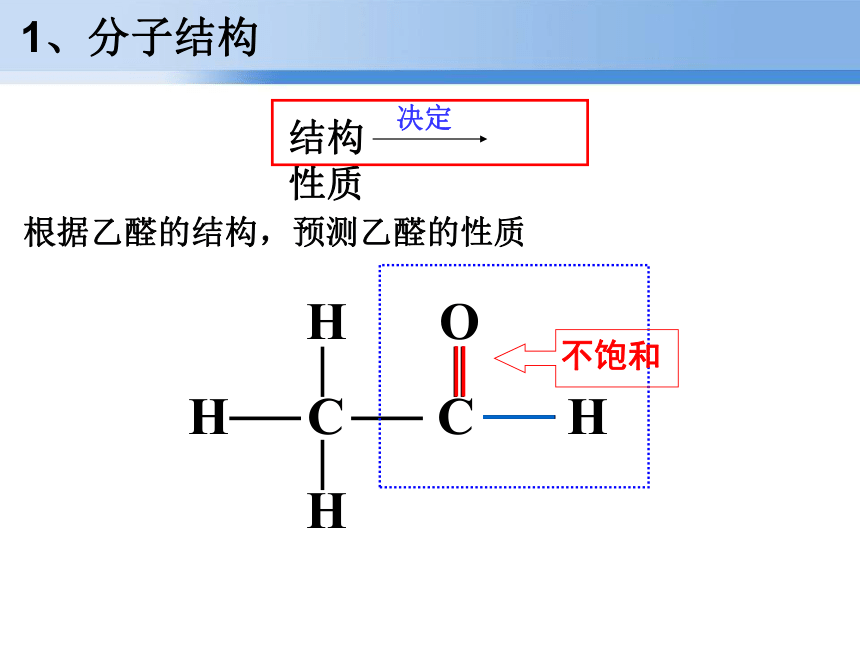
H C C H
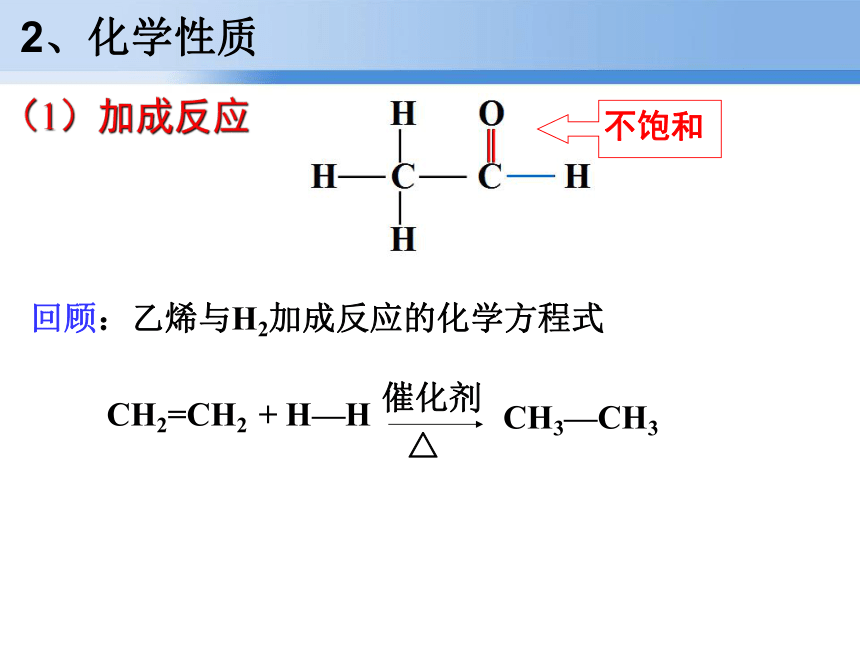
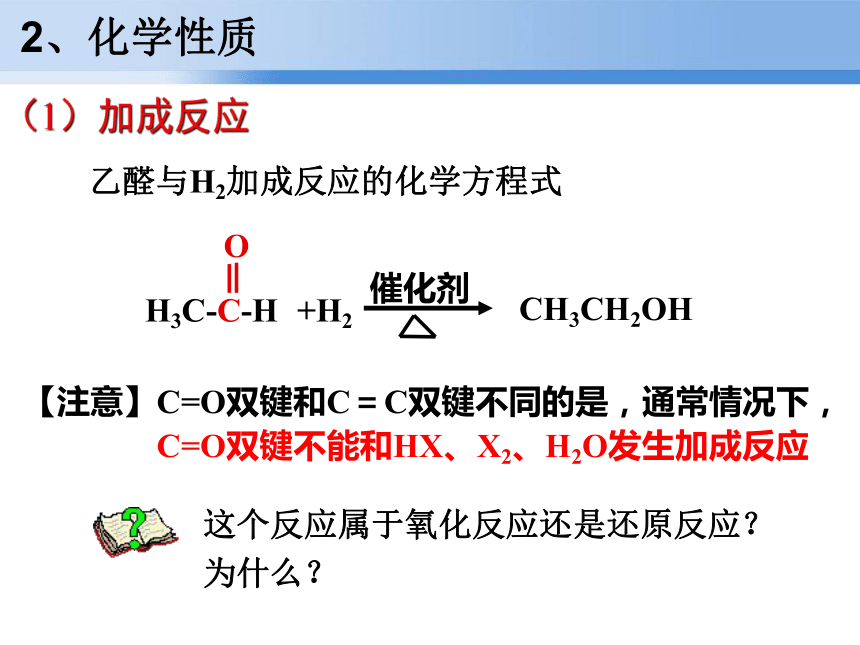
H 根据乙醛的结构,预测乙醛的性质1、分子结构(1)加成反应2、化学性质回顾:乙烯与H2加成反应的化学方程式 乙醛与H2加成反应的化学方程式 2、化学性质(1)加成反应【注意】C=O双键和C=C双键不同的是,通常情况下,
C=O双键不能和HX、X2、H2O发生加成反应这个反应属于氧化反应还是还原反应?为什么? 对于有机反应中的氧化反应和还原反应,我们应该怎样判断呢?氧化反应: 有机物分子中加入氧原子或
失去氢原子的反应还原反应: 有机物分子中加入氢原子或
失去氧原子的反应2、化学性质得氢失氧被还原,得氧失氢被氧化练习、下列反应中,有机物发生氧化反应的是( )A、B、C、D、D得氢失氧被还原,得氧失氢被氧化(2)乙醛的氧化反应(I)催化氧化2、化学性质(2)乙醛的氧化反应(I)催化氧化工业制乙酸2、化学性质2、化学性质(2)乙醛的氧化反应(II)燃烧(III)被弱氧化剂氧化银氨溶液、新制Cu(OH)2悬浊液2 5 4 4醛基葡萄糖的结构简式CH2OH (CHOH)4CHO 与银氨溶液反应:与新制Cu(OH)2反应:CH3CHO是否也能发生类似的反应?2、化学性质2、化学性质(ⅰ)银镜反应①制备银氨溶液AgNO3 + NH3·H2O = AgOH↓+ NH4NO3AgOH + 2NH3·H2O = Ag(NH3)2OH + 2H2O(氢氧化二氨合银)2、化学性质现象:试管内壁出现一层光亮的银②实验过程2、化学性质③作用a、检验醛基的存在b、定量测定醛基的个数1mol–CHO被氧化,就应有2molAg被还原2、化学性质(5)用稀HNO3清洗试管内壁的银镜。④注意事项(1)试管内壁必须洁净;(2)银氨溶液要现配现用;(4)加热过程中不能摇动试管;(3)碱性环境,水浴加热;2、化学性质(ⅱ)与新制Cu(OH)2悬浊液反应 ①新制Cu(OH)2悬浊液的配制 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 在试管里加入10%的NaOH溶液2mL,滴入2%的CuSO4溶液4~6滴。2、化学性质②实验过程现象:试管内有砖红色沉淀产生△△2、化学性质③作用a、检验醛基的存在b、定量测定醛基的个数1mol–CHO被氧化,就应有2molCu被还原2、化学性质④注意事项(1) Cu(OH)2悬浊液必须是新制的;(2)碱性环境,直接加热。两个反应的共同点:
1、均在碱性环境中进行。
2、可用于鉴定-CHO的存在。
3、-CHO与Ag(NH3)2OH或 Cu(OH)2均以
物质的量比1:2反应。【归纳】2、化学性质【小结】 在碱性条件下,乙醛能发生 反应,也能被
新制的氢氧化铜 ,首先生成 , 最后与碱反
应生成 。
这两个反应是醛类物质的特征反应。氧化银镜乙酸乙酸盐醛基的检验方法:(1)与新制的银氨溶液反应有光亮的银镜生成;
(2)与新制的Cu(OH)2共热煮沸有砖红色沉淀生成。【练习】分别写出丙醛与下列物质反应的化学方程式
1、与银氨溶液反应
2、与新制氢氧化铜悬浊液反应
3、与氢气反应能 乙醛能被弱氧化剂(银氨溶液等)氧化,否使溴水、酸性KMnO4、重铬酸钾溶液褪色?①工业上,利用银镜反应来制镜或保温瓶胆。3、应用②医学上,利用菲林试剂来检验病人是否患糖尿病。③乙醛是有机合成工业中的重要原料,主要用来生产
乙酸、乙醇、乙酸乙酯等。乙醛乙酸乙醇( )【课堂小结】( )( )失H氧化得O氧化得H还原醛既有氧化性,又有还原性C—HC=O【巩固练习】1.某学生做乙醛还原性的实验,取l mol/L的硫酸铜
溶液2 mL和0.4mol/L的氢氧化钠溶液 4mL,混合后
加入0.5 mL 40%的乙醛溶液加热至沸腾,无红色沉淀,
实验失败的原因是( )
A. 氧氧化钠的量不够 B. 硫酸铜不够量
C. 乙醛溶液太少 D. 加热时间不够A【巩固练习】2.洗涤做过银镜反应的试管可以选用的试剂是( )
A.氨水 B.NaOH溶液 C.稀硝酸 D.酒精3.关于丙烯醛(CH2=CH-CHO)的叙述不正确的是( )
A.可使溴水和KMnO4溶液褪色
B.与足量的H2加成生成丙醛
C.能发生银镜反应
D.在一定条件下可氧化成酸CB【巩固练习】4.关于乙醛的下列反应中,乙醛被还原的是( )
A.乙醛的银镜反应
B.乙醛制乙醇
C.乙醛与新制氢氧化铜的反应
D.乙醛的燃烧反应B【巩固练习】5.下列物质中不能发生银镜反应的是( )
A. B.CH3CHO
C.葡萄糖
D.D【巩固练习】6.橙花醛是一种香料,其结构简式为
(CH3)2C=CHCH2CH2C(CH3) =CHCHO
下列说法正确的是( )
A.橙花醛不能与Br2发生加成反应
B.橙花醛能发生银镜反应
C.1 mol橙花醛最多可以与2 mol H2发生加成反应
D.橙花醛是乙烯的同系物B【交流2】
乙醛能使溴水或酸性KMnO4溶液褪色吗?为什么? 能。被氧化;
CH3CHO+Br2+H2O CH3COOH+2HBr
【讨论】
与新制Cu(OH)2反应产生砖红色沉淀以及发生银镜反应是醛基的典型性质,通常用于醛基的检验,能否说发生上述两反应的有机化合物一定是醛类?不一定。能发生上述两反应的有机物分子中含醛基,但不一定是醛。例:甲酸、甲酸某酯、甲酸盐、葡萄糖、麦芽糖等都能发生银镜反应。【小结】醛的化学性质
(1)醛的基本性质。
醛基既具有还原性,又具有氧化性,可以发生氧化反应和还原反应。
① —CHO 中的C—H键可断裂,发生氧化反应,生成羧酸;例如:
2R—CHO+O2 2RCOOH,
醛也可被酸性KMnO4溶液等强氧化剂氧化。
②RCHO均可与银氨溶液、新制Cu(OH)2悬浊液反应
③ —CHO 含有碳氧双键,可以与H2等发生加成反应(还原反应),生成相应的醇。
例如:
反应生成羧酸铵,还有一水二银三个氨【讨论】
2.能使溴水和酸性KMnO4溶液褪色的有机物
某醛的结构简式为 :
(1)检验分子中醛基的方法是?_______;
检验 的方法是 ? 。?
(2)实际操作中,哪一种官能团应先检验?
(1)加入银氨溶液水浴加热,若有银镜出现则含—CHO
先加入足量银氨溶液水浴加热 ,充分反应后取反应液少量,用硝酸酸化后再加入溴水,若溴水褪色则含 (2)先检验-CHO,再检验B.加成反应同时也是还原反应还原反应:加氢或失氧氧化反应:加氧或失氢有机的氧化
还原反应乙醛性质的小结:1、氧化反应a 燃烧b 催化氧化c 被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)乙酸d 被强氧化剂氧化
(酸性高锰酸钾溶液)2. 分子结构:一、乙醛或CH3CHO结构式结构简式分子式:C2H4O官能团:二.乙醛的化学性质。
①氧化反应
a.乙醛与银氨溶液反应
b.乙醛与新制Cu(OH)2悬浊液反应
【还能被O2、KMnO4、K2Cr2O4等强氧化剂氧化】【实验3-5】【实验3-6】乙醇乙醛乙酸CO2+H2OCH2=CH2 + Br-Br催化剂
△CH2Br-CH2Br乙烯的加成反应
陈焕龙人喝酒后会产生恶心呕吐、昏迷不适等醉酒症状。你知道吗?乙醛的毒性是乙醇的10倍。高浓度
乙醛有麻醉作用,使体内某些反应
停止,部分组织坏死,从而令人头晕
头痛、嗜睡昏迷, 伤及肝脏、心脑血
管及脑神经系统。是乙醇在体内氧化后的产物乙醛!你知道酒精中毒的罪魁祸首是什么吗?写出乙醇催化氧化成乙醛的化学方程式乙醛乙醛是一种____色,有刺激性气味
的____体,密度比水____,易挥发、
易燃烧、易溶于水及乙醇、乙醚、
氯仿等溶剂。乙醛无液小【知识清单】乙醛、苯、CCl4均为无色液体,如何用最简便的方法鉴别?乙醛分子式符合C2H4O可能有哪些结构式?C2H4O1、分子结构乙醛的核磁共振氢谱图—CHO—CH3乙醛的分子式 ,结构简式: ,
官能团为 。
乙醛从结构上可以看成是______基和______基相连
而构成的化合物,其化学性质主要由_________决定。C2H4OCH3CHO甲醛醛基【知识清单】不能写成-COH 或-CH=O╳ ╳—CHO由烃基跟醛基相连而构成的化合物醛苯甲醛肉桂醛 H O
H C C H
H 根据乙醛的结构,预测乙醛的性质1、分子结构(1)加成反应2、化学性质回顾:乙烯与H2加成反应的化学方程式 乙醛与H2加成反应的化学方程式 2、化学性质(1)加成反应【注意】C=O双键和C=C双键不同的是,通常情况下,
C=O双键不能和HX、X2、H2O发生加成反应这个反应属于氧化反应还是还原反应?为什么? 对于有机反应中的氧化反应和还原反应,我们应该怎样判断呢?氧化反应: 有机物分子中加入氧原子或
失去氢原子的反应还原反应: 有机物分子中加入氢原子或
失去氧原子的反应2、化学性质得氢失氧被还原,得氧失氢被氧化练习、下列反应中,有机物发生氧化反应的是( )A、B、C、D、D得氢失氧被还原,得氧失氢被氧化(2)乙醛的氧化反应(I)催化氧化2、化学性质(2)乙醛的氧化反应(I)催化氧化工业制乙酸2、化学性质2、化学性质(2)乙醛的氧化反应(II)燃烧(III)被弱氧化剂氧化银氨溶液、新制Cu(OH)2悬浊液2 5 4 4醛基葡萄糖的结构简式CH2OH (CHOH)4CHO 与银氨溶液反应:与新制Cu(OH)2反应:CH3CHO是否也能发生类似的反应?2、化学性质2、化学性质(ⅰ)银镜反应①制备银氨溶液AgNO3 + NH3·H2O = AgOH↓+ NH4NO3AgOH + 2NH3·H2O = Ag(NH3)2OH + 2H2O(氢氧化二氨合银)2、化学性质现象:试管内壁出现一层光亮的银②实验过程2、化学性质③作用a、检验醛基的存在b、定量测定醛基的个数1mol–CHO被氧化,就应有2molAg被还原2、化学性质(5)用稀HNO3清洗试管内壁的银镜。④注意事项(1)试管内壁必须洁净;(2)银氨溶液要现配现用;(4)加热过程中不能摇动试管;(3)碱性环境,水浴加热;2、化学性质(ⅱ)与新制Cu(OH)2悬浊液反应 ①新制Cu(OH)2悬浊液的配制 2NaOH+CuSO4=Cu(OH)2↓+Na2SO4 在试管里加入10%的NaOH溶液2mL,滴入2%的CuSO4溶液4~6滴。2、化学性质②实验过程现象:试管内有砖红色沉淀产生△△2、化学性质③作用a、检验醛基的存在b、定量测定醛基的个数1mol–CHO被氧化,就应有2molCu被还原2、化学性质④注意事项(1) Cu(OH)2悬浊液必须是新制的;(2)碱性环境,直接加热。两个反应的共同点:
1、均在碱性环境中进行。
2、可用于鉴定-CHO的存在。
3、-CHO与Ag(NH3)2OH或 Cu(OH)2均以
物质的量比1:2反应。【归纳】2、化学性质【小结】 在碱性条件下,乙醛能发生 反应,也能被
新制的氢氧化铜 ,首先生成 , 最后与碱反
应生成 。
这两个反应是醛类物质的特征反应。氧化银镜乙酸乙酸盐醛基的检验方法:(1)与新制的银氨溶液反应有光亮的银镜生成;
(2)与新制的Cu(OH)2共热煮沸有砖红色沉淀生成。【练习】分别写出丙醛与下列物质反应的化学方程式
1、与银氨溶液反应
2、与新制氢氧化铜悬浊液反应
3、与氢气反应能 乙醛能被弱氧化剂(银氨溶液等)氧化,否使溴水、酸性KMnO4、重铬酸钾溶液褪色?①工业上,利用银镜反应来制镜或保温瓶胆。3、应用②医学上,利用菲林试剂来检验病人是否患糖尿病。③乙醛是有机合成工业中的重要原料,主要用来生产
乙酸、乙醇、乙酸乙酯等。乙醛乙酸乙醇( )【课堂小结】( )( )失H氧化得O氧化得H还原醛既有氧化性,又有还原性C—HC=O【巩固练习】1.某学生做乙醛还原性的实验,取l mol/L的硫酸铜
溶液2 mL和0.4mol/L的氢氧化钠溶液 4mL,混合后
加入0.5 mL 40%的乙醛溶液加热至沸腾,无红色沉淀,
实验失败的原因是( )
A. 氧氧化钠的量不够 B. 硫酸铜不够量
C. 乙醛溶液太少 D. 加热时间不够A【巩固练习】2.洗涤做过银镜反应的试管可以选用的试剂是( )
A.氨水 B.NaOH溶液 C.稀硝酸 D.酒精3.关于丙烯醛(CH2=CH-CHO)的叙述不正确的是( )
A.可使溴水和KMnO4溶液褪色
B.与足量的H2加成生成丙醛
C.能发生银镜反应
D.在一定条件下可氧化成酸CB【巩固练习】4.关于乙醛的下列反应中,乙醛被还原的是( )
A.乙醛的银镜反应
B.乙醛制乙醇
C.乙醛与新制氢氧化铜的反应
D.乙醛的燃烧反应B【巩固练习】5.下列物质中不能发生银镜反应的是( )
A. B.CH3CHO
C.葡萄糖
D.D【巩固练习】6.橙花醛是一种香料,其结构简式为
(CH3)2C=CHCH2CH2C(CH3) =CHCHO
下列说法正确的是( )
A.橙花醛不能与Br2发生加成反应
B.橙花醛能发生银镜反应
C.1 mol橙花醛最多可以与2 mol H2发生加成反应
D.橙花醛是乙烯的同系物B【交流2】
乙醛能使溴水或酸性KMnO4溶液褪色吗?为什么? 能。被氧化;
CH3CHO+Br2+H2O CH3COOH+2HBr
【讨论】
与新制Cu(OH)2反应产生砖红色沉淀以及发生银镜反应是醛基的典型性质,通常用于醛基的检验,能否说发生上述两反应的有机化合物一定是醛类?不一定。能发生上述两反应的有机物分子中含醛基,但不一定是醛。例:甲酸、甲酸某酯、甲酸盐、葡萄糖、麦芽糖等都能发生银镜反应。【小结】醛的化学性质
(1)醛的基本性质。
醛基既具有还原性,又具有氧化性,可以发生氧化反应和还原反应。
① —CHO 中的C—H键可断裂,发生氧化反应,生成羧酸;例如:
2R—CHO+O2 2RCOOH,
醛也可被酸性KMnO4溶液等强氧化剂氧化。
②RCHO均可与银氨溶液、新制Cu(OH)2悬浊液反应
③ —CHO 含有碳氧双键,可以与H2等发生加成反应(还原反应),生成相应的醇。
例如:
反应生成羧酸铵,还有一水二银三个氨【讨论】
2.能使溴水和酸性KMnO4溶液褪色的有机物
某醛的结构简式为 :
(1)检验分子中醛基的方法是?_______;
检验 的方法是 ? 。?
(2)实际操作中,哪一种官能团应先检验?
(1)加入银氨溶液水浴加热,若有银镜出现则含—CHO
先加入足量银氨溶液水浴加热 ,充分反应后取反应液少量,用硝酸酸化后再加入溴水,若溴水褪色则含 (2)先检验-CHO,再检验B.加成反应同时也是还原反应还原反应:加氢或失氧氧化反应:加氧或失氢有机的氧化
还原反应乙醛性质的小结:1、氧化反应a 燃烧b 催化氧化c 被弱氧化剂氧化
(银氨溶液、新制的Cu(OH)2)乙酸d 被强氧化剂氧化
(酸性高锰酸钾溶液)2. 分子结构:一、乙醛或CH3CHO结构式结构简式分子式:C2H4O官能团:二.乙醛的化学性质。
①氧化反应
a.乙醛与银氨溶液反应
b.乙醛与新制Cu(OH)2悬浊液反应
【还能被O2、KMnO4、K2Cr2O4等强氧化剂氧化】【实验3-5】【实验3-6】乙醇乙醛乙酸CO2+H2OCH2=CH2 + Br-Br催化剂
△CH2Br-CH2Br乙烯的加成反应
