4.1原子结构(共19张ppt)化学人教版(2019)必修第一册
文档属性
| 名称 | 4.1原子结构(共19张ppt)化学人教版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 71.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-18 00:00:00 | ||
图片预览


文档简介
(共19张PPT)
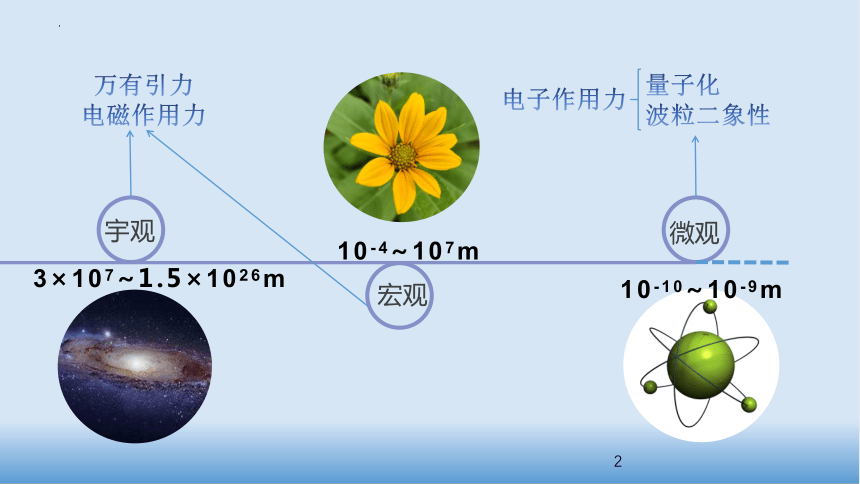
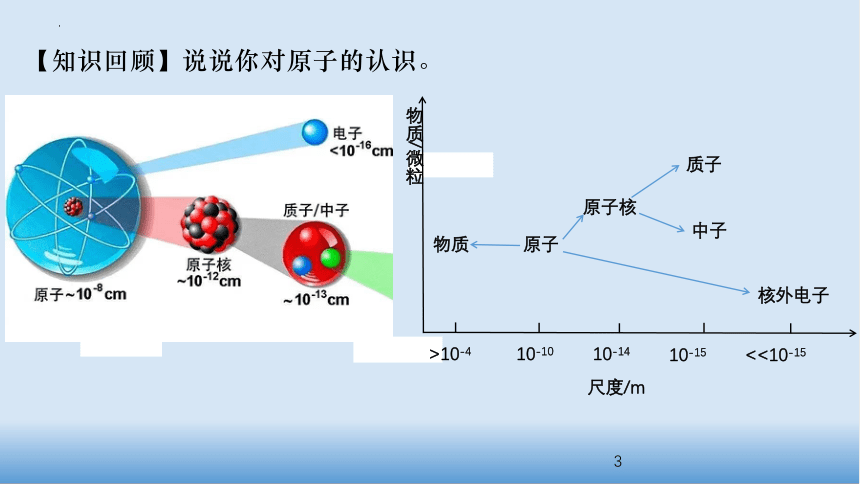
第一节 原子结构与元素周期表第四章 物质结构 元素周期律第一课时 原子结构宇观微观宏观3×107~1.5×1026m10-4~107m10-10~10-9m万有引力电磁作用力量子化波粒二象性电子作用力【知识回顾】说说你对原子的认识。物质原子原子核质子中子核外电子物质/微粒>10-410-1010-1410-15<<10-15尺度/m1个质子带一个单位正电荷1个电子带一个单位负电荷中子不带电质子、中子、电子的电性和电量怎样?原子的核电荷数=核外电子数=核内质子数原子核所带的电荷数1、原子结构模型的演变道尔顿模型(1803年):原子是构成物质的基本粒子,它们是坚实的、不可再分的实心球。道尔顿原子模型:“实心球”模型教材P94:科学史话汤姆孙原子模型:葡萄干面包模型汤姆孙模型(1904年):原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。汤姆孙电子之父阴极射线实验1、原子结构模型的演变卢瑟福卢瑟福原子模型:行星式模型卢瑟福模型:原子中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星环绕太阳运转一样。α粒子衍射实验1、原子结构模型的演变卢瑟福:原子的质量主要集中在原子核≈质子数×1.007+中子数×1.0081个原子的相对质量质子数+中子数≈微粒质子中子电子质量/kg1.673×10-271.675×10-279.109×10-31相对质量①1.0071.0081/1836原子符号:ZXA11Na238O167N146C14≈质子相对总质量+中子相对总质量质量关系:质量数(A)=质子数(Z)+中子数(N)忽略电子的质量,将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。2、原子的表示方法:玻尔玻尔原子模型:量子化轨道模型①原子核外,电子在一系列稳定的轨道上绕核作圆周运动运动时,既不放出能量,也不吸收能量。②多电子原子的电子在不连续的壳层中运动。③每个轨道都具有一个确定的能量值,离核愈远能量愈高。玻尔原子模型:分层轨道模型1、原子结构模型的演变在含有多个电子的原子里,电子分别在能量不同的区域内运动,人们把不同区域简化为不连续的壳层,称之为电子层。表示从内到外的电子层。Q电子层数n = 1,2,3,4,5,6,7KLMNOP原子结构示意图/核外电子的排布:+11281Na请你画出7、8、10、13、16、17号原子的原子结构示意图2、原子的表示方法:高速运动,接近光速;没有确定的轨迹,不能同时准确地测定电子在某一时刻所处的位置和运动速度,也不能描绘出它的运动轨迹。只能用统计的观点指出它在原子核外空间某处出现机会的多少。用“电子云”形象地描述核外电子的运动。1234现代电子云模型1、原子结构模型的演变
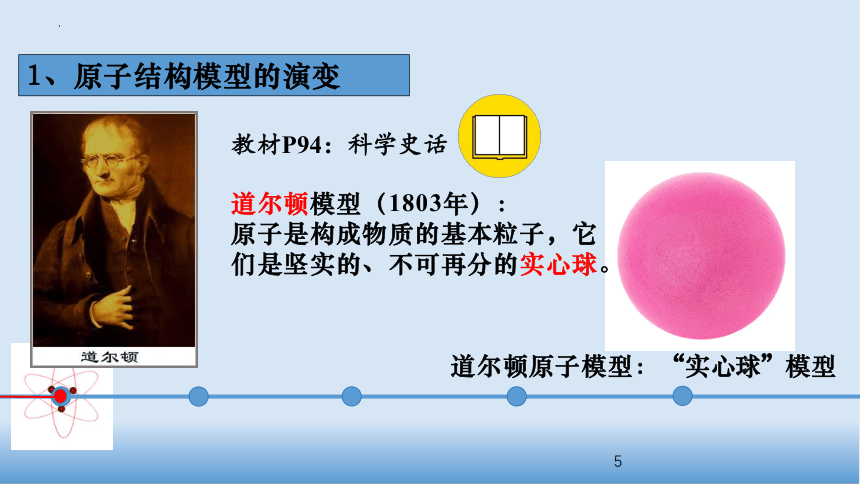
道尔顿模型
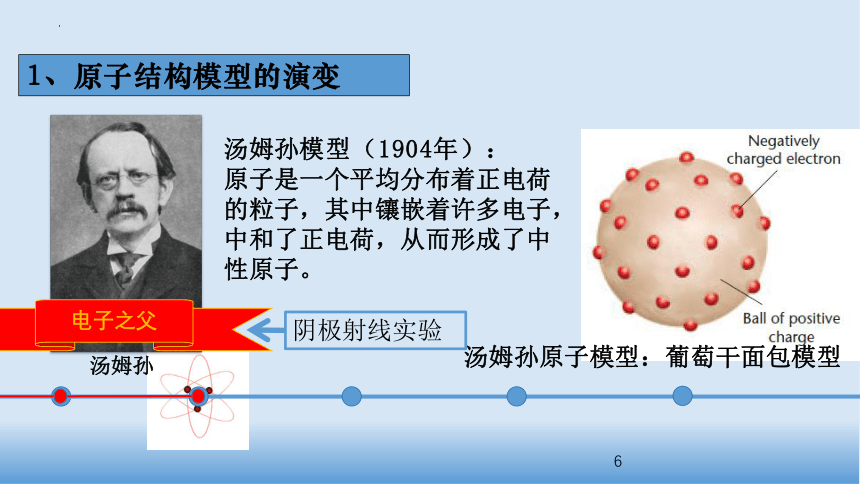
汤姆孙模型
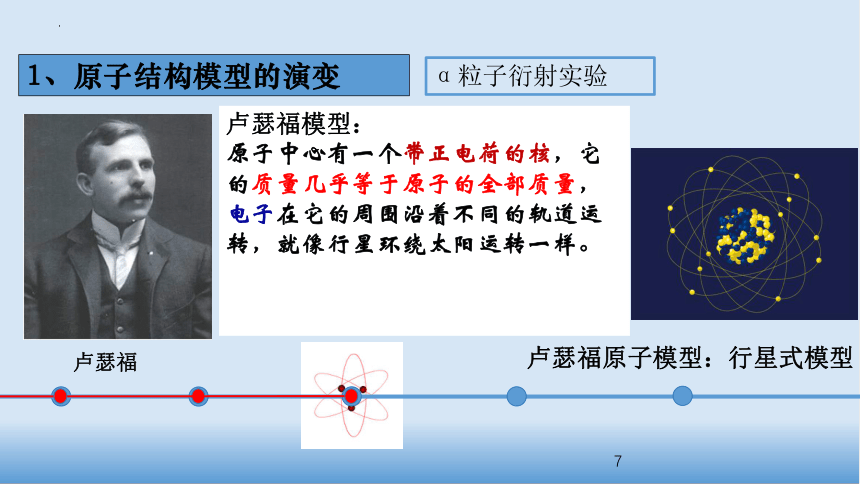
卢瑟福模型
玻尔模型
电子云模型
1、原子结构模型的演变
教材P93核电荷数元素名称元素符号各电子层的电子数KLMNOP2氦He210氖Ne2818氩Ar28836氪Kr2818854氙Xe281818886氡Rn281832188思考·讨论从表中稀有气体的电子排布,你发现什么规律?3.原子核外电子排布规律能量最低由内向外能量较高2n2821832即按K→L→M→N……顺序排列请你画出K、Ca原子的原子结构示意图课堂小结
原子
结构
1.原子结构的发展史
3.原子核外电子排布规律
X
A
Z
2.原子的表示
原子结构示意图
1.科学家于2000年发现了核电荷数为116的元素(Lv)。下列有关质量数为293的Lv原子的描述错误的是( )
A.质子数为116 B.中子数为177
C.电子数为116 D.原子中质子数比中子数多61
D
2、今有甲、乙、丙、丁四种元素,(皆为前20号元素)已知:①甲原子的最外层电子数是次外层的3倍;②乙元素是金属元素,它的原子核外K、L层电子数之和等于M、N层电子数之和;③丙元素的单质及其化合物的焰色试验都显黄色④丁元素单质在氢气中燃烧火焰呈苍白色。试推断并写出甲、乙、丙、丁四种元素的符号。O Ca Na Cl3.A、B两种原子,A的L电子层比B的M电子层少3个电子,B的L电子层电子数恰为A的L电子层电子数的2倍。A和B分别是()A.硅原子和钠原子B.硼原子和氦原子C.碳原子和氯原子D.碳原子和铝原子C01.道尔顿02.汤姆孙03.卢瑟福04.玻尔
第一节 原子结构与元素周期表第四章 物质结构 元素周期律第一课时 原子结构宇观微观宏观3×107~1.5×1026m10-4~107m10-10~10-9m万有引力电磁作用力量子化波粒二象性电子作用力【知识回顾】说说你对原子的认识。物质原子原子核质子中子核外电子物质/微粒>10-410-1010-1410-15<<10-15尺度/m1个质子带一个单位正电荷1个电子带一个单位负电荷中子不带电质子、中子、电子的电性和电量怎样?原子的核电荷数=核外电子数=核内质子数原子核所带的电荷数1、原子结构模型的演变道尔顿模型(1803年):原子是构成物质的基本粒子,它们是坚实的、不可再分的实心球。道尔顿原子模型:“实心球”模型教材P94:科学史话汤姆孙原子模型:葡萄干面包模型汤姆孙模型(1904年):原子是一个平均分布着正电荷的粒子,其中镶嵌着许多电子,中和了正电荷,从而形成了中性原子。汤姆孙电子之父阴极射线实验1、原子结构模型的演变卢瑟福卢瑟福原子模型:行星式模型卢瑟福模型:原子中心有一个带正电荷的核,它的质量几乎等于原子的全部质量,电子在它的周围沿着不同的轨道运转,就像行星环绕太阳运转一样。α粒子衍射实验1、原子结构模型的演变卢瑟福:原子的质量主要集中在原子核≈质子数×1.007+中子数×1.0081个原子的相对质量质子数+中子数≈微粒质子中子电子质量/kg1.673×10-271.675×10-279.109×10-31相对质量①1.0071.0081/1836原子符号:ZXA11Na238O167N146C14≈质子相对总质量+中子相对总质量质量关系:质量数(A)=质子数(Z)+中子数(N)忽略电子的质量,将原子核内所有的质子和中子的相对质量取近似整数值加起来,所得的数值,叫质量数。2、原子的表示方法:玻尔玻尔原子模型:量子化轨道模型①原子核外,电子在一系列稳定的轨道上绕核作圆周运动运动时,既不放出能量,也不吸收能量。②多电子原子的电子在不连续的壳层中运动。③每个轨道都具有一个确定的能量值,离核愈远能量愈高。玻尔原子模型:分层轨道模型1、原子结构模型的演变在含有多个电子的原子里,电子分别在能量不同的区域内运动,人们把不同区域简化为不连续的壳层,称之为电子层。表示从内到外的电子层。Q电子层数n = 1,2,3,4,5,6,7KLMNOP原子结构示意图/核外电子的排布:+11281Na请你画出7、8、10、13、16、17号原子的原子结构示意图2、原子的表示方法:高速运动,接近光速;没有确定的轨迹,不能同时准确地测定电子在某一时刻所处的位置和运动速度,也不能描绘出它的运动轨迹。只能用统计的观点指出它在原子核外空间某处出现机会的多少。用“电子云”形象地描述核外电子的运动。1234现代电子云模型1、原子结构模型的演变
道尔顿模型
汤姆孙模型
卢瑟福模型
玻尔模型
电子云模型
1、原子结构模型的演变
教材P93核电荷数元素名称元素符号各电子层的电子数KLMNOP2氦He210氖Ne2818氩Ar28836氪Kr2818854氙Xe281818886氡Rn281832188思考·讨论从表中稀有气体的电子排布,你发现什么规律?3.原子核外电子排布规律能量最低由内向外能量较高2n2821832即按K→L→M→N……顺序排列请你画出K、Ca原子的原子结构示意图课堂小结
原子
结构
1.原子结构的发展史
3.原子核外电子排布规律
X
A
Z
2.原子的表示
原子结构示意图
1.科学家于2000年发现了核电荷数为116的元素(Lv)。下列有关质量数为293的Lv原子的描述错误的是( )
A.质子数为116 B.中子数为177
C.电子数为116 D.原子中质子数比中子数多61
D
2、今有甲、乙、丙、丁四种元素,(皆为前20号元素)已知:①甲原子的最外层电子数是次外层的3倍;②乙元素是金属元素,它的原子核外K、L层电子数之和等于M、N层电子数之和;③丙元素的单质及其化合物的焰色试验都显黄色④丁元素单质在氢气中燃烧火焰呈苍白色。试推断并写出甲、乙、丙、丁四种元素的符号。O Ca Na Cl3.A、B两种原子,A的L电子层比B的M电子层少3个电子,B的L电子层电子数恰为A的L电子层电子数的2倍。A和B分别是()A.硅原子和钠原子B.硼原子和氦原子C.碳原子和氯原子D.碳原子和铝原子C01.道尔顿02.汤姆孙03.卢瑟福04.玻尔
