2023-2024学年九年级化学人教版下册第十一单元盐化肥基础训练题(含答案)
文档属性
| 名称 | 2023-2024学年九年级化学人教版下册第十一单元盐化肥基础训练题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 205.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-19 00:00:00 | ||
图片预览




文档简介
第十一单元 盐 化肥 基础训练题(有答案)2023—2024学年人教化学九年级下册
一、选择题。
1、人们的日常生活离不开盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
2、中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是( )
食醋 B. 烧碱 C. 草木灰 D. 生石灰
3、下列化学方程式中属于复分解反应的是( )
A. C+O2CO2
B. 2H2O2H2↑+O2↑
C. 3CO+Fe2O32Fe+3CO2
D. HCl+AgNO3===AgCl↓+HNO3
4、下列物质能够反应,且没有明显现象的是( )
A. Na2CO3溶液加入澄清石灰水中
B. Fe2O3加入NaOH溶液中
C. 稀HCl滴入Ba(OH)2溶液中
D. CO2通入澄清石灰水中
5、下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
A.铜和硝酸银溶液 B.氢氧化铜和稀硫酸
C.氢氧化钠和稀盐酸 D.氢氧化钾和硝酸钠
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
9、氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是( )
A.NH4Cl与KCl:观察外观
B.NH4HCO3与KCl:加水
C.K2SO4与Ca3(PO4)2:闻气味
D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味
10、下列各组物质可按溶解、过滤、蒸发的操作顺序将它们分离的是( )
A. 氧化铜和炭粉 B. 氯化钠和氯化钙
C. 水和酒精 D. 碳酸钠和碳酸钙
11、下列鉴别物质所用的方法中,错误的是( )
A.二氧化锰粉末和木炭粉——灼烧 B.氢氧化钠和硝酸铵——加水
C.稀盐酸和稀硫酸——滴加石蕊试液 D.氧化铁和氧化铜——看颜色
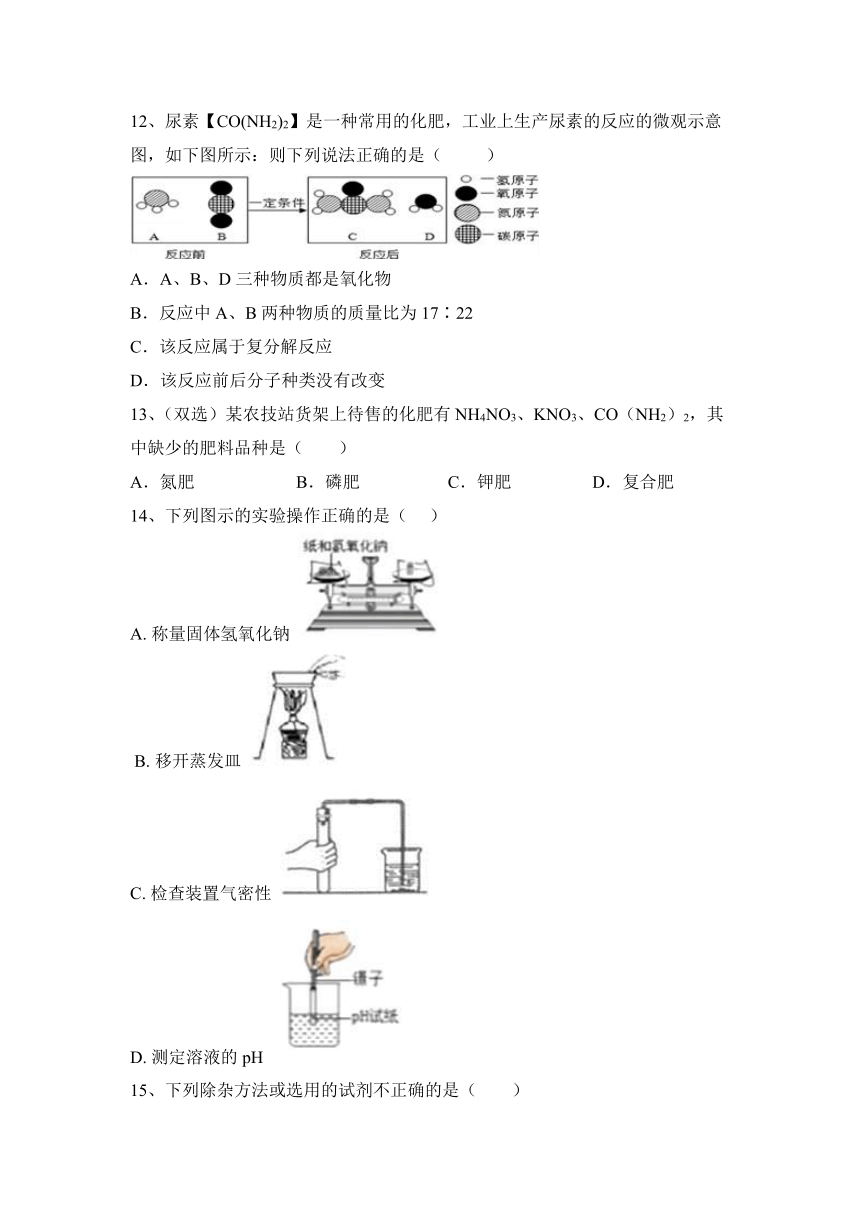
12、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
13、(双选)某农技站货架上待售的化肥有NH4NO3、KNO3、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥
14、下列图示的实验操作正确的是( )
A. 称量固体氢氧化钠
B. 移开蒸发皿
C. 检查装置气密性
D. 测定溶液的pH
15、下列除杂方法或选用的试剂不正确的是( )
选项 物质 所含杂质(少量) 除去杂质的方法
A 碳酸钡 氯化钠 加水溶解,过滤,洗涤,烘干
B N2 O2 通过灼热的铜网
C CaCl2溶液 稀盐酸 加入过量碳酸钙,过滤
D Fe 铁锈 加入足量稀硫酸,过滤
A.A B.B C.C D.D
16、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。 (2)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(3)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
18、下列是有关氨气(NH3)性质的趣味实验。
(1)如图圆底烧瓶中充满氨气,当挤压胶头滴管并打开止弹簧时,烧杯中的水迅速进入烧瓶,形成“红色喷泉”,推测氨气具有哪些性质?
_______________________________。
(2)氨气与酸反应可生成铵盐。将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生,请解释白烟产生的原因___________________。
19、实验室有如图所示装置,回答下列问题:
(1)填写仪器名称:X________;Y________ 。
(2)可以从食盐溶液中获得食盐固体的是________ ,可以把粗盐浊液中的难溶物除去的是________ (填编号)
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有____________(填序号)。
(3)图中⑤处应补充的文字是 (写一种,不能与已有信息重复)。
三、实验题。
21、某研究小组对自动充气气球(示意图如下)进行下列探究。
图1 图2
【查阅资料】该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
探究一:白色粉末成分的探究
【猜想与假设】甲同学认为是碳酸钙;
乙同学认为是碳酸钠;
丙同学认为是碳酸氢钠。
【设计并进行实验】
(1)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想 (填“正确”或 “不正确”)。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的 10%的盐酸(装置如图),记录如下表:
实验编号 锥形瓶内物质 最终得到CO2体积/mL
名称 质量/g
① 碳酸氢钠 0.10 Vl
② 碳酸钠 0.10 V2
③ 白色粉末 a Vl
实验①的化学方程式为 ;表中a= ;
V1 (填“>”“<”或“=”)V2。
(3)如何从上表中获取证据并得出结论?
22、为了测定粗盐(混有少量的泥沙及可溶性杂质)中氯化钠的纯度,进行如下操作:
①a计算产率,b过滤,c溶解,d蒸发,e称量粗盐,f称量精盐。
实验步骤的正确顺序是:________、a(填编号)。
②蒸发时有如下注意事项,你认为错误的是________ (填字母序号)。
A.注入蒸发皿的滤液不超过其容积的2/3
B.蒸发皿必须放在陶土网上加热
C.加热时用玻璃棒搅拌,防止滤液溅出
D.当蒸发皿中出现较多固体时,停止加热
③过滤时用到的玻璃仪器有玻璃棒、烧杯、________,其中玻璃棒的作用是________。
实验过程中发现过滤两次滤液仍然浑浊,可能的原因是________。
④实验结束时发现测得的纯度偏高,可能是________ (填字母序号)。
A. 溶解时加水过多 B. 蒸发过程中液滴飞溅
C. 蒸发后所得精盐很湿 D. 蒸发皿上有精盐残余
四、计算题。
23、某纯碱样品中含有少量NaCl,小丽同学取该样品23 g全部溶解于150 g水中,再逐滴加入160 g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl===2NaCl+H2O+CO2↑)
计算当恰好完全反应时:
(1)产生的二氧化碳的质量是多少克。
(2)此时所得到的溶液中溶质的质量分数是多少?(结果保留到0.1%)。
第十一单元 盐 化肥 基础训练题(有答案)2023—2024学年人教化学九年级下册
一、选择题。
1、人们的日常生活离不开盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
【答案】C
2、中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是( )
食醋 B. 烧碱 C. 草木灰 D. 生石灰
【答案】C
3、下列化学方程式中属于复分解反应的是( )
A. C+O2CO2
B. 2H2O2H2↑+O2↑
C. 3CO+Fe2O32Fe+3CO2
D. HCl+AgNO3===AgCl↓+HNO3
【答案】D
4、下列物质能够反应,且没有明显现象的是( )
A. Na2CO3溶液加入澄清石灰水中
B. Fe2O3加入NaOH溶液中
C. 稀HCl滴入Ba(OH)2溶液中
D. CO2通入澄清石灰水中
【答案】C
5、下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
A.铜和硝酸银溶液 B.氢氧化铜和稀硫酸
C.氢氧化钠和稀盐酸 D.氢氧化钾和硝酸钠
【答案】A
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
【答案】C
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
【答案】B
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
【答案】C
9、氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是( )
A.NH4Cl与KCl:观察外观
B.NH4HCO3与KCl:加水
C.K2SO4与Ca3(PO4)2:闻气味
D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味
【答案】D
10、下列各组物质可按溶解、过滤、蒸发的操作顺序将它们分离的是( )
A. 氧化铜和炭粉 B. 氯化钠和氯化钙
C. 水和酒精 D. 碳酸钠和碳酸钙
【答案】D
11、下列鉴别物质所用的方法中,错误的是( )
A.二氧化锰粉末和木炭粉——灼烧 B.氢氧化钠和硝酸铵——加水
C.稀盐酸和稀硫酸——滴加石蕊试液 D.氧化铁和氧化铜——看颜色
【答案】C
12、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
【答案】B
13、(双选)某农技站货架上待售的化肥有NH4NO3、KNO3、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥
【答案】BC
14、下列图示的实验操作正确的是( )
A. 称量固体氢氧化钠
B. 移开蒸发皿
C. 检查装置气密性
D. 测定溶液的pH
【答案】 C
15、下列除杂方法或选用的试剂不正确的是( )
选项 物质 所含杂质(少量) 除去杂质的方法
A 碳酸钡 氯化钠 加水溶解,过滤,洗涤,烘干
B N2 O2 通过灼热的铜网
C CaCl2溶液 稀盐酸 加入过量碳酸钙,过滤
D Fe 铁锈 加入足量稀硫酸,过滤
A.A B.B C.C D.D
【答案】D
16、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
【答案】D
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。 (2)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(3)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
【答案】(1)CO2 + Ca(OH)2 == CaCO3↓+ H2O
(2)2NaCl+ H2O2NaOH + H2↑+Cl2↑
(3)BaCO3+2HCl == BaCl2 + H2O + CO2↑ 复分解反应
18、下列是有关氨气(NH3)性质的趣味实验。
(1)如图圆底烧瓶中充满氨气,当挤压胶头滴管并打开止弹簧时,烧杯中的水迅速进入烧瓶,形成“红色喷泉”,推测氨气具有哪些性质?
_______________________________。
(2)氨气与酸反应可生成铵盐。将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生,请解释白烟产生的原因___________________。
【答案】(1)氨气易溶于水,溶液显碱性;
(2)浓盐酸易挥发出氯化氢气体,氯化氢气体能与氨气化合生成了氯化铵颗粒。
19、实验室有如图所示装置,回答下列问题:
(1)填写仪器名称:X________;Y________ 。
(2)可以从食盐溶液中获得食盐固体的是________ ,可以把粗盐浊液中的难溶物除去的是________ (填编号)
【答案】漏斗;蒸发皿;b;a
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有____________(填序号)。
(3)图中⑤处应补充的文字是 (写一种,不能与已有信息重复)。
【答案】2KOH+H2SO4===K2SO4+2H2O ④⑥
非金属氧化物和碱或金属氧化物和酸
三、实验题。
21、某研究小组对自动充气气球(示意图如下)进行下列探究。
图1 图2
【查阅资料】该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
探究一:白色粉末成分的探究
【猜想与假设】甲同学认为是碳酸钙;
乙同学认为是碳酸钠;
丙同学认为是碳酸氢钠。
【设计并进行实验】
(1)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想 (填“正确”或 “不正确”)。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的 10%的盐酸(装置如图),记录如下表:
实验编号 锥形瓶内物质 最终得到CO2体积/mL
名称 质量/g
① 碳酸氢钠 0.10 Vl
② 碳酸钠 0.10 V2
③ 白色粉末 a Vl
实验①的化学方程式为 ;表中a= ;
V1 (填“>”“<”或“=”)V2。
(3)如何从上表中获取证据并得出结论?
【答案】(1)不正确;
(2)NaHCO3+HCl=NaCl+H2O+CO2↑,0.1,>;
(3)通过对比可知,碳酸氢钠与盐酸反应的速率比碳酸钠与盐酸反应的速率快。
22、为了测定粗盐(混有少量的泥沙及可溶性杂质)中氯化钠的纯度,进行如下操作:
①a计算产率,b过滤,c溶解,d蒸发,e称量粗盐,f称量精盐。
实验步骤的正确顺序是:________、a(填编号)。
②蒸发时有如下注意事项,你认为错误的是________ (填字母序号)。
A.注入蒸发皿的滤液不超过其容积的2/3
B.蒸发皿必须放在陶土网上加热
C.加热时用玻璃棒搅拌,防止滤液溅出
D.当蒸发皿中出现较多固体时,停止加热
③过滤时用到的玻璃仪器有玻璃棒、烧杯、________,其中玻璃棒的作用是________。
实验过程中发现过滤两次滤液仍然浑浊,可能的原因是________。
④实验结束时发现测得的纯度偏高,可能是________ (填字母序号)。
A. 溶解时加水过多 B. 蒸发过程中液滴飞溅
C. 蒸发后所得精盐很湿 D. 蒸发皿上有精盐残余
【答案】e c b d f;b;漏斗;引流;滤纸破损;
过滤的液体液面高于滤纸;承接滤液的烧杯不洁净;C
四、计算题。
23、某纯碱样品中含有少量NaCl,小丽同学取该样品23 g全部溶解于150 g水中,再逐滴加入160 g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl===2NaCl+H2O+CO2↑)
计算当恰好完全反应时:
(1)产生的二氧化碳的质量是多少克。
(2)此时所得到的溶液中溶质的质量分数是多少?(结果保留到0.1%)。
【答案】(1)8.8 (2)恰好完全反应时所得NaCl溶液中溶质的质量分数为8.4%。
一、选择题。
1、人们的日常生活离不开盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
2、中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是( )
食醋 B. 烧碱 C. 草木灰 D. 生石灰
3、下列化学方程式中属于复分解反应的是( )
A. C+O2CO2
B. 2H2O2H2↑+O2↑
C. 3CO+Fe2O32Fe+3CO2
D. HCl+AgNO3===AgCl↓+HNO3
4、下列物质能够反应,且没有明显现象的是( )
A. Na2CO3溶液加入澄清石灰水中
B. Fe2O3加入NaOH溶液中
C. 稀HCl滴入Ba(OH)2溶液中
D. CO2通入澄清石灰水中
5、下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
A.铜和硝酸银溶液 B.氢氧化铜和稀硫酸
C.氢氧化钠和稀盐酸 D.氢氧化钾和硝酸钠
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
9、氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是( )
A.NH4Cl与KCl:观察外观
B.NH4HCO3与KCl:加水
C.K2SO4与Ca3(PO4)2:闻气味
D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味
10、下列各组物质可按溶解、过滤、蒸发的操作顺序将它们分离的是( )
A. 氧化铜和炭粉 B. 氯化钠和氯化钙
C. 水和酒精 D. 碳酸钠和碳酸钙
11、下列鉴别物质所用的方法中,错误的是( )
A.二氧化锰粉末和木炭粉——灼烧 B.氢氧化钠和硝酸铵——加水
C.稀盐酸和稀硫酸——滴加石蕊试液 D.氧化铁和氧化铜——看颜色
12、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
13、(双选)某农技站货架上待售的化肥有NH4NO3、KNO3、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥
14、下列图示的实验操作正确的是( )
A. 称量固体氢氧化钠
B. 移开蒸发皿
C. 检查装置气密性
D. 测定溶液的pH
15、下列除杂方法或选用的试剂不正确的是( )
选项 物质 所含杂质(少量) 除去杂质的方法
A 碳酸钡 氯化钠 加水溶解,过滤,洗涤,烘干
B N2 O2 通过灼热的铜网
C CaCl2溶液 稀盐酸 加入过量碳酸钙,过滤
D Fe 铁锈 加入足量稀硫酸,过滤
A.A B.B C.C D.D
16、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。 (2)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(3)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
18、下列是有关氨气(NH3)性质的趣味实验。
(1)如图圆底烧瓶中充满氨气,当挤压胶头滴管并打开止弹簧时,烧杯中的水迅速进入烧瓶,形成“红色喷泉”,推测氨气具有哪些性质?
_______________________________。
(2)氨气与酸反应可生成铵盐。将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生,请解释白烟产生的原因___________________。
19、实验室有如图所示装置,回答下列问题:
(1)填写仪器名称:X________;Y________ 。
(2)可以从食盐溶液中获得食盐固体的是________ ,可以把粗盐浊液中的难溶物除去的是________ (填编号)
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有____________(填序号)。
(3)图中⑤处应补充的文字是 (写一种,不能与已有信息重复)。
三、实验题。
21、某研究小组对自动充气气球(示意图如下)进行下列探究。
图1 图2
【查阅资料】该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
探究一:白色粉末成分的探究
【猜想与假设】甲同学认为是碳酸钙;
乙同学认为是碳酸钠;
丙同学认为是碳酸氢钠。
【设计并进行实验】
(1)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想 (填“正确”或 “不正确”)。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的 10%的盐酸(装置如图),记录如下表:
实验编号 锥形瓶内物质 最终得到CO2体积/mL
名称 质量/g
① 碳酸氢钠 0.10 Vl
② 碳酸钠 0.10 V2
③ 白色粉末 a Vl
实验①的化学方程式为 ;表中a= ;
V1 (填“>”“<”或“=”)V2。
(3)如何从上表中获取证据并得出结论?
22、为了测定粗盐(混有少量的泥沙及可溶性杂质)中氯化钠的纯度,进行如下操作:
①a计算产率,b过滤,c溶解,d蒸发,e称量粗盐,f称量精盐。
实验步骤的正确顺序是:________、a(填编号)。
②蒸发时有如下注意事项,你认为错误的是________ (填字母序号)。
A.注入蒸发皿的滤液不超过其容积的2/3
B.蒸发皿必须放在陶土网上加热
C.加热时用玻璃棒搅拌,防止滤液溅出
D.当蒸发皿中出现较多固体时,停止加热
③过滤时用到的玻璃仪器有玻璃棒、烧杯、________,其中玻璃棒的作用是________。
实验过程中发现过滤两次滤液仍然浑浊,可能的原因是________。
④实验结束时发现测得的纯度偏高,可能是________ (填字母序号)。
A. 溶解时加水过多 B. 蒸发过程中液滴飞溅
C. 蒸发后所得精盐很湿 D. 蒸发皿上有精盐残余
四、计算题。
23、某纯碱样品中含有少量NaCl,小丽同学取该样品23 g全部溶解于150 g水中,再逐滴加入160 g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl===2NaCl+H2O+CO2↑)
计算当恰好完全反应时:
(1)产生的二氧化碳的质量是多少克。
(2)此时所得到的溶液中溶质的质量分数是多少?(结果保留到0.1%)。
第十一单元 盐 化肥 基础训练题(有答案)2023—2024学年人教化学九年级下册
一、选择题。
1、人们的日常生活离不开盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
【答案】C
2、中国丝绸有几千年的历史传承。古代染坊常用某种“碱剂”来处理丝绸,该“碱剂”可使丝绸颜色洁白、质感柔软,其主要成分是一种盐,这种“碱剂”可能是( )
食醋 B. 烧碱 C. 草木灰 D. 生石灰
【答案】C
3、下列化学方程式中属于复分解反应的是( )
A. C+O2CO2
B. 2H2O2H2↑+O2↑
C. 3CO+Fe2O32Fe+3CO2
D. HCl+AgNO3===AgCl↓+HNO3
【答案】D
4、下列物质能够反应,且没有明显现象的是( )
A. Na2CO3溶液加入澄清石灰水中
B. Fe2O3加入NaOH溶液中
C. 稀HCl滴入Ba(OH)2溶液中
D. CO2通入澄清石灰水中
【答案】C
5、下列各组中的物质混合,形成溶液的质量比反应前溶液的总质量减少的是( )
A.铜和硝酸银溶液 B.氢氧化铜和稀硫酸
C.氢氧化钠和稀盐酸 D.氢氧化钾和硝酸钠
【答案】A
6、德国化学家弗里茨·哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量。下列说法中正确的是( )
A.氮气和氢气在点燃或光照条件下可合成氨
B.氨水显酸性
C.氨气遇到浓盐酸会发生反应产生白烟
D.干燥氨气可用浓硫酸
【答案】C
7、某同学想要鉴别NH4HCO3、NH4Cl、KCl三种化肥,操作过程如图所示,其中试剂甲和乙可能是( )
A.甲:水,乙:氢氧化钠
B.甲:熟石灰,乙:稀盐酸
C.甲:稀盐酸,乙:氯化钠溶液
D.甲:氢氧化钠,乙:硫酸钠溶液
【答案】B
8、粗盐中难溶性杂质的去除过程中,涉及到称量、溶解、过滤、蒸发等过程。下列说法不正确的是( )
A.称量时粗盐放在天平左盘的称量纸上
B.粗盐溶解时,要用玻璃棒不断搅拌
C.蒸发时,在恰好蒸干时停止加热
D.过滤时漏斗下端尖嘴处紧靠烧杯内壁
【答案】C
9、氮肥、磷肥、钾肥是农业生产中最主要的化肥,用简便的方法区别三种化肥,在农业生产中具有实用性。区别下列相关化肥的方法可行的是( )
A.NH4Cl与KCl:观察外观
B.NH4HCO3与KCl:加水
C.K2SO4与Ca3(PO4)2:闻气味
D.(NH4)2SO4与K2SO4:加熟石灰研磨后闻气味
【答案】D
10、下列各组物质可按溶解、过滤、蒸发的操作顺序将它们分离的是( )
A. 氧化铜和炭粉 B. 氯化钠和氯化钙
C. 水和酒精 D. 碳酸钠和碳酸钙
【答案】D
11、下列鉴别物质所用的方法中,错误的是( )
A.二氧化锰粉末和木炭粉——灼烧 B.氢氧化钠和硝酸铵——加水
C.稀盐酸和稀硫酸——滴加石蕊试液 D.氧化铁和氧化铜——看颜色
【答案】C
12、尿素【CO(NH2)2】是一种常用的化肥,工业上生产尿素的反应的微观示意图,如下图所示:则下列说法正确的是( )
A.A、B、D三种物质都是氧化物
B.反应中A、B两种物质的质量比为17∶22
C.该反应属于复分解反应
D.该反应前后分子种类没有改变
【答案】B
13、(双选)某农技站货架上待售的化肥有NH4NO3、KNO3、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥
【答案】BC
14、下列图示的实验操作正确的是( )
A. 称量固体氢氧化钠
B. 移开蒸发皿
C. 检查装置气密性
D. 测定溶液的pH
【答案】 C
15、下列除杂方法或选用的试剂不正确的是( )
选项 物质 所含杂质(少量) 除去杂质的方法
A 碳酸钡 氯化钠 加水溶解,过滤,洗涤,烘干
B N2 O2 通过灼热的铜网
C CaCl2溶液 稀盐酸 加入过量碳酸钙,过滤
D Fe 铁锈 加入足量稀硫酸,过滤
A.A B.B C.C D.D
【答案】D
16、现有以下物质,对它们的分类正确的是( )
①澄清石灰水 ②氧化铜 ③五氧化二磷
④硝酸钾⑤醋酸 ⑥洁净的空气 ⑦纯碱⑧硫酸钾
A.①⑥属于纯净物 B.④⑧属于复合肥
C.①⑦属于碱 D.②③属于氧化物
【答案】D
二、填空题。
17、写出下列反应的化学方程式,并按要求填空。
(1)用石灰浆粉刷墙壁,干燥后又白又硬:______________________________。 (2)工业上,常用电解氯化钠溶液的方法来制取氢氧化钠,同时还能获得氢气、氯气两种化工产品,其反应的化学方程式为_____________________。
(3)医疗上“钡餐”的主要成分是硫酸钡,不能用碳酸钡替代硫酸钡的原因是用方程式表示_____________,该反应的基本反应类型是__________。
【答案】(1)CO2 + Ca(OH)2 == CaCO3↓+ H2O
(2)2NaCl+ H2O2NaOH + H2↑+Cl2↑
(3)BaCO3+2HCl == BaCl2 + H2O + CO2↑ 复分解反应
18、下列是有关氨气(NH3)性质的趣味实验。
(1)如图圆底烧瓶中充满氨气,当挤压胶头滴管并打开止弹簧时,烧杯中的水迅速进入烧瓶,形成“红色喷泉”,推测氨气具有哪些性质?
_______________________________。
(2)氨气与酸反应可生成铵盐。将分别蘸有浓氨水和浓盐酸的玻璃棒接近(不接触),就有大量白烟产生,请解释白烟产生的原因___________________。
【答案】(1)氨气易溶于水,溶液显碱性;
(2)浓盐酸易挥发出氯化氢气体,氯化氢气体能与氨气化合生成了氯化铵颗粒。
19、实验室有如图所示装置,回答下列问题:
(1)填写仪器名称:X________;Y________ 。
(2)可以从食盐溶液中获得食盐固体的是________ ,可以把粗盐浊液中的难溶物除去的是________ (填编号)
【答案】漏斗;蒸发皿;b;a
20、学习了单质、氧化物、酸、碱、盐的性质后,发现有很多不同类别的物质在发生反应时都有盐生成(其他物质省略),如图所示。请回答:
(1)若盐是硫酸钾,则①中发生反应的化学方程式为:
。
(2)若盐是氯化亚铁,则在已显示的变化中可以通过置换反应来实现的有____________(填序号)。
(3)图中⑤处应补充的文字是 (写一种,不能与已有信息重复)。
【答案】2KOH+H2SO4===K2SO4+2H2O ④⑥
非金属氧化物和碱或金属氧化物和酸
三、实验题。
21、某研究小组对自动充气气球(示意图如下)进行下列探究。
图1 图2
【查阅资料】该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气。
探究一:白色粉末成分的探究
【猜想与假设】甲同学认为是碳酸钙;
乙同学认为是碳酸钠;
丙同学认为是碳酸氢钠。
【设计并进行实验】
(1)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想 (填“正确”或 “不正确”)。
(2)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的 10%的盐酸(装置如图),记录如下表:
实验编号 锥形瓶内物质 最终得到CO2体积/mL
名称 质量/g
① 碳酸氢钠 0.10 Vl
② 碳酸钠 0.10 V2
③ 白色粉末 a Vl
实验①的化学方程式为 ;表中a= ;
V1 (填“>”“<”或“=”)V2。
(3)如何从上表中获取证据并得出结论?
【答案】(1)不正确;
(2)NaHCO3+HCl=NaCl+H2O+CO2↑,0.1,>;
(3)通过对比可知,碳酸氢钠与盐酸反应的速率比碳酸钠与盐酸反应的速率快。
22、为了测定粗盐(混有少量的泥沙及可溶性杂质)中氯化钠的纯度,进行如下操作:
①a计算产率,b过滤,c溶解,d蒸发,e称量粗盐,f称量精盐。
实验步骤的正确顺序是:________、a(填编号)。
②蒸发时有如下注意事项,你认为错误的是________ (填字母序号)。
A.注入蒸发皿的滤液不超过其容积的2/3
B.蒸发皿必须放在陶土网上加热
C.加热时用玻璃棒搅拌,防止滤液溅出
D.当蒸发皿中出现较多固体时,停止加热
③过滤时用到的玻璃仪器有玻璃棒、烧杯、________,其中玻璃棒的作用是________。
实验过程中发现过滤两次滤液仍然浑浊,可能的原因是________。
④实验结束时发现测得的纯度偏高,可能是________ (填字母序号)。
A. 溶解时加水过多 B. 蒸发过程中液滴飞溅
C. 蒸发后所得精盐很湿 D. 蒸发皿上有精盐残余
【答案】e c b d f;b;漏斗;引流;滤纸破损;
过滤的液体液面高于滤纸;承接滤液的烧杯不洁净;C
四、计算题。
23、某纯碱样品中含有少量NaCl,小丽同学取该样品23 g全部溶解于150 g水中,再逐滴加入160 g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示。(提示:相关反应为Na2CO3+2HCl===2NaCl+H2O+CO2↑)
计算当恰好完全反应时:
(1)产生的二氧化碳的质量是多少克。
(2)此时所得到的溶液中溶质的质量分数是多少?(结果保留到0.1%)。
【答案】(1)8.8 (2)恰好完全反应时所得NaCl溶液中溶质的质量分数为8.4%。
同课章节目录
