6.1.2化学能与电能课件(共28张ppt)化学人教版(2019)必修第二册
文档属性
| 名称 | 6.1.2化学能与电能课件(共28张ppt)化学人教版(2019)必修第二册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 18.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-22 00:00:00 | ||
图片预览







文档简介
(共28张PPT)
第一节 化学反应与能量变化
第2课时化学能与电能
天空中释放的闪电能产生巨大的能量
生活中人们使用的电能来自于哪里
能不能直接从自然界获取电能
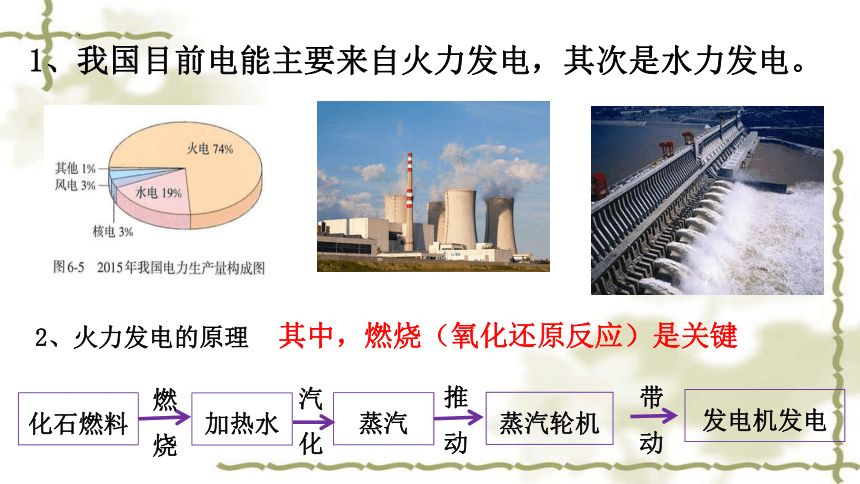
1、我国目前电能主要来自火力发电,其次是水力发电。
2、火力发电的原理
化石燃料
加热水
燃烧
汽化
蒸汽
推动
蒸汽轮机
发电机发电
带动
其中,燃烧(氧化还原反应)是关键
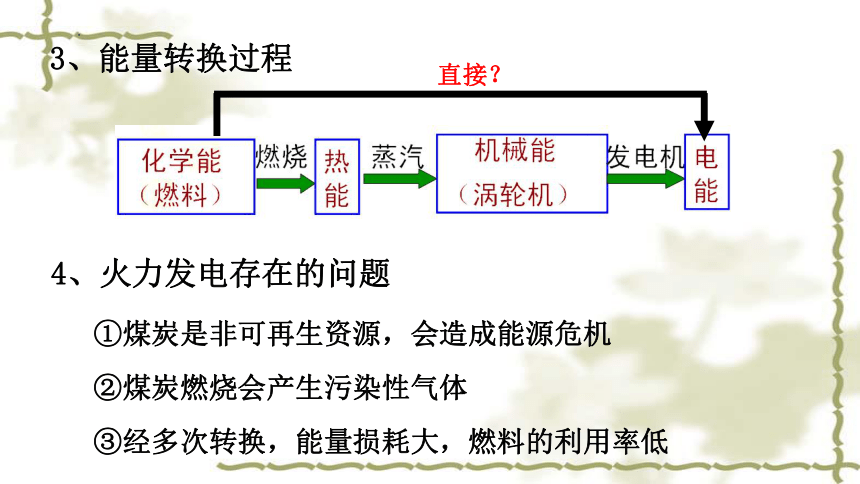
①煤炭是非可再生资源,会造成能源危机
②煤炭燃烧会产生污染性气体
③经多次转换,能量损耗大,燃料的利用率低
4、火力发电存在的问题
直接?
3、能量转换过程
电子定向移动
氧化还原反应
写出锌和稀硫酸反应的化学方程式并用单线桥分析
【思考1】电流是怎样产生的?
【思考2】什么反应中有电子的转移?
探究把化学能直接转变为电能的装置?
Zn+2H+=Zn2++H2 ↑
2e-
什么方法可使Zn与H+分开,从而让电子定向移动呢?
探究实验 讨论与交流
实验一:分别将锌片和铜片插入稀硫酸 溶液中 观察锌片和铜片上现象和
差别?
实验二:锌片和铜片先接触插入稀硫酸 溶液中,然后再用导线连接 观察锌片和铜片上有何现象?推测原因
实验三:锌片和铜片通过导线接电流表 插入稀硫酸溶液中 观察电流表上有何现象?
注意电流表指针偏转方向
【实验探究】
【实验一】
铜锌未连接时,锌片表面有气泡,铜片无明显变化,放热,原因是与金属活动性顺序有关。
铜锌未连接时反应
的离子方程式
Zn+2H+ = Zn2++ H2↑
0
+1
0
+2
失 2e-
得 2×e-
【实验二】
铜锌连接时,铜表面出现大量气泡,锌表面也有少量气泡
【实验三】
电流表指针发生偏转,说明导线中有电流产生
实验操作
实验现象
实验结论
铜片上:无气泡
锌片上:逐渐溶解,有气泡
铜片上:有气泡
锌片上:逐渐溶解
电流表:指针偏转
锌与稀硫酸反应生成氢气,而铜不反应
装置中发生反应生成氢气,导线中有电流通过
化学能转化为电能
原电池
1、概念:将化学能直接转变为电能的装置
A
Zn
Cu
SO42-
H+
H+
正极
负极
e-
2、本质:氧化反应和还原反应分别在
两个不同的区域进行。
锌片:Zn-2e- = Zn2+ (氧化反应)
铜片:2H++2e- = H2↑(还原反应)
化学能转化为电能
?
?
原电池
板书
概念:将化学能直接转变为电能的装置
本质:氧化还原反应
构成条件
前提:能自发进行氧化还原反应
活泼性不同两极(金属或可导电非金属)
电解质溶液
形成闭合回路
酒精
Zn
C
(C)
稀硫酸
Zn
Cu
(D)
Zn
硫酸铜溶液
Zn
(A)
硫酸铜溶液
Zn
Cu
(B)
稀硫酸
稀硫酸
Cu
Zn
(E)
?
?
Cu
Zn
-
-
-
Zn2+
H+
H+
Zn-2e-=Zn2+
2H++2e-=H2↑
氧化反应
还原反应
负极
正极
SO42-
发生溶解
产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
工作原理
宏观
微观
氧化还原
板书
电极判定
1、Fe – Cu– CuSO4溶液
2、Ag – Fe– AgSO4溶液
3、Al – Mg– HCl溶液
4、Al – Mg– NaOH溶液
5、Fe – Cu– 浓HNO3
Cu
Zn
-
-
-
Zn2+
H+
H+
Zn-2e-=Zn2+
2H++2e-=H2↑
氧化反应
还原反应
负极
正极
阳离子
阴离子
SO42-
发生溶解
产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
电子流向:负极 沿导线 正极
电流方向:正极 沿导线 负极
外电路
内电路
阴离子 负极
阳离子 正极
外电路
内电路
e-
I
板书
电极判定
阴离子
负极
阳离子
正极
内电路(溶液)
外电路(导线):正极 负极
电流
电子
比较金属活泼性
保护金属材料
设计电池
加快反应速率
一般:负极>正极
如:制氢气加入少量硫酸铜溶液
如:船体镶锌块
稀硫酸
Al
Mg
A
Al
Mg
A
NaOH
原电池的应用
盐水动力车
化学能
电能
负
氧化反应
H+
H2
正极
还原反应
氧化还原反应
活性不同
形成闭合回路
?
负极正极电极材料电子流动方向电解质溶液中离子定向移动方向发生的反应反应现象 负极 正极
电极材料 活泼性较强的金属
电子流动方向 电子流出极
电解质溶液中离子定向移动方向 阴离子移向的极
发生的反应 氧化反应
反应现象 电极溶解
负极正极电极材料活泼性较强的金属活泼性较弱的金属或能导电的非金属电子流动方向电子流出极电子流入极电解质溶液中离子定向移动方向阴离子移向的极阳离子移向的极发生的反应氧化反应还原反应反应现象电极溶解电极增重或有气泡放出
第一节 化学反应与能量变化
第2课时化学能与电能
天空中释放的闪电能产生巨大的能量
生活中人们使用的电能来自于哪里
能不能直接从自然界获取电能
1、我国目前电能主要来自火力发电,其次是水力发电。
2、火力发电的原理
化石燃料
加热水
燃烧
汽化
蒸汽
推动
蒸汽轮机
发电机发电
带动
其中,燃烧(氧化还原反应)是关键
①煤炭是非可再生资源,会造成能源危机
②煤炭燃烧会产生污染性气体
③经多次转换,能量损耗大,燃料的利用率低
4、火力发电存在的问题
直接?
3、能量转换过程
电子定向移动
氧化还原反应
写出锌和稀硫酸反应的化学方程式并用单线桥分析
【思考1】电流是怎样产生的?
【思考2】什么反应中有电子的转移?
探究把化学能直接转变为电能的装置?
Zn+2H+=Zn2++H2 ↑
2e-
什么方法可使Zn与H+分开,从而让电子定向移动呢?
探究实验 讨论与交流
实验一:分别将锌片和铜片插入稀硫酸 溶液中 观察锌片和铜片上现象和
差别?
实验二:锌片和铜片先接触插入稀硫酸 溶液中,然后再用导线连接 观察锌片和铜片上有何现象?推测原因
实验三:锌片和铜片通过导线接电流表 插入稀硫酸溶液中 观察电流表上有何现象?
注意电流表指针偏转方向
【实验探究】
【实验一】
铜锌未连接时,锌片表面有气泡,铜片无明显变化,放热,原因是与金属活动性顺序有关。
铜锌未连接时反应
的离子方程式
Zn+2H+ = Zn2++ H2↑
0
+1
0
+2
失 2e-
得 2×e-
【实验二】
铜锌连接时,铜表面出现大量气泡,锌表面也有少量气泡
【实验三】
电流表指针发生偏转,说明导线中有电流产生
实验操作
实验现象
实验结论
铜片上:无气泡
锌片上:逐渐溶解,有气泡
铜片上:有气泡
锌片上:逐渐溶解
电流表:指针偏转
锌与稀硫酸反应生成氢气,而铜不反应
装置中发生反应生成氢气,导线中有电流通过
化学能转化为电能
原电池
1、概念:将化学能直接转变为电能的装置
A
Zn
Cu
SO42-
H+
H+
正极
负极
e-
2、本质:氧化反应和还原反应分别在
两个不同的区域进行。
锌片:Zn-2e- = Zn2+ (氧化反应)
铜片:2H++2e- = H2↑(还原反应)
化学能转化为电能
?
?
原电池
板书
概念:将化学能直接转变为电能的装置
本质:氧化还原反应
构成条件
前提:能自发进行氧化还原反应
活泼性不同两极(金属或可导电非金属)
电解质溶液
形成闭合回路
酒精
Zn
C
(C)
稀硫酸
Zn
Cu
(D)
Zn
硫酸铜溶液
Zn
(A)
硫酸铜溶液
Zn
Cu
(B)
稀硫酸
稀硫酸
Cu
Zn
(E)
?
?
Cu
Zn
-
-
-
Zn2+
H+
H+
Zn-2e-=Zn2+
2H++2e-=H2↑
氧化反应
还原反应
负极
正极
SO42-
发生溶解
产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
工作原理
宏观
微观
氧化还原
板书
电极判定
1、Fe – Cu– CuSO4溶液
2、Ag – Fe– AgSO4溶液
3、Al – Mg– HCl溶液
4、Al – Mg– NaOH溶液
5、Fe – Cu– 浓HNO3
Cu
Zn
-
-
-
Zn2+
H+
H+
Zn-2e-=Zn2+
2H++2e-=H2↑
氧化反应
还原反应
负极
正极
阳离子
阴离子
SO42-
发生溶解
产生气泡
原电池总反应:Zn+2H+=Zn2++H2↑
电子流向:负极 沿导线 正极
电流方向:正极 沿导线 负极
外电路
内电路
阴离子 负极
阳离子 正极
外电路
内电路
e-
I
板书
电极判定
阴离子
负极
阳离子
正极
内电路(溶液)
外电路(导线):正极 负极
电流
电子
比较金属活泼性
保护金属材料
设计电池
加快反应速率
一般:负极>正极
如:制氢气加入少量硫酸铜溶液
如:船体镶锌块
稀硫酸
Al
Mg
A
Al
Mg
A
NaOH
原电池的应用
盐水动力车
化学能
电能
负
氧化反应
H+
H2
正极
还原反应
氧化还原反应
活性不同
形成闭合回路
?
负极正极电极材料电子流动方向电解质溶液中离子定向移动方向发生的反应反应现象 负极 正极
电极材料 活泼性较强的金属
电子流动方向 电子流出极
电解质溶液中离子定向移动方向 阴离子移向的极
发生的反应 氧化反应
反应现象 电极溶解
负极正极电极材料活泼性较强的金属活泼性较弱的金属或能导电的非金属电子流动方向电子流出极电子流入极电解质溶液中离子定向移动方向阴离子移向的极阳离子移向的极发生的反应氧化反应还原反应反应现象电极溶解电极增重或有气泡放出
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
