2015年獐沟中学高二化学学业水平测试模拟试题(二)
文档属性
| 名称 | 2015年獐沟中学高二化学学业水平测试模拟试题(二) |

|
|
| 格式 | zip | ||
| 文件大小 | 768.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | |||
| 科目 | 化学 | ||
| 更新时间 | 2015-11-01 00:00:00 | ||
图片预览

文档简介
2015年獐沟中学高二化学学业水平测试模拟试卷(二)
可能用到的相对原子质量 H:1 C:12 N:14 O:16 S:32 Mg:24 Al:27 K:39 Fe:56
一、单项选择题:(本部分23题,每题3分,共69分)
1.燃放烟花爆竹增强春节喜庆,但也造成大气严重污染。烟花中含有的KNO3属于
A.氧化物 B.酸 C. 碱 D.盐
2.下列为人体提供能量的营养物质中,属于高分子化合物的是
A.蛋白质 B.油脂 C.葡萄糖 D.蔗糖
3.从海带中提取碘的实验要用到过滤、萃取实验操作,该两项操作不需要的仪器是
A.烧杯 B.烧瓶 C.玻璃棒 D.分液漏斗
4.下列气体能使品红溶液褪色的是
A.O2 B.CO2 C.SO2 D.CO
5.下列物质属于离子化合物且含有共价键的是
A.HCl B.CaCl2 C.H2O D.NaOH
6.某溶液中存在大量的H+、Clˉ、SO42ˉ,该溶液中还可能大量存在的是
A.OH ˉ B.Ba2+ C.Fe3+ D.CO32ˉ
7.2012年6月24日,“蛟龙号”下潜到深海7020米,创造了我国载人深潜新纪录。“蛟龙号”的耐压舱用钛合金制造。下列有关钛原子()的说法正确的是
A.质子数为48 B.中子数为48 C.质量数为22 D.原子序数为22
8.以下物质间的转化不能通过一步反应实现的是
A.HClO → O2 B.SiO2 → H2SiO3 C.CO2→ CaCO3 D.Cu → CuSO4
9.下列关于Fe2O3和 Al2O3性质和用途的说法符合事实的是
A.都可与盐酸反应 B.都可溶于水
C.都常用作耐火材料 D.都可与氢氧化钠溶液反应
10.下列化学用语正确的是
A.CH4的比例模型: B.HCl的电子式:
C.S原子的结构示意图:
D.Fe2(SO4)3的电离方程式:Fe2(SO4)3 =2Fe2+ + 3SO42ˉ
11.设nA为阿伏加德罗常数的值,下列说法正确的是
A.28g N2含有的原子数为nA
B.标准状况下22.4L水中含有的H2O分子数为nA
C.1mol Zn与足量盐酸反应失去的电子数为2 nA
D.0.1L 2mol /L NaCl溶液中含有Na+个数为2 nA
12.甲烷、乙烯是重要的化工原料。下列叙述正确的是
A.可用酸性高锰酸钾溶液来区别甲烷和乙烯 B.甲烷、乙烯是同分异构体
C.甲烷与氯气在光照条件下发生置换反应
D.乙烯与水在一定条件下发生取代反应生成乙醇
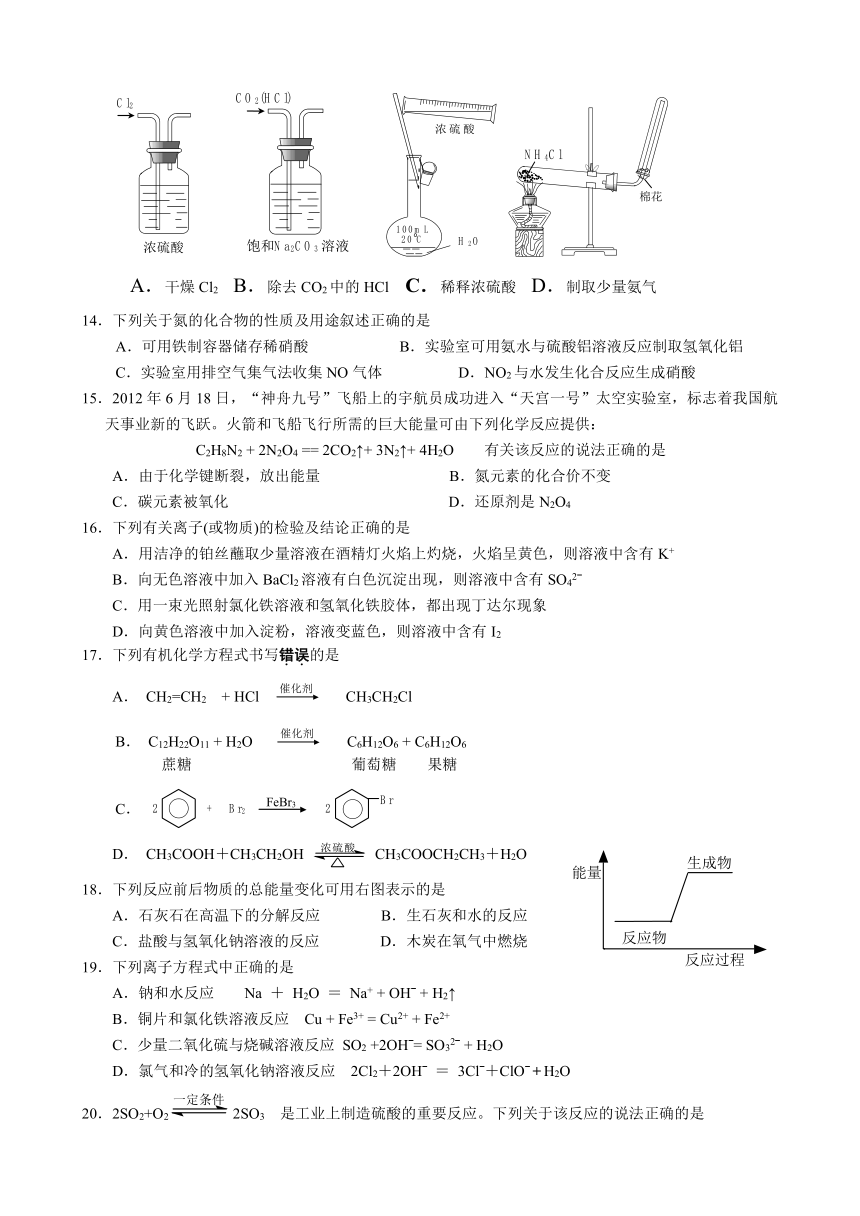
13.下列实验装置、试剂选用或操作正确的是
A.干燥Cl2 B.除去CO2中的HCl C.稀释浓硫酸 D.制取少量氨气
14.下列关于氮的化合物的性质及用途叙述正确的是
A.可用铁制容器储存稀硝酸 B.实验室可用氨水与硫酸铝溶液反应制取氢氧化铝
C.实验室用排空气集气法收集NO气体 D.NO2与水发生化合反应生成硝酸
15.2012年6月18日,“神舟九号” ( http: / / www.21cnjy.com )飞船上的宇航员成功进入“天宫一号”太空实验室,标志着我国航天事业新的飞跃。火箭和飞船飞行所需的巨大能量可由下列化学反应提供:
C2H8N2 + 2N2O4 == 2CO2↑+ 3N2↑+ 4H2O 有关该反应的说法正确的是
A.由于化学键断裂,放出能量 B.氮元素的化合价不变
C.碳元素被氧化 D.还原剂是N2O4
16.下列有关离子(或物质)的检验及结论正确的是
A.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中含有K+
B.向无色溶液中加入BaCl2溶液有白色沉淀出现,则溶液中含有SO42ˉ
C.用一束光照射氯化铁溶液和氢氧化铁胶体,都出现丁达尔现象
D.向黄色溶液中加入淀粉,溶液变蓝色,则溶液中含有I2
17.下列有机化学方程式书写错误的是
A. CH2=CH2 + HCl CH3CH2Cl
B. C12H22O11 + H2O C6H12O6 + C6H12O6
C.
D. CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
18.下列反应前后物质的总能量变化可用右图表示的是
A.石灰石在高温下的分解反应 B.生石灰和水的反应
C.盐酸与氢氧化钠溶液的反应 D.木炭在氧气中燃烧
19.下列离子方程式中正确的是
A.钠和水反应 Na + H2O = Na+ + OHˉ + H2↑
B.铜片和氯化铁溶液反应 Cu + Fe3+ = Cu2+ + Fe2+
C.少量二氧化硫与烧碱溶液反应 SO2 +2OHˉ= SO32ˉ + H2O
D.氯气和冷的氢氧化钠溶液反应 2Cl2+2OHˉ = 3Clˉ+ClOˉ + H2O
20.2SO2+O22SO3 是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是
A.增加O2的浓度能加快反应速率 B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率 D.一定条件下达到反应限度时SO2全部转化为SO3
21.下列关于化学能转化为电能的四种装置的说法正确的是
电池Ⅰ 电池Ⅱ 电池Ⅲ 电池Ⅳ
A.电池Ⅰ中锌是正极 B.电池Ⅱ是一次电池
C.电池Ⅲ工作时,氢气发生还原反应 D.电池Ⅳ工作时,电子由锌通过导线流向碳棒
22.A、B、C、D、E为短周期主族元素, ( http: / / www.21cnjy.com )且原子序数依次增大。A原子的最外层电子数是其电子层数的3倍,B原子的半径在同周期主族元素的原子中最大,A、E同主族,D原子的最高正价与负价的绝对值相等。下列说法正确的是
A.原子半径: D>C B.氢化物的稳定性: E>A
C.氢氧化物的碱性: C>B D.最高价氧化物对应水化物的酸性: E>D
23.在硫酸铝、硫酸和硫酸镁的混合溶液20 ( http: / / www.21cnjy.com )0mL中,c(Al3+) = 0.2mol/L,当加入等体积1.6mol/L KOH溶液时,生成的沉淀最多,再加入过量的KOH溶液后,经过滤、洗涤、干燥,得白色沉淀2.32g。则反应前的混合溶液中c(H2SO4)是
A. 0.20mol/L B.0.30mol/L C.0.40mol/L D.0.60 mol/L
24.(15分)A.《化学与生活》
⑴(3分)促进生态文明,保护生态环境,是实现“中国梦”的重要组成部分。
① 一般垃圾箱上分别会用绿色和黑色字样标有“可回收物”和“其他垃圾”,下图图标表示 ▲ 。 ( http: / / www.21cnjy.com )
② 用明矾处理废水中细小悬浮颗粒的方法属于 ▲ (填字母)。
a.混凝法 b.中和法 c.氧化还原法
③向燃煤中加入石灰石作脱硫剂,可大大减少SO2的排放及酸雨的发生,用这种方法最终可将煤中的硫转化为 ▲ (填化学式)。
⑵(5分)营养平衡、科学使用食品添加剂有助于健康和提高免疫力。
① 医用维生素C片常在药片外包裹一层“糖衣”,其作用除了改善口感外,更重要的作用是 ▲ 。
② 某品牌高钙梳打的配料标 ( http: / / www.21cnjy.com )签如上图所示。在所列配料中,富含糖类的是 ▲ ,植物油在体内水解最终产物是高级脂肪酸和 ▲ 。碳酸钙与胃酸反应的离子方程式为 ▲ 。
⑶(7分)材料的不断发展可以促进社会进步。
① “玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金,选用镁铝合金的优点是 ▲ (任答一点)。
② 生产玻璃时,纯碱与石英反应的化学方程式为
▲ 。碳化硅硬度很大,它属于 ▲ (填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
③ 用于包装食品的塑料袋,应选用 ▲ (填“聚乙烯塑料”或“聚氯乙烯
塑料”),合成该塑料的化学方程式为 ▲ 。
25.(6分)在下图所示的物质转化关系中,A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,且两种元素化合价的绝对值相等。常温下,C、F、K是无色无味的气体单质,D、H是固体单质。E是常见的两性氧化物。B、G是汽车尾气中的主要污染气体,所含元素均为第二周期元素。反应②常用于汽车尾气的处理。
(1)C的电子式 ▲ 。
(2)A的化学式 ▲ 。
(3)反应③的化学方程式 ▲ 。
(4)反应④的离子方程式 ▲ 。
26.(10分)化合物A(其化学式为KxFe(C2O4)y·zH2O,其中铁元素为+3价)是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下:
① 上述流程中,检验“过滤”后的固体已洗涤干净的方法是 ▲ 。
② 上述流程“操作X”中加入H2O2的目的是 ▲ 。
(2)测定化合物A的化学式实验步骤如下:
a、准确称取A样品4.91g,干燥脱水至恒重,残留物质的质量为4.37g;
b、将步骤a所得固体溶于水,加入还原铁粉0.28g,恰好完全反应;
c、另取A样品4.91g置于锥形瓶中, ( http: / / www.21cnjy.com )加入足量的3 mol/L的H2SO4溶液和适量蒸馏水,再加入0.50mol/L的KMnO4溶液24.0 mL,微热,恰好完全反应:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O请通过计算填空:
4.91g A样品中含结晶水的物质的量为 ▲ mol。② A样品中= ▲ 。
③ A的化学式为 ▲ 。
高二化学学业水平测试模拟试题(二)参考答案
单项选择题(本部分23题,每题3分,共69分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
选项 D A B C D C D B A A C A
题号 13 14 15 16 17 18 19 20 21 22 23
选项 A B C D C A C A D D B
24A.《化学与生活》(15分)
⑴①可回收物(1分) ②a(1分) ③CaSO4(1分)
⑵①防止维生素C被氧化(或其他合理表述)(1分)
②小麦粉(1分) 丙三醇(或甘油)(1分)
CaCO3+2H+=Ca2++CO2↑+H2O(2分)
⑶ ①密度小、强度大、耐腐蚀或其它合理答案(1分)
②Na2CO3+SiO2Na2SiO3+CO2↑(2分) b(1分)
③聚乙烯塑料(1分) nCH2=CH2 (2分)
25.(6分)
(1)(1分) (2) AlN(1分)
(3)2Al2O3 4Al+3O2(2分)(4)2Al + 2OHˉ+ 2H2O = 2AlO2ˉ+ 3 H2(2分)
26.(10分)
(1)① 取少量最后一次洗涤液于试管中,滴加BaCl2溶液,无白色沉淀,说明已洗涤干净。(2分)
② 把Fe2+全部氧化成Fe3+(2分,只答“氧化”给1分)
(2)① 0.03 (2分) ② 1:3(2分) ③ K3Fe(C2O4)3·3H2O(2分)
计算过程:n(H2O)=
n(Fe3+)=2n(Fe)=
n(C2O42-)=n(KMnO4)=0.50mol L-10.024L=0.03mol
=1:3
根据离子电荷守恒:n(K+)+3n(Fe3+)=2n (C2O42-) 得n(K+)=0.03mol
因此A为 K3Fe(C2O4)3·3H2O
蔗糖 葡萄糖 果糖
可能用到的相对原子质量 H:1 C:12 N:14 O:16 S:32 Mg:24 Al:27 K:39 Fe:56
一、单项选择题:(本部分23题,每题3分,共69分)
1.燃放烟花爆竹增强春节喜庆,但也造成大气严重污染。烟花中含有的KNO3属于
A.氧化物 B.酸 C. 碱 D.盐
2.下列为人体提供能量的营养物质中,属于高分子化合物的是
A.蛋白质 B.油脂 C.葡萄糖 D.蔗糖
3.从海带中提取碘的实验要用到过滤、萃取实验操作,该两项操作不需要的仪器是
A.烧杯 B.烧瓶 C.玻璃棒 D.分液漏斗
4.下列气体能使品红溶液褪色的是
A.O2 B.CO2 C.SO2 D.CO
5.下列物质属于离子化合物且含有共价键的是
A.HCl B.CaCl2 C.H2O D.NaOH
6.某溶液中存在大量的H+、Clˉ、SO42ˉ,该溶液中还可能大量存在的是
A.OH ˉ B.Ba2+ C.Fe3+ D.CO32ˉ
7.2012年6月24日,“蛟龙号”下潜到深海7020米,创造了我国载人深潜新纪录。“蛟龙号”的耐压舱用钛合金制造。下列有关钛原子()的说法正确的是
A.质子数为48 B.中子数为48 C.质量数为22 D.原子序数为22
8.以下物质间的转化不能通过一步反应实现的是
A.HClO → O2 B.SiO2 → H2SiO3 C.CO2→ CaCO3 D.Cu → CuSO4
9.下列关于Fe2O3和 Al2O3性质和用途的说法符合事实的是
A.都可与盐酸反应 B.都可溶于水
C.都常用作耐火材料 D.都可与氢氧化钠溶液反应
10.下列化学用语正确的是
A.CH4的比例模型: B.HCl的电子式:
C.S原子的结构示意图:
D.Fe2(SO4)3的电离方程式:Fe2(SO4)3 =2Fe2+ + 3SO42ˉ
11.设nA为阿伏加德罗常数的值,下列说法正确的是
A.28g N2含有的原子数为nA
B.标准状况下22.4L水中含有的H2O分子数为nA
C.1mol Zn与足量盐酸反应失去的电子数为2 nA
D.0.1L 2mol /L NaCl溶液中含有Na+个数为2 nA
12.甲烷、乙烯是重要的化工原料。下列叙述正确的是
A.可用酸性高锰酸钾溶液来区别甲烷和乙烯 B.甲烷、乙烯是同分异构体
C.甲烷与氯气在光照条件下发生置换反应
D.乙烯与水在一定条件下发生取代反应生成乙醇
13.下列实验装置、试剂选用或操作正确的是
A.干燥Cl2 B.除去CO2中的HCl C.稀释浓硫酸 D.制取少量氨气
14.下列关于氮的化合物的性质及用途叙述正确的是
A.可用铁制容器储存稀硝酸 B.实验室可用氨水与硫酸铝溶液反应制取氢氧化铝
C.实验室用排空气集气法收集NO气体 D.NO2与水发生化合反应生成硝酸
15.2012年6月18日,“神舟九号” ( http: / / www.21cnjy.com )飞船上的宇航员成功进入“天宫一号”太空实验室,标志着我国航天事业新的飞跃。火箭和飞船飞行所需的巨大能量可由下列化学反应提供:
C2H8N2 + 2N2O4 == 2CO2↑+ 3N2↑+ 4H2O 有关该反应的说法正确的是
A.由于化学键断裂,放出能量 B.氮元素的化合价不变
C.碳元素被氧化 D.还原剂是N2O4
16.下列有关离子(或物质)的检验及结论正确的是
A.用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,则溶液中含有K+
B.向无色溶液中加入BaCl2溶液有白色沉淀出现,则溶液中含有SO42ˉ
C.用一束光照射氯化铁溶液和氢氧化铁胶体,都出现丁达尔现象
D.向黄色溶液中加入淀粉,溶液变蓝色,则溶液中含有I2
17.下列有机化学方程式书写错误的是
A. CH2=CH2 + HCl CH3CH2Cl
B. C12H22O11 + H2O C6H12O6 + C6H12O6
C.
D. CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O
18.下列反应前后物质的总能量变化可用右图表示的是
A.石灰石在高温下的分解反应 B.生石灰和水的反应
C.盐酸与氢氧化钠溶液的反应 D.木炭在氧气中燃烧
19.下列离子方程式中正确的是
A.钠和水反应 Na + H2O = Na+ + OHˉ + H2↑
B.铜片和氯化铁溶液反应 Cu + Fe3+ = Cu2+ + Fe2+
C.少量二氧化硫与烧碱溶液反应 SO2 +2OHˉ= SO32ˉ + H2O
D.氯气和冷的氢氧化钠溶液反应 2Cl2+2OHˉ = 3Clˉ+ClOˉ + H2O
20.2SO2+O22SO3 是工业上制造硫酸的重要反应。下列关于该反应的说法正确的是
A.增加O2的浓度能加快反应速率 B.降低体系温度能加快反应速率
C.使用催化剂不影响反应速率 D.一定条件下达到反应限度时SO2全部转化为SO3
21.下列关于化学能转化为电能的四种装置的说法正确的是
电池Ⅰ 电池Ⅱ 电池Ⅲ 电池Ⅳ
A.电池Ⅰ中锌是正极 B.电池Ⅱ是一次电池
C.电池Ⅲ工作时,氢气发生还原反应 D.电池Ⅳ工作时,电子由锌通过导线流向碳棒
22.A、B、C、D、E为短周期主族元素, ( http: / / www.21cnjy.com )且原子序数依次增大。A原子的最外层电子数是其电子层数的3倍,B原子的半径在同周期主族元素的原子中最大,A、E同主族,D原子的最高正价与负价的绝对值相等。下列说法正确的是
A.原子半径: D>C B.氢化物的稳定性: E>A
C.氢氧化物的碱性: C>B D.最高价氧化物对应水化物的酸性: E>D
23.在硫酸铝、硫酸和硫酸镁的混合溶液20 ( http: / / www.21cnjy.com )0mL中,c(Al3+) = 0.2mol/L,当加入等体积1.6mol/L KOH溶液时,生成的沉淀最多,再加入过量的KOH溶液后,经过滤、洗涤、干燥,得白色沉淀2.32g。则反应前的混合溶液中c(H2SO4)是
A. 0.20mol/L B.0.30mol/L C.0.40mol/L D.0.60 mol/L
24.(15分)A.《化学与生活》
⑴(3分)促进生态文明,保护生态环境,是实现“中国梦”的重要组成部分。
① 一般垃圾箱上分别会用绿色和黑色字样标有“可回收物”和“其他垃圾”,下图图标表示 ▲ 。 ( http: / / www.21cnjy.com )
② 用明矾处理废水中细小悬浮颗粒的方法属于 ▲ (填字母)。
a.混凝法 b.中和法 c.氧化还原法
③向燃煤中加入石灰石作脱硫剂,可大大减少SO2的排放及酸雨的发生,用这种方法最终可将煤中的硫转化为 ▲ (填化学式)。
⑵(5分)营养平衡、科学使用食品添加剂有助于健康和提高免疫力。
① 医用维生素C片常在药片外包裹一层“糖衣”,其作用除了改善口感外,更重要的作用是 ▲ 。
② 某品牌高钙梳打的配料标 ( http: / / www.21cnjy.com )签如上图所示。在所列配料中,富含糖类的是 ▲ ,植物油在体内水解最终产物是高级脂肪酸和 ▲ 。碳酸钙与胃酸反应的离子方程式为 ▲ 。
⑶(7分)材料的不断发展可以促进社会进步。
① “玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金,选用镁铝合金的优点是 ▲ (任答一点)。
② 生产玻璃时,纯碱与石英反应的化学方程式为
▲ 。碳化硅硬度很大,它属于 ▲ (填字母)。
a.金属材料 b.无机非金属材料 c.有机高分子材料
③ 用于包装食品的塑料袋,应选用 ▲ (填“聚乙烯塑料”或“聚氯乙烯
塑料”),合成该塑料的化学方程式为 ▲ 。
25.(6分)在下图所示的物质转化关系中,A是用于制造汽车发动机的耐高温陶瓷材料,A由两种元素组成,且两种元素化合价的绝对值相等。常温下,C、F、K是无色无味的气体单质,D、H是固体单质。E是常见的两性氧化物。B、G是汽车尾气中的主要污染气体,所含元素均为第二周期元素。反应②常用于汽车尾气的处理。
(1)C的电子式 ▲ 。
(2)A的化学式 ▲ 。
(3)反应③的化学方程式 ▲ 。
(4)反应④的离子方程式 ▲ 。
26.(10分)化合物A(其化学式为KxFe(C2O4)y·zH2O,其中铁元素为+3价)是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下:
① 上述流程中,检验“过滤”后的固体已洗涤干净的方法是 ▲ 。
② 上述流程“操作X”中加入H2O2的目的是 ▲ 。
(2)测定化合物A的化学式实验步骤如下:
a、准确称取A样品4.91g,干燥脱水至恒重,残留物质的质量为4.37g;
b、将步骤a所得固体溶于水,加入还原铁粉0.28g,恰好完全反应;
c、另取A样品4.91g置于锥形瓶中, ( http: / / www.21cnjy.com )加入足量的3 mol/L的H2SO4溶液和适量蒸馏水,再加入0.50mol/L的KMnO4溶液24.0 mL,微热,恰好完全反应:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O请通过计算填空:
4.91g A样品中含结晶水的物质的量为 ▲ mol。② A样品中= ▲ 。
③ A的化学式为 ▲ 。
高二化学学业水平测试模拟试题(二)参考答案
单项选择题(本部分23题,每题3分,共69分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
选项 D A B C D C D B A A C A
题号 13 14 15 16 17 18 19 20 21 22 23
选项 A B C D C A C A D D B
24A.《化学与生活》(15分)
⑴①可回收物(1分) ②a(1分) ③CaSO4(1分)
⑵①防止维生素C被氧化(或其他合理表述)(1分)
②小麦粉(1分) 丙三醇(或甘油)(1分)
CaCO3+2H+=Ca2++CO2↑+H2O(2分)
⑶ ①密度小、强度大、耐腐蚀或其它合理答案(1分)
②Na2CO3+SiO2Na2SiO3+CO2↑(2分) b(1分)
③聚乙烯塑料(1分) nCH2=CH2 (2分)
25.(6分)
(1)(1分) (2) AlN(1分)
(3)2Al2O3 4Al+3O2(2分)(4)2Al + 2OHˉ+ 2H2O = 2AlO2ˉ+ 3 H2(2分)
26.(10分)
(1)① 取少量最后一次洗涤液于试管中,滴加BaCl2溶液,无白色沉淀,说明已洗涤干净。(2分)
② 把Fe2+全部氧化成Fe3+(2分,只答“氧化”给1分)
(2)① 0.03 (2分) ② 1:3(2分) ③ K3Fe(C2O4)3·3H2O(2分)
计算过程:n(H2O)=
n(Fe3+)=2n(Fe)=
n(C2O42-)=n(KMnO4)=0.50mol L-10.024L=0.03mol
=1:3
根据离子电荷守恒:n(K+)+3n(Fe3+)=2n (C2O42-) 得n(K+)=0.03mol
因此A为 K3Fe(C2O4)3·3H2O
蔗糖 葡萄糖 果糖
同课章节目录
