第九单元溶液复习试题(含答案)---2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第九单元溶液复习试题(含答案)---2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 249.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-23 00:00:00 | ||
图片预览


文档简介
人教版化学九年级下册第九单元《溶液》复习试题
一.选择题(共15小题)
1.现有200g硝酸钠的不饱和溶液,若再加入10g硝酸钠或蒸发掉20g水,都恰好使溶液达到饱和,则原200g硝酸钠溶液中溶质的质量分数为( )
A.5% B.15% C.30% D.60%
2.现有编号为①、②、③的三个烧杯中均分别盛有100克水,20℃时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示。下列判断正确的是( )
A.①中所得溶液一定是不饱和溶液 B.②③中所得溶液溶质的质量分数相等
C.若②中溶液升温到30℃,溶液的质量一定变大 D.若③中溶液恒温蒸发,溶质的质量分数一定变大
3.少量下列物质放入水中充分搅拌后不能形成溶液的是( )
A.蔗糖 B.食盐 C.白醋 D.花生油
4.溶液与人们的生活息息相关,下列有关溶液的说法中,正确的是( )
A.溶液一定是无色的,且溶剂一定是水 B.凡是均一的、稳定的液体一定是溶液
C.质量分数为20%的某溶液,其中溶质与溶剂的质量比为1:5 D.汽油去除油污,是利用了溶解作用
5.下列物质溶于水后温度明显升高的是( )
A.氢氧化钠 B.硝酸铵 C.食盐 D.蔗糖
6.向100g溶质质量分数为20%的硝酸钾溶液中加入3g硝酸钾固体和12g水,使其完全溶解,所得溶液中溶质的质量分数是( )
A.20% B.22.5% C.25% D.30%
7.关于饱和溶液和不饱和溶液的有关说法正确的是( )
A.只要是饱和溶液就不能继续溶解任何溶质
B.降温一定能使接近饱和的溶液变成饱和溶液
C.加水可以使饱和溶液变成不饱和溶液
D.饱和溶液的浓度一定比不饱和溶液大
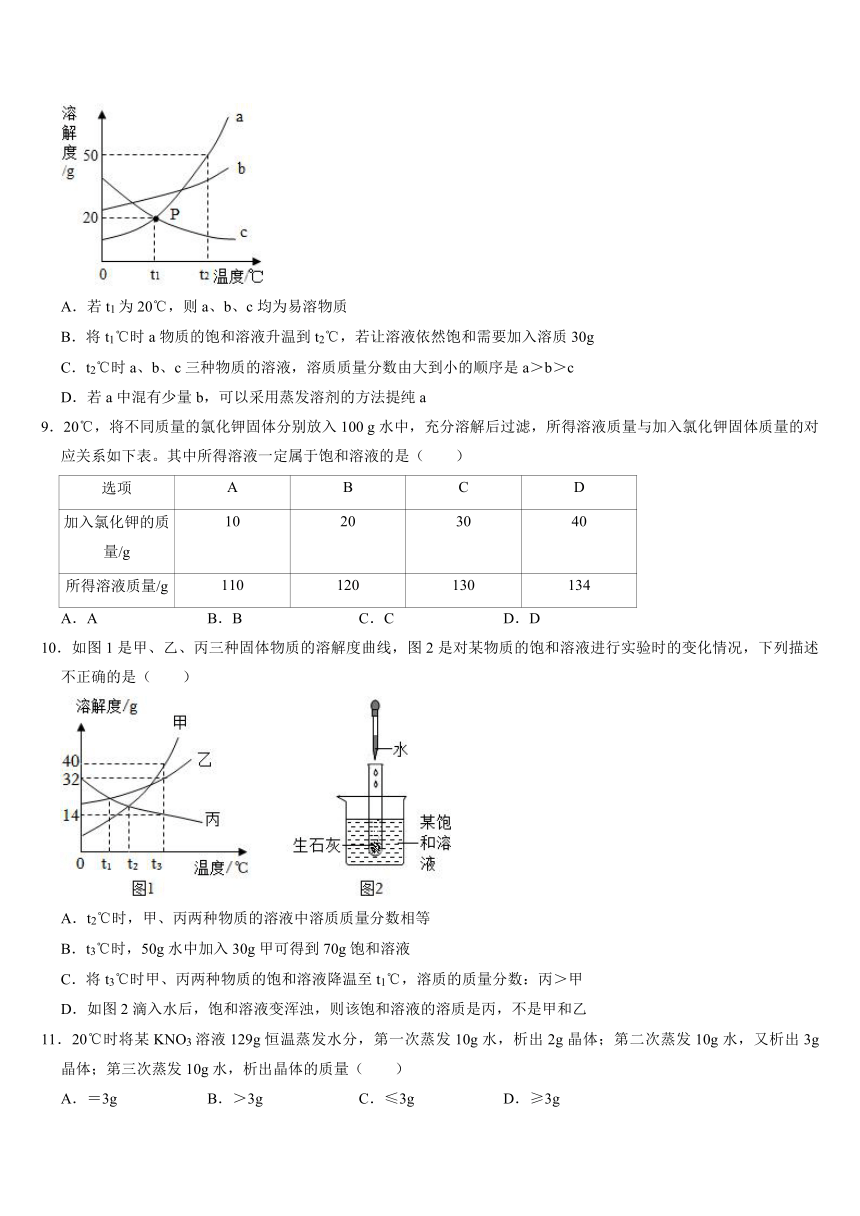
8.如图是a、b、c三种固体物质的溶解度曲线,下列叙述正确的是( )
A.若t1为20℃,则a、b、c均为易溶物质
B.将t1℃时a物质的饱和溶液升温到t2℃,若让溶液依然饱和需要加入溶质30g
C.t2℃时a、b、c三种物质的溶液,溶质质量分数由大到小的顺序是a>b>c
D.若a中混有少量b,可以采用蒸发溶剂的方法提纯a
9.20℃,将不同质量的氯化钾固体分别放入100 g水中,充分溶解后过滤,所得溶液质量与加入氯化钾固体质量的对应关系如下表。其中所得溶液一定属于饱和溶液的是( )
选项 A B C D
加入氯化钾的质量/g 10 20 30 40
所得溶液质量/g 110 120 130 134
A.A B.B C.C D.D
10.如图1是甲、乙、丙三种固体物质的溶解度曲线,图2是对某物质的饱和溶液进行实验时的变化情况,下列描述不正确的是( )
A.t2℃时,甲、丙两种物质的溶液中溶质质量分数相等
B.t3℃时,50g水中加入30g甲可得到70g饱和溶液
C.将t3℃时甲、丙两种物质的饱和溶液降温至t1℃,溶质的质量分数:丙>甲
D.如图2滴入水后,饱和溶液变浑浊,则该饱和溶液的溶质是丙,不是甲和乙
11.20℃时将某KNO3溶液129g恒温蒸发水分,第一次蒸发10g水,析出2g晶体;第二次蒸发10g水,又析出3g晶体;第三次蒸发10g水,析出晶体的质量( )
A.=3g B.>3g C.≤3g D.≥3g
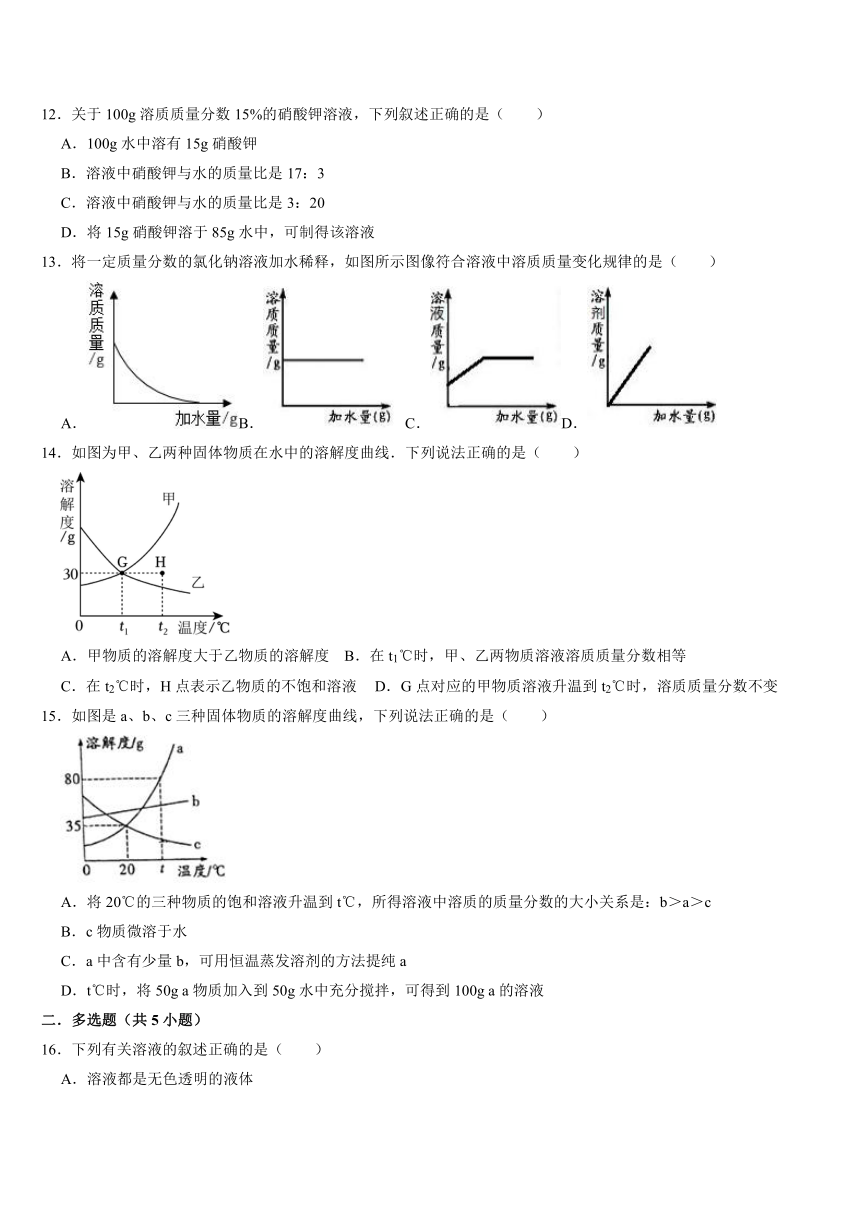
12.关于100g溶质质量分数15%的硝酸钾溶液,下列叙述正确的是( )
A.100g水中溶有15g硝酸钾
B.溶液中硝酸钾与水的质量比是17:3
C.溶液中硝酸钾与水的质量比是3:20
D.将15g硝酸钾溶于85g水中,可制得该溶液
13.将一定质量分数的氯化钠溶液加水稀释,如图所示图像符合溶液中溶质质量变化规律的是( )
A.B. C.D.
14.如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度 B.在t1℃时,甲、乙两物质溶液溶质质量分数相等
C.在t2℃时,H点表示乙物质的不饱和溶液 D.G点对应的甲物质溶液升温到t2℃时,溶质质量分数不变
15.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
A.将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a>c
B.c物质微溶于水
C.a中含有少量b,可用恒温蒸发溶剂的方法提纯a
D.t℃时,将50g a物质加入到50g水中充分搅拌,可得到100g a的溶液
二.多选题(共5小题)
16.下列有关溶液的叙述正确的是( )
A.溶液都是无色透明的液体
B.溶液都是均一稳定的混合物
C.溶质可以是固、液和气态,溶剂一定是水
D.某些固体物质溶于水后凝固点会降低
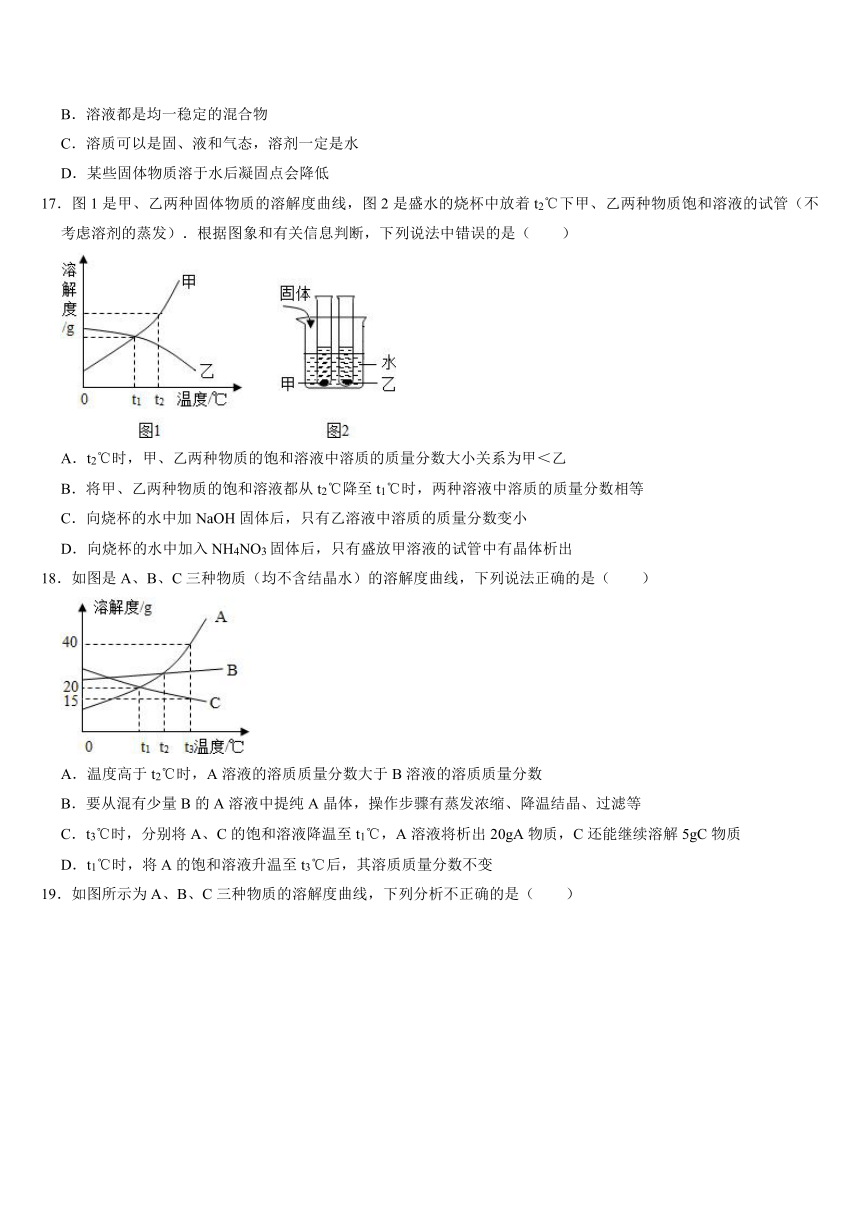
17.图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发).根据图象和有关信息判断,下列说法中错误的是( )
A.t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲<乙
B.将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,两种溶液中溶质的质量分数相等
C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D.向烧杯的水中加入NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出
18.如图是A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A.温度高于t2℃时,A溶液的溶质质量分数大于B溶液的溶质质量分数
B.要从混有少量B的A溶液中提纯A晶体,操作步骤有蒸发浓缩、降温结晶、过滤等
C.t3℃时,分别将A、C的饱和溶液降温至t1℃,A溶液将析出20gA物质,C还能继续溶解5gC物质
D.t1℃时,将A的饱和溶液升温至t3℃后,其溶质质量分数不变
19.如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
A.20℃时,A、B、C三种物质的溶解度由大到小的顺序是B<A=C
B.50℃时,把50gA放入50g水中能得到A的饱和溶液
C.将C的饱和溶液变为不饱和溶液,可采用降温的方法
D.将50℃时A、B、C三种物质的饱和溶液降温到20℃时,所得溶液的溶质质量分数的大小关系是B>C=A
20.如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )
A.50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C
B.50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶液的质量比为1:2
C.将C的饱和溶液变为不饱和溶液,采用降温结晶方法
D.将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A>C
三.填空题(共5小题)
21.A、B、C三种固体的溶解度曲线如图所示,请回答下列问题:
(1)P点表示的含义是 。
(2)在50℃时,将40gA物质投入到50g水中,形成溶液的质量为 g。
(3)A物质中混有少量的B物质,若提纯A物质,可采取的结晶方法是 。
22.识别图像是学习化学的必备能力。室温时,将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,均有固体剩余,如图一所示,剩余固体物质的质量与温度的关系如图二所示。
(1)甲的溶解度随温度升高而 (选填“增大”或“减小”)。
(2)t1℃时,乙的溶解度为 g。若t1℃时将25g乙物质加入50g水中,形成溶液质量是 g,溶质质量分数是 (精确到0.1%)。
(3)室温时,将两烧杯中的物质倒入另一个大烧杯中,充分搅拌后,可得到甲、乙两种物质的 (选填“饱和”或“不饱和)溶液。
(4)a、b、c三点溶液中溶质的质量分数由大到小的顺序是 。
23.下表是甲、乙两种物质在不同温度时的溶解度,根据此表回答问题:
温度/℃ 20 40 50 60 80
溶解度/g 甲 110 117 121 126 139
乙 31.6 63.9 85.5 110 169
(1)60℃时,乙的饱和溶液中溶质与溶剂的质量比为 (填最简整数比)。
(2)某同学取甲、乙中的一种物质(表示为W)进行如图实验:
W代表的物质是 ;②中未溶解的固体为 g;③中的溶液是 (填“饱和”或“不饱和”)溶液。
24.如图是A、B、C三种固体物质(均不含结晶水)的溶解度曲线图。请回答:
(1)气体溶解度随温度的变化规律与 (填“B”或“C”)物质的溶解度曲线相似。
(2)若使A、B、C的饱和溶液都能析出晶体,可选择的同一种方法是 。
(3)关于图1的说法中不正确的是 (填字母)。
A.t1℃时,将10gA物质加入50g水中,所得为t1℃下A的饱和溶液
B.将t1℃的三种物质的饱和溶液升温至t2℃,溶质的质量分数大小关系为B>A=C
C.将t2℃时三种物质的饱和溶液恒温蒸发等质量的水,析出晶体质量最多的是A
(4)甲烧杯中为t2℃时的A的溶液(其中含120g水),经图2所示过程最终得到10gA固体。
经分析:甲烧杯中溶液质量为 g;若将烧杯丙加热至t2℃,至少需加入 gA物质,才能恰好得到饱和溶液。
25.如表是某物质M的部分溶解度数据。
温度/℃ 0 20 30 40 50 60 80 100
溶解度/g 7 21.8 39.7 48.8 47.3 46.4 45.1 44.7
(1)由表中数据可知,M属于 (填“易溶”“可溶”或“微溶”)物质。由表中数据可知,M的溶解度随温度升高 。
(2)40℃时,74.4gM的饱和溶液中,溶质的质量为 g。
(3)在20℃时,将30gM加入盛有100g水的烧杯中,实验过程如图(水的蒸发忽略不计)。
根据如图实验过程及现象分析,x的取值范围是 ;A、B、C溶液中,溶质的质量分数由大到小的顺序是 (用字母表示)。
四.实验题(共3小题)
26.同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液,整个操作如图所示:
(1)配制100g溶质质量分数为10%的氯化钠溶液,所需氯化钠 g,需要水的质量为 g。
(2)溶解时玻璃棒的作用为 。
(3)上述步骤的正确顺序为 (填序号),请改正步骤②中的一处明显错误 。
(4)若利用配制的10%的氯化钠溶液加水稀释成100g溶质质量分数为5%的氯化钠溶液,则需要10%的氯化钠溶液 g,加水 g。
(5)将氯化钠和水依次倒入烧杯中,若倾倒时有少量水溅出,会导致所配制溶液的溶质质量分数 (选填“偏大”“偏小”“无影响”)。
27.硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组的同学进行了如图2所示的实验。
(1)t1℃时,将30g氯化铵固体溶解在50g水中,形成溶液的质量是 g。
(2)②的溶液中溶质质量分数为 (只列出表达式)。
(3)若要提纯含有少量氯化铵的硝酸钾时,应用 (填“降温结晶”或“蒸发结晶”)方法
(4)关于图2中烧杯内的物质,以下几种说法正确的有 (填序号)。
A.①、②、③中,只有③中上层清液是饱和溶液
B.若使③中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数大
五.计算题(共2小题)
28.如表是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,阅读后计算:
浓硫酸(H2SO4)500毫升
浓度(质量分数) 98%
密度 1.84克/厘米3
相对分子质量 98
强腐蚀性,阴冷,密封贮藏
(1)欲配制600克溶质质量分数为19.6%的稀硫酸,需要这种浓硫酸多少克?再加水多少毫升?
(2)50克浓度为98%的浓硫酸与150克水混合后所得溶液的质量分数为多少?
29.可乐是青少年特别喜爱的一种饮料,但是可乐含糖量较高,经常饮用会引发肥胖,还有可能引起龋齿、糖尿病等。国际卫生组织建议人体每日摄入糖的量不应超过50克。已知一瓶550mL的可乐含有54克糖,请根据材料回答问题。
(1)喝上几口冰镇可乐往往会打嗝,根据如图分析其主要原因是 ;
(2)求550毫升可乐中糖的质量分数(该可乐溶液的密度约为1g/cm3);
(3)可乐主要由糖水和碳酸水按一定比例混合而成。现用含糖量10%的可乐,配制含糖量5%的低糖可乐300克,需要10%的可乐多少克?需加水的质量多少克?
参考答案
一.选择题(共15小题)
1.C。
2.B。
3.D。
4.D。
5.A。
6.A。
7.C。
8.A。
9.D。
10.A。
11.A。
12.D。
13.B。
14.D。
15.A。
二.多选题(共5小题)
16.BD。
17.AB。
18.BD。
19.AD。
20.AD。
三.填空题(共5小题)
21.(1)50℃时,A、B两物质的溶解度相等;
(2)70;
(3)降温结晶。
22.(1)减小;
(2)40;70;28.6%;
(3)不饱和;
(4)c>a>b。
23.(1)11:10。
(2)甲;11;不饱和溶液。
24.(1)C;
(2)蒸发;
(3)B;
(4)150;20。
25.
(1)易溶;先增大后减小;
(2)24.4;
(3)16.4<x≤18.8;C>B>A。
四.实验题(共3小题)
26.同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液,整个操作如图所示:
(1)配制100g溶质质量分数为10%的氯化钠溶液,所需氯化钠 10 g,需要水的质量为 90 g。
(2)溶解时玻璃棒的作用为 搅拌,加速溶解 。
(3)上述步骤的正确顺序为 ④②①⑤③ (填序号),请改正步骤②中的一处明显错误 将氯化钠放在天平左盘称量 。
(4)若利用配制的10%的氯化钠溶液加水稀释成100g溶质质量分数为5%的氯化钠溶液,则需要10%的氯化钠溶液 50 g,加水 50 g。
(5)将氯化钠和水依次倒入烧杯中,若倾倒时有少量水溅出,会导致所配制溶液的溶质质量分数 偏大 (选填“偏大”“偏小”“无影响”)。
【解答】解:(1)10;90;
(2)搅拌,加速溶解;
(3)④②①⑤③;将氯化钠放在天平左盘称量;
(4)50;50;
(5)偏大。
27.(1)70;
(2);
(3)降温结晶;
(4)BC。
五.计算题(共2小题)
28.解:(1)设需要这种硫酸的质量为x,则x×98%=600g×19.6%,解得x=120g;需要水的质量为600g﹣120g=480g,体积为=480mL。
(2)溶液稀释前后,溶质的质量不变,50克浓度为98%的浓硫酸与150克水混合后所得溶液的质量分数为×100%=24.5%。
答:(1)需要这种浓硫酸120g,再加水480mL;
(2)50克浓度为98%的浓硫酸与150克水混合后所得溶液的质量分数为24.5%。
29.解:(1)人体内温度较高,二氧化碳的溶解度随温度的上升而下降,二氧化碳逸出。
故答案为:温度升高,二氧化碳的溶解度减小,有二氧化碳逸出。
(2)溶液的质量为550mL×1g/cm3=550g。
糖的质量分数是=×100%≈9.8%。
(3)设需用10%的糖水质量为x,根据溶液稀释前后溶质的质量不变,则10%x=300g×10%,x=150g。
水的质量=300g﹣150g=150g。
故答案为:
答:(2)550毫升可乐中糖的质量分数为9.8%;
(3)需要10%的150g,需加水的质量150g。
声明:试题解析著作权属所有,未经书面同意,不得复制发布日期:2024/4/22 22:03:07;用户:马丹;邮箱:18845904881;学号:49967352
一.选择题(共15小题)
1.现有200g硝酸钠的不饱和溶液,若再加入10g硝酸钠或蒸发掉20g水,都恰好使溶液达到饱和,则原200g硝酸钠溶液中溶质的质量分数为( )
A.5% B.15% C.30% D.60%
2.现有编号为①、②、③的三个烧杯中均分别盛有100克水,20℃时向三个烧杯中分别加入36克、56克、76克的同种物质,充分溶解,实验结果如图所示。下列判断正确的是( )
A.①中所得溶液一定是不饱和溶液 B.②③中所得溶液溶质的质量分数相等
C.若②中溶液升温到30℃,溶液的质量一定变大 D.若③中溶液恒温蒸发,溶质的质量分数一定变大
3.少量下列物质放入水中充分搅拌后不能形成溶液的是( )
A.蔗糖 B.食盐 C.白醋 D.花生油
4.溶液与人们的生活息息相关,下列有关溶液的说法中,正确的是( )
A.溶液一定是无色的,且溶剂一定是水 B.凡是均一的、稳定的液体一定是溶液
C.质量分数为20%的某溶液,其中溶质与溶剂的质量比为1:5 D.汽油去除油污,是利用了溶解作用
5.下列物质溶于水后温度明显升高的是( )
A.氢氧化钠 B.硝酸铵 C.食盐 D.蔗糖
6.向100g溶质质量分数为20%的硝酸钾溶液中加入3g硝酸钾固体和12g水,使其完全溶解,所得溶液中溶质的质量分数是( )
A.20% B.22.5% C.25% D.30%
7.关于饱和溶液和不饱和溶液的有关说法正确的是( )
A.只要是饱和溶液就不能继续溶解任何溶质
B.降温一定能使接近饱和的溶液变成饱和溶液
C.加水可以使饱和溶液变成不饱和溶液
D.饱和溶液的浓度一定比不饱和溶液大
8.如图是a、b、c三种固体物质的溶解度曲线,下列叙述正确的是( )
A.若t1为20℃,则a、b、c均为易溶物质
B.将t1℃时a物质的饱和溶液升温到t2℃,若让溶液依然饱和需要加入溶质30g
C.t2℃时a、b、c三种物质的溶液,溶质质量分数由大到小的顺序是a>b>c
D.若a中混有少量b,可以采用蒸发溶剂的方法提纯a
9.20℃,将不同质量的氯化钾固体分别放入100 g水中,充分溶解后过滤,所得溶液质量与加入氯化钾固体质量的对应关系如下表。其中所得溶液一定属于饱和溶液的是( )
选项 A B C D
加入氯化钾的质量/g 10 20 30 40
所得溶液质量/g 110 120 130 134
A.A B.B C.C D.D
10.如图1是甲、乙、丙三种固体物质的溶解度曲线,图2是对某物质的饱和溶液进行实验时的变化情况,下列描述不正确的是( )
A.t2℃时,甲、丙两种物质的溶液中溶质质量分数相等
B.t3℃时,50g水中加入30g甲可得到70g饱和溶液
C.将t3℃时甲、丙两种物质的饱和溶液降温至t1℃,溶质的质量分数:丙>甲
D.如图2滴入水后,饱和溶液变浑浊,则该饱和溶液的溶质是丙,不是甲和乙
11.20℃时将某KNO3溶液129g恒温蒸发水分,第一次蒸发10g水,析出2g晶体;第二次蒸发10g水,又析出3g晶体;第三次蒸发10g水,析出晶体的质量( )
A.=3g B.>3g C.≤3g D.≥3g
12.关于100g溶质质量分数15%的硝酸钾溶液,下列叙述正确的是( )
A.100g水中溶有15g硝酸钾
B.溶液中硝酸钾与水的质量比是17:3
C.溶液中硝酸钾与水的质量比是3:20
D.将15g硝酸钾溶于85g水中,可制得该溶液
13.将一定质量分数的氯化钠溶液加水稀释,如图所示图像符合溶液中溶质质量变化规律的是( )
A.B. C.D.
14.如图为甲、乙两种固体物质在水中的溶解度曲线.下列说法正确的是( )
A.甲物质的溶解度大于乙物质的溶解度 B.在t1℃时,甲、乙两物质溶液溶质质量分数相等
C.在t2℃时,H点表示乙物质的不饱和溶液 D.G点对应的甲物质溶液升温到t2℃时,溶质质量分数不变
15.如图是a、b、c三种固体物质的溶解度曲线,下列说法正确的是( )
A.将20℃的三种物质的饱和溶液升温到t℃,所得溶液中溶质的质量分数的大小关系是:b>a>c
B.c物质微溶于水
C.a中含有少量b,可用恒温蒸发溶剂的方法提纯a
D.t℃时,将50g a物质加入到50g水中充分搅拌,可得到100g a的溶液
二.多选题(共5小题)
16.下列有关溶液的叙述正确的是( )
A.溶液都是无色透明的液体
B.溶液都是均一稳定的混合物
C.溶质可以是固、液和气态,溶剂一定是水
D.某些固体物质溶于水后凝固点会降低
17.图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发).根据图象和有关信息判断,下列说法中错误的是( )
A.t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲<乙
B.将甲、乙两种物质的饱和溶液都从t2℃降至t1℃时,两种溶液中溶质的质量分数相等
C.向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D.向烧杯的水中加入NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出
18.如图是A、B、C三种物质(均不含结晶水)的溶解度曲线,下列说法正确的是( )
A.温度高于t2℃时,A溶液的溶质质量分数大于B溶液的溶质质量分数
B.要从混有少量B的A溶液中提纯A晶体,操作步骤有蒸发浓缩、降温结晶、过滤等
C.t3℃时,分别将A、C的饱和溶液降温至t1℃,A溶液将析出20gA物质,C还能继续溶解5gC物质
D.t1℃时,将A的饱和溶液升温至t3℃后,其溶质质量分数不变
19.如图所示为A、B、C三种物质的溶解度曲线,下列分析不正确的是( )
A.20℃时,A、B、C三种物质的溶解度由大到小的顺序是B<A=C
B.50℃时,把50gA放入50g水中能得到A的饱和溶液
C.将C的饱和溶液变为不饱和溶液,可采用降温的方法
D.将50℃时A、B、C三种物质的饱和溶液降温到20℃时,所得溶液的溶质质量分数的大小关系是B>C=A
20.如图是A、B、C三种物质的溶解度曲线,下列分析正确的是( )
A.50℃时A、B、C三种物质的溶解度由大到小的顺序是A>B>C
B.50℃时把50gA放入50g水中能得到A的饱和溶液,其中溶质与溶液的质量比为1:2
C.将C的饱和溶液变为不饱和溶液,采用降温结晶方法
D.将50℃时A、B、C三种物质的饱和溶液降温至20℃时,这三种溶液的溶质质量分数的大小关系是B>A>C
三.填空题(共5小题)
21.A、B、C三种固体的溶解度曲线如图所示,请回答下列问题:
(1)P点表示的含义是 。
(2)在50℃时,将40gA物质投入到50g水中,形成溶液的质量为 g。
(3)A物质中混有少量的B物质,若提纯A物质,可采取的结晶方法是 。
22.识别图像是学习化学的必备能力。室温时,将质量均为30g的甲、乙两种固体分别加入到50g水中,充分搅拌后,均有固体剩余,如图一所示,剩余固体物质的质量与温度的关系如图二所示。
(1)甲的溶解度随温度升高而 (选填“增大”或“减小”)。
(2)t1℃时,乙的溶解度为 g。若t1℃时将25g乙物质加入50g水中,形成溶液质量是 g,溶质质量分数是 (精确到0.1%)。
(3)室温时,将两烧杯中的物质倒入另一个大烧杯中,充分搅拌后,可得到甲、乙两种物质的 (选填“饱和”或“不饱和)溶液。
(4)a、b、c三点溶液中溶质的质量分数由大到小的顺序是 。
23.下表是甲、乙两种物质在不同温度时的溶解度,根据此表回答问题:
温度/℃ 20 40 50 60 80
溶解度/g 甲 110 117 121 126 139
乙 31.6 63.9 85.5 110 169
(1)60℃时,乙的饱和溶液中溶质与溶剂的质量比为 (填最简整数比)。
(2)某同学取甲、乙中的一种物质(表示为W)进行如图实验:
W代表的物质是 ;②中未溶解的固体为 g;③中的溶液是 (填“饱和”或“不饱和”)溶液。
24.如图是A、B、C三种固体物质(均不含结晶水)的溶解度曲线图。请回答:
(1)气体溶解度随温度的变化规律与 (填“B”或“C”)物质的溶解度曲线相似。
(2)若使A、B、C的饱和溶液都能析出晶体,可选择的同一种方法是 。
(3)关于图1的说法中不正确的是 (填字母)。
A.t1℃时,将10gA物质加入50g水中,所得为t1℃下A的饱和溶液
B.将t1℃的三种物质的饱和溶液升温至t2℃,溶质的质量分数大小关系为B>A=C
C.将t2℃时三种物质的饱和溶液恒温蒸发等质量的水,析出晶体质量最多的是A
(4)甲烧杯中为t2℃时的A的溶液(其中含120g水),经图2所示过程最终得到10gA固体。
经分析:甲烧杯中溶液质量为 g;若将烧杯丙加热至t2℃,至少需加入 gA物质,才能恰好得到饱和溶液。
25.如表是某物质M的部分溶解度数据。
温度/℃ 0 20 30 40 50 60 80 100
溶解度/g 7 21.8 39.7 48.8 47.3 46.4 45.1 44.7
(1)由表中数据可知,M属于 (填“易溶”“可溶”或“微溶”)物质。由表中数据可知,M的溶解度随温度升高 。
(2)40℃时,74.4gM的饱和溶液中,溶质的质量为 g。
(3)在20℃时,将30gM加入盛有100g水的烧杯中,实验过程如图(水的蒸发忽略不计)。
根据如图实验过程及现象分析,x的取值范围是 ;A、B、C溶液中,溶质的质量分数由大到小的顺序是 (用字母表示)。
四.实验题(共3小题)
26.同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液,整个操作如图所示:
(1)配制100g溶质质量分数为10%的氯化钠溶液,所需氯化钠 g,需要水的质量为 g。
(2)溶解时玻璃棒的作用为 。
(3)上述步骤的正确顺序为 (填序号),请改正步骤②中的一处明显错误 。
(4)若利用配制的10%的氯化钠溶液加水稀释成100g溶质质量分数为5%的氯化钠溶液,则需要10%的氯化钠溶液 g,加水 g。
(5)将氯化钠和水依次倒入烧杯中,若倾倒时有少量水溅出,会导致所配制溶液的溶质质量分数 (选填“偏大”“偏小”“无影响”)。
27.硝酸钾和氯化铵的溶解度曲线如图1所示,某化学兴趣小组的同学进行了如图2所示的实验。
(1)t1℃时,将30g氯化铵固体溶解在50g水中,形成溶液的质量是 g。
(2)②的溶液中溶质质量分数为 (只列出表达式)。
(3)若要提纯含有少量氯化铵的硝酸钾时,应用 (填“降温结晶”或“蒸发结晶”)方法
(4)关于图2中烧杯内的物质,以下几种说法正确的有 (填序号)。
A.①、②、③中,只有③中上层清液是饱和溶液
B.若使③中的固体溶解,可采用加水或升温的方法
C.①和②的溶液中,溶质质量相等
D.①的溶液中溶质质量分数一定比③的上层清液中溶质质量分数大
五.计算题(共2小题)
28.如表是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,阅读后计算:
浓硫酸(H2SO4)500毫升
浓度(质量分数) 98%
密度 1.84克/厘米3
相对分子质量 98
强腐蚀性,阴冷,密封贮藏
(1)欲配制600克溶质质量分数为19.6%的稀硫酸,需要这种浓硫酸多少克?再加水多少毫升?
(2)50克浓度为98%的浓硫酸与150克水混合后所得溶液的质量分数为多少?
29.可乐是青少年特别喜爱的一种饮料,但是可乐含糖量较高,经常饮用会引发肥胖,还有可能引起龋齿、糖尿病等。国际卫生组织建议人体每日摄入糖的量不应超过50克。已知一瓶550mL的可乐含有54克糖,请根据材料回答问题。
(1)喝上几口冰镇可乐往往会打嗝,根据如图分析其主要原因是 ;
(2)求550毫升可乐中糖的质量分数(该可乐溶液的密度约为1g/cm3);
(3)可乐主要由糖水和碳酸水按一定比例混合而成。现用含糖量10%的可乐,配制含糖量5%的低糖可乐300克,需要10%的可乐多少克?需加水的质量多少克?
参考答案
一.选择题(共15小题)
1.C。
2.B。
3.D。
4.D。
5.A。
6.A。
7.C。
8.A。
9.D。
10.A。
11.A。
12.D。
13.B。
14.D。
15.A。
二.多选题(共5小题)
16.BD。
17.AB。
18.BD。
19.AD。
20.AD。
三.填空题(共5小题)
21.(1)50℃时,A、B两物质的溶解度相等;
(2)70;
(3)降温结晶。
22.(1)减小;
(2)40;70;28.6%;
(3)不饱和;
(4)c>a>b。
23.(1)11:10。
(2)甲;11;不饱和溶液。
24.(1)C;
(2)蒸发;
(3)B;
(4)150;20。
25.
(1)易溶;先增大后减小;
(2)24.4;
(3)16.4<x≤18.8;C>B>A。
四.实验题(共3小题)
26.同学们查阅NaCl的溶解度曲线后,欲配制20℃时100g溶质质量分数为10%的NaCl溶液,整个操作如图所示:
(1)配制100g溶质质量分数为10%的氯化钠溶液,所需氯化钠 10 g,需要水的质量为 90 g。
(2)溶解时玻璃棒的作用为 搅拌,加速溶解 。
(3)上述步骤的正确顺序为 ④②①⑤③ (填序号),请改正步骤②中的一处明显错误 将氯化钠放在天平左盘称量 。
(4)若利用配制的10%的氯化钠溶液加水稀释成100g溶质质量分数为5%的氯化钠溶液,则需要10%的氯化钠溶液 50 g,加水 50 g。
(5)将氯化钠和水依次倒入烧杯中,若倾倒时有少量水溅出,会导致所配制溶液的溶质质量分数 偏大 (选填“偏大”“偏小”“无影响”)。
【解答】解:(1)10;90;
(2)搅拌,加速溶解;
(3)④②①⑤③;将氯化钠放在天平左盘称量;
(4)50;50;
(5)偏大。
27.(1)70;
(2);
(3)降温结晶;
(4)BC。
五.计算题(共2小题)
28.解:(1)设需要这种硫酸的质量为x,则x×98%=600g×19.6%,解得x=120g;需要水的质量为600g﹣120g=480g,体积为=480mL。
(2)溶液稀释前后,溶质的质量不变,50克浓度为98%的浓硫酸与150克水混合后所得溶液的质量分数为×100%=24.5%。
答:(1)需要这种浓硫酸120g,再加水480mL;
(2)50克浓度为98%的浓硫酸与150克水混合后所得溶液的质量分数为24.5%。
29.解:(1)人体内温度较高,二氧化碳的溶解度随温度的上升而下降,二氧化碳逸出。
故答案为:温度升高,二氧化碳的溶解度减小,有二氧化碳逸出。
(2)溶液的质量为550mL×1g/cm3=550g。
糖的质量分数是=×100%≈9.8%。
(3)设需用10%的糖水质量为x,根据溶液稀释前后溶质的质量不变,则10%x=300g×10%,x=150g。
水的质量=300g﹣150g=150g。
故答案为:
答:(2)550毫升可乐中糖的质量分数为9.8%;
(3)需要10%的150g,需加水的质量150g。
声明:试题解析著作权属所有,未经书面同意,不得复制发布日期:2024/4/22 22:03:07;用户:马丹;邮箱:18845904881;学号:49967352
同课章节目录
