江苏省泰州市姜堰区2015-2016学年高二上学期期中考试 化学(必修) Word版含答案
文档属性
| 名称 | 江苏省泰州市姜堰区2015-2016学年高二上学期期中考试 化学(必修) Word版含答案 |

|
|
| 格式 | zip | ||
| 文件大小 | 828.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-11-05 00:00:00 | ||
图片预览

文档简介
姜堰区2015~2016学年度第一学期期中考试
高二化学(学测)试题
可能用到的相对原子质量 H—1 C—12 O—16 S—32 Fe—56 Cu—64
一、单项选择题(本部分23题,每题3分, ( http: / / www.21cnjy.com )共69分)。
1.中共十八大报告中提出:“加强生态文明宣 ( http: / / www.21cnjy.com )传教育,增强全民节约意识、环保意识、生态意识,形成合理消费的社会风尚,营造爱护生态环境的良好风气。”下列行为不利于“生态文明”建设的是
A.在化学反应中要考虑“原子经济性”以提高效率
B.资源的开发和利用,要考虑可持续发展的原则
C.将废弃的塑料袋回收进行露天焚烧,以解决“白色污染”问题
D.要加强对工业“三废”的治理,以保护环境
2.下列物质的主要成分属于天然纤维素的是 A.聚乙烯 B.天然橡胶 C.棉花 D.涤纶
3.某些装修材料会缓慢释放出某种化学物质,可引起过敏性皮炎、免疫功能异常,这种化学物质可能是
A.HCHO B.SO2 C.Rn D.CO
4.下列材料属于复合材料的是
A.硬币 B.聚氯乙烯塑料
C.氮化硅陶瓷 D.钢筋混凝土
5.制造焊锡时,把铅加入锡的重要原因是为了
A.增加强度 B.降低熔点 C.增加硬度 D.增强抗腐蚀能力
6.下列关于糖类、蛋白质和油脂的说法正确的是
A.它们的组成都含有C、H、O、N等元素
B.在一定条件下,它们都能发生水解反应
C.人体需要的二十多种氨基酸,都可以通过人体自身合成
D.油脂都是高级脂肪酸的甘油酯,是一种高热量营养素
7.3月22日是世界水日,今年世界水日的主 ( http: / / www.21cnjy.com )题是“涉水卫生”。混凝法是净化水常用的方法,在天然水或污水中加入一定的混凝剂,可使水中的悬浮物变为沉淀而除去,下列可以作为混凝剂的是
A.明矾 B.氯气 C.小苏打 D.氯化钠
8.人生病时要合理用药。下列药品与其作用相匹配的是
A.氢氧化铝:麻醉剂 B.阿司匹林:消炎抗菌
C.麻黄碱:止咳平喘 D.青霉素:解热镇痛
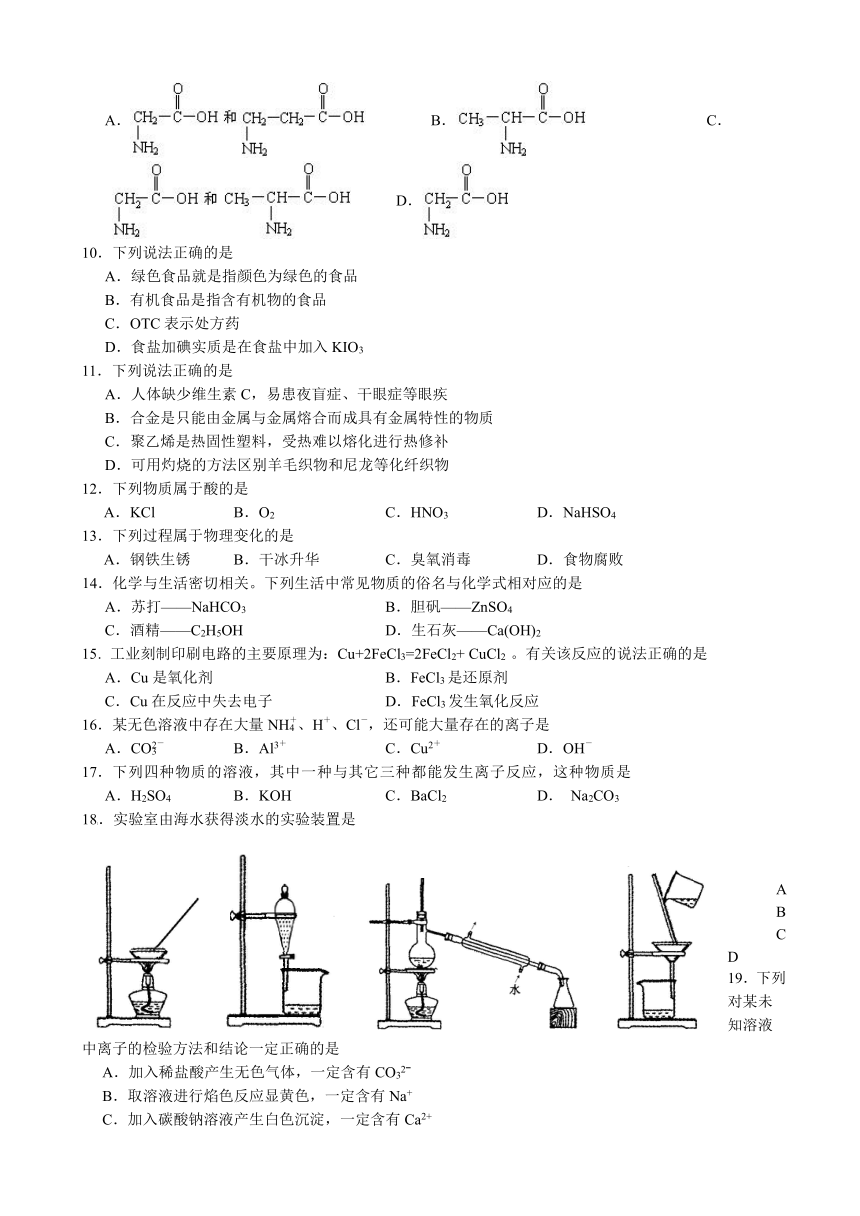
9.一种二肽的结构简式为:,合成这种二肽的氨基酸是 A. ( http: / / www.21cnjy.com ) B. ( http: / / www.21cnjy.com ) C. ( http: / / www.21cnjy.com ) D. ( http: / / www.21cnjy.com )
10.下列说法正确的是
A.绿色食品就是指颜色为绿色的食品
B.有机食品是指含有机物的食品
C.OTC表示处方药
D.食盐加碘实质是在食盐中加入KIO3
11.下列说法正确的是
A.人体缺少维生素C,易患夜盲症、干眼症等眼疾
B.合金是只能由金属与金属熔合而成具有金属特性的物质
C.聚乙烯是热固性塑料,受热难以熔化进行热修补
D.可用灼烧的方法区别羊毛织物和尼龙等化纤织物
12.下列物质属于酸的是
A.KCl B.O2 C.HNO3 D.NaHSO4
13.下列过程属于物理变化的是
A.钢铁生锈 B.干冰升华 C.臭氧消毒 D.食物腐败
4.化学与生活密切相关。下列生活中常见物质的俗名与化学式相对应的是
A.苏打——NaHCO3 B.胆矾——ZnSO4
C.酒精——C2H5OH D.生石灰——Ca(OH)2
15.工业刻制印刷电路的主要原理为:Cu+2FeCl3=2FeCl2+ CuCl2 。有关该反应的说法正确的是
A.Cu是氧化剂 B.FeCl3是还原剂
C.Cu在反应中失去电子 D.FeCl3发生氧化反应
16.某无色溶液中存在大量NH、H+、Cl-,还可能大量存在的离子是
A.CO B.Al3+ C.Cu2+ D.OH-
17.下列四种物质的溶液,其中一种与其它三种都能发生离子反应,这种物质是
A.H2SO4 B.KOH C.BaCl2 D. Na2CO3
18].实验室由海水获得淡水的实验装置是
A B C D
19.下列对某未知溶液中离子的检验方法和结论一定正确的是
A.加入稀盐酸产生无色气体,一定含有CO32ˉ
B.取溶液进行焰色反应显黄色,一定含有Na+
C.加入碳酸钠溶液产生白色沉淀,一定含有Ca2+
D.加入氯化钡溶液产生白色沉淀,一定含有SO42ˉ
20.下列电离方程式错误的是
A.CaCl2 =Ca2++2Cl- B.NaHCO3=Na++H++CO32-
C.HNO3=H++NO3- D.Ba(OH)2=Ba2++2OH-
21.下列反应的离子方程式书写正确的是
A.盐酸与氨水的反应:H++OH-===H2O
B.铝与NaOH溶液的反应:Al+2OH-===AlO+H2↑
C.氯气与氯化亚铁溶液的反应:Cl2+2Fe2+=== 2Cl-+ 2Fe3+
D.铜与稀硝酸的反应:Cu+2H++NO===Cu2++NO2↑+H2O
22.用NA表示阿伏加德罗常数的值,下列判断正确的是
A.2 g H2含有的氢原子数目为NA
B.常温下,1 mol Cl2与足量NaOH溶液完全反应,转移的电子数为2NA
C.常温常压下,11.2 L氧气含有的原子数目为NA
D.1 L 1 mol·L-1 KOH溶液中含有的钾离子数目为NA
23.Cl2、HCl的混合气体通入足量 ( http: / / www.21cnjy.com )的NaOH溶液,充分反应后,溶液中除大量OH-外,还有Cl-、ClO-、 ClO3- ,且这三种离子的物质的量之比为9:2:1,则原混合气体中Cl2和HCl体积之比为
A.5:2 B.2:5 C. 3:1 D.1:3
二、非选择题(本部分3题,共31分)
24.(15分)(1))材料是人类赖以生存和发展的重要物质基础。
现有下列材料: A.有机玻璃 B. 普通玻璃 C.石英玻璃
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是
▲ (填化学式)。
②与光导纤维主要成分相同的是 ▲ (填字母)。
③属于塑料的是 ▲ (填字母)。
(2)保证食品安全、保持营养均衡,是保障人体健康的基础。
①维生素是人体需要的营养物质。右图为某品牌维生素C
泡腾片说明书的部分内容。该泡腾片中添加的着色剂是
▲ ,泡腾片溶于水时产生“沸腾”效果,
是由于添加的酒石酸和 ▲ 反应释放出了气体。
② 缺乏某种微量元素将导致甲状腺肿大,该微量元素是 ▲ (填字母)。
a. 碘 b.铁 c.钙
③在鸡蛋清溶液中加入饱和硫酸铵溶液有沉淀析出的过程称为 ▲ 。
④ 使用青霉素可能会产生过敏,在用药前患者一定要进行 ▲ 。
(3)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
① 生活中一次性物品的使用会大大增加生态压力,一次性纸巾使用后应投入贴
有 ▲ (填字母)标志的垃圾桶内。
②漂白粉用于生活用水的杀菌消毒,漂 ( http: / / www.21cnjy.com )白粉的有效成份是 ▲ (填化学式)。治理废水中的重金属污染物可用沉淀法。例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为 ▲ (填化学式)沉淀而除去。
③铁器件在潮湿的空气中会发生电化学 ( http: / / www.21cnjy.com )腐蚀,铁锈的化学式是 ▲ 发生该腐蚀时的正极反应式为 ▲ 。
④向煤中加入石灰石作为脱硫剂,可以减少SO2的排放,生成CaSO4,发生的总反应化学方程式为 ▲ 。
25.(6分)现有下列十种物质:①Na2O ( http: / / www.21cnjy.com ) ②Cu(OH)2 ③Zn ④CaCO3 ⑤硫酸溶液 ⑥Ba(OH)2 ⑦干冰 ⑧A12(SO4)3 ⑨HCl水溶液 ⑩KHSO4
(1)其中属于非电解质的有 ▲ (填序号)。
(2)写出下列物质在水溶液中相互反应的离子方程式:
⑤ + ⑥ ▲
④ + ⑨ ▲
(3)往②中加入过量的0. ( http: / / www.21cnjy.com )1 mol/L⑩的水溶液,发生反应的离子方程式是 ▲ ,向所得溶液中继续加入③,会产生无色气泡,该反应的离子方程式是 ▲ 。
26.(10分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
(1)步骤②加入过量H2O2的目的是 ▲ 。
(2)步骤③中反应的离子方程式为 ▲ 。
(3)步骤④中一系列处理的操作步骤: ▲ 、洗涤、 ▲ 、冷却、称量。
(4)实验中用浓硫酸配制250mL1 mol/L的稀硫酸,配制时用到的玻璃仪器除了烧杯以外,还有 ▲ 。
(5)若实验无损耗,则每片补血剂含铁元素的质量 ▲ g(用含a的代数式表示)。
姜堰区2015~2016学年度第一学期期中考试
高二化学(学测)参考答案
(每题只有一个正确选项,每题3分,共69分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 C C A D B D A C C D D C
题号 13 14 15 16 17 18 19 20 21 22 23
答案 B C C B A C B B C D A
24.(15分)
(1) ①CaCO3(1分) ②C(1分) ③A(1分)
(2) ①喹啉黄 (1分)碳酸氢钠(1分)
②a(1分)
③盐析(1分)
④皮肤敏感试验(1分)
(3)①B(1分)
②Ca(ClO)2(1分) Cr(OH)3(1分)
③ Fe2O3.xH2O (1分 O2+2H2O+4e—=4OH—(1分
④2CaCO3 +O2+ 2SO2 == 2CaSO4 +2CO2(2分)
25.(6分)
(1)⑦(2分)
(2)2H++SO42—+Ba2++2OH—== BaSO 4↓+2H2O (1分)
CaCO3+2H+==Ca2++CO2↑+H2O(1分)
(3)Cu(OH)2+2H+== Cu2+ + 2H2O (1分) Zn+2H+== Zn2++H2↑(1分)
26.(10分)
(1)将Fe2+全部氧化为Fe3+ (1分)
(2)Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ (2分)
(3)过滤(1分) 灼烧(1分)
(4)250mL容量瓶、量筒、玻璃棒、胶头滴管(2分,少1个扣1分,扣完为止)
(5)0.07a (3分)
注 意 事 项
考生在答题前请认真阅读本注意事项及各题答题要求
本次考试时间为75分钟,试卷满分100分。
本试卷包含单项选择题(第1题~第23题,共23题69分)、非选择题(第24题~第26题,共3题31分)共两部分。考生答题全部答在答题纸上,答在本试卷上一律无效。
答题前,请务必将自己的姓名、班学号用书写黑色字迹的0.5毫米签字笔填写在答题纸上。
【药品名称】
维生素C泡腾片
【主要成分】
本品每片含维生素C 1g。
辅料为柠檬香精、橙味香精、喹啉黄、糖精钠、蔗糖、氯化钠、碳酸氢钠、酒石酸。
高二化学(学测)试题
可能用到的相对原子质量 H—1 C—12 O—16 S—32 Fe—56 Cu—64
一、单项选择题(本部分23题,每题3分, ( http: / / www.21cnjy.com )共69分)。
1.中共十八大报告中提出:“加强生态文明宣 ( http: / / www.21cnjy.com )传教育,增强全民节约意识、环保意识、生态意识,形成合理消费的社会风尚,营造爱护生态环境的良好风气。”下列行为不利于“生态文明”建设的是
A.在化学反应中要考虑“原子经济性”以提高效率
B.资源的开发和利用,要考虑可持续发展的原则
C.将废弃的塑料袋回收进行露天焚烧,以解决“白色污染”问题
D.要加强对工业“三废”的治理,以保护环境
2.下列物质的主要成分属于天然纤维素的是 A.聚乙烯 B.天然橡胶 C.棉花 D.涤纶
3.某些装修材料会缓慢释放出某种化学物质,可引起过敏性皮炎、免疫功能异常,这种化学物质可能是
A.HCHO B.SO2 C.Rn D.CO
4.下列材料属于复合材料的是
A.硬币 B.聚氯乙烯塑料
C.氮化硅陶瓷 D.钢筋混凝土
5.制造焊锡时,把铅加入锡的重要原因是为了
A.增加强度 B.降低熔点 C.增加硬度 D.增强抗腐蚀能力
6.下列关于糖类、蛋白质和油脂的说法正确的是
A.它们的组成都含有C、H、O、N等元素
B.在一定条件下,它们都能发生水解反应
C.人体需要的二十多种氨基酸,都可以通过人体自身合成
D.油脂都是高级脂肪酸的甘油酯,是一种高热量营养素
7.3月22日是世界水日,今年世界水日的主 ( http: / / www.21cnjy.com )题是“涉水卫生”。混凝法是净化水常用的方法,在天然水或污水中加入一定的混凝剂,可使水中的悬浮物变为沉淀而除去,下列可以作为混凝剂的是
A.明矾 B.氯气 C.小苏打 D.氯化钠
8.人生病时要合理用药。下列药品与其作用相匹配的是
A.氢氧化铝:麻醉剂 B.阿司匹林:消炎抗菌
C.麻黄碱:止咳平喘 D.青霉素:解热镇痛
9.一种二肽的结构简式为:,合成这种二肽的氨基酸是 A. ( http: / / www.21cnjy.com ) B. ( http: / / www.21cnjy.com ) C. ( http: / / www.21cnjy.com ) D. ( http: / / www.21cnjy.com )
10.下列说法正确的是
A.绿色食品就是指颜色为绿色的食品
B.有机食品是指含有机物的食品
C.OTC表示处方药
D.食盐加碘实质是在食盐中加入KIO3
11.下列说法正确的是
A.人体缺少维生素C,易患夜盲症、干眼症等眼疾
B.合金是只能由金属与金属熔合而成具有金属特性的物质
C.聚乙烯是热固性塑料,受热难以熔化进行热修补
D.可用灼烧的方法区别羊毛织物和尼龙等化纤织物
12.下列物质属于酸的是
A.KCl B.O2 C.HNO3 D.NaHSO4
13.下列过程属于物理变化的是
A.钢铁生锈 B.干冰升华 C.臭氧消毒 D.食物腐败
4.化学与生活密切相关。下列生活中常见物质的俗名与化学式相对应的是
A.苏打——NaHCO3 B.胆矾——ZnSO4
C.酒精——C2H5OH D.生石灰——Ca(OH)2
15.工业刻制印刷电路的主要原理为:Cu+2FeCl3=2FeCl2+ CuCl2 。有关该反应的说法正确的是
A.Cu是氧化剂 B.FeCl3是还原剂
C.Cu在反应中失去电子 D.FeCl3发生氧化反应
16.某无色溶液中存在大量NH、H+、Cl-,还可能大量存在的离子是
A.CO B.Al3+ C.Cu2+ D.OH-
17.下列四种物质的溶液,其中一种与其它三种都能发生离子反应,这种物质是
A.H2SO4 B.KOH C.BaCl2 D. Na2CO3
18].实验室由海水获得淡水的实验装置是
A B C D
19.下列对某未知溶液中离子的检验方法和结论一定正确的是
A.加入稀盐酸产生无色气体,一定含有CO32ˉ
B.取溶液进行焰色反应显黄色,一定含有Na+
C.加入碳酸钠溶液产生白色沉淀,一定含有Ca2+
D.加入氯化钡溶液产生白色沉淀,一定含有SO42ˉ
20.下列电离方程式错误的是
A.CaCl2 =Ca2++2Cl- B.NaHCO3=Na++H++CO32-
C.HNO3=H++NO3- D.Ba(OH)2=Ba2++2OH-
21.下列反应的离子方程式书写正确的是
A.盐酸与氨水的反应:H++OH-===H2O
B.铝与NaOH溶液的反应:Al+2OH-===AlO+H2↑
C.氯气与氯化亚铁溶液的反应:Cl2+2Fe2+=== 2Cl-+ 2Fe3+
D.铜与稀硝酸的反应:Cu+2H++NO===Cu2++NO2↑+H2O
22.用NA表示阿伏加德罗常数的值,下列判断正确的是
A.2 g H2含有的氢原子数目为NA
B.常温下,1 mol Cl2与足量NaOH溶液完全反应,转移的电子数为2NA
C.常温常压下,11.2 L氧气含有的原子数目为NA
D.1 L 1 mol·L-1 KOH溶液中含有的钾离子数目为NA
23.Cl2、HCl的混合气体通入足量 ( http: / / www.21cnjy.com )的NaOH溶液,充分反应后,溶液中除大量OH-外,还有Cl-、ClO-、 ClO3- ,且这三种离子的物质的量之比为9:2:1,则原混合气体中Cl2和HCl体积之比为
A.5:2 B.2:5 C. 3:1 D.1:3
二、非选择题(本部分3题,共31分)
24.(15分)(1))材料是人类赖以生存和发展的重要物质基础。
现有下列材料: A.有机玻璃 B. 普通玻璃 C.石英玻璃
①生产硅酸盐水泥和普通玻璃都需用到的共同原料是
▲ (填化学式)。
②与光导纤维主要成分相同的是 ▲ (填字母)。
③属于塑料的是 ▲ (填字母)。
(2)保证食品安全、保持营养均衡,是保障人体健康的基础。
①维生素是人体需要的营养物质。右图为某品牌维生素C
泡腾片说明书的部分内容。该泡腾片中添加的着色剂是
▲ ,泡腾片溶于水时产生“沸腾”效果,
是由于添加的酒石酸和 ▲ 反应释放出了气体。
② 缺乏某种微量元素将导致甲状腺肿大,该微量元素是 ▲ (填字母)。
a. 碘 b.铁 c.钙
③在鸡蛋清溶液中加入饱和硫酸铵溶液有沉淀析出的过程称为 ▲ 。
④ 使用青霉素可能会产生过敏,在用药前患者一定要进行 ▲ 。
(3)我国新修订的《环境保护法》,使环境保护有了更严格的法律依据。
① 生活中一次性物品的使用会大大增加生态压力,一次性纸巾使用后应投入贴
有 ▲ (填字母)标志的垃圾桶内。
②漂白粉用于生活用水的杀菌消毒,漂 ( http: / / www.21cnjy.com )白粉的有效成份是 ▲ (填化学式)。治理废水中的重金属污染物可用沉淀法。例如,往含铬(Cr3+)废水中加入石灰乳使Cr3+转变为 ▲ (填化学式)沉淀而除去。
③铁器件在潮湿的空气中会发生电化学 ( http: / / www.21cnjy.com )腐蚀,铁锈的化学式是 ▲ 发生该腐蚀时的正极反应式为 ▲ 。
④向煤中加入石灰石作为脱硫剂,可以减少SO2的排放,生成CaSO4,发生的总反应化学方程式为 ▲ 。
25.(6分)现有下列十种物质:①Na2O ( http: / / www.21cnjy.com ) ②Cu(OH)2 ③Zn ④CaCO3 ⑤硫酸溶液 ⑥Ba(OH)2 ⑦干冰 ⑧A12(SO4)3 ⑨HCl水溶液 ⑩KHSO4
(1)其中属于非电解质的有 ▲ (填序号)。
(2)写出下列物质在水溶液中相互反应的离子方程式:
⑤ + ⑥ ▲
④ + ⑨ ▲
(3)往②中加入过量的0. ( http: / / www.21cnjy.com )1 mol/L⑩的水溶液,发生反应的离子方程式是 ▲ ,向所得溶液中继续加入③,会产生无色气泡,该反应的离子方程式是 ▲ 。
26.(10分)硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量。实验步骤如下:
(1)步骤②加入过量H2O2的目的是 ▲ 。
(2)步骤③中反应的离子方程式为 ▲ 。
(3)步骤④中一系列处理的操作步骤: ▲ 、洗涤、 ▲ 、冷却、称量。
(4)实验中用浓硫酸配制250mL1 mol/L的稀硫酸,配制时用到的玻璃仪器除了烧杯以外,还有 ▲ 。
(5)若实验无损耗,则每片补血剂含铁元素的质量 ▲ g(用含a的代数式表示)。
姜堰区2015~2016学年度第一学期期中考试
高二化学(学测)参考答案
(每题只有一个正确选项,每题3分,共69分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 C C A D B D A C C D D C
题号 13 14 15 16 17 18 19 20 21 22 23
答案 B C C B A C B B C D A
24.(15分)
(1) ①CaCO3(1分) ②C(1分) ③A(1分)
(2) ①喹啉黄 (1分)碳酸氢钠(1分)
②a(1分)
③盐析(1分)
④皮肤敏感试验(1分)
(3)①B(1分)
②Ca(ClO)2(1分) Cr(OH)3(1分)
③ Fe2O3.xH2O (1分 O2+2H2O+4e—=4OH—(1分
④2CaCO3 +O2+ 2SO2 == 2CaSO4 +2CO2(2分)
25.(6分)
(1)⑦(2分)
(2)2H++SO42—+Ba2++2OH—== BaSO 4↓+2H2O (1分)
CaCO3+2H+==Ca2++CO2↑+H2O(1分)
(3)Cu(OH)2+2H+== Cu2+ + 2H2O (1分) Zn+2H+== Zn2++H2↑(1分)
26.(10分)
(1)将Fe2+全部氧化为Fe3+ (1分)
(2)Fe3++3NH3·H2O=Fe(OH)3↓+3NH4+ (2分)
(3)过滤(1分) 灼烧(1分)
(4)250mL容量瓶、量筒、玻璃棒、胶头滴管(2分,少1个扣1分,扣完为止)
(5)0.07a (3分)
注 意 事 项
考生在答题前请认真阅读本注意事项及各题答题要求
本次考试时间为75分钟,试卷满分100分。
本试卷包含单项选择题(第1题~第23题,共23题69分)、非选择题(第24题~第26题,共3题31分)共两部分。考生答题全部答在答题纸上,答在本试卷上一律无效。
答题前,请务必将自己的姓名、班学号用书写黑色字迹的0.5毫米签字笔填写在答题纸上。
【药品名称】
维生素C泡腾片
【主要成分】
本品每片含维生素C 1g。
辅料为柠檬香精、橙味香精、喹啉黄、糖精钠、蔗糖、氯化钠、碳酸氢钠、酒石酸。
同课章节目录
