物理人教版(2019)选择性必修第三册2.3气体的等压变化和等容变化(共31张ppt)
文档属性
| 名称 | 物理人教版(2019)选择性必修第三册2.3气体的等压变化和等容变化(共31张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 67.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2024-04-27 00:00:00 | ||
图片预览










文档简介
(共31张PPT)
第三节
气体的等压变化和等容变化
第二章 气体、固体和气体
学习目标
1
新课讲解
3
新课导入
2
经典例题
4
课堂练习
5
本课小结
6
目录
学习目标
1.了解理想气体模型,知道实际气体在什么情况下可以看成理想气体。
2.能用分子动理论和统计观点解释气体实验定律。
新课导入
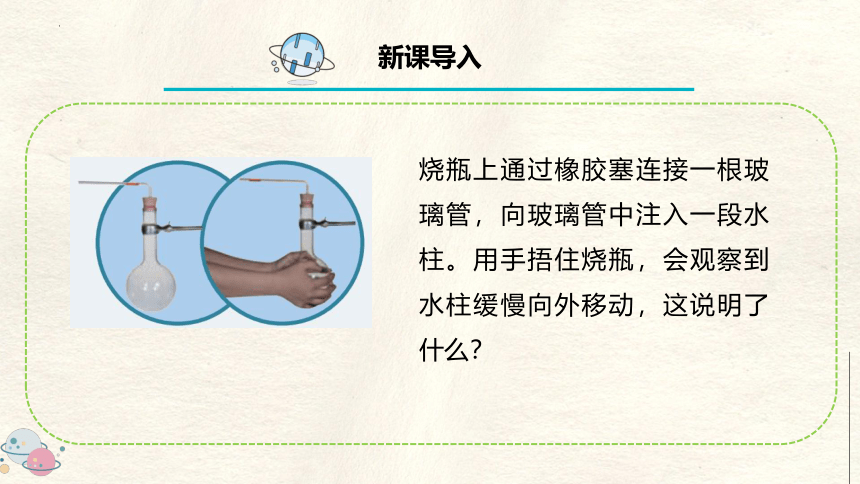
烧瓶上通过橡胶塞连接一根玻璃管,向玻璃管中注入一段水柱。用手捂住烧瓶,会观察到水柱缓慢向外移动,这说明了什么?
第一节
气体的等压变化
气体的等压变化
气体的等温变化
盖·吕萨克定律
一定质量的气体,在压强不变时,体积随温度变化的过程
一定质量的某种气体,在压强不变的情况下,体积V 与热力学温度T 成正比(V ∝ T)
公式可写成
气体的等压变化
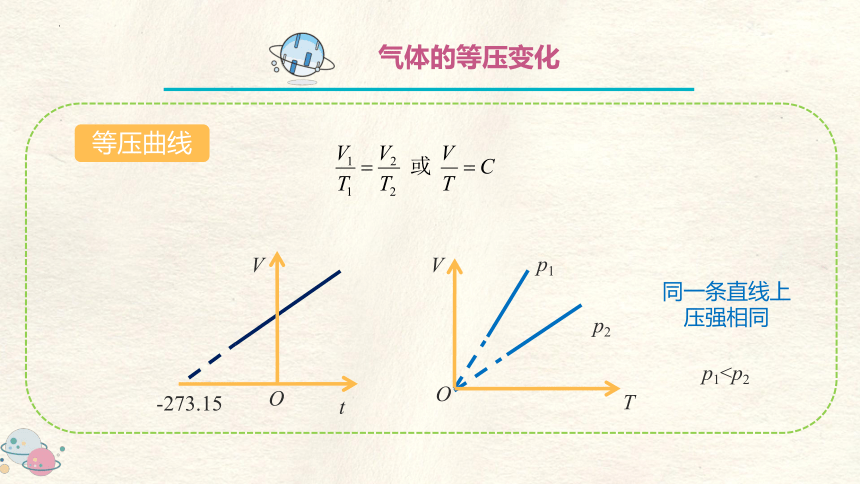
等压曲线
t
O
V
-273.15
p1
T
O
V
p2
p1同一条直线上压强相同
气体的等压变化
③压强越大,斜率越小。如图2:p1>p2>p3>p4。
对等压线的理解
V t图像中的等压线
①延长线通过(-273.15 ℃,0)的倾斜直线。
②纵轴截距V0是气体在0 ℃时的体积。
V T图像中的等压线
①延长线通过原点的倾斜直线。
②压强越大,斜率越小。如图3:p1>p2>p3>p4。
适用条件:
①气体的质量不变
②气体的压强不变
气体的等压变化
第二节
气体的等容变化
气体的等容变化
气体的等容变化
一定质量的气体,在体积不变时,压强随温度变化的过程
查理定律
一定质量的某种气体,在体积不变的情况下,压强P 与热力学温度T 成正比 (P ∝ T)
公式可写成
气体的等容变化
等容线
V1 V2
<
t
O
p
-273.15
V1
T
O
p
V2
气体的等容变化
气体实验定律
玻意耳定律
查理定律
盖-吕萨克定律
压强不太大(相对大气压),温度不太低(相对室温)
这些定律的适用范围:
p1V1=p2V2
第三节
理想气体
理想气体
特点
假设有这样一种气体,它在任何温度和任何压强下都能严格地遵从气体实验定律,我们把这样的气体叫做“理想气体”。
理想气体
(1)理想气体是不存在的,是一种理想模型。
(2)在温度不太低,压强不太大时的气体可看成是理想气体。
理想气体
特点
(4)从能量上说:理想气体的微观本质是忽略了分子力,没有分子势能,理想气体的内能只有分子动能。
(3)从微观上说:分子间以及分子和器壁间,除碰撞外无其他作用力,分子本身没有体积,即它所占据的空间认为都是可以被压缩的空间。
一定质量的理想气体的内能仅由温度决定 ,与气体的体积无关。
理想气体
理想气体的状态方程
(1)内容:一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
(2)公式:
或
注:恒量C由理想气体的质量和种类决定,即由理想气体的物质的量决定
理想气体
理想气体的状态方程
(3)使用条件:
一定质量的某种理想气体。
①当T1=T2时,p1V1 = p2V2 (玻意耳定律)
②当V1=V2时, (查理定律)
③当 p1=p2时, (盖-铝萨克定律)
(4)气体的三个实验定律是理想气体状态方程的特例:
理想气体
理想气体状态方程的应用
(1)解题步骤
①确定研究对象,即某一定质量的理想气体,分析它的变化过程;
②确定初、末两状态,准确找出初、末两状态的六个状态参量,特别是压强;
③用理想气体状态方程列式,并求解。
(2)注意:
①气体质量保持不变
②T 必须是热力学温度,公式两边 p 和 V 单位需统一
经典例题
如图所示,A、B两个大容器装有同种气体,容器间用一根细玻璃管连接,管中有一水银滴D做活塞,当左边容器的温度为-10 ℃,右边容器的温度为10 ℃时,水银滴刚好在玻璃管中央保持平衡,当两个容器的温度都下降10 ℃时,下列说法正确的是( )
A.水银滴将不运动 B.水银滴将向右运动
C.水银滴将向左运动 D.水银滴的运动方向无法判断
C
答案:C
解析:假设水银滴不动,两边气体都发生等容变化,根据 可知,对左侧气体有 ,
对右侧气体有 ,
整理可得 ,
因此水银滴将向左运动,故选C
一定质量的理想气体被活塞封闭在气缸中,气缸和活塞的绝热性、密封性良好,如图所示。现接通电热丝加热气体,活塞缓慢向上移动,不计活塞与气缸间的摩擦,外界大气压强保持不变,则该过程( )
A.气体压强不变
B.气体中每个分子热运动的动能都增加
C.电热丝产生的热量小于气体对活塞做的功
D.在单位时间内,气体分子与单位面积活塞碰撞的次数增加
A
答案:A
解析:A.活塞向上运动,不计活塞与气缸间的摩擦,外界大气压强保持不变,整个过程气体压强与外界大气压强之差保持不变,属于等压变化,故A正确;
B.由于气体温度升高,气体内能升高,则气体分子的平均动能升高,但不是每个分子的动能都增加,故B错误;
C.活塞向上移动,气体对外做功,根据热力学第一定律
气体内能升高,可知气体从电热丝处吸收的热量大于气体对活塞做的功,故C错误;
D.气体分子的平均动能升高,撞击活塞的平均作用力增大,而气体压强不变,则气体分子在单位时间内撞击活塞单位面积的次数减少,故D错误。
故选A。
热力学循环是指工作物质经过一系列状态的变化后回到它的初始状态这种周而复始的全过程,我们将一定质量的理想气体热学循环简化后如图所示,且 ,下列说法正确的是( )
A.从A 到C 过程中气体向外界放热
B.从C 到A 过程中气体对外界做功
C.从A 到C 过程中气体分子热运动的平均速率先变大后变小
D.从A 到最终回到A 的循环过程中气体与外界热量交换为0
C
答案:C
解析:A.从A到C过程中,气体体积变大,对外界做功
由
可知,从A 到C 过程中气体吸热,故A错误;
B.由图可知,从 ,体积变小,外界对气体做功,故B错误;
C.由图可得 温度先升高后降低,温度是平均动能标志,则从A到C过程中气体分子热运动的平均速率先变大后变小,故C正确;
D.全过程面积代表功的大小,合功为负,由
可知气体吸收热量,故D错误。
故选C。
民间常用“拔火罐”来治疗某些疾病,方法是将点燃的纸片放入一个小罐内,当纸片燃烧完时,迅速将火罐开口端紧压在皮肤上,火罐就会被紧紧地“吸”在皮肤上.其原因是当火罐内的气体( )
A.温度不变时,体积减小,压强增大
B.体积不变时,温度降低,压强减小
C.压强不变时,温度降低,体积减小
D.质量不变时,压强增大,体积减小
B
当堂检测
答案:B
解析:把火罐扣在皮肤上,罐内空气的体积等于火罐的容积,之后罐内气体温度不断降低,气体发生等容变化,由查理定律可知,气体压强减小,火罐内气体压强小于外界大气压强,火罐被紧紧地压在皮肤上,故选B.
如图所示,某次实验时,试管中用水银柱封闭了一定质量的理想气体,一段时间后,发现水银柱往下移动了一定距离。则关于这个实验,下列说法正确的是( )
A.封闭气体的分子平均动能增大
B.在相等时间内封闭气体的分子对单位面积器壁的冲量不变
C.封闭气体在单位时间内与单位面积器壁碰撞的分子数不变
D.由于水银对玻璃不浸润,附着层内的分子比水银内部的分子密集
B
答案:B
解析:气体压强不变,发生等压变化,有 ,又 ,
所以 ,所以温度降低,分子平均动能减小,在相等时间内封闭气体的分子对单位面积器壁的冲量不变,故A错误,B正确;由于压强不变,而分子平均动能减小,所以单位时间内撞击的分子数应增加,故C错误;不浸润时,附着层内的分子比水银内部的分子稀疏,故D错误。
本课小结
气体的等压变化和等容变化
理想气体:
理想气体的状态方程
在任何温度和任何压强下都能严格地遵从气体实验定律的气体
或
三个实验定律是理想气体状态方程的特例
适用条件
应用步骤
第三节
气体的等压变化和等容变化
第二章 气体、固体和气体
学习目标
1
新课讲解
3
新课导入
2
经典例题
4
课堂练习
5
本课小结
6
目录
学习目标
1.了解理想气体模型,知道实际气体在什么情况下可以看成理想气体。
2.能用分子动理论和统计观点解释气体实验定律。
新课导入
烧瓶上通过橡胶塞连接一根玻璃管,向玻璃管中注入一段水柱。用手捂住烧瓶,会观察到水柱缓慢向外移动,这说明了什么?
第一节
气体的等压变化
气体的等压变化
气体的等温变化
盖·吕萨克定律
一定质量的气体,在压强不变时,体积随温度变化的过程
一定质量的某种气体,在压强不变的情况下,体积V 与热力学温度T 成正比(V ∝ T)
公式可写成
气体的等压变化
等压曲线
t
O
V
-273.15
p1
T
O
V
p2
p1
气体的等压变化
③压强越大,斜率越小。如图2:p1>p2>p3>p4。
对等压线的理解
V t图像中的等压线
①延长线通过(-273.15 ℃,0)的倾斜直线。
②纵轴截距V0是气体在0 ℃时的体积。
V T图像中的等压线
①延长线通过原点的倾斜直线。
②压强越大,斜率越小。如图3:p1>p2>p3>p4。
适用条件:
①气体的质量不变
②气体的压强不变
气体的等压变化
第二节
气体的等容变化
气体的等容变化
气体的等容变化
一定质量的气体,在体积不变时,压强随温度变化的过程
查理定律
一定质量的某种气体,在体积不变的情况下,压强P 与热力学温度T 成正比 (P ∝ T)
公式可写成
气体的等容变化
等容线
V1 V2
<
t
O
p
-273.15
V1
T
O
p
V2
气体的等容变化
气体实验定律
玻意耳定律
查理定律
盖-吕萨克定律
压强不太大(相对大气压),温度不太低(相对室温)
这些定律的适用范围:
p1V1=p2V2
第三节
理想气体
理想气体
特点
假设有这样一种气体,它在任何温度和任何压强下都能严格地遵从气体实验定律,我们把这样的气体叫做“理想气体”。
理想气体
(1)理想气体是不存在的,是一种理想模型。
(2)在温度不太低,压强不太大时的气体可看成是理想气体。
理想气体
特点
(4)从能量上说:理想气体的微观本质是忽略了分子力,没有分子势能,理想气体的内能只有分子动能。
(3)从微观上说:分子间以及分子和器壁间,除碰撞外无其他作用力,分子本身没有体积,即它所占据的空间认为都是可以被压缩的空间。
一定质量的理想气体的内能仅由温度决定 ,与气体的体积无关。
理想气体
理想气体的状态方程
(1)内容:一定质量的某种理想气体在从一个状态变化到另一个状态时,尽管p、V、T都可能改变,但是压强跟体积的乘积与热力学温度的比值保持不变。
(2)公式:
或
注:恒量C由理想气体的质量和种类决定,即由理想气体的物质的量决定
理想气体
理想气体的状态方程
(3)使用条件:
一定质量的某种理想气体。
①当T1=T2时,p1V1 = p2V2 (玻意耳定律)
②当V1=V2时, (查理定律)
③当 p1=p2时, (盖-铝萨克定律)
(4)气体的三个实验定律是理想气体状态方程的特例:
理想气体
理想气体状态方程的应用
(1)解题步骤
①确定研究对象,即某一定质量的理想气体,分析它的变化过程;
②确定初、末两状态,准确找出初、末两状态的六个状态参量,特别是压强;
③用理想气体状态方程列式,并求解。
(2)注意:
①气体质量保持不变
②T 必须是热力学温度,公式两边 p 和 V 单位需统一
经典例题
如图所示,A、B两个大容器装有同种气体,容器间用一根细玻璃管连接,管中有一水银滴D做活塞,当左边容器的温度为-10 ℃,右边容器的温度为10 ℃时,水银滴刚好在玻璃管中央保持平衡,当两个容器的温度都下降10 ℃时,下列说法正确的是( )
A.水银滴将不运动 B.水银滴将向右运动
C.水银滴将向左运动 D.水银滴的运动方向无法判断
C
答案:C
解析:假设水银滴不动,两边气体都发生等容变化,根据 可知,对左侧气体有 ,
对右侧气体有 ,
整理可得 ,
因此水银滴将向左运动,故选C
一定质量的理想气体被活塞封闭在气缸中,气缸和活塞的绝热性、密封性良好,如图所示。现接通电热丝加热气体,活塞缓慢向上移动,不计活塞与气缸间的摩擦,外界大气压强保持不变,则该过程( )
A.气体压强不变
B.气体中每个分子热运动的动能都增加
C.电热丝产生的热量小于气体对活塞做的功
D.在单位时间内,气体分子与单位面积活塞碰撞的次数增加
A
答案:A
解析:A.活塞向上运动,不计活塞与气缸间的摩擦,外界大气压强保持不变,整个过程气体压强与外界大气压强之差保持不变,属于等压变化,故A正确;
B.由于气体温度升高,气体内能升高,则气体分子的平均动能升高,但不是每个分子的动能都增加,故B错误;
C.活塞向上移动,气体对外做功,根据热力学第一定律
气体内能升高,可知气体从电热丝处吸收的热量大于气体对活塞做的功,故C错误;
D.气体分子的平均动能升高,撞击活塞的平均作用力增大,而气体压强不变,则气体分子在单位时间内撞击活塞单位面积的次数减少,故D错误。
故选A。
热力学循环是指工作物质经过一系列状态的变化后回到它的初始状态这种周而复始的全过程,我们将一定质量的理想气体热学循环简化后如图所示,且 ,下列说法正确的是( )
A.从A 到C 过程中气体向外界放热
B.从C 到A 过程中气体对外界做功
C.从A 到C 过程中气体分子热运动的平均速率先变大后变小
D.从A 到最终回到A 的循环过程中气体与外界热量交换为0
C
答案:C
解析:A.从A到C过程中,气体体积变大,对外界做功
由
可知,从A 到C 过程中气体吸热,故A错误;
B.由图可知,从 ,体积变小,外界对气体做功,故B错误;
C.由图可得 温度先升高后降低,温度是平均动能标志,则从A到C过程中气体分子热运动的平均速率先变大后变小,故C正确;
D.全过程面积代表功的大小,合功为负,由
可知气体吸收热量,故D错误。
故选C。
民间常用“拔火罐”来治疗某些疾病,方法是将点燃的纸片放入一个小罐内,当纸片燃烧完时,迅速将火罐开口端紧压在皮肤上,火罐就会被紧紧地“吸”在皮肤上.其原因是当火罐内的气体( )
A.温度不变时,体积减小,压强增大
B.体积不变时,温度降低,压强减小
C.压强不变时,温度降低,体积减小
D.质量不变时,压强增大,体积减小
B
当堂检测
答案:B
解析:把火罐扣在皮肤上,罐内空气的体积等于火罐的容积,之后罐内气体温度不断降低,气体发生等容变化,由查理定律可知,气体压强减小,火罐内气体压强小于外界大气压强,火罐被紧紧地压在皮肤上,故选B.
如图所示,某次实验时,试管中用水银柱封闭了一定质量的理想气体,一段时间后,发现水银柱往下移动了一定距离。则关于这个实验,下列说法正确的是( )
A.封闭气体的分子平均动能增大
B.在相等时间内封闭气体的分子对单位面积器壁的冲量不变
C.封闭气体在单位时间内与单位面积器壁碰撞的分子数不变
D.由于水银对玻璃不浸润,附着层内的分子比水银内部的分子密集
B
答案:B
解析:气体压强不变,发生等压变化,有 ,又 ,
所以 ,所以温度降低,分子平均动能减小,在相等时间内封闭气体的分子对单位面积器壁的冲量不变,故A错误,B正确;由于压强不变,而分子平均动能减小,所以单位时间内撞击的分子数应增加,故C错误;不浸润时,附着层内的分子比水银内部的分子稀疏,故D错误。
本课小结
气体的等压变化和等容变化
理想气体:
理想气体的状态方程
在任何温度和任何压强下都能严格地遵从气体实验定律的气体
或
三个实验定律是理想气体状态方程的特例
适用条件
应用步骤
同课章节目录
- 第一章 分子动理论
- 1 分子动理论的基本内容
- 2 实验:用油膜法估测油酸分子的大小
- 3 分子运动速率分布规律
- 4 分子动能和分子势能
- 第二章 气体、固体和液体
- 1 温度和温标
- 2 气体的等温变化
- 3 气体的等压变化和等容变化
- 4 固体
- 5 液体
- 第三章 热力学定律
- 1 功、热和内能的改变
- 2 热力学第一定律
- 3 能量守恒定律
- 4 热力学第二定律
- 第四章 原子结构和波粒二象性
- 1 普朗克黑体辐射理论
- 2 光电效应
- 3 原子的核式结构模型
- 4 氢原子光谱和玻尔的原子模型
- 5 粒子的波动性和量子力学的建立
- 第五章 原子核
- 1 原子核的组成
- 2 放射性元素的衰变
- 3 核力与结合能
- 4 核裂变与核聚变
- 5 “基本”粒子
