2024年安徽省中考化学模拟试题(含答案)
文档属性
| 名称 | 2024年安徽省中考化学模拟试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 130.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-04-29 00:00:00 | ||
图片预览


文档简介
2024年安徽省中考化学模拟试题
温馨提示:
1、化学试卷共二大题17小题,满分40分物理和化学的考试时间共120分钟。
2、试卷包括“试题卷"和“答题卷"两部分请务必在“答题卷”上答题,在“试题卷"上答题是无效的。
3、附相对原子质量:H-1;C-12;N-14;O-16;Al-27。
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
附相对原子质量:H-1;C-12;N-14;O-16;Al-27;
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、化学与生产、生活息息相关,下列叙述不正确的是( )
A.二氧化碳和氮气均是造成酸雨的主要气体
B.硬水洗涤衣物既浪费肥皂也洗不干净
C.在树木上涂刷含硫磺粉的石灰浆可保护树木
D.用某些塑料代替钢和其他合金制造管道、齿轮等有利于节约金属资源
2、党的二十大报告中指出,要推动绿色发展,促进人与自然和谐共生。下列举措不符合这一要求的是( )
A.应用新技术、新工艺减少和处理“三废”排放
B.开发利用太阳能、风能等新能源替代化石燃料
C.实行塑料制品回收再生、循环利用
D.大力开采矿物资源,加快经济发展
3、如图为某元素在元素周期表中的相关信息,下列说法正确的是( )
A.图示方框中应填写“锌”,该元素属于非金属元素
B.该元素原子的中子数为30,相对原子质量为65.38
C.该元素的原子在化学反应中易失去电子形成Zn3+
D.在钢板表面电镀一层该元素的单质可以防止钢板锈蚀
4、实验是学习化学的一条重要途径,下列图示实验操作中正确的是( )
A.量取8.0mL水 B.稀释浓硫酸 C.向试管中加入石灰石 D.蒸发溶液
5、生产航天服的原料之一是二苯甲烷二异氰酸酯(Cl5H10N2O2),关于二苯甲烷二异氰酸酯的说法正确的是( )
A.是一种氧化物
B.含有1个氮分子和1个氧分子
C.由碳元素、氢元素、氮元素和氧元素组成
D.由15个碳原子、10个氢原子、2个氮原子、2个氧原子构成
6、下列物质的性质与用途具有对应关系的是( )
A.浓硫酸具有脱水性,可用作干燥剂
B.食醋具有挥发性,可用于家庭除水垢
C.熟石灰具有碱性,可用于改良酸性土壤
D.小苏打受热易分解,可用于治疗胃酸过多
7、下列与氢氧化钠有关的说法错误的是( )
A.氢氧化钠俗名叫火碱、烧碱或苛性钠
B.氢氧化钠能与油脂反应,在生活中可用来去除油污
C.氢氧化钠固体具有吸水性,可作为食品干燥剂
D.氢氧化钠如不慎沾到皮肤上,应用大量水冲洗,再涂上硼酸溶液
8、我国科学家首次实现了在温和条件下,将二氧化碳一步转化为乙醇,转化率近100%。该反应的微观示意图如图,下列说法正确的是( )
A.乙醇的化学式是C2H5O
B.反应前后原子数目改变
C.参加反应的甲、乙分子个数比为1:4
D.该反应能使无机物转化为有机物
9、树状分类法是日常生活和科学研究中常用的一种方法。如图所示的是一种树状分类的运用实例。如表所列的分类与如图分类不相符的是( )
选项 甲 乙 丙 丁 ...
A 溶液 碘酒 糖水 铁水 ...
B 单质 金刚石 氦气 氮气 ...
C 人体所需营养素 蛋白质 糖类 无机盐 ...
D 化肥 氮肥 磷肥 钾肥 ...
A.A B.B C.C D.D
10、化学学科核心素养展现了化学课程对学生发展的重要价值。下列说法正确的是( )
A.科学思维:催化剂能改变化学反应速率,所以要改变化学反应速率必须添加催化剂
B.化学观念:单质由同种元素组成,所以由同种元素组成的物质一定是单质
C.科学探究与实践:用隔绝空气加强热的方法除去氧化铜中的炭粉
D.科学态度与责任:实验后的废液集中回收处理,避免污染环境
11、将铁粉和活性炭的混合物用食盐溶液润湿后,置于如图所示装置中,进行铁的锈蚀实验。下列有关说法正确的是( )
A.铁锈蚀后生成四氧化三铁
B.导管内的液面低于试管内的液面
C.活性炭的存在会加速铁的锈蚀
D.以水代替食盐溶液,铁不能发生锈蚀
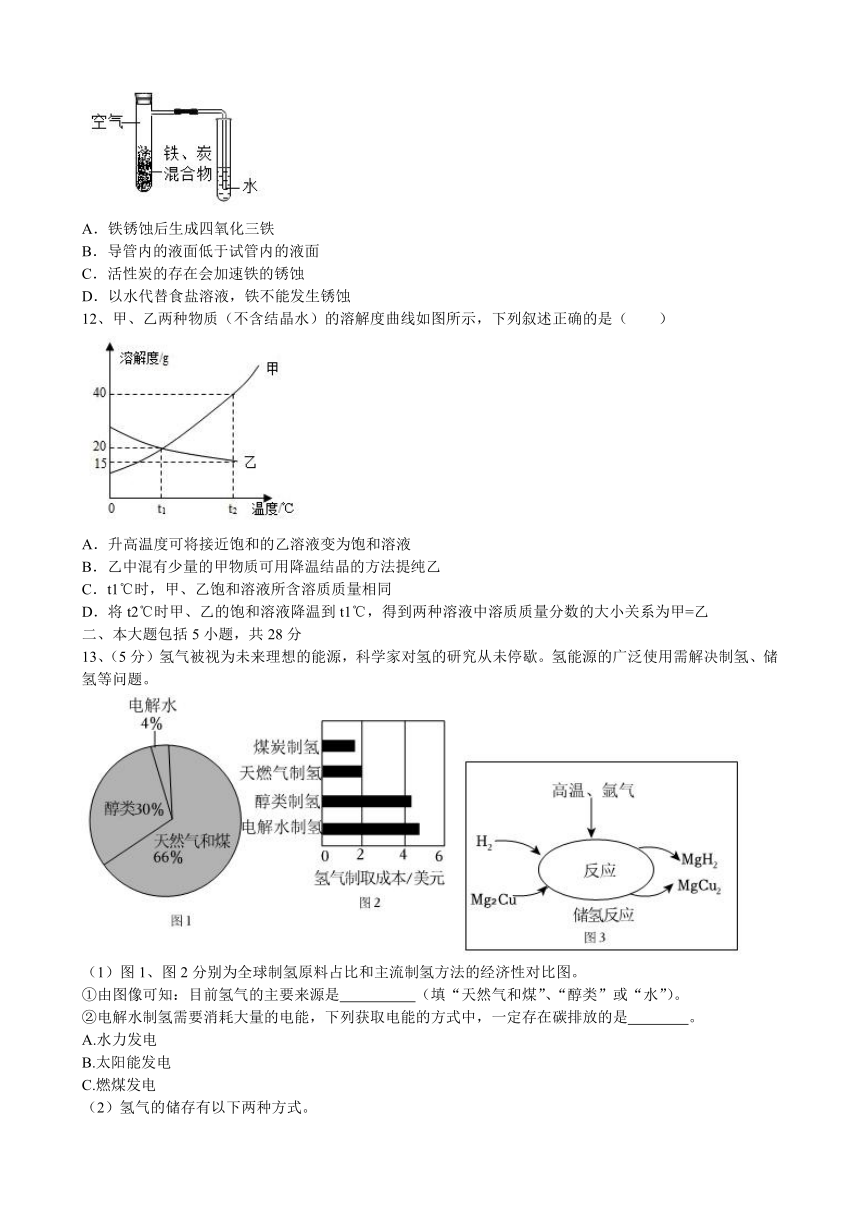
12、甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( )
A.升高温度可将接近饱和的乙溶液变为饱和溶液
B.乙中混有少量的甲物质可用降温结晶的方法提纯乙
C.t1℃时,甲、乙饱和溶液所含溶质质量相同
D.将t2℃时甲、乙的饱和溶液降温到t1℃,得到两种溶液中溶质质量分数的大小关系为甲=乙
二、本大题包括5小题,共28分
13、(5分)氢气被视为未来理想的能源,科学家对氢的研究从未停歇。氢能源的广泛使用需解决制氢、储氢等问题。
(1)图1、图2分别为全球制氢原料占比和主流制氢方法的经济性对比图。
①由图像可知:目前氢气的主要来源是 (填“天然气和煤”、“醇类”或“水”)。
②电解水制氢需要消耗大量的电能,下列获取电能的方式中,一定存在碳排放的是 。
A.水力发电
B.太阳能发电
C.燃煤发电
(2)氢气的储存有以下两种方式。
①方法一:将氢气直接加压储存在由某种镁铝合金制造的储氢罐中备用。
②方法二:先通过Mg、Cu与氢气反应,将氢气转化为MgH2暂时“储存”起来,此为储氢反应(如图3),需要使用氢气时,可通过释氢反应实现:MgH2+2HCl═MgCl2+2H2↑。请写出储氢反应的化学方程式
。
(3)采用氢能源的“未来汽车”正逐渐出现在我们的生活中,氢能源汽车主要有氢内燃汽车和氢燃料电池车两种。从理论上讲,在其它条件相同的情况下,携带相同质量的燃料,氢内燃汽车要比普通燃油汽车行驶更远的距离,这主要是因为氢气的 大。
14、(6分)化学兴趣小组同学利用下列装置对氢气的制取和性质进行了实验探究。
资料:无水硫酸铜是白色固体,遇到水会变蓝。
氢气的制取
(1)连接装置并检查装置气密性后,关闭K1、K2和K3。在注射器中分别加入锌粒和稀硫酸,打开阀门K1、K2,将稀硫酸注入注射器2中,该反应的化学方程式是 。
(2)利用装置A制取氢气的优点是 。
探究氢气的性质
(3)关闭K1,打开K3,固定注射器2,通一会氢气目的是 。
(4)点燃酒精灯,一段时间后,观察到a处现象是 。
(5)无水硫酸铜变蓝,证明反应中有水生成。M处加入的试剂是 。
15、(6分)白云石除了用于城市布置景观之外,还可以用来制备金属镁,同时得到超细碳酸钙粉末,其制备的主要流程图如图所示:
(1)通常将白云石粉碎加工后再投入煅烧窑中,其目的是 。
(2)煅烧窑中CaMg(CO3)2分解时发生的化学方程式是 。
(3)制浆池中一段时间后温度会明显上升,其主要原因是 。
(4)电解槽中生成的一种气体单质是 。
(5)该流程中可循环使用的物质除水外,还有 (填化学式)。
16、(6分)某化学兴趣小组同学对氢氧化钠溶液与稀盐酸是否发生了化学反应进行如下实验探究。
【实验一】借助指示剂的颜色变化判断酸碱是否发生了反应,如图1所示。
(1)判断试管中两种物质发生反应的现象是 ,该反应的化学方程式为 。
【实验二】借助温度和pH的变化判断酸碱是否发生了反应,图2所示是小组同学利用数字传感器绘制的氢氧化钠溶液与稀盐酸反应的有关曲线。
(2)该实验烧杯中盛放的化学药品是 ,你从图2中哪些信息可以判断氢氧化钠溶液和稀盐酸恰好反应 。
【实验三】
(3)兴趣小组同学将图2中b点处的溶液蒸干,此时得到的固体是 。
同学们继续就酸和碱的反应进行了探究。
【若正确回答下列问题加3分,总分不超过40分】
(4)取等质量、等质量分数的氢氧化钠溶液和稀盐酸加入烧杯中混合,充分反应后向溶液中滴加石蕊溶液,溶液颜色为 色。
(5)氢氧化钠溶液和稀盐酸反应前的微观示意图如图1所示,请你结合所学知识,在图2中画出两者恰好完全反应时的微观示意图。
17、(5分)纳米铝冰作为火箭固体推进剂具有广阔的应用前景。480℃以上时,发生的主要反应为
2Al+3H2OAl2O3+3H2↑。该反应中,若有54kgAl发生反应计算参加反应的H2O的质量(写出计算过程及结果)。
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1 2 3 4 5 6 7 8 9 10
A D D B C C C D A D
11 12
C A
二、本大题包括5小题,共28分
13、(5分)(1)①天然气和煤;②C;
(2)2Mg2Cu+3H2MgCu2+3MgH2;(3)热值。
14、(6分)(1)Zn+H2SO4=ZnSO4+H2↑;(2)节约药品;(3)把装置B中空气排净;
(4)黑色粉末变成亮红色;(5)碱石灰。
15、(6分)(1)增大反应物的接触面积,加快反应速率;
(2)2 CaMg(CO3)22CaO+2MgO+4CO2↑;
(3)氧化钙与水反应放热;
(4)氯气;
(5)CO2、NH4Cl。
16、(6+3分)(1)溶液由红色变为无色;NaOH+HCl=NaCl+H2O;
(2)稀盐酸;恰好完全反应时溶液pH=7;
(3)氯化钠;
(4)红色;
(5)。
17、(5分)解:设参加反应的H2O的质量为x。
2Al+3H2OAl2O3+3H2↑
54 54
54kg x
x=54kg
答:参加反应的H2O的质量为54kg。
温馨提示:
1、化学试卷共二大题17小题,满分40分物理和化学的考试时间共120分钟。
2、试卷包括“试题卷"和“答题卷"两部分请务必在“答题卷”上答题,在“试题卷"上答题是无效的。
3、附相对原子质量:H-1;C-12;N-14;O-16;Al-27。
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
附相对原子质量:H-1;C-12;N-14;O-16;Al-27;
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1、化学与生产、生活息息相关,下列叙述不正确的是( )
A.二氧化碳和氮气均是造成酸雨的主要气体
B.硬水洗涤衣物既浪费肥皂也洗不干净
C.在树木上涂刷含硫磺粉的石灰浆可保护树木
D.用某些塑料代替钢和其他合金制造管道、齿轮等有利于节约金属资源
2、党的二十大报告中指出,要推动绿色发展,促进人与自然和谐共生。下列举措不符合这一要求的是( )
A.应用新技术、新工艺减少和处理“三废”排放
B.开发利用太阳能、风能等新能源替代化石燃料
C.实行塑料制品回收再生、循环利用
D.大力开采矿物资源,加快经济发展
3、如图为某元素在元素周期表中的相关信息,下列说法正确的是( )
A.图示方框中应填写“锌”,该元素属于非金属元素
B.该元素原子的中子数为30,相对原子质量为65.38
C.该元素的原子在化学反应中易失去电子形成Zn3+
D.在钢板表面电镀一层该元素的单质可以防止钢板锈蚀
4、实验是学习化学的一条重要途径,下列图示实验操作中正确的是( )
A.量取8.0mL水 B.稀释浓硫酸 C.向试管中加入石灰石 D.蒸发溶液
5、生产航天服的原料之一是二苯甲烷二异氰酸酯(Cl5H10N2O2),关于二苯甲烷二异氰酸酯的说法正确的是( )
A.是一种氧化物
B.含有1个氮分子和1个氧分子
C.由碳元素、氢元素、氮元素和氧元素组成
D.由15个碳原子、10个氢原子、2个氮原子、2个氧原子构成
6、下列物质的性质与用途具有对应关系的是( )
A.浓硫酸具有脱水性,可用作干燥剂
B.食醋具有挥发性,可用于家庭除水垢
C.熟石灰具有碱性,可用于改良酸性土壤
D.小苏打受热易分解,可用于治疗胃酸过多
7、下列与氢氧化钠有关的说法错误的是( )
A.氢氧化钠俗名叫火碱、烧碱或苛性钠
B.氢氧化钠能与油脂反应,在生活中可用来去除油污
C.氢氧化钠固体具有吸水性,可作为食品干燥剂
D.氢氧化钠如不慎沾到皮肤上,应用大量水冲洗,再涂上硼酸溶液
8、我国科学家首次实现了在温和条件下,将二氧化碳一步转化为乙醇,转化率近100%。该反应的微观示意图如图,下列说法正确的是( )
A.乙醇的化学式是C2H5O
B.反应前后原子数目改变
C.参加反应的甲、乙分子个数比为1:4
D.该反应能使无机物转化为有机物
9、树状分类法是日常生活和科学研究中常用的一种方法。如图所示的是一种树状分类的运用实例。如表所列的分类与如图分类不相符的是( )
选项 甲 乙 丙 丁 ...
A 溶液 碘酒 糖水 铁水 ...
B 单质 金刚石 氦气 氮气 ...
C 人体所需营养素 蛋白质 糖类 无机盐 ...
D 化肥 氮肥 磷肥 钾肥 ...
A.A B.B C.C D.D
10、化学学科核心素养展现了化学课程对学生发展的重要价值。下列说法正确的是( )
A.科学思维:催化剂能改变化学反应速率,所以要改变化学反应速率必须添加催化剂
B.化学观念:单质由同种元素组成,所以由同种元素组成的物质一定是单质
C.科学探究与实践:用隔绝空气加强热的方法除去氧化铜中的炭粉
D.科学态度与责任:实验后的废液集中回收处理,避免污染环境
11、将铁粉和活性炭的混合物用食盐溶液润湿后,置于如图所示装置中,进行铁的锈蚀实验。下列有关说法正确的是( )
A.铁锈蚀后生成四氧化三铁
B.导管内的液面低于试管内的液面
C.活性炭的存在会加速铁的锈蚀
D.以水代替食盐溶液,铁不能发生锈蚀
12、甲、乙两种物质(不含结晶水)的溶解度曲线如图所示,下列叙述正确的是( )
A.升高温度可将接近饱和的乙溶液变为饱和溶液
B.乙中混有少量的甲物质可用降温结晶的方法提纯乙
C.t1℃时,甲、乙饱和溶液所含溶质质量相同
D.将t2℃时甲、乙的饱和溶液降温到t1℃,得到两种溶液中溶质质量分数的大小关系为甲=乙
二、本大题包括5小题,共28分
13、(5分)氢气被视为未来理想的能源,科学家对氢的研究从未停歇。氢能源的广泛使用需解决制氢、储氢等问题。
(1)图1、图2分别为全球制氢原料占比和主流制氢方法的经济性对比图。
①由图像可知:目前氢气的主要来源是 (填“天然气和煤”、“醇类”或“水”)。
②电解水制氢需要消耗大量的电能,下列获取电能的方式中,一定存在碳排放的是 。
A.水力发电
B.太阳能发电
C.燃煤发电
(2)氢气的储存有以下两种方式。
①方法一:将氢气直接加压储存在由某种镁铝合金制造的储氢罐中备用。
②方法二:先通过Mg、Cu与氢气反应,将氢气转化为MgH2暂时“储存”起来,此为储氢反应(如图3),需要使用氢气时,可通过释氢反应实现:MgH2+2HCl═MgCl2+2H2↑。请写出储氢反应的化学方程式
。
(3)采用氢能源的“未来汽车”正逐渐出现在我们的生活中,氢能源汽车主要有氢内燃汽车和氢燃料电池车两种。从理论上讲,在其它条件相同的情况下,携带相同质量的燃料,氢内燃汽车要比普通燃油汽车行驶更远的距离,这主要是因为氢气的 大。
14、(6分)化学兴趣小组同学利用下列装置对氢气的制取和性质进行了实验探究。
资料:无水硫酸铜是白色固体,遇到水会变蓝。
氢气的制取
(1)连接装置并检查装置气密性后,关闭K1、K2和K3。在注射器中分别加入锌粒和稀硫酸,打开阀门K1、K2,将稀硫酸注入注射器2中,该反应的化学方程式是 。
(2)利用装置A制取氢气的优点是 。
探究氢气的性质
(3)关闭K1,打开K3,固定注射器2,通一会氢气目的是 。
(4)点燃酒精灯,一段时间后,观察到a处现象是 。
(5)无水硫酸铜变蓝,证明反应中有水生成。M处加入的试剂是 。
15、(6分)白云石除了用于城市布置景观之外,还可以用来制备金属镁,同时得到超细碳酸钙粉末,其制备的主要流程图如图所示:
(1)通常将白云石粉碎加工后再投入煅烧窑中,其目的是 。
(2)煅烧窑中CaMg(CO3)2分解时发生的化学方程式是 。
(3)制浆池中一段时间后温度会明显上升,其主要原因是 。
(4)电解槽中生成的一种气体单质是 。
(5)该流程中可循环使用的物质除水外,还有 (填化学式)。
16、(6分)某化学兴趣小组同学对氢氧化钠溶液与稀盐酸是否发生了化学反应进行如下实验探究。
【实验一】借助指示剂的颜色变化判断酸碱是否发生了反应,如图1所示。
(1)判断试管中两种物质发生反应的现象是 ,该反应的化学方程式为 。
【实验二】借助温度和pH的变化判断酸碱是否发生了反应,图2所示是小组同学利用数字传感器绘制的氢氧化钠溶液与稀盐酸反应的有关曲线。
(2)该实验烧杯中盛放的化学药品是 ,你从图2中哪些信息可以判断氢氧化钠溶液和稀盐酸恰好反应 。
【实验三】
(3)兴趣小组同学将图2中b点处的溶液蒸干,此时得到的固体是 。
同学们继续就酸和碱的反应进行了探究。
【若正确回答下列问题加3分,总分不超过40分】
(4)取等质量、等质量分数的氢氧化钠溶液和稀盐酸加入烧杯中混合,充分反应后向溶液中滴加石蕊溶液,溶液颜色为 色。
(5)氢氧化钠溶液和稀盐酸反应前的微观示意图如图1所示,请你结合所学知识,在图2中画出两者恰好完全反应时的微观示意图。
17、(5分)纳米铝冰作为火箭固体推进剂具有广阔的应用前景。480℃以上时,发生的主要反应为
2Al+3H2OAl2O3+3H2↑。该反应中,若有54kgAl发生反应计算参加反应的H2O的质量(写出计算过程及结果)。
参考答案
一、本大题包括12小题,每小题1分,共12分。每小题的4个备选答案中只有一个答案符合题意。
1 2 3 4 5 6 7 8 9 10
A D D B C C C D A D
11 12
C A
二、本大题包括5小题,共28分
13、(5分)(1)①天然气和煤;②C;
(2)2Mg2Cu+3H2MgCu2+3MgH2;(3)热值。
14、(6分)(1)Zn+H2SO4=ZnSO4+H2↑;(2)节约药品;(3)把装置B中空气排净;
(4)黑色粉末变成亮红色;(5)碱石灰。
15、(6分)(1)增大反应物的接触面积,加快反应速率;
(2)2 CaMg(CO3)22CaO+2MgO+4CO2↑;
(3)氧化钙与水反应放热;
(4)氯气;
(5)CO2、NH4Cl。
16、(6+3分)(1)溶液由红色变为无色;NaOH+HCl=NaCl+H2O;
(2)稀盐酸;恰好完全反应时溶液pH=7;
(3)氯化钠;
(4)红色;
(5)。
17、(5分)解:设参加反应的H2O的质量为x。
2Al+3H2OAl2O3+3H2↑
54 54
54kg x
x=54kg
答:参加反应的H2O的质量为54kg。
同课章节目录
